氧化石墨烯吸附废水中氨氮的探究
2019-09-10孙菱翎霍建利
孙菱翎 霍建利
摘要:制备氧化石墨烯(GO),以氧化石墨烯(GO)作为吸附剂,探究在不同初始浓度的氨氮废水中,石墨烯的用量、pH值、反应温度、反应时间对氨氮吸附量及吸附率的影响,并使用等温吸附曲线研究了其吸附性能.
关键词:氨氮废水;吸附;氧化石墨烯
中图分类号:O613;X703 文献标识码:A 文章编号:1673-260X(2019)12-0042-03
石墨烯是一种单分子层物质,具有蜂窝状孔的结构,因此其有吸附性作用[1].氧化石墨烯是在石墨烯基础上进行氧化得到的,亲水性很好[2],可以应用在吸附过程中,并且在半导体、光伏、电池、航天等新领域都将有很大的应用前景[3].随着近年来化工业与制造业的发展,排放的大量的氨氮废水,使大气、土壤、淡水[4]等水的污染问题越来越严重.因此需要找到合理而有效的处理方法是现如今社会的一个重难点.目前氨氮处理分为传统技术和新技术两种,传统技术包括生物法[5]、化学沉淀法[6]、离子交换法[7]、折点氯化法[8]、吸附法[9]等,新技术包含微波辅助法[10-11]和超声波法[12].
本文采用传统的吸附法,加入氧化石墨烯(以下简称GO),处理废水中的氨氮.采用不同的吸附剂用量、pH、时间,温度及初始浓度对氨氮的影响,旨在降低工业及生活中水的氨氮量,减少污水排放,保护地球环境.
1 实验部分
1.1 步骤
第一步,配制标准浓度的NH4Cl溶液,作标准曲线.
第二步,用改进Hummers法[13]得到GO.
第三步,进行单因素实验研究,在不同GO用量、温度、pH、时间及初始浓度对吸附的影响;并探讨GO的氨氮吸附机理.
1.2 仪器与试剂
1.2.1 实验仪器
1.2.2 实验试剂
石墨粉,高锰酸钾,硝酸钠,浓硫酸,过氧化氢,氯化铵,磷酸二氢钾,碘化钾,氢氧化钾,酒石酸钾钠,氢氧化钠,氯化汞,盐酸,均为分析纯.
1.2.3 实验原料准备
(1)制备GO:用改进的Hummer法制备GO.
(2)酒石酸钾钠溶液:准确配制500g/L的溶液.
(3)纳氏试剂:准确配制纳氏试剂,放置于黑暗处备用.
(4)模拟氨氮废水:配制100mg/L氯化铵溶液2L备用.
1.3 氨氮标准曲线的绘制
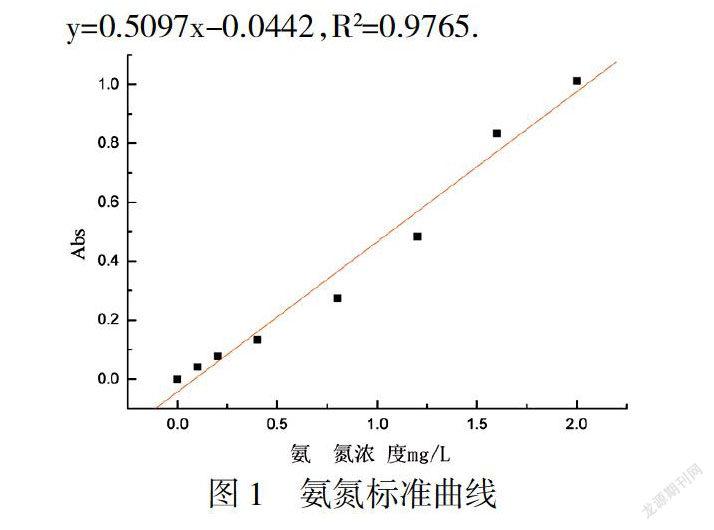
采用纳氏试剂分光光度法[14]绘制氨氮的含量与吸光度的标准曲线,得出的线性关系是:
y=0.5097x-0.0442,R2=0.9765.
1.4 实验方法
1.4.1 用量的影响
取废水100ml,投入0.2g的GO为吸附剂,分别加入0.025、0.05、0.1、0.125、0.15、0.2gGO的条件下,调pH值为8,设置温度为50℃,震荡2小时后取出,测定吸光度.
1.4.2 pH的影响
观察不同的pH值对吸附的影响.取100ml废水,投入0.2g的GO,分别在4、5、7、8、9、10的条件下,设置温度为50℃,震荡2小时后取出,测量吸光度.
1.4.3 温度的影响
通过考察不同的温度对氨氮吸附的影响.找出合适的反应温度.取100ml废水,投入0.2g的GO为吸附剂,分别在温度为15℃、25℃、35℃、55℃、65℃、75℃的条件下,震荡2小时后,取上层清液测吸光度.
1.4.4 时间的影响
取100ml废水,投入0.2gGO,调节pH值和反应温度.分别在5min、10min、15min、35min、40min、45min、55min、90min、110min和115min的温度下进行反应,并测定吸光度.
1.4.5 初始浓度的影响
考察不同初始氨氮浓度时,吸附剂对氨氮吸附率的影响.分别采用6mg/L,7mg/L,11mg/L,15mg/L,21mg/L,30mg/L,35 mg/L的氨氮废水取100ml,加入0.2gGO,调pH为9,在温度为35℃的振荡器中,振荡90min后.测量其每种浓度的吸光度.
1.4.6 等温吸附实验
以不同温度下氨氮吸附率数据计算平衡吸附浓度ce和平衡吸附量qe,得到数据为等温吸附标准曲线.
1.4.7 吸附动力学实验
取不同时间的氨氮吸附率数据,作t和Ln(Qe-Qt)的吸附动力学趋势图.
2 实验结果分析
2.1 用量的影响
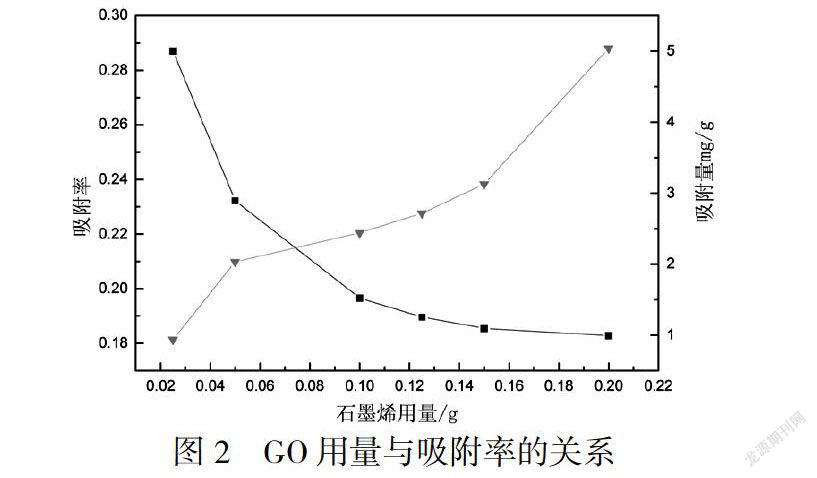
由图2,不同量的GO对废水中氨氮的具有不同的影响,随着GO量的增大,吸附率逐渐增大,吸附量递减.所以,说明GO量愈多,吸附更多的氨氮,吸附率变大.分析原因如下,随着GO量的增多,更多的氨氮分子被吸附到GO表面,吸附量增多,吸附量的增加幅度大,而用量增加幅度小,因此,吸附率是降低的.
2.2 pH的影响
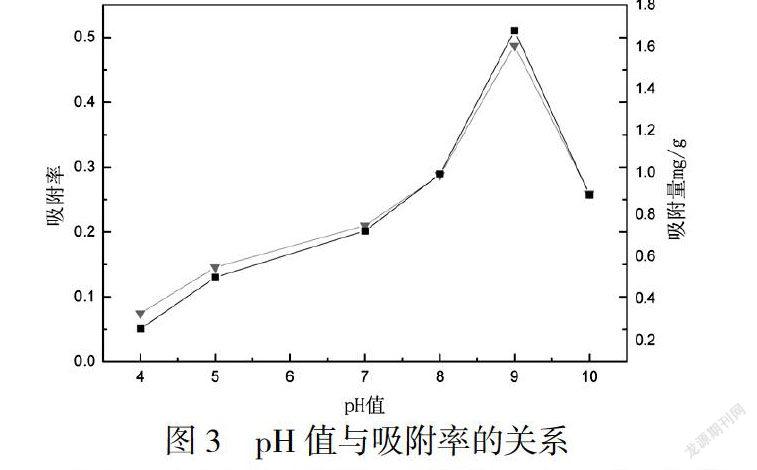
通过图3可以得出,伴随pH值的逐渐上升,吸附率开始呈现出提高趋向,达到最大吸附率,又快速降低的趋向,当pH值为9,GO的吸附率达到吸附的最大值为50%.因此,可判斷出GO吸附氨氮是在碱性条件下进行吸附.分析原因如下:酸性条件下,氨氮主要存在方式是NH4+,静电斥力阻止了与GO的接触,故吸附量低.
2.3 时间的影响
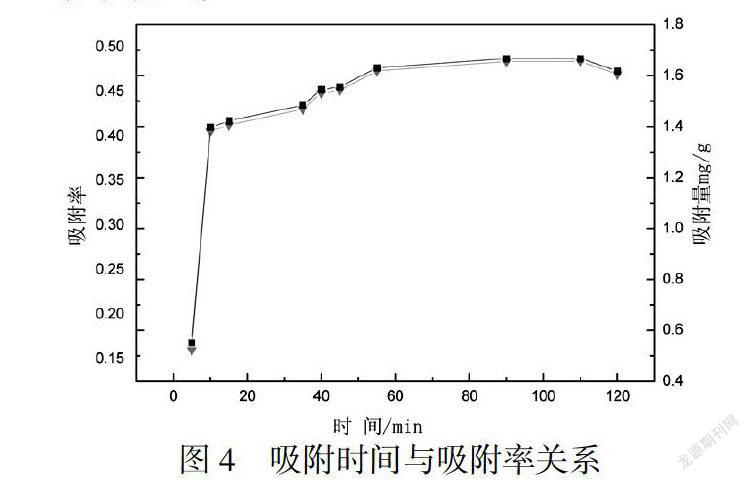
由图4可以得出,跟着吸附时段的伸长,吸附率随之逐步上升,吸附量也上涨,当反应时间到55min之后,时间的趋势基于平缓.是由于反应初始时GO吸附剂与废水中氨氮充分接触的原因,直至吸附量趋于饱和,55min后,GO对废水中氨氮的吸附量基本没有变化,说明达到吸附平衡.
2.4 温度的影响
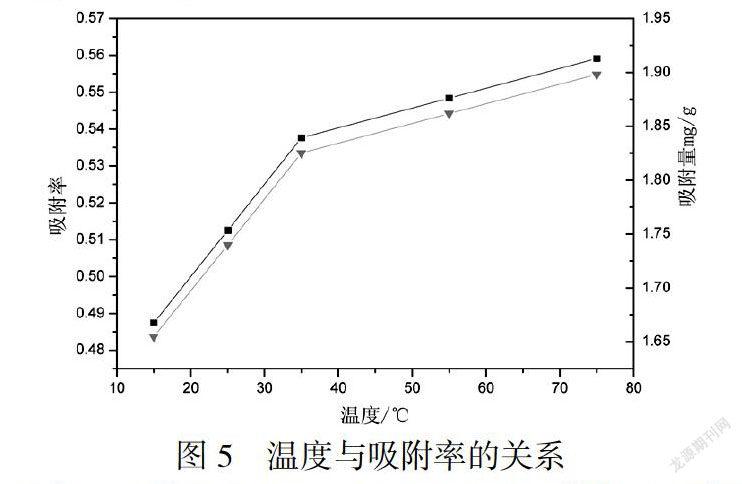
由图5可以得出,温度逐渐升高,氨氮的吸附率急剧升高后又趋于平缓.分析原因如下:反应温度升高,增加了分子间的活动能力,使分子间相互碰撞机会增加,吸附量和吸附率增加.
2.5 初始浓度的影响
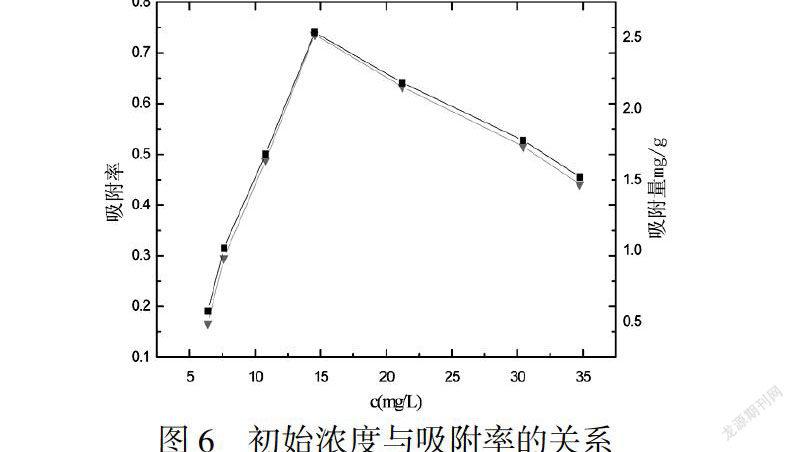
从图6可以看出,随着初始浓度的变化,吸附速率快速增加后迅速降低,当初始浓度为15mg/g时,GO对废水中氨氮的吸附率是75%.因为在氨氮初始浓度低的条件下,分子间空隙大,更有利于分子的吸附;而在吸附平衡后,增大初始浓度会抑制了吸附,引起了解吸的产生.
2.6 等温吸附实验
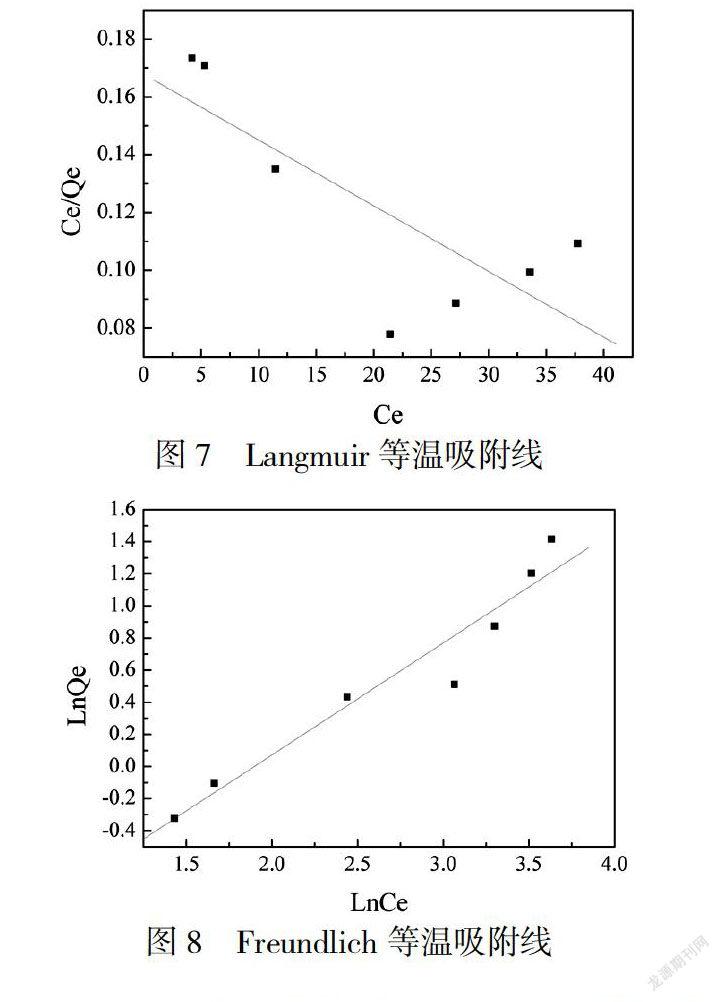
本实验采用吸附方程Langmuir与Freundlich对数据进行拟合,用以探究GO吸附氨氮的能力.
从上述两图中分析可以得出,Freundlich吸附线的回归性相对比较好,具有比较明显的线性关系.所以,GO的吸附率更合适Freundlich型的吸附.所以,GO有利于吸附工业及生活中含有氨氮废水的化合物.
2.7 吸附动力学
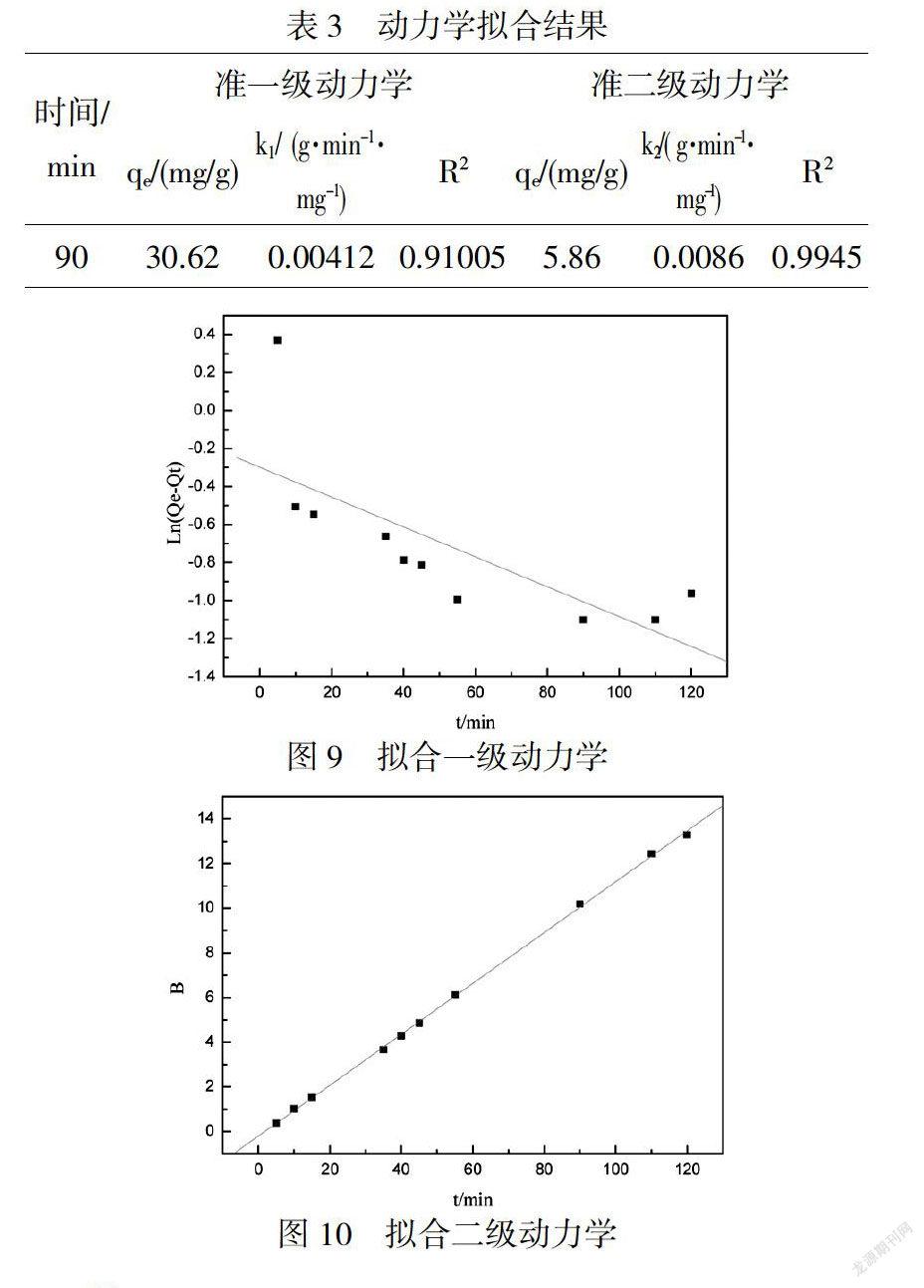
将GO吸附废水中氨氮的吸附过程分别用准一级动力学与准二级动力学模型进行拟合,结果如下表和图.
从上述两图中可以得出,准二级动力学的回归性比准一级动力学的好,能呈现出良好的线性关系.于是,GO吸附率更合适于准二级动力学拟合模型.
3 实验结论
本实验考察GO对含有氨氮废水的吸附变化以及吸附的性能.主要有以下结论:
(1)实验主要通过探究GO用量、pH值、时间、温度以及氨氮初始浓度对氨氮吸附的影响,得出较佳的反应条件,在氨氮废水中投入GO0.2g,pH值为9,温度为35℃的条件下,时间为55min,初始浓度为15mg/L,吸附率为75%.
(2)通过机理的探讨分析,GO对氨氮的吸附符合Freundlich型和准二级动力学拟合方程.
(3)此方法针对工业、农业、以及生活中含有氨氮废水的吸附有一定的作用,通过加入GO吸附剂可以减少废水中氨氮的含量,减少排放量.在氨氮脱除方面有一定的参考价值.
(4)但是因为GO在水中的易分散,吸附后很难与水分离,故此项分离技术还有待进一步的探讨和研究.
参考文献:
〔1〕王国祥.改性GO/TiO2的制备及在氨氮废水处理中的应用[J].湖南理工学院学报(自然科学版),2017,30(04):45-47.
〔2〕吴瑶瑶,李登辉,王军.GO(GO)对聚偏二氟乙烯(PVDF)超滤膜亲水化改性研究[J].广东化工,2019,46(05):5-7.
〔3〕王庆.石墨烯废水处理及回用工艺研究[J].化工设计通讯,2016,42(11):49.
〔4〕叶辉,许建华,饮用水中的氨氮问题[J].中国给水排水,2000,16(11):31-32.
〔5〕张银超.化工企业排放污水的生物法处理[J].化工管理,2018(34):38-39.
〔6〕张海娥.化学工艺在废水处理中的应用研究[J].化工管理,2018(35):112.
〔7〕曾青云,薛丽燕,曾繁钢,等.氨氮废水处理技术的研究现状[J].有色金属科学与工程,2018,9(04):83-88.
〔8〕陈星宇,马鑫铭,史明,等.折点氯化法除钨冶炼厂氨氮废水研究[J].中国钨业,2019,34(01):45-49+69.
〔9〕马安博.吸附法在污水处理中的应用及研究[J].合成材料老化与应用,2018,47(02):119-123.
〔10〕张平.微波技术处理氨氮废水的实验分析[J].化工设计通讯,2017,43(12):203.
〔11〕梁博.微波法改性竹炭催化剂制备工艺及其降解有机废液应用研究[D].西北大学,2018.
〔12〕杨晓伟,汪洋,刘秀生,等.含油污水处理技术研究进展[J].能源化工,2016,37(04):83-88.
〔13〕邢翠娟,夏愛清,董丽丽,等.石墨烯/GO的制备及吸附性能的研究进展[J].广州化工,2018,46(13):9-11+26.
〔14〕何羽,孙林江.HJ535-2009《水质氨氮的测定纳氏试剂分光光度法》不确定度评定[J].轻工科技,2013,29(02):107-108.
