Box-Behnken响应面法优化炒赤芍炮制工艺
2019-09-10许天阳董坤园宋凤媛钱圳熊金璐于澎
许天阳 董坤园 宋凤媛 钱圳 熊金璐 于澎





中圖分类号 R283.3 文献标志码 A 文章编号 1001-0408(2019)20-2845-06
DOI 10.6039/j.issn.1001-0408.2019.20.21
摘 要 目的:优化炒赤芍的炮制工艺,为该炮制品的质量控制提供参考。方法:采用高效液相色谱法对炒赤芍中的芍药苷进行含量测定。色谱柱为Agilent ZORBAX SB-C18,流动相为乙腈-0.05 mol/L磷酸二氢钾溶液(15 ∶ 85,V/V),流速为1.0 mL/min,柱温为30 ℃,检测波长为230 nm,进样量为10 μL。以表面颜色、断面颜色、硬度、气味考察炒赤芍的外观性状;以外观性状评分和芍药苷含量评分的综合评分为考察指标,分别对投药量、炒制温度、炒制时间进行单因素考察,并根据单因素试验结果对上述3个因素进行Box-Behnken响应面法优化,并对优化后的炮制工艺进行验证。结果:芍药苷检测质量浓度的线性范围为0.02~4.15 mg/mL(r=0.999 9);精密度、稳定性、重复性、加样回收率均符合要求。炒赤芍的最优工艺为投药量374.60 g、炒制温度101.61 ℃、炒制时间20 min。在最优工艺条件下,6次平行验证试验所得炒赤芍的综合评分为97.39~98.82分,RSD为0.54%,与预测值(98.18分)相接近;炒赤芍颜色较赤芍生品略有加深,质脆,有香味。结论:优化所得炒赤芍的炮制工艺稳定、可行,适用于该炮制品的制备。
关键词 炒赤芍;芍药苷;外观性状;响应面法;Box-Behnken设计
ABSTRACT OBJECTIVE: To optimize the processing technology of fried Radix Paeoniae, and to provide reference for quality control of the processed products. METHODS: The content of paeoniflorin in fried Radix Paeoniae was determined by HPLC. The determination was performed on Agilent ZORBAX SB-C18 column with mobile phase consisted of acetonitrile-0.05 mol/L potassium dihydrogen phosphate solution (15 ∶ 85, V/V) at the flow rate of 1.0 mL/min. The column temperature was 30 ℃, and detection wavelength was set at 230 nm. The sample size was 10 μL. The appearance character of fried Radix Peaoniae were investigated by appearance color, crosssection color, hardness and smell. Taking the comprehensive score of appearance character and paeoniflorin content as evaluation index, the dosage, stir-frying temperature and stir-frying time were investigated. According to the results of single factor test, Box-Behnken response surface methodology was used to optimize above 3 factors. The optimized processing technology was validated. RESULTS: The linear range of paeoniflorin were 0.02-4.15 mg/mL (r=0.999 9); precision, stablity, repeatability and sample recovery rate meet the requirements. The optimal technology of fried Radix Paeoniae included the dosage of 374.60 g, frying temperature of 101.61 ℃, frying time of 20 min. Under optimal technology, comprehensive score of fried Radix Paeoniae ranged 97.39-98.82 in 6 times of parallel verification tests (RSD=0.54%), which was close to predicted value 98.18. The color of fried Radix Paeoniae was slightly deeper than Radix Paeoniae, which was crisp and fragrant. CONCLUSIONS: The optimized processing technology of fried Radix Paeoniae is stable and feasible, and is suitable for the preparation of the processed products.
KEYWORDS Fried Radix Paeoniae; Paeoniflorin; Appearance character; Response surface method; Box-Behnken design
赤芍为毛茛科植物芍药(Paeonia lactiflora Pall.)或川赤芍(P. veitchii Lynch)的干燥根[1]。赤芍饮片炮制方法包括炒赤芍、酒赤芍等,其中炒赤芍是舒经活络、祛风行血的常用药参桂再造丸的重要药味之一。目前,全国有34家药品生产企业生产参桂再造丸,其中吉林省有9家[2]。但2015年版《中国药典》(一部)以及《吉林省中药炮制标准》(1986年版)中并未收载炒赤芍的炮制规范及质量标准,因此对于吉林省中药生产企业而言,炒赤芍尚无明确标准可依。《全国中药炮制规范》(1988年版)虽然规定炒赤芍为“取赤芍片置锅内,用文火加热,炒至颜色加深,偶有焦斑,取出放凉”[3],但具体工艺参数并不明确,仅以炮制品表面颜色判断炮制终点,无法有效控制炒赤芍质量。本课题组在参与《吉林省中药饮片炮制规范》编制项目过程中,尝试建立了炒赤芍的炮制规范与质量标准,并通过吉林省炮制规范项目定点中试企业对结果进行了验证。
由于炒赤芍的炮制工艺涉及炒制时间、炒制温度、投药量等因素的交互作用,而Box-Behnken响应面设计法适用于多因素、多水平的工艺考察试验,其可通过指标量化和非线性拟合建立直观的数学模型,预测科学客观、准确性较高[4],因此本研究采用该设计法优化炒赤芍的炮制工艺,以期为该炮制品的质量控制提供参考。
1 材料
1.1 仪器
LC-2030型高效液相色谱仪,包括四元梯度泵、自动进样器、紫外检测器(日本 Shimadzu公司);KQ-250B型超声波清洗器(昆山市超声仪器有限公司);HH-2型数显恒温水浴锅(金坛市江南仪器厂);DE-100型高速万能粉碎机(浙江红景天工贸有限公司);JM-A5002型电子天平(诸暨市超泽衡器设备有限公司);MS-5型炒货机(常州市金坛迈斯机械有限公司);DT-810迷你型红外测温仪(深圳华盛昌机械实业有限公司)。
1.2 药材与试剂
赤芍饮片(批号:20171031)购于长春市北京同仁堂大药房,经长春中医药大学药学院蔡广知副教授鉴定为毛茛科植物芍药(P. lactiflora Pall.)的根,并经实验室检测符合2015年版《中国药典》(一部)赤芍饮片项下规定,芍药苷含量高于1.5%[1];芍药苷对照品(中国食品药品检定研究院,批号:110736-201741,纯度:95.7%);乙腈、甲醇为色谱纯,磷酸二氢钾为分析纯,水为纯化水。
2 方法与结果
2.1 炒赤芍饮片样品的制备
按《全国中药炮制规范》(1988年版)赤芍项下炒赤芍相关规定,取赤芍饮片适量,用文火加热,炒至颜色加深,偶有焦斑,取出放凉,即得炒赤芍饮片[3];参照2015年版《中国药典》(一部)赤芍项下方法[1],取炒赤芍饮片经粉粹机粉碎,过筛得到粗粉。
2.2 炒赤芍饮片质量评分规则
中药饮片炮制过程中,炮制的程度及终点的判断对饮片质量优劣有着重要影响。《全国中药炮制规范》(1988年版)仅以炒赤芍饮片的外观性状判断炮制程度,不够客观。综合考虑《全国中药炮制规范》(1988年版)对炒赤芍炮制程度及2015年版《中国药典》(一部)对赤芍饮片质控指标的有关要求,本研究拟从外观性状及芍药苷含量两方面评价炒赤芍饮片质量。
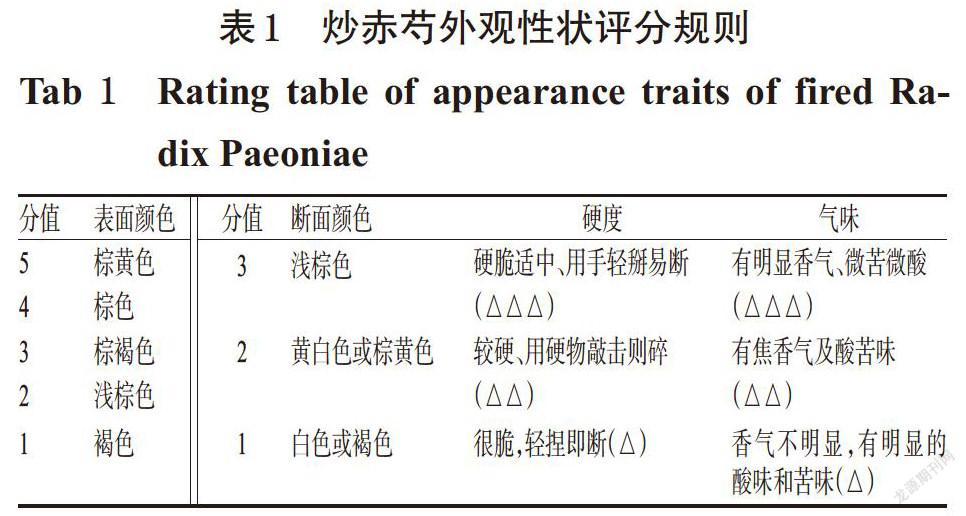
2.2.1 外观性状评分规则 根据《全国中药炮制规范》(1988年版)赤芍项下对炒赤芍炮制程度的要求[3],炒赤芍外观性状评价应包括表面颜色、断面颜色、硬度以及气味的评分,分别记为W1~W4,即外观性状评分W=W1+W2+W3+W4,评分高者为佳,具体规则见表1。
2.2.2 含量测定评分规则 赤芍中含有芍药苷、芍药内酯苷、儿茶素、没食子酰葡萄糖、丹皮酚、没食子酸等活性成分,其中芍药苷含量较高,历版《中国药典》中也一直以芍药苷作为药材质量检测的指标。因此,本研究参照2015年版《中国药典》(一部)赤芍项下的含量测定指标[1],以芍药苷作为炒赤芍含量测定的指标性成分,并以同批次生品中芍药苷含量值为参照将数据进行归一化处理。
2.2.3 综合评分 为使试验结果能够全面反映炒赤芍质量,本研究对外观性状分值与含量测定分值分别赋予了一定的权重。由于外观性状依靠个人感官判断,客观性不足,权重不宜过高,因此笔者根据经验赋予外观性状评分权重为30%、芍药苷含量评分权重为70%。综合评分(Y)=[Wi Wmax] ×30+[Hi
Hr] ×70,满分为100分。其中,Wi为某批次炒赤芍外观性状得分,Wmax为其外观性状最大值;Hi是指该批次炒赤芍中芍药苷含量,Hr是指该批次生品中芍药苷的含量。
2.3 芍药苷的含量测定
2.3.1 色谱条件 色谱柱:Agilent ZORBAX SB-C18(250 mm×4.6 mm,5 μm);流動相:乙腈-0.05 mol/L磷酸二氢钾溶液(15 ∶ 85,V/V);流速:1.0 mL/min;柱温:30 ℃;检测波长:230 nm;进样量:10 μL。
2.3.2 对照品溶液的制备 取经五氧化二磷减压干燥器中干燥36 h的芍药苷对照品适量,精密称定,加甲醇制成每1 mL含0.5 mg的溶液,即得。
2.3.3 炒赤芍供试品溶液的制备 取“2.1”项下的炒赤芍粗粉约0.5 g,精密称定,置于具塞锥形瓶中,精密加入甲醇25 mL,称定质量,浸泡4 h,超声(功率:250 W,频率:40 kHz)处理20 min,放冷;再次称定质量,用甲醇补足减失的质量,摇匀,滤过;取续滤液1 mL,用甲醇定容至10 mL,摇匀,即得。
2.3.4 赤芍供试品溶液的制备 以炒赤芍同批次生品制备赤芍供试品溶液。参照2015年版《中国药典》(一部)赤芍项下方法[1],取赤芍饮片经粉粹机粉碎,过筛得到粗粉。 取上述赤芍粗粉约0.5 g,精密称定,置于具塞锥形瓶中,精密加入甲醇25 mL,称定质量,浸泡4 h,超声(功率:250 W,频率:40 kHz)处理20 min,放冷;再次称定质量,用甲醇补足减失的质量,摇匀,滤过;取续滤液1 mL,用甲醇定容至10 mL,摇匀,即得。
2.3.5 阴性对照溶液的制备 以甲醇为阴性对照溶液。
2.3.6 系统适用性试验 精密吸取上述对照品溶液、炒赤芍供试品溶液、赤芍供试品溶液以及阴性对照溶液各10 μL,按“2.3.1”项下色谱条件进样测定,记录色谱,详见图1。由图1可见,在该色谱条件下,理论板数按芍药苷峰计不低于3 000,芍药苷与其他成分的分离度均大于1.5,阴性对照无干扰。
2.3.7 方法学考察 取“2.3.2”项下对照品溶液适量,加甲醇稀释,制得系列对照品工作溶液,按“2.3.1”项下色谱条件进样测定,记录峰面积。以待测成分质量浓度(x,mg/mL)为横坐标、峰面积(y)为纵坐标进行线性回归,得回归方程为y=13 905 683.93x+119 418.553 2(r=0.999 9),結果表明芍药苷质量浓度在0.02~4.15 mg/mL范围内线性关系良好。另经方法学验证,精密度(芍药苷峰面积RSD=1.08%,n=6)、稳定性(芍药苷峰面积RSD=3.51%,n=8)、重复性(芍药苷峰面积RSD=3.65%,n=6)、加样回收率(芍药苷平均加样回收率为99.91%,RSD=1.68%,n=6)均符合2015年版《中国药典》(四部)要求[4]。
2.4 炒赤芍炮制工艺单因素试验
中药饮片炒制过程中,由于投药量(A)、炒制温度(B)、炒制时间(C)对炒制结果有着重要影响,因此本研究根据“2.2”项下评分规则,对上述因素进行考察。
2.4.1 投药量 根据试验所用的炒货机容量以及样品物理性状,经预试验考察,发现炒货机正常工作的最大投药量为600 g,最小投药量为200 g。因此,取净赤芍饮片5份,每份不同质量(200、300、400、500、600 g),分别于110 ℃下炒制15 min,考察投药量对外观性状及芍药苷含量的影响,结果见表2、表3(注:同批次赤芍饮片生品中芍药苷的含量为4.30%,下同,表中“△”越多说明硬度/气味越大)。
由表2、表3结果可知,投药量对炒赤芍外观性状影响较为明显,对芍药苷含量影响不大;投药量为300~500 g时炒赤芍的外观性状评分较高。考虑到炒药机容量,确定投药量的优化范围为300~500 g。
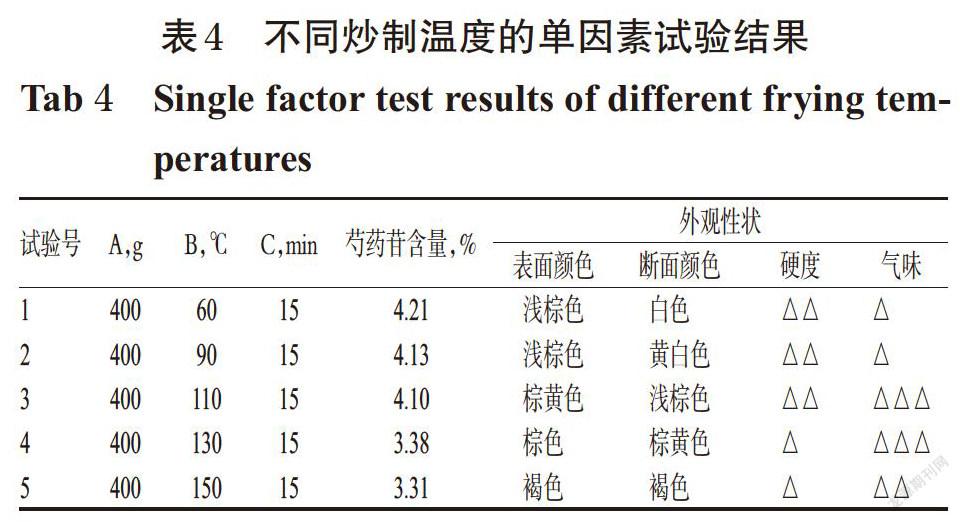
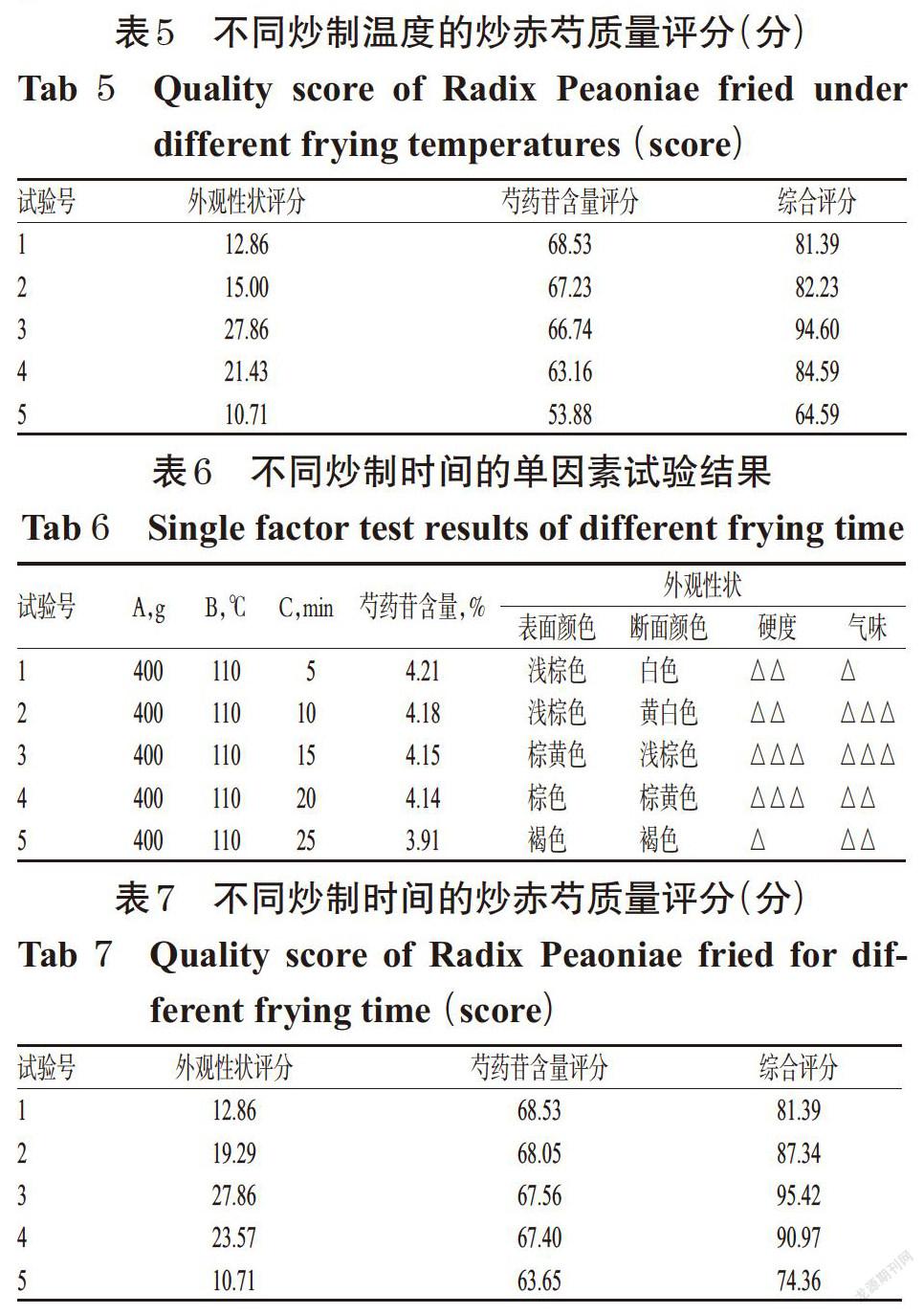
2.4.2 炒制温度 取净赤芍饮片5份,每份400 g,分别于不同温度(60、90、110、130、150 ℃)下炒制15 min,考察炒制温度对外观性状及芍药苷含量的影响,结果见表4、表5。
由表4、表5结果可知,炒制温度对炒赤芍外观性状及芍药苷含量皆有显著影响。因此,确定炒制温度的优化范围为90~130 ℃。
2.4.3 炒制时间 取净赤芍饮片5份,每份400 g,分别于110 ℃下炒制不同时间(5、10、15、20、25 min),考察炒制时间对外观性状及芍药苷含量的影响,结果见表6、表7。
由表6、表7结果可知,炒制时间对炒赤芍的外观性状及芍药苷含量皆有显著影响,当炒制时间为10~20 min时,其综合评分较高。因此,确定炒制时间的优化范围为10~20 min。
2.5 Box-Behnken响应面优化炒赤芍炮制工艺
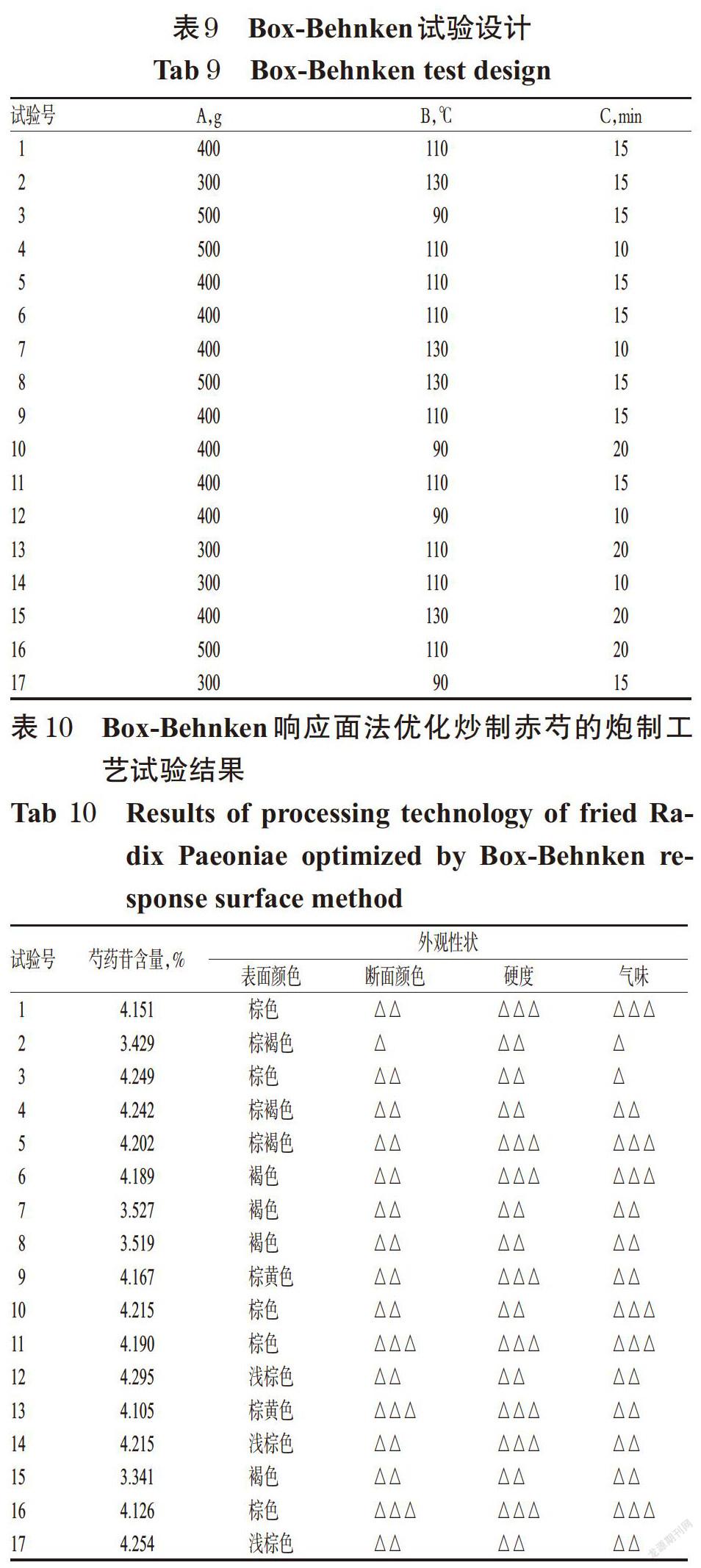
2.5.1 Box-Behnken试验设计 在单因素试验的基础上,根据中心组合试验设计原理,采用响应面法在3因素3水平上对炒赤芍炮制工艺进行优化。因素与水平见表8。以投药量(A)、炒制温度(B)、炒制时间(C)为自变量,以外观性状评价和芍药苷含量的综合评分(Y)为因变量,Box-Behnken试验设计见表9。
2.5.2 模型拟合 参照表9进行响应面法工艺优化试验,并按“2.2”项下综合评分公式进行评分,结果见表10、表11,回归模型方差分析结果见表12。
由表12可知,失拟项F值为4.07,表明该回归方程对试验的拟合较好。回归模型的F值为34.23,表明回归模型具有高度显著性。回归方程具有显著性,相关系数为0.949 2,说明响应值的变化有94.92%来源于可选变量,因此回归方程可以较好地描述各因素与响应值之间的真实关系,可以利用此模型对炒赤芍炮制质量的综合评分进行分析。通过拟合,得到响应值水平的二次方程为:Y=94.78+0.23×A-8.92×B+2.22×C+0.39×AB-0.56×AC-2.06×BC-1.41×A2-13.19×B2-1.19×C2。
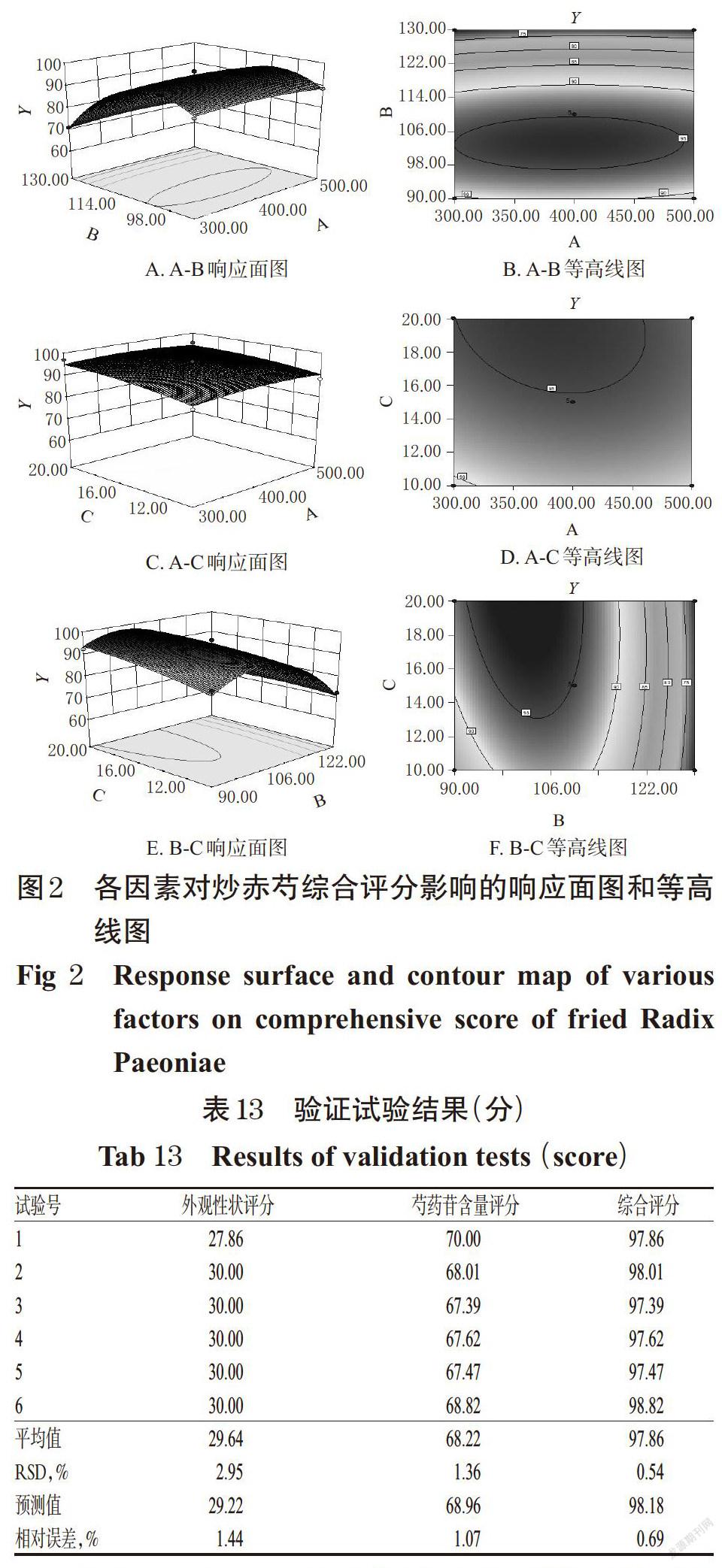
2.5.3 各因素交互作用分析 根据回归分析结果作相应的响应曲面图及其等高线图,以确认投药量(A)、炒制温度(B)、炒制时间(C)等3个因素对炒赤芍质量综合评分(Y)的影响,结果见图2。
依据各因素对响应值所构成的三维空间的曲面图,可直观地反映各因素对响应值的影响,曲线越陡则表明该因素对响应值的影响越大。由图2可见,投药量与炒制温度、炒制温度与炒制时间的曲面较陡,说明炒制温度与炒制时间对炒赤芍的质量综合评分有显著影响;而投药量与炒制时间曲面较平,说明投药量影响较小。
2.5.4 最优制备工艺的确定 基于Design-Expert V8.0.6.1
实验设计软件对所建模型进行参数最优分析,得最优制备工艺为投药量374.60 g、炒制温度101.61 ℃、炒制时间20 min;炒赤芍的性状外观评分为29.22,芍药苷含量评分为68.96,综合评分为98.18。
2.5.5 工艺验证 取“1.2”项下赤芍饮片适量,按上述最优制备工艺进行验证,平行操作6次,结果见表13。
由表13可知,6次验证试验所得炒赤芍的颜色较其生品略有加深,质脆,有香味;综合评分平均值为97.86,RSD值为0.54%;与预测分值(98.18)相对误差较小。这说明该工艺条件稳定可行,模型拟合效果好。
3 讨论
近些年,国内学者将Box-Behnken响应面法广泛应用于药学研究领域[5-7]。该方法突破了传统数理统计不能在已有“点”的基础上对整体的“面”数据进行预测的局限性[8],具有实验次数少、精密度高、预测性好、科学可行的优点。
研究中发现,以甲醇-0.05 mol/L磷酸二氢钾溶液(40 ∶ 65,V/V)为流动相时,色谱峰分离度与拖尾因子都不符合要求。因此,优化流动相比例,分别以甲醇-0.05 mol/L磷酸二氢钾溶液(35 ∶ 65、40 ∶ 60,V/V)、甲醇-水(40 ∶ 60、35 ∶ 65,V/V)以及乙腈-0.05 mol/L磷酸二氢钾溶液(20 ∶ 80、15 ∶ 85,V/V)为流动相进行测定,结果发现,以乙腈-0.05 mol/L磷酸二氢钾溶液(15 ∶ 85,V/V)为流动相时,色谱峰分离度更好,因此最终确定以该流动相进行含量测定。
本研究采用Box-Behnken响应面法优化了炒赤芍的炮制工艺,提出了具体可控的工艺参数,经吉林省炮制规范研究中试定点生产企业吉林省国安药业有限公司在本研究结果的基础上进行相应的调整,经实际生产验证,该工艺稳定、可靠。
炒制后芍药苷的减少,可能是因炒制造成的损失。炒赤芍中芍药苷较生品在不同程度上有所降低,有可能起到稍缓其药性的作用,使其功效以养血敛阴为主,但具体内在关联需后续开展相关研究进行探索。赤芍中含有芍药苷、芍药内酯苷、儿茶素、丹皮酚、没食子酸等多种活性成分[9],经炒制后含量发生变化的成分不仅只有芍药苷。因此,本研究仅以芍药苷作为炒赤芍唯一活性成分含量检测指标不够全面,后续工作中可建立多种活性成分同时检测或采用指纹图谱[10]等相关方法,对炒赤芍进一步进行全面的质量控制。
在以往的研究中,更多的是关注药材指标性成分含量而忽视对外观性状的考察[11],本试验将外观性状评价与指标性成分含量测定结果赋予分值和不同权重后,共同作为工艺考察指标,是中药现代化研究的一种探索。但外观性状评价易受感官因素影响,建议在类似的研究中引入色度仪、硬度计、电子鼻等设备[12-13],使外观评价指标更加可视化、数据化,以避免主观因素的干扰。
综上所述,本研究优化了炒赤芍的炮制工艺,得到了具体的炮制温度、炮制时间以及相应设备的投药量;经验证,优化所得炒赤芍炮制工艺稳定、可行,适用于该炮制品的制备。
参考文献
[ 1 ] 国家药典委员会.中华人民共和国药典:一部[S].2015年版.北京:中国医药科技出版社,2015:158-159、附录ⅩⅤ.
[ 2 ] 国家药品监督管理局.药品查询数据库[DB/OL]. (2015-07-30)[2019-09-10]. http://qy1.sfda.gov.cn/datasearchc-nda/face3/base.jsp?tableId=25&tableName=TABLE25&ti-tle=%E5%9B%BD%E4%BA%A7%E8%8D%AF%E5%93%81&bcId=152904713761213296322795806604.
[ 3 ] 卫生部药政管理局.全国中药炮制规范[S].北京:人民卫生出版社,1988:60-61.
[ 4 ] 国家药典委员会.中华人民共和国药典:四部[S].2015年版.北京:中国医药科技出版社,2015:59-60.
[ 5 ] 孔征,毛乐静,霍仕霞,等. Box-Behnken响应面法优化管花肉苁蓉中毛蕊花糖苷的提取工艺研究[J].中国药房,2019,30(14):1970-1974.
[ 6 ] 谢伟杰,张永萍,徐剑,等.正交设计联用Box-Behnken效应面法优选复方石斛清肺散提取工艺[J].中成药,2015,37(8):1683-1688.
[ 7 ] 张文秀,朱卫丰,聂鹤云,等. Box-Behnken响应面法优化马钱子提取工艺[J].中成药,2015,37(9):1932-1936.
[ 8 ] 徐璐,汪涛,郭巧生,等.响应面法优化超声辅助法提取昆仑雪菊色素的工艺研究[J].中国中药杂志,2014,39(24):4792-4797.
[ 9 ] 段文娟,姜艳,靳鑫,等.赤芍的化学成分研究[J].中国药物化学杂志,2009,19(1):55-58.
[10] 孙冬梅,陈秋谷,毕晓黎,等.二基原赤芍HPLC指纹图谱的建立和5种成分的含量测定[J].中药材,2018,41(4):898-903.
[11] 周慧,宋凤瑞,刘志强,等. ESI-MS和HPLC-UV法研究大黄、黄柏、赤芍炮制前后化学成分变化[J].药物分析杂志,2009,29(6):883-888.
[12] 李文敏,吴纯洁,艾莉,等.基于电子鼻、电子舌技术实现中药性状气味客观化表达的展望[J].中成药,2009,31(2):282-284.
[13] 卢一.基于“气味”信息分析的中药饮片快速鉴别研究[D].成都:成都中医藥大学,2017.
(收稿日期:2018-11-16 修回日期:2019-09-11)
(编辑:余庆华)
