2017 ISHNE/HRS动态心电图和体外心电监测/远程监测专家共识(2):诊断适应证及临床预测
2019-09-09,,,
, , ,
高洁 肖美凤 王新康 卢喜烈 薛求真 译
1 临床诊断的适应证
1.1 晕厥
晕厥是指由于心输出量低使脑部血流量突然或持续下降而导致的意识丧失,可能是由原发性心电问题(如心动过缓、心动过速)或血流动力学方面的原因引起的。AECG的作用是识别缓慢性心律失常(如窦性停搏、房室阻滞),或者快速性心律失常(如持续性室性心动过速)。
在过去十年间,关于晕厥患者诊断和治疗的若干指南、评分和建议相继发表。它们大多建议高危患者住院并接受进一步的诊断检查,以明确或排除晕厥的高危因素。绝大多数低风险患者无须入院做进一步治疗,可在门诊接受AECG检测。
症状和心律的相关性仍是晕厥诊断的基石,可用来确认心脏电活动是否引起晕厥。监测方式的选择取决于事件发生的频率。有时一份体表12导联心电图可能就足以建立症状与心律之间的联系(如完全性心脏阻滞),然而,由于晕厥通常短暂和间歇性出现,在评估时难以捕捉,因此长时程监测更常用。对儿科人群的监测是一个特殊的挑战,特别是当监测对象为那些可能无法表达症状或遵从复杂指示的婴幼儿。这些年幼患者可能需要量身定制的更自动化的记录系统。
1.1.1 AECG可检出的缓慢性心律失常 (1) 短暂性和阵发性高度房室阻滞:AECG可检测到房室传导的突然中断且不伴有缓慢窦性激动发放。后者提示迷走神经或神经心源性机制,而非原发性心脏传导系统疾病(不建议植入起搏器)。(2) 窦房结功能障碍:窦性自律性缺陷包括窦房阻滞、窦性心动过缓、心动过速-心动过缓综合征、窦性停搏和转复后心脏停搏(通常与心房颤动相关)。尽管窦性心率<40次/min被认为是有症状患者的潜在致病因素,但仅凭经验性的临界值界定来诊断是武断的,因此强烈建议证实症状与节律之间的相关性。多种AECG记录仪可以揭示出窦房结功能是否不足以满足患者的代谢需求并产生症状。该选择何种特性的监测仪取决于症状发生的频率和性质。
1.1.2 动态远程监测可检出的快速性心律失常 (1) 室上性心动过速是晕厥的罕见原因,合并有心力衰竭、心肌病或转复后的窦性停搏除外。室上性心动过速大多可通过类似于窦性心律的窄QRS波心动过速来诊断。它存在多种发生机制,有些具有特征性的波形和激动顺序。在一些患者中,室上性快速性心律失常会产生宽大畸形的QRS波,并表现为宽QRS波心动过速。由于AECG通常不具有完整的心电图导联体系,因此异常传导的节律可能难以被识别为室上性起源。(2) 室性快速性心律失常包括室性心动过速(单形性和多形性)、心室颤动和尖端扭转型室性心动过速。AECG监测只是它的检测方式之一,症状发作期间记录最为有效。根据左心室射血分数(LVEF)的范围,许多左室功能低下者适合植入心律转复除颤器(ICD),而其他患者则需要行腔内电生理检查,以程序性刺激诱发室速。
AECG监护仪适用于不明原因晕厥的患者。对AECG记录的使用基于以下两个目的:① 捕获到足以解释晕厥的严重心律失常事件,预示着可能发生更严重的心律失常事件,或本身就足以明确应当采取何种治疗或干预措施。② 若心律失常事件与复发症状相关,则可以指导治疗。同样有意义的是,如果能证明在症状复发期间没有心律失常发生,则可有效排除晕厥与心律失常的相关性。例如,当观察到更高级的房室阻滞,尤其是束支阻滞(如二度Ⅱ型房室阻滞或一过性三度房室阻滞)时,满足第一条诊断目的。在验证第二条目的时,一项短程Holter监测研究发现,4%的患者的临床症状与记录到的心律失常相关,17%的患者症状与监测仪记录的心律失常无关。
AECG记录仪的类型和记录的持续时间应根据患者的病史进行调整,但一般诊断率不高,其取决于临床症状的发作频率。延长记录时间或许能提高诊断率。在一项试验中,与48 h AECG监测相比,从一个月的心电图循环记录中获知症状-节律相关性的总概率从22%升高到56%。在另一项研究中,对于将植入式循环记录仪(implantable loop recorder,ILR)指定为首要诊断策略的患者,症状-节律相关性记录时间的中位值为16 d;经过一个月的监测,87%的患者被证实症状与节律相关。延长ILR的监测可进一步提高晕厥的诊断率,据报道可高达85%。
尽管运动诱发的心律失常通常用平板运动试验来诊断,但AECG记录或许也有一定的价值,尤其是对青少年。这有助于在更自然的活动状态下进行心电记录,并且还可能记录到在人为设置的平板运动条件下达不到的运动水平,从而增强症状-节律的相关性。
1.2 心悸
心悸是AECG最常见的指征,也是最初研发AECG的主要动因之一。高达20%的门诊患者出现心悸,大多数为良性病因。虽然1/3的心悸患者可通过详细的病史、体格检查和12导联心电图确诊,但对其余患者而言,AECG用于临床诊断的性价比最高。
对以下不明原因的心悸患者,AECG监测有助于揭示症状-心电相关性:① 病史、体格检查和12导联心电图检查结果提示可能存在心律失常;② 已确诊为结构性心脏病、有心脏性猝死家族史或遗传性离子通道病(有发生心律失常的风险);③ 患者需要确认自身症状并获得具体的解释;④ 根据症状制定治疗方案,且特殊治疗方法(如射频消融、抗心律失常治疗)的选用取决于正式的心律失常诊断。
AECG监测对于不明原因的、耐受良好的复发性心悸的诊断非常关键。在选择监测设备时,应考虑患者的临床表现和心悸的发作频率。传统AECG监测仪(24~48 h)适用于每天经常出现心悸的患者,或总能再现症状的患者(如体位性或劳累性心悸患者)。患者每天坚持记录下心悸发生的时间非常重要。心电图上识别出的自发性心律失常与心悸的相关性是可变的,有时可能相关性很小。循环事件记录仪和交互式心电图应用软件适用于偶发性心悸和不可预测性心悸患者,其仅在患者激活监护仪时才能保存和传输心电图。这些装置有助于揭示症状与节律的相关性,但要求患者保持警惕并能及时激活记录仪。与24 h Holter相比,连续循环记录仪的诊断率更高,且已被证实更具成本效益。研究表明,2周的心电图监测在晕厥诊断率和相关成本之间达到最佳平衡。AECG的诊断率与监测持续时间直接相关(表1),且取决于研究人群中“准确报告者”所占比例。在通常情况下,节律的诊断结果可反映研究对象中心律失常的患病率。
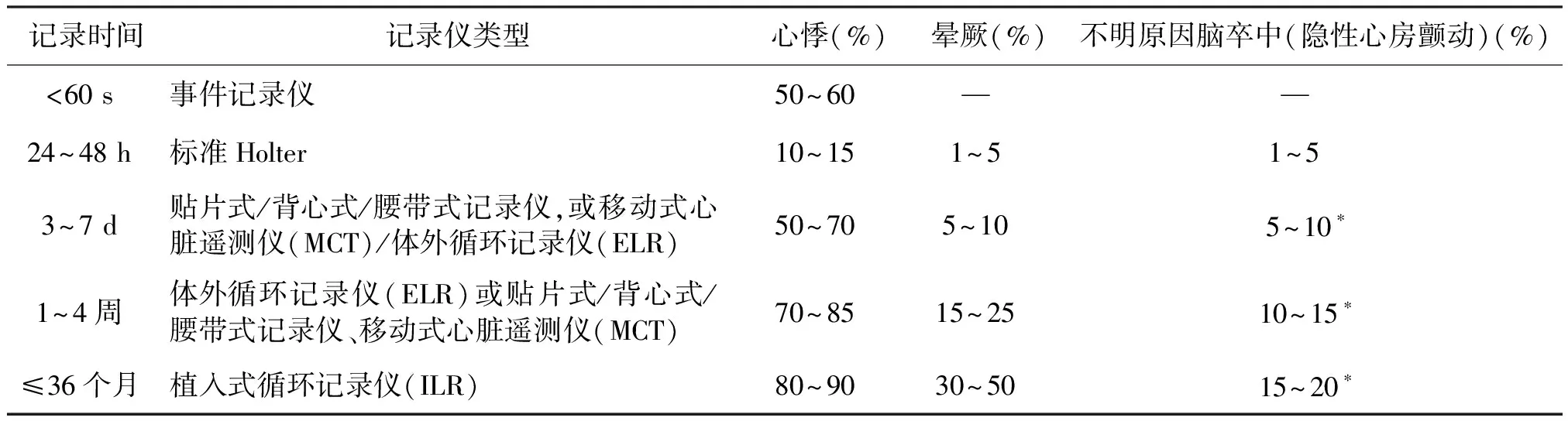
表1 不同动态心电记录方式的诊断率估计值
*: 估计值不确定。编写委员会参考了已发表的研究资料和未发表的相关信息,但由于缺少对照试验或检测到的心律失常与长期预后的相关性试验结果,而未能获得准确的估计值
1.3 胸痛和冠脉缺血
AECG监测可用于诊断胸痛的病因(动脉粥样硬化性冠状动脉疾病和Prinzmetal变异型心绞痛)、识别体表心电图上无明显表现的非典型胸痛,并评估“缺血负荷”的大小、缺血持续时间与ST段压低程度。在冠状动脉疾病患者中,动态缺血的发作大多是无症状的,因此可使用客观的心电图监测(如AECG)来确定患者日常活动中缺血的严重程度。
缺血的诊断标准是ST段压低至少0.5~1.0 mV(0.5~1.0 mm),且至少持续1 min才恢复正常。据报道,对经血管造影确定的胸痛和已知冠状动脉疾病患者,通过连续心电图检测到的ST段压低诊断缺血的敏感性(62%)、特异性(61%)与使用相同导联记录的平板运动试验结果相近(分别为67%和65%)。AECG监测显示,近半数稳定型冠脉疾病患者表现为一过性ST段压低,可能意味着缺血性事件的发生。AECG监测所提供的这一重要的预后信息,可能超出了在平板运动试验中的发现。在一项研究中,经过多变量校正后,仅在AECG监测期间有ST段压低而在平板运动试验中未见ST段压低,强烈提示预后不良。在不稳定型冠脉综合征患者中,无症状性缺血可预测短期和长期风险。
AECG监测也被用于诊断和管理患有Prinzmteal变异型心绞痛这种罕见综合征的患者,但至于要采取何种恰当的措施来预防血管痉挛的发作,主要是基于心导管实验室的有创性测试。
在ST段抬高型心肌梗死(ST-segment elevation myocardial infarction,STEMI)患者中,经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)的早期再灌注仍然是关键的治疗干预措施。由于只有特定的医疗机构才能开展PCI,因此院前诊断在实践中具有优势,具体表现为,绕过急诊科,将救护车辆引导至最佳场所,并在患者接收场所做好紧急PCI及相关治疗的准备。紧急运输系统必须能记录12导联心电图并将其发送到诊断中心,由能够熟练读图的技师出具诊断报告。这样的紧急运输系统已在丹麦卫生系统中正式运行多年,每年处理约4000例心电图,已有81%的院前诊断为STEMI的患者接受了急诊PCI,且诊断的假阳性率在可接受范围内较低。随着这种快速分诊系统的应用,STEMI患者的30 d死亡率有所下降,不仅证实了其技术可行性,而且也意味着能给临床带来显著影响。
1.4 对儿科患者的特殊考虑因素
对儿科患者行AECG检查应予以特殊考虑。对患儿行AECG检查的适应证与成年患者类似,主要取决于症状发作的频率及持续时间;AECG检查也可用于危险分层和疗效评估。
心悸是一种常见症状。AECG在10%~15%的心悸患儿中记录到相关的心律失常;相反,具有相同症状的患者中近半数表现为窦性心动过速。在一项纳入495名患儿的单中心研究中,电话传输心电事件监测仪(transtelephonic electrocardiographic event monitor, TTM)的诊断率达48%;相反,该研究中超过半数的患儿在症状发作时未能传输出单个、清晰的心电图,由此凸显出患者触发设备应用于儿科人群的局限性。与年龄相关的依从性更加复杂:大多数5岁以下的幼儿无法完成事件触发监控。临床医生可以让患儿的父母、看护者甚至教师在患儿症状发作时触发设备,从而规避上述问题。尽管如此,在时间紧迫的事件中,这种方式也不尽合理,因此仍是这类设备主要的局限性。
晕厥的发生限制了患者利用触发式AECG进行病因诊断。由于暂时丧失意识,晕厥患者往往无法触发设备,因此,临床医生建议对门诊患者使用无须患者触发的连续记录装置进行心脏远程监测。在某些情况下,ILR可能捕捉到晕厥事件。心源性胸痛在儿科人群中极少发生。在一项大型前瞻性研究中,<5%的儿科患者被确诊为心源性胸痛。因此,尽管AECG的诊断率较低,但可用于排除与心脏或节律相关病因的症状,给患者及其家属提供进一步的确认。
AECG可用于风险评估。对于无症状预激综合征患者,2012年美国儿科和先天性电生理学会(PACES)/美国心律协会(HRS)发布的专家共识建议,可利用运动负荷测试来检测预激性的逐搏消失。这可以通过AECG实现,尽管常规导联分析和心电图质量不如在正式压力负荷测试期间进行12导联节律评估所获得的。AECG是先天性心脏病患儿系列评估中的常规检测项目之一。例如,针对已治愈的先心病患儿或是仍有显著的血流动力学异常的患者,AECG是Ⅰ类推荐;针对患有先天性心脏病的成年患者,AECG被认为是用来监测心律失常和/或传导障碍的Ⅱa类推荐。非持续性室性心动过速是肥厚型心肌病患者猝死的重要危险因素。对于先天性完全性心脏传导阻滞患者,心脏起搏器植入指征主要是Holter监测中是否存在长时间停搏、平均心率低下或出现复杂的室性异位节律。
尽管在儿科患者中的应用存在局限性,但AECG已成为节律评估的标准诊断工具。随着技术的改进、设备兼容性的提高且年幼患者也能轻松携带(如能连续监测的贴片式设备),这些设备的效用和诊断能力无疑将得到提高。
2 预测和危险分层的临床适应证
AECG检测的一过性心律失常、电生理信号波动或自主神经紊乱可用于危险分层,但其预测价值视临床情况而定。如果没有结构性心脏病和/或电活动性发生改变的心脏病,那么这些记录对预后的预测价值通常很小,甚至可以忽略不计。
2.1 缺血性心脏病和心梗后患者
长期以来,人们认为室性早搏(室早)和非持续性室性心动过速(室速)与急性心梗后患者风险增加有关。近年来,心肌梗死的护理性质变化很大,因此,更多的新分析方法适用于指导现代护理。对非ST段抬高型急性冠脉综合征(non-ST-segment ele-vation acute coronary syndrome,NSTE-ACS)患者而言,入院后最初48 h后发生非持续性室速(持续≥3个心搏, 频率≥100次/min)预示着死亡风险的增加。在雷诺嗪对NSTE-ACS患者中再发心血管事件影响(MERLIN-TIMI)的36项试验中,经过持续7 d 的心电监测,半数以上患者至少发作过一次非持续性室速。此外,非持续性室速发作的持续心搏不论长短(4~7个或≥8个心搏),均与心脏性猝死一年内风险增加2.3~2.8倍显著相关,尤其是与心肌缺血相关时,而与既往是否存在心肌梗死无关。入院48 h后发生短暂的非持续性室速与心脏性猝死一年内风险增加2.9~3.7倍显著相关,而入院后最初48 h内发生短暂的非持续性室速则没有类似的风险。在临床实践中,我们没有根据AECG的监测结果进行有效的治疗干预,因此可能限制了AECG的应用。
在急性心梗后患者住院晚期(>24 h),AECG检测到的非持续性室速发作与较高的持续性室速发生率及随后的死亡率升高有关;出院后,非持续性室速对心梗后患者预后的预测价值有限。对急性心梗幸存者进行非持续性室速检测,对随后的死亡率预测价值不大,而仅考虑心律失常事件时,其完全没有预后价值。虽然在24 h心电记录中存在非持续性室速是心肌梗死后自主神经张力及反射试验(ATRAMIT)不良预后的独立预测因子,并且使Holter监测用于危险分层的获益增大,但目前心梗后患者仍是接受再灌注和β受体阻滞剂治疗,非持续性室速可能无法作为长期死亡率的独立预测因子,尤其是考虑到LVEF等其他协变量时。鉴于上述原因,目前AECG并不常用。
心肌梗死患者出院后,左心室瘢痕的形成和重塑可能会产生适当的电生理基质,引发非持续性和持续性室性心律失常。尽管20世纪80年代和90年代初发表的心梗后患者的相关研究指出,对于左心室功能障碍的心肌梗死幸存者,频发室速和非持续性室速是其发生心律失常风险及心脏性猝死的强独立预测因子,然而在现代,非持续性室速的独立预测价值尚未得到确证。之所以会出现这种矛盾,是因为Holter记录时间差异很大,在不同患者群体中监测到的非持续性室速极具时间变异性。
另一方面,非持续性室速被证明是LVEF相对稳定(LVEF> 35%)的心梗后患者发生心脏性猝死的重要预测因子,独立于糖尿病、年龄和LVEF。在程序性心室刺激期间,非持续性室速伴持续性室速的诱发与心脏性猝死风险的增加相关。在多中心非持续性心动过速试验(MUSTT)开展后,随着电生理指导下ICD植入患者生存率的提高,AECG对LVEF在35%~40%的心梗后患者的非持续性室速检测能发挥一定的作用。
总之,在采用再灌注和β受体阻滞剂治疗的既往心梗患者中,如果考虑到其他协变量(如LVEF),那么非持续性室速就不是长期死亡率的独立预测因子。在针对缺血性心力衰竭患者的相关研究中,对于动态Holter记录中不规则心室活动的预测价值仍存在争议。然而,如果监测到长时程(>8个心搏)和快速(心率>120次/min)发作的非持续性室速,就有理由利用非侵入性甚至侵入性手段进一步探索心脏性猝死风险。在射血分数(EF)居于临界值(如35%~40%)的患者中,一旦检测到任何非持续性室速,临床医师就可能做进一步的危险分层,并确定是否要在电生理检查指导下植入ICD。
2.2 非缺血性扩张型心肌病
非缺血性扩张型心肌病(nonischemic dilated cardiomyopathy,NIDCM)可能是由多种原因引起的,包括病毒介导的自身免疫性疾病,以及中毒和代谢、遗传和心动过速等引起的多种病症。心动过速性心肌病可由房性心律失常引起,伴有快速和/或不规则的心室反应或频繁的室性异位节律。在这种情况下,AECG监测可用于评估心率或异位节律的频率及复杂性,以便做出诊断和/或确定侵入性治疗方法(如射频消融)的适应证。
NIDCM患者大多死于进展的心脏性猝死或心力衰竭。从理论上讲,AECG监测通过检测非持续性室速的发作和评估其他基于Holter的风险标记,可能有助于进行心脏性猝死的危险分层。然而,与缺血性心肌病患者的相关文献报道相反,AECG对NIDCM患者的预后价值相当低,且仍然存在争议。
据报道,NIDCM患者中非持续性室速的发生率从33%到79%不等。Iacoviello等研究发现,非持续性室速与随访期间心律失常事件发生风险增加3倍相关;结合低LVEF和异常QT间期变化这两项指标,非持续性室速的预后价值有所提高。在德国马尔堡心肌病研究中,单独评估的非持续性室速与心律失常事件风险的增加无关,但与低LVEF结合后,联合预测风险增加了8倍。一项荟萃分析显示,对于NIDCM合并LVEF降低的患者,非持续性室速是独立于LVEF的统计学上显著的心脏性猝死的预测因子。最近一项基于45项研究、囊括6000例以上患者的荟萃分析得出结论:单独评估的非持续性室速是心律失常性终点(定义为突发性或心律失常性死亡、心脏骤停、记录的ICD治疗及室速/室颤)的重要风险预测因子(OR=2.92,P<0.001)。非持续性室速的阴性预测值高达90%,然而,阳性预测值仅为20%。该研究总结了多种危险分层方法的预后价值,发现不良预后的最佳预测因子为T波电交替(T-wave alternans,TWA)、左心室舒张末期直径、电生理检查、信号平均心电图、LVEF、QRS间期和非持续性室速;而自主神经功能障碍的标志物(如压力反射敏感性)、心率变异性(heart rate variability,HRV)和心率震荡(heart rate turbulence,HRT)则没有统计学意义。总体而言,在NIDCM患者中,非持续性室速的危险分层作用不大,因此不支持在这类人群中常规使用非侵入性检测技术。
2.3 肥厚型心肌病
肥厚型心肌病(hypertrophic cardiomyopathy,HCM)的不良临床过程与心脏性猝死风险增加、进行性心力衰竭和房颤引起的并发症有关。HCM是年轻人,尤其是运动员发生心脏性猝死最常见的原因。
晕厥和心悸是HCM患者的主诉症状,最常被报道。晕厥事件可能由传导障碍、阵发性快心室率型房性心律失常、左室流出道梗阻或神经介导性事件,甚至是潜在的致命性室性心律失常引起。高达30%的HCM患者在Holter监测中出现非持续性室速,其发作频率与心肌纤维化程度有关。由于晕厥被认为是HCM患者心脏性猝死的危险因素,因此,应进行包括心电图、运动试验和AECG在内的仔细检查。2011年,美国心脏病学会基金会(ACCF)/美国心脏病协会/(AHA)发布的指南推荐24 h AECG监测,而2014年欧洲心脏病学会(ESC)指南建议在患者患病初期临床评估中,采用更长时程的48 h AECG监测,以检测房性及室性心律失常(推荐证据级别Ⅰb)。
在高达38%的HCM患者中观察到了阵发性室上性心律失常(包括房颤),并且患者对其耐受性差,导致晕厥发作或心力衰竭。根据ESC指南,HCM患者如果左心房直径≥45 mm(被认为是房颤和卒中的风险预测因子),即使没有症状,也应每6~12个月行48 h AECG检测房颤。
AECG监测是HCM患者心脏性猝死危险分层的重要组成部分,尤其是在较年轻的受试者中。然而,非持续性室速的特征是对心脏性猝死危险分层的阴性预测值高(95%)、阳性预测值低。最近发布的ESC指南建议根据HCM心脏性猝死风险公式估算5年猝死率。该“预后指数”将检测到的非持续性室速与心脏结构异常和心脏性猝死家族史、不明原因的晕厥和年龄相结合(推荐证据级别Ⅰb类)。在非持续性室速(定义为心率≥120 次/min,持续≥3个室早)的检测中,48 h AECG结合临床病史和超声心动图被认为是一线评估推荐。如果ICD植入前,在AECG上能观察到较长的非持续性室速片段,则预示着随访期间进行ICD治疗是恰当的。非持续性室速的严重程度指数(心率×时长/100>28)与ICD干预风险增加5倍以上相关。如果使用药物治疗室性心律失常,则可以重复开展AECG检测。
在随访期间,一旦出现任何提示心律失常的症状,应重复AECG监测,或是每隔1~2年常规监测一次,以评估非持续性室速发作的证据(Ⅱa类)或检测无症状房颤发作(Ⅱb类)。2014年的ESC指南建议在所有受试者中进行更长时间的记录(48 h),并对有窦性心律且左心房直径≥45 mm的患者进行更频繁的监测(每隔6~12个月)。
2.4 致心律失常性右室发育不良/心肌病
致心律失常性右室发育不良/心肌病(arrhythmogenic right ventricular dysplasia/cardiomyopathy,ARVD/C) 与发生心脏性猝死和/或进行性心力衰竭的风险相关。ARVD/C患者可能无症状,或是伴有心悸、头晕或晕厥,可能与频繁的心室异位节律或室性心动过速发作有关。重要的是,心脏性猝死可能是疾病的首发表现,特别是在年轻运动员中。
根据ARVC诊断标准(2010)专家共识,ARVD/C可基于多维评分系统进行诊断。心律失常的诊断和危险分层标准主要是存在呈左束支阻滞形态伴电轴左偏的非持续性或持续性室速;次要标准:① 呈右室流出道形态的非持续性或持续性室速;② 具有右偏或未知电轴的左束支阻滞;③ 室早负荷>500/24 h。因此,所有疑似ARVD/C患者在初步评估中,都应接受24 h AECG监测,且为了捕捉到心律失常,可考虑延长监测时间。我们注意到在ARVD/C患者中,室早负荷的日变化差异很大。然而,据Camm等报道,在近90%的病例中,24 h AECG足以记录到ARVC专家共识所要求的每24 h发作500次以上的室早;如果将监测时间延长至96 h,则被正确分层的患者比例可提高至95.5%。
AECG还能用于经ICD治疗的患者。非持续性室速或室早负荷>1000/24 h可预测适当的ICD放电,而后者则与ICD放电风险增加3倍以上有关。识别房性心律失常很重要,因为它可能预示着ICD治疗不恰当,且与ARVD/C患者的心脏移植风险较高和心脏性死亡率相关。
在评估ARVD患者的所有一级亲属时,应进行AECG监测。右心室起源的室速发作或室早负荷>200/24 h提示家族性受累。对于疑似ARVD/C的受试者应每隔多长时间重新做系列评估,目前尚未达成共识,但每年一次评估是合理的。在对ARVD/C患者亲属的一项为期4年的随访中,记录到的电信号异常,如心电图和/或AECG异常可能先于心脏结构性改变而发生。ARVC患者即使体表心电图正常,也可能在AECG检测中观察到复杂的室性心律失常。
2.5 预激综合征
AECG监测可能有助于评估预激综合征患者的旁路传导特性。如果前传不应期较短,则猝死风险与该旁路的快速传导有关,尤其是在房颤发作期间。在AECG连续记录期间,间歇性预激或伴有窦性心律加速的突然无预激提示“猝死风险较低”,例如,房颤发作时,预激的最短RR间期> 250 ms。AECG可能也有助于识别患有非持续性房颤的预激综合征患者。
2.6 遗传性原发性心律失常
心脏离子通道病是一组异质性遗传性疾病,如长/短QT综合征、Brugada综合征、儿茶酚胺敏感性多形性室速、早期复极综合征和特发性室颤,通常由编码离子通道或调节蛋白的基因突变所引起。该病的特征是患者无明显的结构性心脏病,且由室性快速性心律失常引起的猝死风险较高。体表心电图是诊断这些疾病和预测猝死风险的必要条件。离子通道病可表现为多种心电图表型,因此,AECG监测可用于评估提示疾病的瞬时电生理信号变化。然而,在遗传性原发性心律失常综合征患者中,AECG最重要的作用是心律失常检测和危险分层。值得注意的是,HRS/EHRA/APHRS有关遗传性原发性心律失常综合征的专家共识强调,应对离子通道病患者的晕厥发作起源进行详尽的评估。晕厥被认为是心脏性猝死的重要风险标志。
2.6.1 长QT综合征 长QT综合征(long QT syndrome,LQTS)是一种遗传性离子通道病,其特征包括QT间期延长,以及易发生晕厥、心脏骤停,或是与尖端扭转型多形性室速(可能恶化为室颤)相关的猝死。最近的修订版指南建议,LQTS的诊断应基于风险评分≥3分和/或重复多次心电图所提示的QTc间期≥480 ms,或病原性基因突变。风险评分的增加与QTc间期显著延长、尖端扭转型心律失常和晕厥相关。基于体表心电图可测量QT间期;然而,AECG可能揭示QT间期的短暂性延长和/或与不顺应心率的QT间期改变。复极异常通常与心率突变有关。在RR间期逐渐延长或缩短的情况下,QT间期在生理范围内与心率呈线性相关;然而,在RR间期突变的情况下,QT间期与心率没有线性相关性。据报道,在LQTS患者的室速发作前,RR间期可能呈“短-长”周期变化。AECG可能有助于提示T波异常、评估R-on-T现象、捕捉TWA的不良信号、检测非持续性或持续性室速(特别是尖端扭转型室速),以及识别QT间期本身的延长。除了QTc间期>500 ms的受试者,QTc间期<500 ms的患者也必须经常进行运动心电图检测和24 h Holter监测。在运动测试或Holter记录期间,心率<100次/min时QTc间期>500 ms可能提示LQTS,而QTc间期<500 ms则考虑是在生理范围内。QT间期对心率变化的不恰当的适应性改变,甚或是短暂的QT间期延长具有一定的临床价值。
是否需要通过AECG监测来确诊或帮助制定治疗策略(如ICD植入或药物剂量)仍未明确,但12导联心电图仍然是诊断的金标准。在随访期间,AECG可用于评估药物治疗的效果及其潜在的不良反应(如心动过缓)。关于无创性心电图的危险分层,可以考虑使用AECG来检测增加的QT间期变异性/离散度,这被认为是电活动不稳定性的标志,因此与心脏性猝死风险的升高相关。
2.6.2 短QT综合征 短QT综合征(short QT syndrome,SQTS)是心脏离子通道病,表现为QTc间期≤340 ms、QT间期持续缩短,且无结构性心脏病患者易发房颤和心脏性猝死。SQTS的临床表现差异很大,可能完全无症状,也可能以心脏性猝死为首发症状。在目前全球最大的SQTS患者数据库中,有晕厥史者占24%;以晕厥为首发症状者占14%;31%的患者出现心悸,且大多是由记录到的房颤或房扑引起的。对于SQTS患者而言,AECG可用于确定晕厥和心悸的原因,尤其是检测房颤的发作,但对诊断或指导预防性治疗几乎不起作用。
2.6.3 Brugada综合征 Brugada综合征是一种与原发性遗传性电活动相关的心脏病,其特征是右心前区心电图导联复极异常且易发生危及生命的室性心律失常。1型Brugada综合征的心电图诊断标准是J点抬高2 mm伴有ST段弓背向上型抬高,且V1、V2导联T波倒置,其自发性发作或由激发试验所诱发。Brugada综合征患者的心电图变化很大,可随时间的推移从1型转变到其他类型,甚或趋于正常化,反之亦可。因此,一些人认为12导联AECG可能有助于显示出Brugada综合征疑似患者的瞬时Brugada心电图波形。最近,Cerrato等以Brugada登记中的251例患者为研究对象,分析了其12导联24 h AECG记录显示为1型Brugada综合征的患病情况,其中30%为自发型,70%为药物诱发。他们发现,主要来自药物诱导组的患者中有20%可以检测到“自发”但间歇性出现的1型Brugada综合征的心电图改变。瞬时Brugada波形好发于下午时段(12:00—18:00)。研究人员建议,先应用12导联AECG监测对Brugada综合征进行筛查,以避免使用药物的风险。据报道,相较于重复做12导联心电图检查或常规放置电极的Holter检测,将V1、V2导联电极移至第三肋间隙的12导联Holter记录检测1型Brugada综合征的敏感性更高。此外,AECG可用于评估其他心律失常,或可能支持无症状性Brugada综合征诊断的心电图图形,如房颤、ST-T波电交替、自发性左束支阻滞和室早等。
挽救生命疗法即ICD植入术,适用于治疗Brugada综合征。然而,由于对有症状性患者难以确诊,因此当不明原因晕厥患者疑似有Brugada综合征时(如基于家族史或存在发热、特定药物等特征性触发因素),可以考虑延长AECG记录时间,并将导联作常规或特殊放置。
2.6.4 儿茶酚胺敏感性多形性室速 儿茶酚胺敏感性多形性室速(catecholaminergic polymorphic ventricular tachycardia,CPVT)是一种罕见却高度致命的遗传性离子通道病,其特征是无结构性心脏病的受试者在青春期早期,出现运动或情绪诱发的心悸和/或晕厥。CPVT患者发生心脏性猝死的风险与肾上腺素诱导的双向和多形性室速有关。由于静息体表心电图无法诊断疑似CPVT,因此应进一步开展心电评估和激发试验,可能包括AECG监测,以评估日常活动和情绪压力下是否发生室性快速性心律失常;最重要的是运动负荷测试,以评估室性心律失常与儿茶酚胺水平升高的关系。心室异位节律通常在心率达110~130 次/min时出现,且其数量和复杂性随着心率的加快而增大。肾上腺素引起的房性心律失常也很常见。
AECG可被推荐用于评价CPVT患者药物治疗的效果。2013年,HRS/EHRA/APHRS共同发布了《遗传性原发性心律失常综合征诊断治疗专家共识》,建议定期进行AECG监测和运动试验,以确定室性心律失常发作时的心率并评估抗心律失常治疗的效果,尽管Holter监测中出现无症状的室早并不意味着预后不良。
2.6.5 早期复极综合征 继Haïssaguerre等2008年首次报道以来,人们越来越关注早期复极的心电图模式,其多年来一直被认为是一种良性的心电图表现。多项研究报道,在特发性室速患者中经常观察到下壁和/或侧壁导联J点抬高。然而,在高达31%的一般人群中也可观察到这种心电图波形。根据2013年HRS/EHRA/APHRS专家共识,AECG监测可能有助于记录早期复极波形,特别是在室颤幸存者心动过缓发作期间,尽管绝大多数是通过标准心电图完成的。在植入ICD的电风暴患者中,曾报道过室性心律失常发作前J点抬高幅度增大的现象。
2.6.6 特发性室颤 特发性室颤是排除性诊断,定义为在已排除心脏、呼吸、代谢和毒理学病因的条件下的心脏骤停复苏,最好有室颤的心电图记录。对心脏骤停患者的详细分析应包括:个人及其家族病史、心电图(体表心电图、信号平均心电图和AECG)、排除结构性心脏病的影像学检查、激发试验、电生理试验、心室活检和基因检测。在评估特发性室颤患者的一级亲属时,建议进行Holter监测。
2.7 透析和慢性肾病
慢性肾病的患病率正在升高,目前在成年人中至少达15%。终末期肾病(end-stage renal disease,ESRD)的特点是死亡率极高(每年20%),其心血管死亡率比一般人群高100倍。心脏性猝死是透析患者中最常见的死亡原因。电解质和体液的波动(一种慢性炎症状态)、保持收缩功能,但左心室肥大伴舒张功能障碍、无症状心肌缺血,以及透析所致心肌顿抑引起的重复性心肌损伤是心脏性猝死发作的基础。
然而,透析期间ESRD患者无症状心律失常发生率的数据有限。在之前的24~48 h AECG研究中,关于透析期间和透析后心律失常负荷和心脏性猝死心电图标记的研究结果存在矛盾。Burton等研究表明,与透析后监测相比,透析期间监测到的室早和室速更常见,且与心肌顿抑有关。Holter在22%的透析患者中诊断出无症状心肌缺血,且其与透析期间和透析后发生室速或室颤高度相关。有趣的是,无症状心肌缺血与冠心病显著无关,并且它被认为是由微血管疾病和冠脉痉挛引起的。在AECG中,可观察到QRS电压的逐渐升高、心率的逐渐加快、T波振幅的减小,以及透析期间心律失常发作频率的升高。Green等报道,在透析期间微伏级的TWA现象增多,但在2.6年的随访期内未发现TWA与心血管结局有关。最近的研究揭示,透析期间血清血红蛋白水平的升高与室早发作频率有关,这可能解释了高血红蛋白水平对血液透析患者的不利影响。Poulikakos等指出,在透析过程中T波形态随心率作一致性变化,而QRS-T夹角的变化因人而异,且与甲状旁腺激素水平相关。
最近,Buiten等研究表明,透析过程本身与房颤的发展有关。接受腹膜透析的患者房颤发作明显较少。在血液透析疗程期间和透析过程中,房颤发作得更频繁。因此,透析期间进行AECG监测有助于早期诊断无症状房颤,从而可能完善包括抗凝治疗在内的房颤管理。
2.8 神经和肌肉疾病
AECG,尤其是HRV分析可用于研究自主神经系统紊乱。HRV的降低通常与交感神经张力升高或副交感神经活动减少有关。自主神经系统的激活可以促成各种心律失常的发生,包括缓慢性和快速性心律失常。已有研究揭示,癫痫与心律失常的发作密切相关。癫痫发作期间的记录提示,癫痫发作前的窦性心动过速很常见,同时也观察到心房和心室异位节律。然而,癫痫患者发生危及生命的心律失常和猝死并不常见,其发生率约2‰。激发心律失常的分子机制可能与癫痫的发病机制相同。
强直性肌营养不良是一种进行性遗传疾病,主要影响骨骼肌,但也会导致重要的心脏并发症,如已观察到的各种缓慢性心律失常,包括窦房结功能障碍、束支阻滞和完全性房室阻滞;患者还可能出现房颤和持续性室速。据报道,猝死是由心脏停搏和室颤引起的,并且一些患者可能因安装起搏器或ICD而获益。AECG可用于检测心律失常,从而指导起搏器、ICD等设备的安装及临床管理,但几乎没有公开数据来指导AECG在这种临床环境中的具体应用。
2.9 睡眠呼吸暂停
睡眠呼吸暂停综合征是一种常见的呼吸障碍,发病率约2%~4%,男性受累几乎是女性的两倍。这种情况与心血管疾病发病率及死亡率升高、心律失常、白天嗜睡、机动车事故和神经性认知功能障碍明确相关,但它的危害性却被严重低估了。
最近的研究表明,心律失常和传导障碍在睡眠呼吸暂停患者中很常见。各类心律失常的电学机制考虑为心脏结构和电学重构,而其主要源于自主神经功能失调、全身性和肺动脉高压、间歇性缺氧和炎症。
诊断睡眠呼吸暂停的基础是多导睡眠监测,监测期间可以检测到各种心律失常(如房室阻滞、窦性停搏、非持续性室速和阵发性房颤)。由于多导睡眠监测尚未普及且算法较麻烦,因此,在面向更大患病风险群体的筛查中,更简单和更廉价的诊断测试将更有优势。有人提议,Holter监护仪或许能填补这个角色。除了传统监测数据外,Holter记录还能提供其他信息,包括患者对睡眠时间的描述。一些商用监护系统带有呼吸暂停分析算法,要用到下述至少一种:① 窦性心律的呼吸相关变化,即受自主神经系统调节的窦性心律失常;② R波振幅变化,由胸壁呼吸运动所致心电图电极间距的微小偏移。这些技术还需进行更多的验证。
2.10 运动员及赛前筛查
对运动员的心律失常监测在某些方面与其他情况下的监测不同。对于运动员而言,疑似心律失常的症状很少是心脏性猝死的先兆,它可能提示其他潜在的严重但可治疗的疾病或心律失常。另一方面,当运动员存在可疑但良性的症状时,过度限制其从事一定强度的体育项目可能是毫无根据的。
对运动员应考虑采用逐步评估的方法。首先,了解所涉症状的病史特征及其是否与特定的竞争性或体力活动有关是很重要的。其次,要排除可能伴发或引发心律失常的重要的心血管疾病。
心电图等非侵入性检查可用于确定是否存在需要采取运动限制的潜在结构性病变。心电图上可能会显示明显的波形特征,指向某种特定的致心律失常基质。然而,对许多竞技运动员而言,运动本身就会引发症状和潜在的心律失常。此外,任何症状和/或心律失常可能不一定会再次出现。因此,对从事运动的患者、运动员,以及有症状、并发症及家族史的患者而言,AECG是评估患者的方法之一。
在下列情况下,对运动员进行AECG监测特别有用:① 已确诊的心血管疾病未对运动员造成限制;② 没有其他方法可确定诊断或症状的病因;③ 参加体育运动引起症状,可能有利于心律失常的诊断。AECG监测可用于初步诊断,或是作为监测工具以确定心律失常经治疗已消除。应考虑利用AECG 将症状(如晕厥、心悸)与心律失常关联起来。此外,在对无症状患者进行初步筛选时,AECG通过提示高密度或复杂心室异位节律,可能有助于量化室性心律失常负荷。非常频繁的心室异位节律可能提示存在基础心脏病。此外,一些已知的心脏疾病(如先天性主动脉瓣狭窄、低风险心肌病)和基线心电图异常(如房室阻滞、束支阻滞)或许能进一步使用AECG进行诊疗。
监测的类型取决于症状发生频率、严重程度、持续时间和症状发作时的情形,还取决于所参与的运动类型、需评估的心律失常及症状。没有哪种监测技术是最好的,监测技术的选择应基于个性化决策。
节律紊乱本身并不一定会引起症状,有些节律紊乱可伴有或不伴有症状发生。另一方面,患者可能有多种节律紊乱,记录到无症状的节律紊乱并不一定意味着高风险。
(参考文献略)
