聚醚醚酮表面多孔羟基化改性对MC3T3-E1细胞黏附、增殖的影响*
2019-09-09吴九平朴颖鑫于海驰张郡石禹刘钦毅
吴九平 朴颖鑫 于海驰 张郡 石禹 刘钦毅*
聚醚醚酮(polyetheretherketone,PEEK)是一种新型的半结晶性的芳香族高分子聚合物,其基本分子结构主要由羰基和醚基连接芳香环组成[1]。基于其耐高温、耐腐蚀、耐磨、耐疲劳、阻燃以及绝缘等优异性能,PEEK 材料已经在诸多领域(如医疗、航空航天、汽车、电子电气、能源、涂料等)获得了广泛的应用,是一种不可或缺的特种工程塑料[2-4]。在医疗领域,PEEK 材料物化性能稳定、弹性模量与人体骨骼相近、良好的射线可透过性和无毒性等特性促使其广泛应用于外伤、整形、口腔、脊柱及关节外科内植物等领域[5]。20 世纪90 年代末,PEEK 材料首次被美国食品药物监督管理局(FDA)批准应用于骨科内植物领域,其主要被设计成人工椎间盘、椎间融合器、创伤内固定器械及股骨柄假体等[1,6]。
相比于传统的金属及合金内固定材料,作为一种新型高分子材料的PEEK,在一定领域具有更加巨大的临床应用前景。然而,PEEK 材料表面的生物学惰性和高度疏水性,极大程度地限制了其在生物医学领域的广泛应用[7-8]。因此,对医用PEEK 材料进行表面改性,改善其材料表面生物学惰性和提高其材料表面的亲水性,成为目前PEEK 材料一个研究热点。近年来,许多表面改性方法(如等离子体处理、紫外辐照、激光处理以及湿化学法等)被尝试应用于PEEK 材料表面改性研究,并取得了一定的进展[9-11]。众所周知,植入物的生物相容性一般受表面形貌和化学性质两大因素影响[12-13]。因此,本研究拟应用浓硫酸腐蚀构建PEEK 表面多孔化结构和湿化学还原形成PEEK 羟基化表面两种改性方法,改善PEEK 材料表面生物学活性,并通过与MC3T3-E1 细胞共培养,探究此改性方法对细胞黏附和增殖的影响。
1 材料与方法
1.1 主要材料与仪器
PEEK 薄膜(Victrex,厚度100 m)购自英国ICI 公司;浓硫酸、丙酮、乙醇、甲醇、0.5M 盐酸、二甲基亚砜(DMSO)、硼氢化钠(NaBH4)(北京化工厂);DMEM 培养基、胎牛血清及胰蛋白酶(Gibco,美国);噻唑蓝(MTT)、异硫氰酸荧光素(FITC)(Sigma,美国);场发射扫描电子显微镜(SEM)(Philips,荷兰),真空型傅里叶变换红外光谱仪(FT-IR)(Bruker,德国),VCA2000 型水接触角测试仪(AST,美国)。
1.2 PEEK 材料表面多孔化处理
打孔器将PEEK 薄膜均匀地制作成直径为1 cm 的圆形薄片,将PEEK 圆片在超声清洗机中依次经丙酮、75%乙醇、蒸馏水各10 min,清洗3 遍,真空干燥箱中保存。随后,室温下,在超声清洗机中,将洁净的PEEK 圆片浸入98%浓硫酸中30 s,快速取出,再依次放入装有蒸馏水、甲醇、蒸馏水的烧杯中各5 min,于光滑的PEEK 薄片表面制备大量均匀的微孔结构。
1.3 PEEK 材料表面羟基化改性
参照既往文献[14],应用强还原剂NaBH4将PEEK 分子中稳定的羰基(—C=O—)还原成活性较高的羟基(—OH),实现PEEK 材料表面羟基化,具体步骤如下:100 mg NaBH4加入经真空蒸馏的50 mL DMSO 溶液中,密闭真空环境下,磁力搅拌器搅拌至充分溶解。再将洁净的PEEK 圆片和多孔化的PEEK 圆片分别加入上述溶液中,120℃、氩气保护下反应24 h。待自然冷却后,将PEEK 材料依次浸入装有甲醇、蒸馏水、0.5M 盐酸、蒸馏水、75%乙醇的烧杯中各10min,完成PEEK 材料表面羟基化改性。
1.4 改性后材料表面检测
1.4.1 SEM 检测
应用场发射扫描电子显微镜对所获取的样品进行扫描,获取样品表面微观形貌的变化,观察处理样品表面的多孔结构。
1.4.2 FT-IR 检测
应用真空型傅里叶变换红外光谱仪对所获取的样品进行反射红外光谱检测,获取样品表面化学基团的变化,验证PEEK 材料表面羟基化结果。
1.4.3 表面亲水性检测
应用静态水接触角测试仪检测PEEK材料表面改性前后材料表面亲水性能变化。
1.5 PEEK材料表面多孔羟基化改性对细胞黏附、增殖的影响
前成骨MC3T3-E1 细胞培养于混有63 mg/L 青霉素和100 mg/L 链霉素的高糖培养基(DMEM)中,每2 天换液1 次。材料样品分组分别为未处理PEEK 组、多孔化PEEK组、羟基化PEEK 组、多孔羟基化PEEK 组4 组,每组设立3 个平行样本。在24 孔培养板中,所有材料样本分别经75%乙醇(30 min)、3 次蒸馏水(3 遍,每遍10 min)进行消毒灭菌处理。随后,将样本置于加有1 mL DMEM 培养基的洁净24 孔培养板中,37℃、5%CO2环境下预处理12 h,之后以每孔2×104细胞数接种前成骨MC3T3-E1 细胞,进行共培养。培养6h,12 h 后,取出培养板,吸去培养基,10%磷酸缓冲液(PBS)洗涤3 遍,去除孔板中剩余培养基和未吸附细胞。再各孔中加入1 mL 多聚甲醛,37℃下固定15min,之后吸去多聚甲醛,10% PBS 洗涤3 遍;随之向各孔中分别加入500 L 10%PBS 和FITC 混合液(450∶50,v/v),37℃条件下孵育10 min,最后吸去混合液,10%PBS 洗涤3 遍,于荧光反射显微镜下观察细胞黏附情况。
上述相同方法培养和接种细胞,共培养1、3、7 d 后,每孔中加入100 L 5 mg/mL MTT 溶液,放回培养箱中继续孵育4 h,随后吸去培养基,每孔中加入400 L DMSO 溶液,反复吹打混匀,最后每孔取150 L 转移入96 孔细胞培养板,490 nm 波长下全自动酶标仪检测各孔吸光度值(A值),分析各组细胞增殖情况。
1.6 统计学方法
使用SPSS 18.0 统计学分析软件进行统计分析,计量资料均以均数±标准差表示,组间比较采用单因素方差分析处理,<0.05 为差异有统计学意义。
2 结果
2.1 SEM 检测
扫描电子显微镜(SEM)显示,未经处理的PEEK 薄片表面相对光滑,无明显的粗糙形貌;而浓硫酸处理后的PEEK薄片表面可见一层密集的空隙大小相对均匀的微孔结构,同时多孔化PEEK 材料再经NaBH4表面羟基化还原后,其表面多孔结构无明显改变。PEEK 表面多孔结构的形成将有利于提高材料表面的亲水性能,同时有助于细胞在其表面附着和伸展。见图1。

图1 PEEK 材料表面改性前后微观形貌(SEM):A、B.未经处理的PEEK 表面;C、D.表面多孔化的PEEK 表面;E、F.表面多孔羟基化的PEEK 表面
2.2 FT-IR 检测
傅里叶变换红外光谱仪显示,经表面羟基化改性后的PEEK 薄片在波长3 400 ~3 600 cm-1附近出现相对低平的波峰,证明NaBH4还原后的PEEK 表面形成了较多的羟基基团(—OH)。同时,与未经羟基化的PEEK 材料相比,羟基化处理后的PEEK 表面在波长1 700 cm-1处的波峰出现了一定程度的降低,说明PEEK 表面的羟基基团是由PEEK 结构中本有的羰基基团(—C=O—)还原而来的。此外,FTIR 检测结果还证明多孔化的表面改性未对PEEK 薄片的表面基团产生明显改变。见图2。

图2 PEEK 材料表面改性前后表面化学基团变化(FT-IR): A. 未经处理的PEEK 薄片;B.表面多孔化的PEEK 薄片;C.表面羟基化的PEEK 薄片;D.表面多孔羟基化的PEEK 薄片
2.3 表面亲水性检测
表面亲水性能检测结果显示,无论是表面多孔化改性还是表面羟基化改性均可有效提高PEEK 薄片的表面亲水性能,同时两种改性方法的结合将进一步改善PEEK 材料的表面亲水性。亲水性能的改善有助于提高材料的生物相容性,促进细胞的黏附与增殖。见图3。
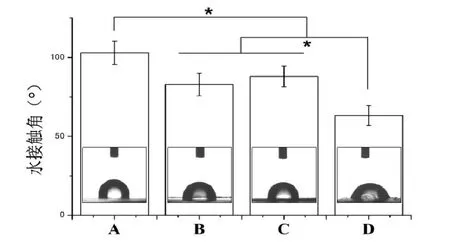
图3 PEEK材料表面改性前后表面亲水性测定:A.未经处理的PEEK薄片; B. 表面多孔化的PEEK 薄片; C. 表面羟基化的PEEK 薄片;D.表面多孔羟基化的PEEK 薄片;*表示<0.05
2.4 细胞黏附检测
不同处理的PEEK 薄片与MC3T3-E1 细胞共培养,分别接种6 h 和12 h 后行细胞蛋白FITC 染色,检测细胞黏附于材料表面情况。结果显示,无论是接种6 h 还是12 h,表面多孔化和羟基化改性均可有效促进细胞黏附,而在表面多孔羟基化改性的材料上,细胞黏附效果则更佳。同时,表面多孔化和羟基化改性也在一定程度上有利于黏附细胞的伸展。见图4。

图4 不同PEEK材料分组与MC3T3-E1共培养细胞黏附性能测定(FITC染色): A. 未经处理的PEEK 薄片组; B. 表面多孔化的PEEK 薄片组;C.表面羟基化的PEEK 薄片组;D.表面多孔羟基化的PEEK 薄片组
2.5 细胞增殖检测
不同处理的PEEK 薄片与MC3T3-E1 细胞分别共培养1、4、7 d 后,利用MTT 法检测细胞增殖情况。结果显示,共培养1 d 时,4 组细胞增殖情况未见明显差异;而共培养4 d 时,可发现多孔化、羟基化和多孔羟基化改性均可有效促进细胞增殖;共培养7 d 时,这种促进作用更加显著,两种改性方法的结合使促进细胞增殖效果更佳。见图5。

图5 不同PEEK 材料分组与MC3T3-E1 共培养细胞增殖性能测定(MTT 法):*表示<0.05
3 讨论
PEEK材料是一种性能非常优异的生物医学高分子材料,在医疗领域,特别是骨科内植物方面,具有广泛的应用。然而,由于PEEK 材料自身化学结构的过稳定性,导致其生物学惰性和疏水性严重,这一不足极大程度地限制了其在医学领域的进一步扩大应用[7-8]。通常来说,材料生物学应用程度的大小往往取决于与外界环境直接接触的表面界面的生物学性能[15]。因此,对PEEK 材料的表面改性研究,提高其表面的生物学性能,是促进PEEK 材料医学应用的重要步骤。近年来,许多学者应用不同表面改性方法对PEEK 材料进行表面改性研究,以提高其表面的生物学活性,并取得了一定的进展,但同时也存在一定程度的缺陷和不足,例如绑定不牢固、方法不稳定、操作过程复杂、反应条件苛刻、其自身优良性能损害、实用性不高等[16]。因此,探究一种相对简单、实用性高且可重复性强的基础改性方法,作为PEEK材料表面深入改性的研究基础,具有重要意义。
本研究结合两种相对简单稳定且可重复性高的表面改性方法对PEEK 材料进行表面改性,提高其表面的生物相容性和亲水性,促进早期细胞黏附和增殖等生物学行为。本研究将为PEEK 材料表面进一步接枝不同化学基团以及生物因子,以实现不同目的的功能化改性提供共同的探索基础,具有重要的扩展研究价值。首先,笔者利用浓硫酸的腐蚀作用在光滑的PEEK 材料表面,构建大量微孔结构。通常认为,表面腐蚀增加材料表面的粗糙度和表面积,可使材料表面具有更高的表面自由能和润湿性,有利于提高材料的表面生物活性[17]。SEM 结果可清晰显示该微孔结构是一种分布均匀、空隙适度的粗糙结构,该形貌将有助于生物细胞在其表面黏附、攀爬和扩增,后期体外细胞实验也证明这一结果。再次,笔者应用强还原剂NaBH4在多孔化的PEEK 表面将稳定的羰基还原成活性较高的羟基,并通过红外光谱证实PEEK表面羟基来源于羰基的还原。在PEEK 表面制备大量活性较高的羟基,将为下一步尝试利用羟基基团共价枝接活性化学物质或生物因子奠定基础,实现促成骨、促成纤维、促成血管等功能化定向改性,提供充足的延展研究空间。许多学者利用PEEK表面化学基团的改变共价枝接不同的化学基团和生物因子如类骨磷灰石、GRGD 等,改善PEEK 表面性征和生物学活性,并取得了一定的进展[18-19]。笔者利用PEEK材料与MC3T3-E1 细胞共培养体外实验也证实了这种羟基化改性有助于细胞早期的黏附和增殖。此外,表面亲水性能是影响材料生物相容性的重要因素之一,笔者利用材料表面亲水性检测证实了这两种改性方法均可有效改善PEEK材料的疏水缺陷,提高PEEK 材料的亲水性能。
PEEK 材料表面多孔羟基化改性方法是一种简单、有效的表面改性方法,能有效改善PEEK 表面生物学惰性和提高其表面亲水性能,并显著促进细胞黏附和增殖。在未来的扩展研究中,我们可以此为基础,进一步探索更高效、更有价值的不同功能定向PEEK 材料表面改性。
