精氨酸修饰磁性海泡石对Pb2+的吸附研究
2019-09-04潘婷戴文灿朱翼洋关智杰肖洪涛
潘婷,戴文灿,朱翼洋,关智杰,肖洪涛
(广东工业大学 环境科学与工程学院,广东 广州 510006)
近年,铅的大量使用以及含铅废水的大量排放对生态环境造成严重危害。化学沉淀法[1]、电化学还原法[2]、离子交换法[3]和吸附法[4]等常作为含铅废水的处理方法。吸附法简单易行,吸附材料价格低廉,已成为研究热点[5]。
天然海泡石实际比表面积较小[6],且其粉末状分离回收性能差[7],故需要对其改性来提高吸附性能。磁性Fe3O4既可负载在海泡石表面,又可与氨基酸类有效结合,引入氨基[8],实现对重金属的有效捕集。故通过对海泡石磁改性和L-精氨酸修饰得到一种既有良好固液分离效果又有功能基团氨基的磁性-有机复合改性海泡石(L-Arg-MSEP)。探讨L-Arg-MSEP对Pb2+的吸附性能,并研究其吸附动力学和吸附热力学。
1 实验部分
1.1 材料与仪器
海泡石原粉(SEP,粒度200目),购于河北灵寿县丰丰矿产加工厂。其主要成分见表1;L-精氨酸,分析纯;无水乙醇、三氯化铁、氯化亚铁、氨水均为化学纯。
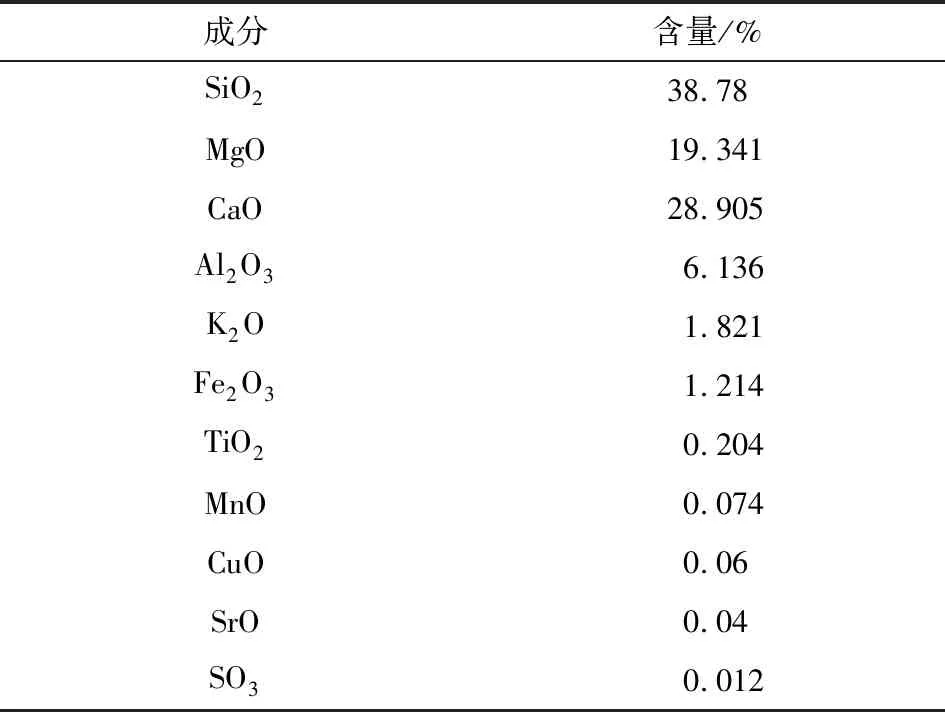
表1 海泡石主要成分Table 1 Main component of sepiolite
Z-2000型原子吸收仪器;HH-1型数显恒温水浴锅;PHS-25型pH计;DZF-6050型真空干燥箱;ZD-85A型数显气浴恒温振荡器;PW3040/60型X射线粉末衍射仪;PPMS-9型综合物性测量系统;ASAP 2020 PLUS HB88比表面积与孔径测定仪;Nicolet380傅里叶变换红外光谱仪。
1.2 L-Arg-MSEP的制备与表征
1.2.1L-Arg-MSEP的制备 将天然海泡石通过自然沉降法进行提纯,烘干,研磨至200目,取筛下物备用,记作SEP。
制备过程为:称取1.988 g FeCl2·4H2O和4.730 g FeCl3·6H2O配制成总铁浓度为0.3 mol/L的混合溶液100 mL。将10 g海泡石加入混合溶液中,在通氮气、60 ℃恒温搅拌的条件下,逐滴加浓氨水至混合液的pH值约为10.0;然后升温至85 ℃,继续搅拌1 h,调节溶液pH为7.0后加入4.791 g/L精氨酸继续反应30 min,产物经磁分离、去离子水洗涤至pH恒定为7,60 ℃真空干燥过200目筛,制得了L-精氨酸修饰的磁性海泡石材料,记为L-Arg-MSEP。其改性工艺流程示意图见图1。
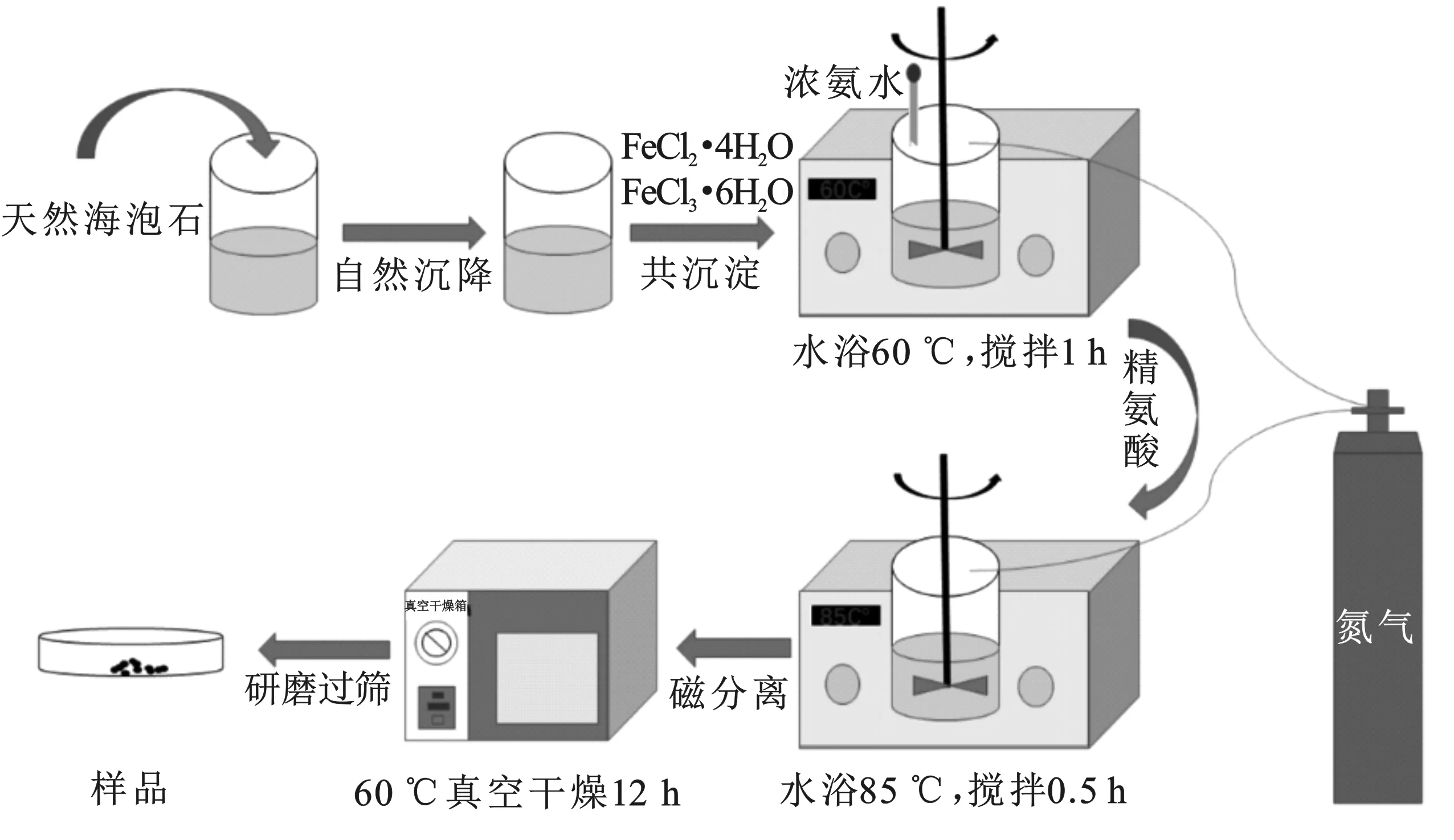
图1 海泡石的改性工艺流程示意图Fig.1 Schematic diagram of the modification process of sepiolite
1.2.2L-Arg-MSEP的表征 采用VSM测定材料的室温磁滞回线,系统磁场强度:纵向磁体:±9 T,扫描速度为1~200 Gauss/s,磁场分辨率为0.02 mT;SEM观察吸附材料的表面形貌;XRD鉴别材料的晶型结构变化;X-射线管选用铜靶,管压为60 kV;管流为55 mA,扫描范围2θ为5~70°;采用KBr压片法,红外光谱分析改性前后材料的官能团变化,分辨率为4 cm-1,扫描波数范围为4 000~400 cm-1;采用BET对材料的比表面积进行分析,测试条件为:氦气作为载气,在393 K下脱气12 h,分别用N2吸附法、t-plot方法和BJH方法测定吸附剂的比表面积、外表面积和微孔体积以及计算平均孔径。
1.3 吸附实验
将Pb2+作为吸附试验的靶向污染物,含Pb2+模拟溶液由适量试剂Pb2(NO)3和去离子水配成。分别称取SEP、L-Arg-MSEP各0.05 g,放在100 mL锥形瓶中,分别与25 mL浓度为200 mg/L的Pb2+溶液混合,调节pH值至5.0,在30 ℃的条件下恒温振荡12 h。反应完毕,磁分离,取上清液并用Z-2000型原子吸收仪器测定溶液中Pb2+的浓度。在其余吸附条件相同情况下,分别测定在不同含铅废水的初始pH值(1.0~6.0)、吸附剂投加量(1~10 g/L)、吸附时间(10~180 min)、Pb2+初始浓度(70~550 mg/L)以及吸附温度(293~323 K)下溶液中Pb2+的残余浓度。通过公式(1)、(2)得到吸附量q(mg/g)和去除率R。
(1)
(2)
式中C0和C——分别为溶液中铅离子的初始浓度和平衡浓度,mg/L;
V——重金属溶液的体积,mL;
m——黏土矿物的投加量,g。
2 结果与讨论
2.1 材料的表征
2.1.1 微区扫描电镜分析(SEM) 图2a与图2b为海泡石(SEP)和复合改性海泡石(L-Arg-MSEP)的扫描电镜图。


图2 SEP(a)和L-Arg-MSEP(b)的扫描电镜图Fig.2 SEM images of the natural SEP(a) and L-Arg-MSEP(b)
对比图2a与图2b可知,SEP呈纤维束状的聚合体,表面光滑,覆盖了部分滑石、方解石等片状杂质,影响了它对水中Pb2+的吸附能力[9];L-Arg-MSEP表面粗糙,纤维束表面附着了许多Fe3O4颗粒,颗粒呈球状且粒径较小,只有少部分Fe3O4颗粒相互聚集。这是因为氨基酸对其的表面修饰,减轻了Fe3O4颗粒之间的团聚现象。由于负载的Fe3O4颗粒具有较小的粒径和孔隙使得其比表面积增加,改善了海泡石表面性质,使得该复合材料更易与水中的Pb2+相结合,有利于溶液中重金属Pb2+的吸附去除。这与下文的BET表征结果相一致。
2.1.2 X射线衍射分析(XRD)及红外光谱分析(FTIR) SEP和L-Arg-MSEP的X射线衍射图见图3。
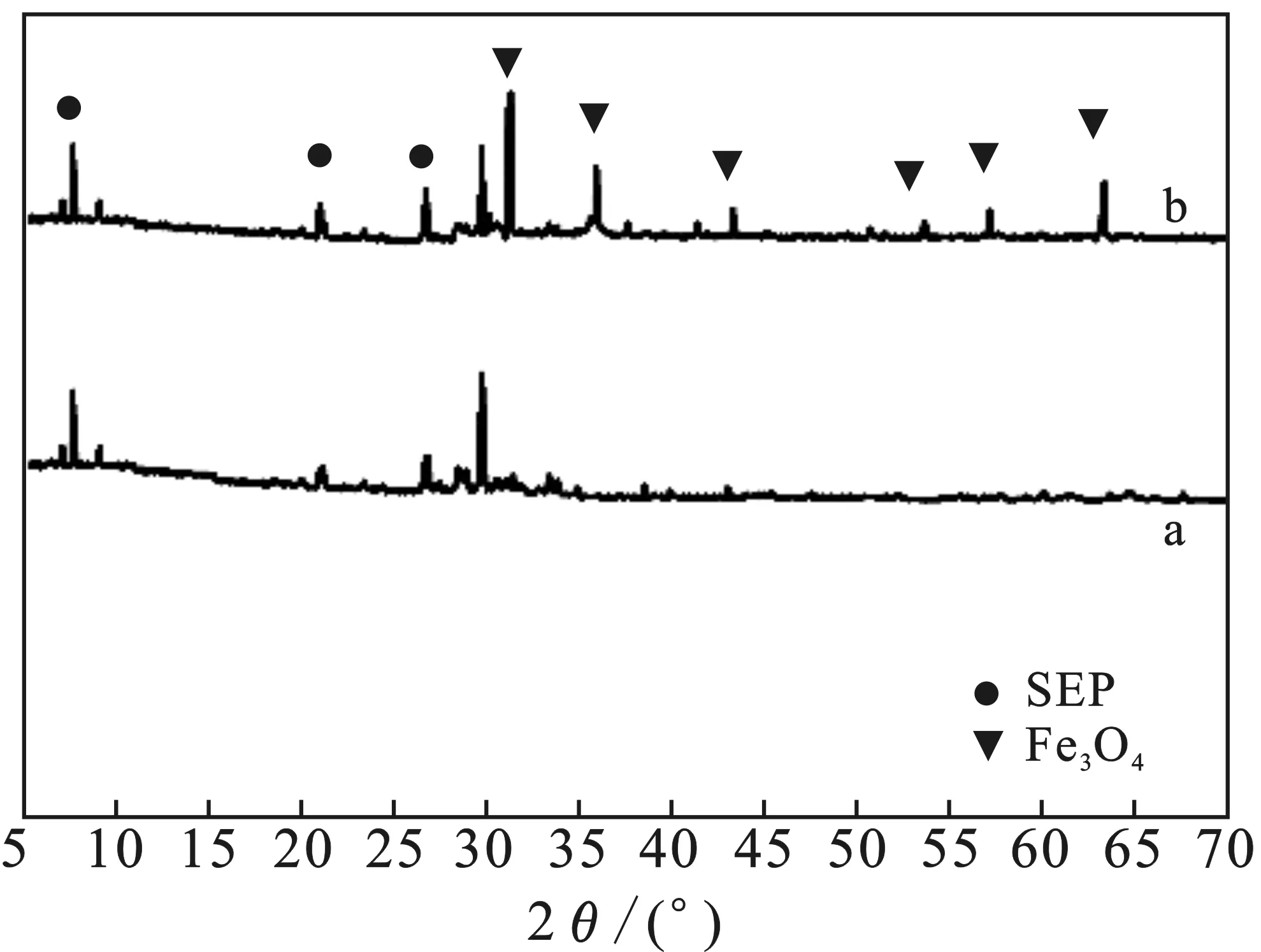
图3 SEP(a)和L-Arg-MSEP(b)的X射线衍射分析Fig.3 XRD spectra of sepiolite and modified sepiolite
由图3可知,两种材料均在2θ约为7.3,20.53,26.70°时出现海泡石的特征衍射峰,改性前后的特征衍射峰处的2θ角度基本不变,根据布拉格方程2dsinθ=nλ,改性后的海泡石层间距基本没有变化。改性后的海泡石在2θ为30.09,35.68,43.10,53.44,56.95,62.39°处新增的6个特征峰为Fe3O4的特征衍射峰[10],表明Fe3O4已成功负载于海泡石上。结合扫描电镜表征结果,海泡石经复合改性后,海泡石的主体结构没有被破坏,且经精氨酸修饰的Fe3O4附着于海泡石表面。
图4中a、b分别为海泡石与复合改性海泡石的红外光谱图。

图4 SEP(a)和L-Arg-MSEP(b)的红外光谱分析Fig.4 FTIR spectra of sepiolite and modified sepiolite
由图4可知,两种材料均在高频区3 345,3 671 cm-1处出现海泡石层间 —OH的伸缩振动、Si—OH基团中O—H的拉伸振动吸收峰[11]、1 027 cm-1处的Si—O—Si的反对称伸缩振动吸收峰[12],以及低频区447,669 cm-1处的Si—O的弯曲振动和八面体Mg—O伸缩的振动吸收峰[13],这些红外特征峰都与海泡石的结构特性有关,表明复合改性海泡石的基础骨架结构仍存在。改性后海泡石在3 345 cm-1和1 621 cm-1处的新增峰是由于L-Arg分子中N—H键和C—CH2键伸缩振动产生的[14];586 cm-1处的峰是Fe—O键[15]的振动,说明有Fe3O4的存在。这表明L-Arg成功负载在海泡石的Fe3O4表面。
2.1.3 磁性能分析(VSM)L-Arg-MSEP和实验室分析纯Fe3O4的室温磁滞回线见图5。

图5 Fe3O4和L-Arg-MSEP的室温磁滞回线Fig.5 Hysteresis loops of L-Arg-MSEP and Fe3O4
由图5可知,在磁化过程中Fe3O4及L-Arg-MSEP的磁化率均随磁场强度的增大而急剧增强,而后趋于饱和;当磁场强度逐渐趋于零时,Fe3O4及L-Arg-MSEP的磁化率随之急剧趋于零;当反向施加磁场,其磁化率也随之反向达到饱和状态。Fe3O4及L-Arg-MSEP的磁滞回线大致为一重合的S型曲线,说明具有良好的超顺磁性。由磁化曲线计算可得,L-Arg-MSEP和Fe3O4的饱和磁化率分别为15.53 emu/g 和70.51 emu/g,表明制备的L-Arg-MSEP可通过设置一个外加磁场将其与作用体系分离。
2.1.4 表面积与孔结构分析(BET) SEP和L-Arg-MSEP的N2吸附-脱附曲线和孔径分布图见图6。
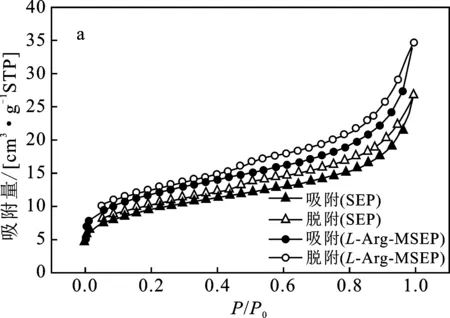
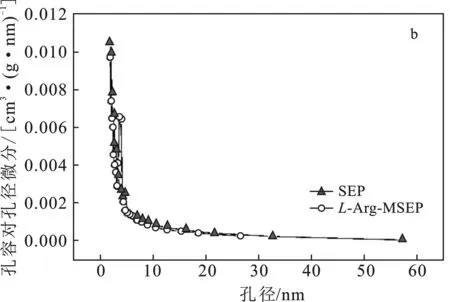
图6 SEP和L-Arg-MSEP的吸附-脱附 曲线(a)和孔径分布(b)Fig.6 N2 adsorption-desorption curves(a) and pore size distribution(b) of SEP and APTES-SEP
由图6a可知,SEP和L-Arg-MSEP的吸附-脱附曲线在低P/P0区曲线凸向上,与Ⅱ型等温线类似;在较高P/P0区,吸附质发生毛细管凝聚,等温线迅速上升,故属于IV型等温线。由图6b可知,在0~60 nm 孔径区域内,SEP和L-Arg-MSEP均有分布,但孔径分布在2 nm左右的区域居多,说明两种材料分布广泛但不均匀。由表2数据可知,经L-精氨酸修饰后的磁性海泡石微孔体积增大,平均孔径增大,微孔孔容由改性前的0.003 4 cm3/g增至0.004 6 cm3/g,平均孔径由原始海泡石的3.79 nm增至3.92 nm。利用BET法计算所得SEP和L-Arg-MSEP的比表面积分别为32.87 m2/g和40.46 m2/g。结合电镜分析,复合改性海泡石的比表面积略有增大,这很可能是因为Fe3O4成功负载于海泡石上。

表2 SEP与L-Arg-MSEP的比表面与孔结构特性Table 2 Structure information of SEP and L-Arg-MSEP
2.2 吸附实验结果
2.2.1 含铅废水初始pH及吸附剂投加量对吸附的影响 改性前后海泡石对Pb2+吸附量随pH变化的情况见图7。在其他吸附条件不变情况下,将溶液的初始pH值作为唯一变量,探讨初始pH值对吸附过程的影响。实验过程pH取值最高为6.0,因为氢氧化铅沉淀在溶液pH值高于6时形成。

图7 pH对吸附性能的影响Fig.7 Effect of pH on adsorption capacity
由图7可知,在相同pH条件下,L-Arg-MSEP对Pb2+的吸附量远大于SEP对其的吸附量。原因在于SEP的吸附作用主要是离子交换和表面络合吸附作用的结果,而L-Arg-MSEP的吸附作用除了海泡石本身的吸附作用外,是以海泡石表面功能团氨基的配位吸附作用为主,氨基的配位吸附强度远高于海泡石自身吸附作用力。在pH为1.0~6.0范围内随着pH值的增加,SEP和L-Arg-MSEP的吸附能力增强。当pH在1.0~5.0时,上升较快,吸附量变化大;当pH在5.0~6.0时,上升速率缓慢,吸附量变化甚微。这是因为,在低pH值时,溶液中的H+含量相对较高,溶液中大量的H+与Pb2+彼此竞争吸附,部分与Pb2+结合的吸附位点被H+占据,同时SEP和L-Arg-MSEP表面的氨基质子化,因此吸附剂对Pb2+的吸附量偏低;溶液pH不断增加,H+浓度相对减小,一方面H+与Pb2+竞争吸附减弱,另一方面其氨基质子化程度减弱,因而吸附量随着pH值的增加而增加,而后达到饱和,趋于稳定。故体系环境pH=5为最佳。
改性前后海泡石对Pb2+吸附率随吸附剂量变化的情况见图8。

图8 吸附剂投加量对吸附的影响Fig.8 Effect of adsorbent dosages on adsorption capacities
由图8可知,SEP和L-Arg-MSEP对Pb2+的吸附率随着吸附剂用量的增加而增大。在同一吸附剂投加量下,L-Arg-MSEP对Pb2+的吸附率显著大于SEP;当吸附剂投加量为1~2 g/L时,随着吸附剂量增加,吸附率迅速增加;当吸附剂投加量超过2 g/L时,吸附率趋于平衡。原因在于Pb2+浓度一定时,随着投加量的增加,吸附剂表面的吸附位点由最大不饱和状态逐渐过渡为向饱和状态,并趋于平衡,继续增加吸附剂投加量无法进一步提高其吸附率,反而增加投入成本。故认为最佳吸附剂量为2 g/L。
2.2.2 时间对吸附的影响及吸附动力学 SEP和L-Arg-MSEP对Pb2+的吸附量随吸附时间变化的情况见图9。
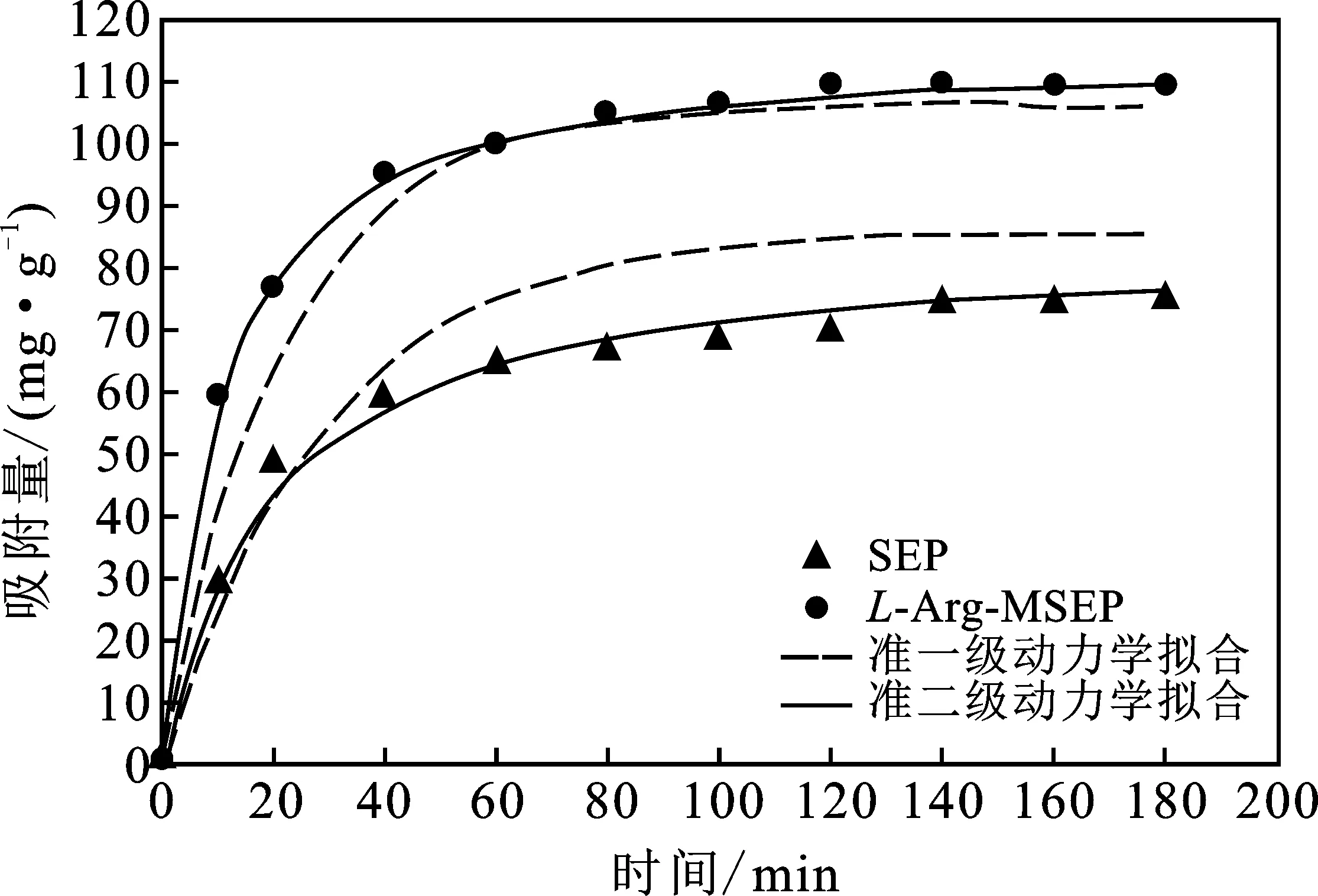
图9 反应时间对Pb2+吸附的影响及吸附动力学Fig.9 Effect of contact time and adsorption kinetic of Pb2+ adsorption on SEP and L-Arg-MSEP
由图9可知,L-Arg-MSEP和SEP对Pb2+的吸附量均随吸附时间的增加而提高,但L-Arg-MSEP对Pb2+的吸附能力显然优于SEP。当反应时间在30 min 内,吸附量迅速增加,吸附速率最快,为高效快速阶段;当反应时间在30~60 min内,吸附量持续增加,但吸附速率略有减缓,为慢速平衡反应;当反应时间在60 min以后,吸附量增加缓慢,无明显变化,逐渐达到平衡阶段。
为进一步探究Pb2+在SEP和L-Arg-MSEP上的吸附平衡规律,实验数据带入准一级和准二级动力学方程拟合,结果见表3。
由表3可知,L-Arg-MSEP的k值高于SEP,说明改性后海泡石的吸附速率明显高于原始海泡石;SEP和L-Arg-MSEP的准二级动力学方程的吸附数据拟合相关系数R2均高于准一级动力学方程,且准二级动力学方程拟合的理论最大吸附量与准一级动力学方程拟合结果相比,准二级方程拟合结果与实验实际饱和吸附量更相近,表明准二级动力学方程更能准确描述对SEP和L-Arg-MSEP对Pb2+的吸附过程。
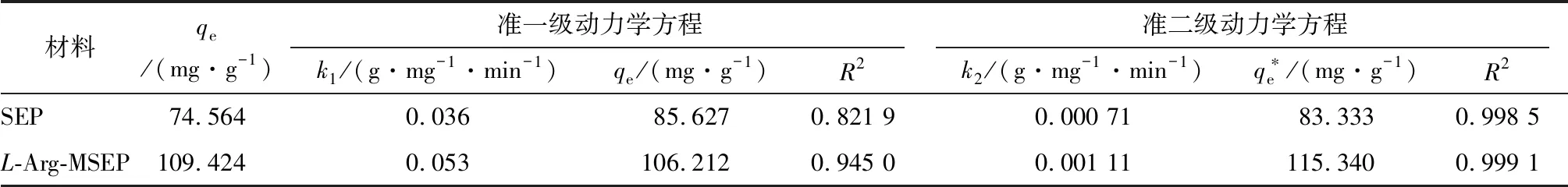
表3 吸附动力学拟合方程Table 3 Parameters of adsorption kinetics of Pb2+ on SEP and L-Arg-MSEP
2.2.3 初始浓度对吸附的影响及等温吸附线 通过设置不同的Pb2+初始浓度(70,130,180,240,260,390,440,550 mg/L)来探究SEP和L-Arg-MSEP对Pb2+吸附容量,Langmuir和Freundlich等温吸附模型的拟合结果见图10。
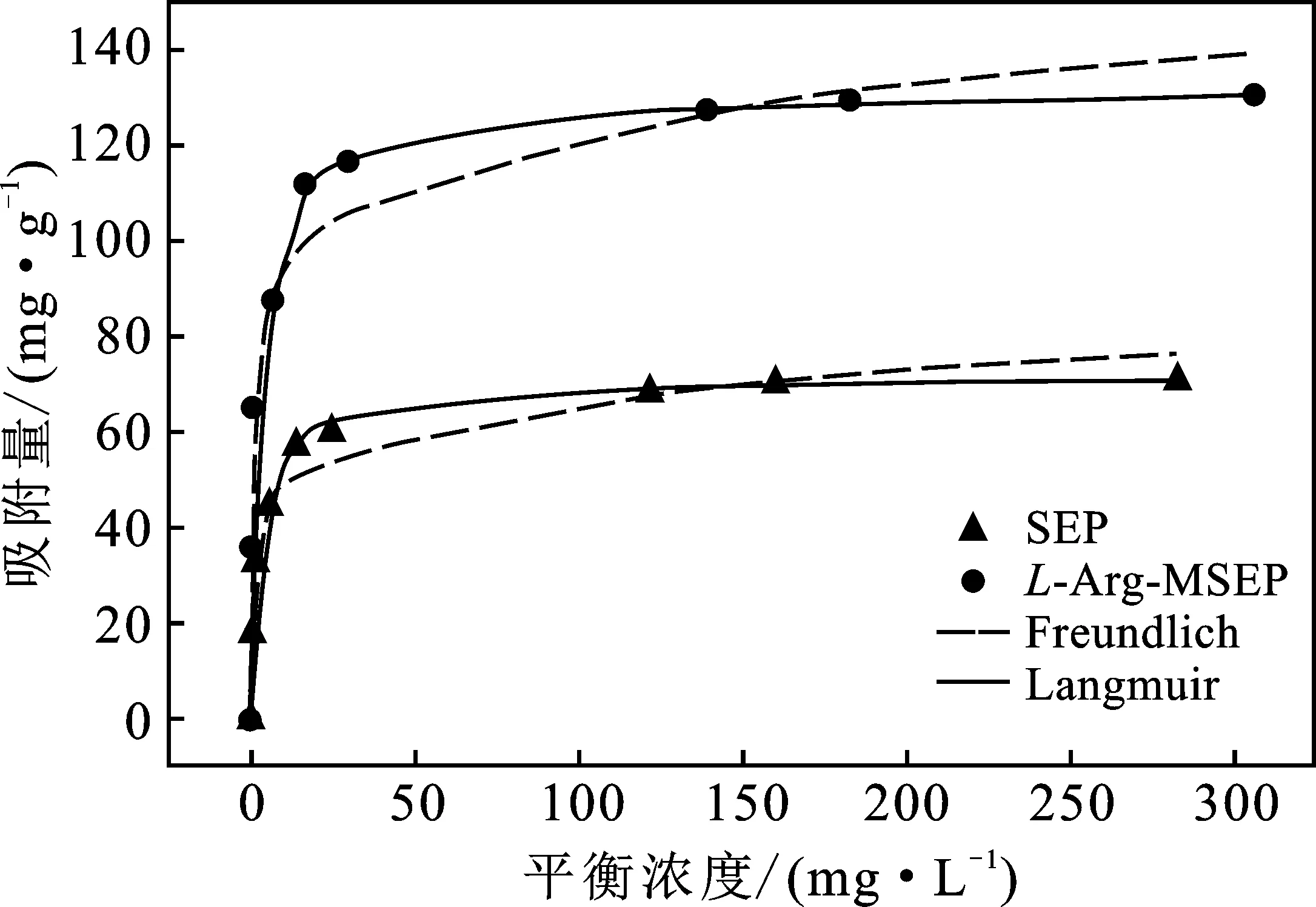
图10 Pb2+的吸附及等温吸附模型拟合图Fig.10 Adsorption isotherms of Pb2+ sepiolite and modified sepiolite
由图10可知,当初始浓度为80~240 mg/L时,随着Pb2+初始浓度的不断增加,SEP和L-Arg-MSEP对Pb2+的吸附量均快速增加;当初始浓度为240~550 mg/L时,SEP和L-Arg-MSEP对Pb2+的吸附量均有所增加,但增加速率缓慢,最后趋于平衡。这是由于初始浓度偏低时,吸附剂表面的吸附位点处于未饱和状态,Pb2+吸附量迅速增加;当Pb2+浓度逐渐增大时,吸附剂表面的吸附位点也随之到达饱和状态,吸附容量不再随着初始浓度的增大而增大。
两种等温吸附模型的拟合数据见表4。

表4 等温吸附模型拟合参数Table 4 Equilibrium isotherm model parameters for Pb2+ adsorption on SEP and L-Arg-MSEP
由表4可知,SEP和L-Arg-MSEP的Langmuir模型拟合相关系数R2分别为0.999 5和0.999 8,均比Freundlich模型拟合效果好,这表明Pb2+在SEP和L-Arg-MSEP上的吸附过程为单层吸附。经过复合改性后的海泡石最大吸附量由原始的71.261 mg/g 增至130.593 mg/g。结合上文的表征结果可知,复合改性后海泡石的比表面积变大,为Pb2+提供了更多的吸附位点。另外,天然海泡石经过复合改性后表面附带有效功能基团氨基,与溶液中的Pb2+形成配位吸附模式,增大了海泡石对Pb2+的吸附量。
2.2.4 吸附热力学行为 图11为SEP和L-Arg-MSEP吸附Pb2+的热力学拟合图。表5为热力学公式求得的热力学参数。
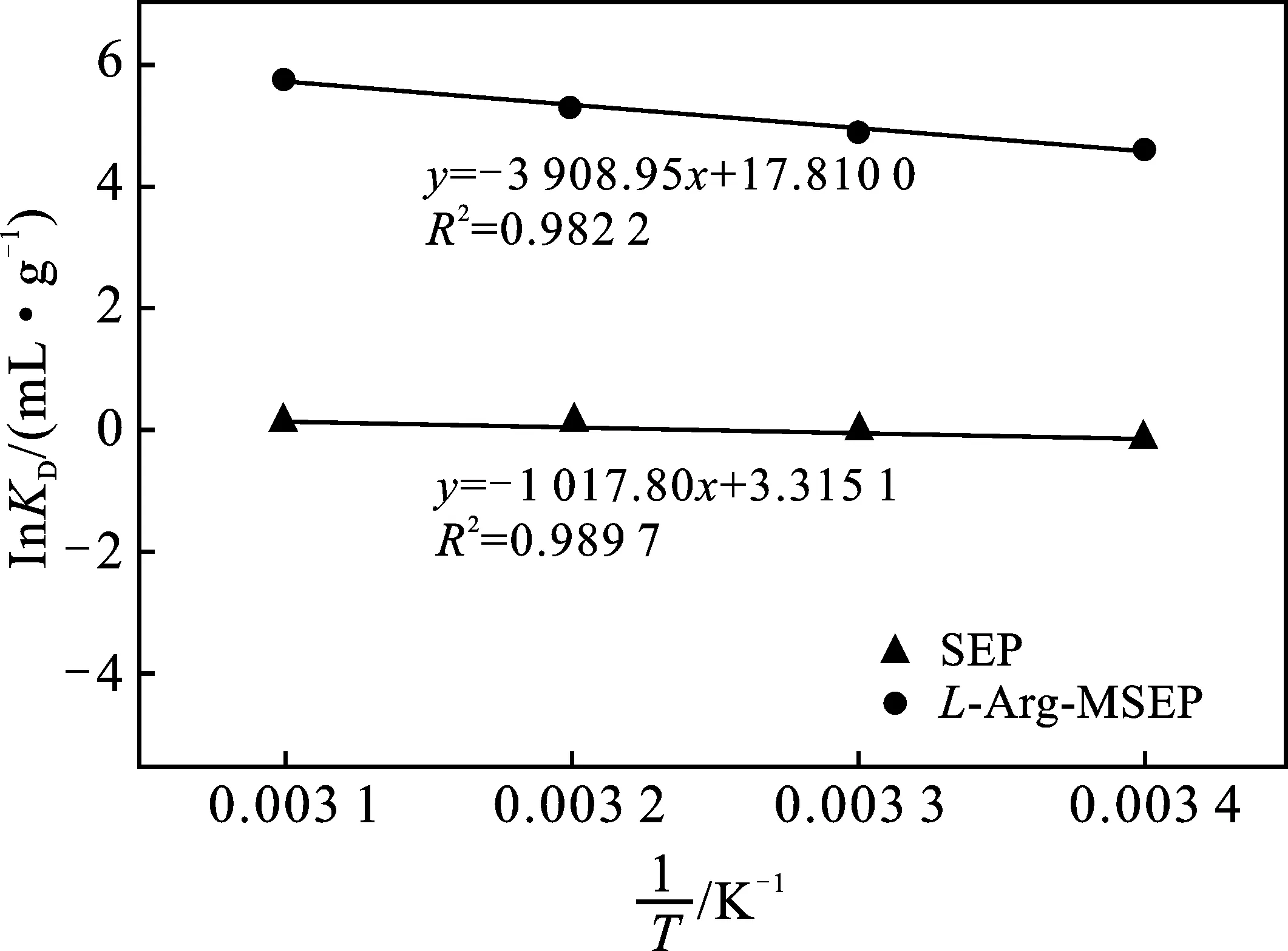
图11 SEP和L-Arg-MSEP吸附Pb2+热力学拟合Fig.11 Thermodynamic fitting of SEP and L-Arg-MSEP adsorbed Pb2+

表5 SEP和APTES-SEP吸附Pb2+热力学参数Table 5 Thermodynamic parameters of Pb2+ adsorbed by SEP and L-Arg-MSEP
由表5可知,两种吸附剂在对Pb2+吸附过程中,焓变(ΔH<0),熵变(ΔS>0),吉布斯自由能(ΔG<0)。对于固-液吸附体系来说,ΔH<0,说明吸附过程为放热过程,增加体系温度,吸附在吸附剂表面的Pb2+易从表面逃逸;ΔG<0,说明吸附剂吸附过程为自发进行的,L-Arg-MSEP吸附过程的ΔG绝对值比SEP高,说明L-Arg-MSEP的自发程度更高,改性提高了海泡石的吸附效果;系统体系的混乱程度由熵(S)值决定,熵(S)值与反应体系混乱程度呈正相关,而L-Arg-MSEP吸附Pb2+过程的ΔS比SEP大,说明复合改性后吸附剂在固-液体系混乱程度更高,对Pb2+的亲和力增强,吸附性能更好,这也与实际实验数据相一致。
3 结论
(1)与原始海泡石(SEP)相比,经过精氨酸表面修饰的磁性的海泡石(L-Arg-MSEP),比表面积增大,孔容与孔径增大,饱和磁化率为15.53 emu/g,可在外加磁场的作用下固液分离,同时引入的功能基团氨基与Pb2+进行配位吸附作用,提高了L-Arg-MSEP对Pb2+的吸附性能。
(2)在30 ℃,溶液pH=5.0,Pb2+的初始浓度200 mg/L,吸附剂投加量2 g/L的实验条件下,L-Arg-MSEP对Pb2+的最大吸附量达到130.593 mg/g。
(3)SEP与L-Arg-MSEP对Pb2+的吸附过程可以很好的通过准二级动力学和Langmuir等温吸附模型进行解释,且L-Arg-MSEP的最大理论吸附量和吸附速率都大于SEP。吸附热力学中的ΔG、ΔH均为负,说明L-Arg-MSEP对Pb2+的吸附是自发的放热过程。
