多参数磁共振成像在脑胶质瘤中的应用研究
2019-08-30许超,俞茜,王鸿
许 超,俞 茜,王 鸿
(1.延安大学附属医院放射科,陕西 延安 716000;2.西安市高新医院放射科,陕西 西安 710075)
脑胶质瘤是一种常见原发性颅脑肿瘤,是大脑、脊髓中胶质细胞发生癌变导致,由先天遗传高危因素及后天外界致癌因素共用作用引起[1]。脑胶质瘤按照肿瘤细胞形态可分为星型细胞瘤、少枝细胞瘤、混合胶质瘤及室管膜瘤,按照肿瘤恶性程度分为低级别胶质瘤及高级别胶质瘤,按照肿瘤位置分为幕上胶质瘤、幕下胶质瘤及桥脑胶质瘤[2]。脑胶质瘤临床病症与其肿瘤占位效应及影响的脑部功能有关,通常会造成患者头痛、癫痫、视线模糊等[3]。不同级别胶质瘤引起病症速度也有所不同,低级别胶质瘤患者病史可长达几年,高级别胶质瘤患者则几个月内即出现明显临床症状。由于不同级别脑胶质瘤治疗方案不同,因此术前准确分级十分关键[4]。磁共振成像(MRI)是常用影像学检测手段[5],随着MRI技术发展,通过多种参数显示,可更有效评估胶质瘤分级情况。
1 资料与方法
1.1 一般资料2016年1月到2018年1月到延安大学附属医院就诊脑胶质瘤患者80例,年龄37~61岁[(43.38±4.55)岁];男49例,女31例;按照不同恶化情况分为低级别组36例(I级胶质瘤10例,II级胶质瘤26例),高级别组44例(III级胶质瘤28例,IV级胶质瘤16例)。纳入标准:①经过病理学检查确诊为脑胶质瘤者;②患者及家属知情并签署知情同意书,医院伦理委员会同意该研究。排除标准:①心血管疾病患者;②合并其他脑部疾病者;③糖尿病者;④肝肾功能严重异常者;⑤合并其他恶性肿瘤患者;⑥哺乳、妊娠期者;⑦精神疾病者;⑧对所用造影剂过敏者。
1.2 检测方法所有患者均进行颅脑部位MRI平扫、弥散加权成像(DWI)、磁共振灌注成像(PWI)、定量动态对比加强磁共振(DCE-MRI)、多体素共振波谱(MRS)、扩散张量成像(DTI)。选择德国西门子公司生产3.0 t MRI仪器(verio,32通道头线圈),患者呈仰卧位,检查期间叮嘱患者制动,避免出现运动伪影,依次进行MRI平扫、DWI、PWI、DCE-MRI、DTI、MRS检查,平扫层厚选择5 mm,层间距1.5 mm;多体素MRS检查时应避免血管、颅骨、钙化部位,以肿瘤最大截面为中心扫描;DTI扫描时选择层厚5 mm,选择层间距1.5 mm,弥散方向选择15;患者进行动态加强扫描第二个加强期后通过高压注射器向患者静脉注射钆双胺对比剂(国药准字J20100061,通用电气药业上海有限公司,10 ml),注射剂量0.2 ml/kg,注射速度3 ml/s;PWI采用二维测量,扫描参数为矩阵128×128,TR/TE为1200/23 ms,每个层面收集50时相,扫描80 s;感兴趣区(ROI)按照常规MRI中T1 WI、T2 WI及增强T1 WI图像共同确定放置,测量5次取平均值,脑实质区为T1 WI增强扫描中最大强化程度区域,脑周水肿区为肿瘤组织周围T1 WI低信号而T2 WI高信号区域,并在病灶对侧正常脑组织区域选择大小相同ROI,ROI范围为30像素左右,需避开血管、脑沟、脑池等影响。
1.3 观察指标①统计两组病灶处异性分数(FA)、平均扩散系数(DCavg)、表观扩散系数(ADC),胆碱(Cho)/N-乙酰天门冬氨酸(NAA)及胆碱(Cho)/肌酸(Cr);②统计两组病灶处渗透性参数(Ktrans)、血液回流常数(kep)、血浆容积(vp)、脑血流量(CBF)、脑血容量(CBV)及平均通过时间(MTT);③统计两组病灶处肿瘤实质部分相对脑血容量(rCBVt)、相对脑血流(rCBFt),肿瘤周围水肿部分rCBVe、rCBFe;④统计上述指标诊断阈值及多种参数MRI联合诊断效能。
1.4 统计学方法采用SPSS 17.0软件处理数据。计量资料比较采取t检验;采用ROC曲线分析诊断阈值。P<0.05为差异有统计学意义。
2 结果
2.1 两组FA、DCavg、ADC、Cho/NAA、Cho/Cr水平比较高级别组Cho/NAA、Cho/Cr水平高于低级别组,ADC水平低于低级别组(P<0.05);ADC诊断阈值为1.02×10-3mm2/s,ROC下面积0.905;Cho/NAA诊断阈值为2.03,ROC下面积0.787;Cho/Cr诊断阈值为2.10,ROC下面积0.810;两组FA、DCavg水平比较,差异无统计学意义(P>0.05)。见表1,图1、图2。

表1 两组FA、DCavg、ADC、Cho/NAA、Cho/Cr水平比较

图1 ADC参数的ROC曲线

图2 Cho/NAA、Cho/Cr的ROC曲线
2.2 两组Ktrans、kep、vp、CBF、CBV、MTT水平比较高级别组Ktrans、CBF、CBV高于低级别组(P<0.05);Ktrans诊断阈值为0.25 mm2/s,ROC下面积0.782;CBF诊断阈值为1.51 ml/(g·min),ROC下面积0.870;CBV诊断阈值为0.19 ml/g,ROC下面积0.742;两组kep、vp比较,差异无统计学意义(P>0.05)。见表2,图3。

图3 Ktrans、CBF、CBV的ROC曲线
2.3 两组rCBVt、rCBFt、rCBVe、rCBFe水平比较
高级别组rCBVt、rCBFt、rCBVe、rCBFe水平均高于低水平组(P<0.05);rCBVt诊断阈值为2.33 ml/g,ROC下面积0.833;rCBFt诊断阈值为2.08 ml/(g·min),ROC下面积0.843;rCBVe诊断阈值为1.04 ml/g,ROC下面积0.784;rCBFe诊断阈值为0.96 ml/(g·min),ROC下面积0.813。见表3,图4。

表2 两组Ktrans、kep、vp、CBF、CBV、MTT水平比较

表3 两组rCBVt、rCBFt、rCBVe、rCBFe水平比较
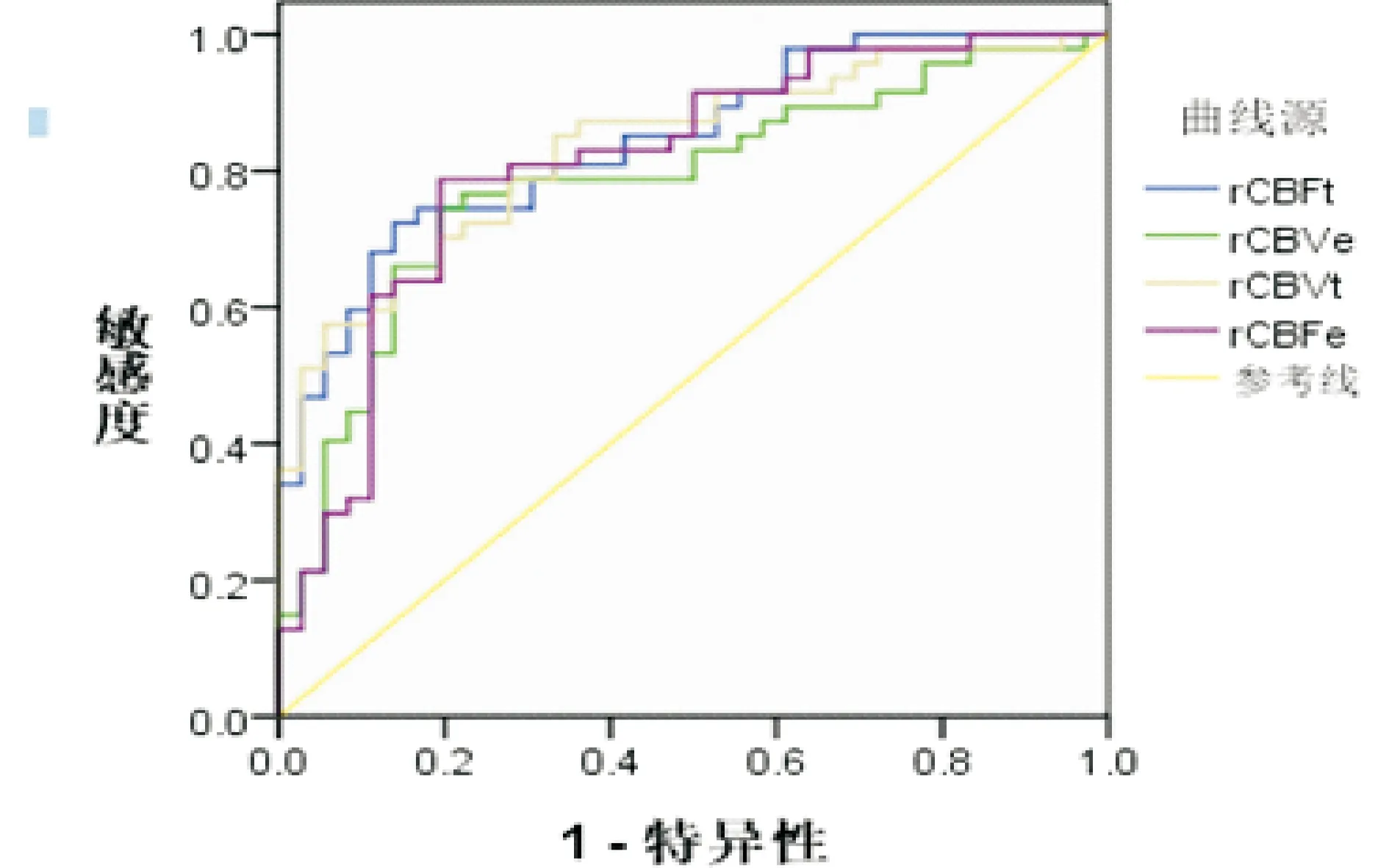
图4 rCBVt、rCBFt、rCBVe、rCBFe的ROC曲线
2.4 多种参数MRI联合诊断效能与病理学标准比较,多种参数MRI联合诊断效能准确率为92.50%,灵敏度94.44%,特异度90.91%。
3 讨论
原发性脑肿瘤为肿瘤相关死亡十大原因之一,在全身肿瘤中占比5%左右,在全身恶性肿瘤导致死亡中占比3%左右[6]。脑胶质瘤是最常见发生于脑实质中原发肿瘤,占比45%,多见于40岁以上人群[7]。随着恶性程度加重将影响治疗方式及预后,低级别肿瘤可仅采取保守治疗及随访,高级别肿瘤则需进行手术治疗及放化疗方式,且高级别肿瘤预后更差[8]。临床上需要根据分级结果选择治疗方式及评估预后,因此需准确对患者术前进行分级。单纯MRI扫描在胶质瘤分级上存在局限,无法通过强化程度准确判断肿瘤恶性程度。
功能MRI是新型成像技术,包括PWI、DTI、MRS等,对肿瘤生理代谢、血流动力学及弥散等可进行全面评估。DTI技术是通过水分子扩散存在各向异性得到FA及DCavg等参数,其中FA值取决于不同组织微结构,DCavg取决于肿瘤细胞密集程度[9]。MRS可显示肿瘤内部代谢状况,得到NAA、Cho等代谢产物参数进行分析[10]。DWI是目前成像方法中唯一可微观反应水分子扩散运动成像方式,通过ADC值可量化水分子弥散能力,有研究显示ADC值与胶质瘤恶性程度负相关[11]。PWI可评估患者组织微血管分布及血流灌注情况,患者生存期与胶质瘤血管化程度有关,因此可利于评估患者预后[12]。DCE-MRI是基于血容量、细胞外液成分等影响血脑屏障通透性,从而提供血管渗透性等参数信息[13]。
本研究发现高级别组ADC值更低,可能原因为高级别脑胶质瘤细胞分布密集,导致水分弥散受限;高级别组Cho/NAA、Cho/Cr水平更高,可能原因为高级别肿瘤细胞增殖能力更强,细胞膜转换速率更快,冯贵堂等[14]研究发现高级别脑胶质瘤患者ADC值低于低级别脑胶质瘤患者,Cho/NAA、Cho/Cr高于低级别脑胶质瘤患者。本研究发现高级别组Ktrans、CBF、CBV水平更高,可能原因为高级别胶质瘤患者肿瘤血管生成更多,血管通透性更高,提升脑部血流量及血容量,孙胜杰等[15]研究发现通过DCE-MRI联合灌注多参数分析高级别脑胶质瘤患者Ktrans、CBF、CBV水平均高于低级别患者。本研究发现高级别组rCBVt、rCBFt、rCBVe、rCBFe水平均更高,说明高级别患者肿瘤实质及周围水肿部分血容量及血流量更高。
综上所述,通过多参数MRI检测脑胶质瘤患者,高级别患者Cho/NAA、Cho/Cr水平高于低级别组,ADC水平低于低级别组;Ktrans、CBF、CBV高于低级别组;rCBVt、rCBFt、rCBVe、rCBFe水平均高于低水平组。
