腹腔镜结肠次全剔除创面腹膜化处理联合经自然腔道取标本手术治疗慢传输型便秘6例
2019-08-30陶永泽张维民朱绍凤陈德兴
陶永泽 张维民 朱绍凤 徐 刚 陈德兴
(吉林省前卫医院普外科,长春 130012)
便秘虽然是一种良性疾病,但严重影响人们的生活。我国便秘患病率7.0%~20.3%,平均9.18%,近年来,患病率有逐渐升高的趋势,且与年龄呈正相关[1~3]。部分顽固性便秘经内科保守治疗无效,不仅生活质量低下,且容易发生肠梗阻,危及生命。结肠慢传输型便秘仅行结肠全切除或次全切除,并发症多、复发率高[4]。徐刚等[5]认为腹腔镜下创面腹膜化的全结肠剔除式切除术,降低手术难度,同时减少术后腹腔内因创面大而发生粘连的可能。2017 年1~12月我科对6例结肠慢传输型便秘采用腹腔镜结肠次全剔除后创面腹膜化处理联合经自然腔道取标本手术(natural orifice specimen extraction surgery,NOSES),取得良好效果,报道如下。
1 临床资料与方法
1.1 一般资料
本组6例一般情况见表1。6例每周排便1~2次,且均在泻药、灌肠辅助下排便;排便费力均超过50%的时间;每次排便结束都有“不尽感”存在。6例均符合罗马Ⅲ便秘诊断标准(必须包括以下2个或2个以上症状)[6]:①至少有25%的排便感到费力;②至少25%的排便为块状便或硬便;③至少有25%的排便有排便不尽感;④至少25%的排便有肛门直肠的阻塞感;⑤至少25%的时间需要人工辅助(如指抠、盆底支持);⑥每周少于3次排便。6例均行便秘症状自评问卷PAC-SYM[7]、Wexner便秘评分[8]、汉密尔顿焦虑量表(HAMA)评估、焦虑自评量表SAS[9]评估、耶鲁-布朗强迫量表[10]评估,量表评分情况见表2。
病例选择标准:①符合罗马Ⅲ便秘诊断标准;②排除结肠器质性病变、出口梗阻型便秘、肠易激综合征、甲状腺疾病及钙离子异常(术前检查情况见表3);③经非手术治疗5年以上,严重影响生活、工作、学习,强烈要求手;④无严重焦虑、抑郁及精神异常;⑤无手术禁忌证。
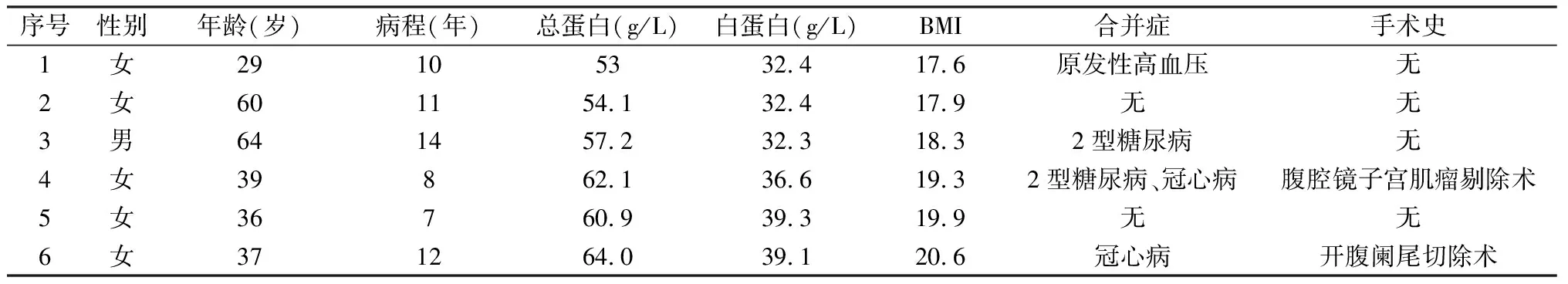
表1 6例一般情况
BMI正常范围:18.5~23.9

表2 量表评分、评估情况
*口服抗焦虑药物
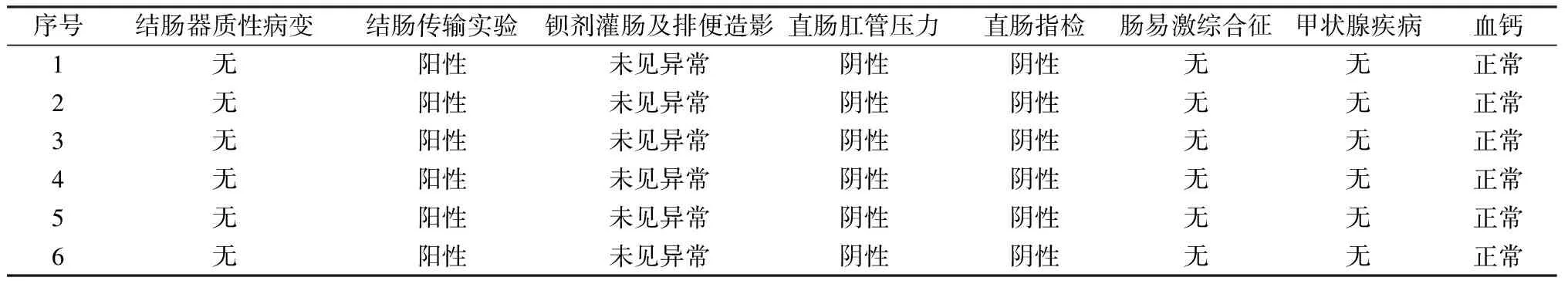
表3 术前检查情况
1.2 方法
术前均给予心理疏导、营养支持、肠道准备,术前预防性应用抗生素。
气管插管全麻。取截石位,左腿放置略高于腹部,根据操作需要可适当调整手术床倾斜角度。取脐下缘切口,逐层进腹,置入10 mm trocar,建立气腹,压力10~12 mm Hg。取右锁骨中线和右肋缘下3 cm交点,右侧麦氏点,左锁骨中线和左肋缘下5 cm交点,左侧反麦氏点分别放置5、12、12、5 mm 4个trocar,置入操作器械,探查腹腔。超声刀沿结肠系膜缘剔除结肠:距回盲部20 cm处紧贴系膜边缘直线切割闭合器切断回肠,完整保留系膜,沿回肠系膜边缘切断系膜至回肠末端。切开右结肠旁沟壁层腹膜,游离回盲部及升结肠至结肠肝曲(图1)。沿结肠系膜边缘紧贴结肠切断系膜,完整保留结肠系膜,同样方法游离结肠肝曲,保留系膜,可吸收线连续内翻缝合回肠系膜断缘与后腹壁层腹膜、升结肠系膜与右结肠旁沟切开的壁层腹膜边缘,完整关闭暴露的腹膜后创面。沿横结肠系膜边缘游离横结肠至结肠脾区,完整保留大网膜,横结肠系膜确切止血。切开左结肠旁沟壁层腹膜,紧贴结肠壁游离降结肠及部分乙状结肠,沿结肠系膜边缘紧贴结肠切断系膜,完整保留结肠系膜,直线切割闭合器切断乙状结肠。可吸收线连续内翻缝合降结肠及部分乙状结肠系膜与侧腹壁壁层腹膜(图2),关闭腹膜后创面[1]。乙状结肠保留长度:切除标本末端有神经节存在(根据术中快速冰冻病理结果)。扩肛后置入结肠镜(或卵圆钳),腹腔镜、结肠镜相结合将病变结肠标本放入结肠镜取物网篮或取物袋,标本沿乙状结肠、直肠经肛门取出(图3)。空肠末端与乙状结肠行侧侧吻合。吻合口浆肌层缝合。再次置入肠镜检查吻合口有无狭窄及出血。常规放置引流管。
术后24~48 h拔除胃、尿管。鼓励患者早期离床,加快康复。大部分患者排气后会出现腹泻,及时调整饮食结构,必要时用蒙脱石散止泻。根据患者肠道恢复情况逐渐由全流食、半流食过渡至正常饮食。密切观察患者心理变化,及时干预。

图1 沿结肠系膜缘剔除结肠 图2 结肠系膜缘与侧腹膜内翻缝合 图3 经自然腔道取标本
2 结果
6例均顺利完成手术,手术时间(216±44)min,术中出血量(65±35)ml。标本顺利经肛门取出,术中快速冰冻病理示乙状结肠断端有神经节存在,提示病变结肠已切除。术后(18±3)h排气排便,术后(12±3)d顺利出院,住院期间无并发症发生。1例术后出现轻度排便失禁,口服止泻剂后3~5 d改善。术后3 d大便9~21次/d,术后1个月4~10次/d,术后3个月2~8次/d,术后>6个月1~5次/d。6例随访7~14个月,平均9个月,经罗马Ⅲ便秘诊断标准判定已无便秘表现,且术后>6个月大便1~5次/d,效果满意。
3 讨论
便秘是临床最常见的症候群,只有明确便秘的具体类型才能更有效地制定具体的治疗方案。顽固性便秘患者多伴有精神疾病,详尽的病史采集、术前评估非常重要。
腹膜为全身面积最大、分布最复杂的浆膜,分壁腹膜(腹膜壁层)和脏腹膜(腹膜脏层)。壁腹膜与脏腹膜互相延续、移行,形成网膜、系膜和韧带。从胚胎发育上说, 它们属于同一个部分, 关系比较密切。腹腔镜下结肠次全“剔除”,而不是切除,目的是最大程度地保留系膜及腹膜,保留膜结构的完整性,避免术后肠粘连的发生。可吸收线连续内翻缝合回肠系膜断缘与后腹膜壁层腹膜、升结肠系膜与右结肠旁沟切开的壁层腹膜边缘、降结肠系膜及部分乙状结肠与侧腹壁壁层腹膜,使手术后的创面最大程度腹膜化,封闭各腔隙避免形成内疝。腹部手术后粘连发生率50%~97%[11]。腹腔内粘连通常是由于腹部手术、感染性疾病、子宫内膜异位症等诸多因素造成,但80 %是腹部手术后引起的粘连[12,13]。治疗腹部疾病时,具有腹腔镜手术条件时应尽量采用腹腔镜手术,减小手术切口能有效预防术后肠粘连的发生。腹腔镜手术粘连主要是大网膜粘连腹壁形式,而开腹手术多以各个脏器间的粘连为主。手术创面腹膜化处理可最大程度保证腹腔膜性结构的完整与连续,最大程度避免腹腔粘连性肠梗阻的发生。
NOSES是腹腔镜技术与NOTES “无切口”理念的巧妙结合,最主要、最直观的优势表现在避免腹壁切口取标本。切口大小与手术创伤呈正相关,切口越大,手术对体表神经的损伤越大[14,15]。NOSES降低切口感染、切口疝、粘连性肠梗阻等情况的发生。手术注意事项:截石位,左腿放置略高于腹部即可。在切除右侧结肠时取头低左倾位,切除横结肠时取头高位,切除左侧结肠时取头低右倾位,体位摆放与术中体位变化相结合,能够更方便术野观察及手术操作。沿肠壁切除肠管时最大程度保护肠系膜,同时避免切破肠管污染腹腔。游离升结肠后即缝合右侧,减少创面渗出,减少术后粘连;横结肠系膜无须缝合,切除时应确切止血,避免二次止血。切除病变肠管、空肠末端与乙状结肠行侧侧吻合后再行降结肠系膜与侧腹膜的缝合。扩肛后置入结肠镜或卵圆钳,将病变结肠标本一端放入结肠镜取物网篮或取物袋,裸化的肠管一端沿乙状结肠、直肠由肛门取出。断乙状结肠前应给予结肠减压,避免标本取出困难,有利于NOSES的实施。取病理时需要将乙状结肠或直肠残端敞开,避免肠内容物污染腹腔,尽可能做到“无菌操作”。根据术中快速病理判断乙状结肠断端是否有神经节的存在,提示“病变结肠”是否已经切除。
NOSES结肠次全剔除后创面腹膜化处理治疗慢传输型便秘,术后患者肠道功能恢复快,排气时伴有肠内容物(黏液)排出。随着饮水进食的开始,肠道功能开始变得更加活跃,部分患者可能出现严重腹泻及便失禁的情况,主要原因是结肠切除后粪便中水分吸收减少,同时与进食过多半流质有关。本组1例术后出现轻度排便失禁,口服蒙脱石散止泻,应用生长抑素减少胃肠道消化液分泌,调整补液量、监测电解质变化,症状3~5 d缓解。6例术后2~4周腹泻症状明显改善,术后>6个月大便1~5次/d,术后均未出现便秘复发、粘连性肠梗阻等情况,达到患者满意状态。快速病理为结肠切除范围找到最佳平衡点,避免切除过多、切除不足的情况发生。尽可能多保留乙状结肠能有效预防顽固性腹泻及便失禁的发生。
由于便秘患者对该疾病认识程度不同,能够主动接受外科治疗的患者较少,进一步扩大样本量、总结临床经验,才能更科学、规范地治疗慢传输型便秘。
