一种改性腐植酸基吸附树脂的制备及表征
2019-08-29穆林聪郭雅妮卢亚楠刘梦雅骆晓琳
穆林聪,郭雅妮,卢亚楠,刘梦雅,骆晓琳
(西安工程大学 环境与化学工程学院,陕西 西安 710048)
0 引 言
我国重金属废水排放量较大,污染严重[1-3]。不论是对生态自然环境,还是对人类健康,都会造成潜在而长久的严重危害[4-5]。 如何高效而经济地处理重金属废水, 已经成为学者们的研究重点。探索更多性能优良的水处理材料是解决这一问题的有效办法之一[6]。 腐植酸是一种芳香族混合物[7-8],含有羧基、羟基和甲氧基等多种活性基团[9-10],可以与烯类单体接枝共聚, 与苯酚、 甲醛等缩聚,与木质素磺酸盐及其他聚合物交联改性[12-13],从而提高其吸附性能[14-15]。风化煤作为一种煤炭资源储量丰富, 如果不进行合理利用,不仅是资源闲置浪费, 而且也对环境造成污染。风化煤的来源不同,其腐植酸含量和成份也各不相同[16-17]。
本文从风化煤中提取腐植酸, 并改性为不溶性腐植酸, 以降低其水溶性, 既可防止应用过程中对水体造成污染, 同时可提高其吸附性能[9-10]。 然后采用交联法将不溶性腐植酸与丙烯酸合成改性腐植酸基吸附树脂, 能使其吸附性能得到进一步提高[10-17]。
1 实 验
1.1 试剂和仪器
1.1.1 试剂 腐植酸(由风化煤中提取);丙烯酸(AA,广东光华科技股份有限公司);N,N′-亚甲基双丙烯酰胺(MBA,天津市科密欧化学试剂有限公司);过硫酸钾(KPS,西安化学试剂厂);硝酸钠(NaNO3,天津市河东区红岩试剂厂);氯化钙(CaCl2,天津市科密欧化学试剂有限公司);氢氧化钠(NaOH,郑州派尼化学试剂厂);硝酸(HNO3,西安三浦化学试剂有限公司);盐酸(HCl,西安三浦精细化工厂);氯化钠(NaCl,天津市北方天医化学试剂厂);重铬酸钾(K2Cr2O7,天津市科密欧化学试剂有限公司)。
1.1.2 仪器 集热式恒温加热磁力搅拌器(DF-101S,巩义市予华仪器有限责任公司);红外光谱分析(Nicolet5700型,美国Thermo Electron公司);扫描电镜(Quanta-450-FEG,美国FEI公司);水浴恒温振荡(SHAC,金坛市天竟实验仪器厂);低速离心机(80-1A,北京时代北利离心机有限公司);马弗炉(SX2系列,宜兴市华阳窑炉设备有限公司)。
1.2 风化煤腐植酸的提取
取定量的风化煤样放入锥形瓶中,加入18 %的盐酸溶液,加热煮沸活化,冷却后洗涤至中性并干燥。将活化后的风化煤样放入锥形瓶中,加0.8 mol/L的碱溶液, 100 ℃水浴60 min后冷却、离心;将离心液倒入烧杯中,向烧杯内加入盐酸调节pH值,至pH=2左右有絮状沉淀生成。静置分层,用布氏漏斗过滤并洗涤、干燥,即为腐植酸产物。
1.3 不溶性腐植酸的制备
取定量腐植酸于马弗炉中,330 ℃下加热脱水。用2 mol/L CaCl2溶液浸泡一段时间,经1 mol/L的硝酸和蒸馏水洗涤后,用1 mol/L硝酸钠溶液浸泡一段时间,80 ℃干燥,密封保存,即得到不溶性腐植酸。
1.4 改性腐植酸树脂的制备
在三口烧瓶内加入适量去离子水和不溶性腐植酸,放入恒温加热磁力搅拌器中均匀分散;取适量丙烯酸溶液加入三口烧瓶,混合均匀后逐滴加入定量NaOH溶液、KPS溶液和MBA溶液。升温至75 ℃,当反应体系形成稳定的黏性物质时停止搅拌。将产物冷却,洗涤后放入托盘切块,低温干燥,研磨过筛,即得到IHA-PAA树脂。
1.5 吸附效果实验
以Cr(Ⅵ)吸附量为评价指标,采用静态吸附进行吸附实验[18-20]。称量0.1g吸附剂分别放入体积20 mL、质量浓度5 mg/L的Cr(Ⅵ)溶液中,测定吸附后溶液中残余Cr(Ⅵ)浓度,计算HA、IHA和IHA-PAA对Cr(Ⅵ)的吸附量。Cr(Ⅵ)的测定采用二苯碳酰二肼分光光度法[21],吸附量Q和去除率E分别由式(1)和(2)计算。以Cr(Ⅵ)浓度为横坐标,吸光度为纵坐标绘制标准曲线,并得出标准曲线的回归方程。
(1)
(2)
式中:C0是Cr(Ⅵ)初始质量浓度(mg/L);C1是吸附后质量浓度(mg/L);V是Cr(Ⅵ)溶液的体积(mL);m是IHA.PAA的用量(g)。
1.6 改性腐植酸树脂的表征
通过红外光谱(FTIR)、扫描电镜(SEM)进行结构表征;采用Langmuir等温吸附和Freundlich等温吸附、拟一级动力学过程和拟二级动力学过程对吸附值进行拟合[21]。
2 结果与讨论
2.1 最佳合成条件
选用交联法合成IHA-PAA,确定合成温度为75 ℃,AA加入量为1.3 mL,选取单体配比IHA∶AA、MBA用量、KPS用量和NaOH中和度4个因素,各因素取4个水平,以Cr(Ⅵ)吸附量为评价指标,进行吸附实验。分别计算IHA-PAA对Cr(Ⅵ)的吸附量、各因素的极差R值与不同因素、不同水平的均值,并分析单因素对IHA-PAA对Cr(Ⅵ)吸附性能的影响,确定合成IHA-PAA的最佳条件,具体的实验设计及结果见表1及图1~5。
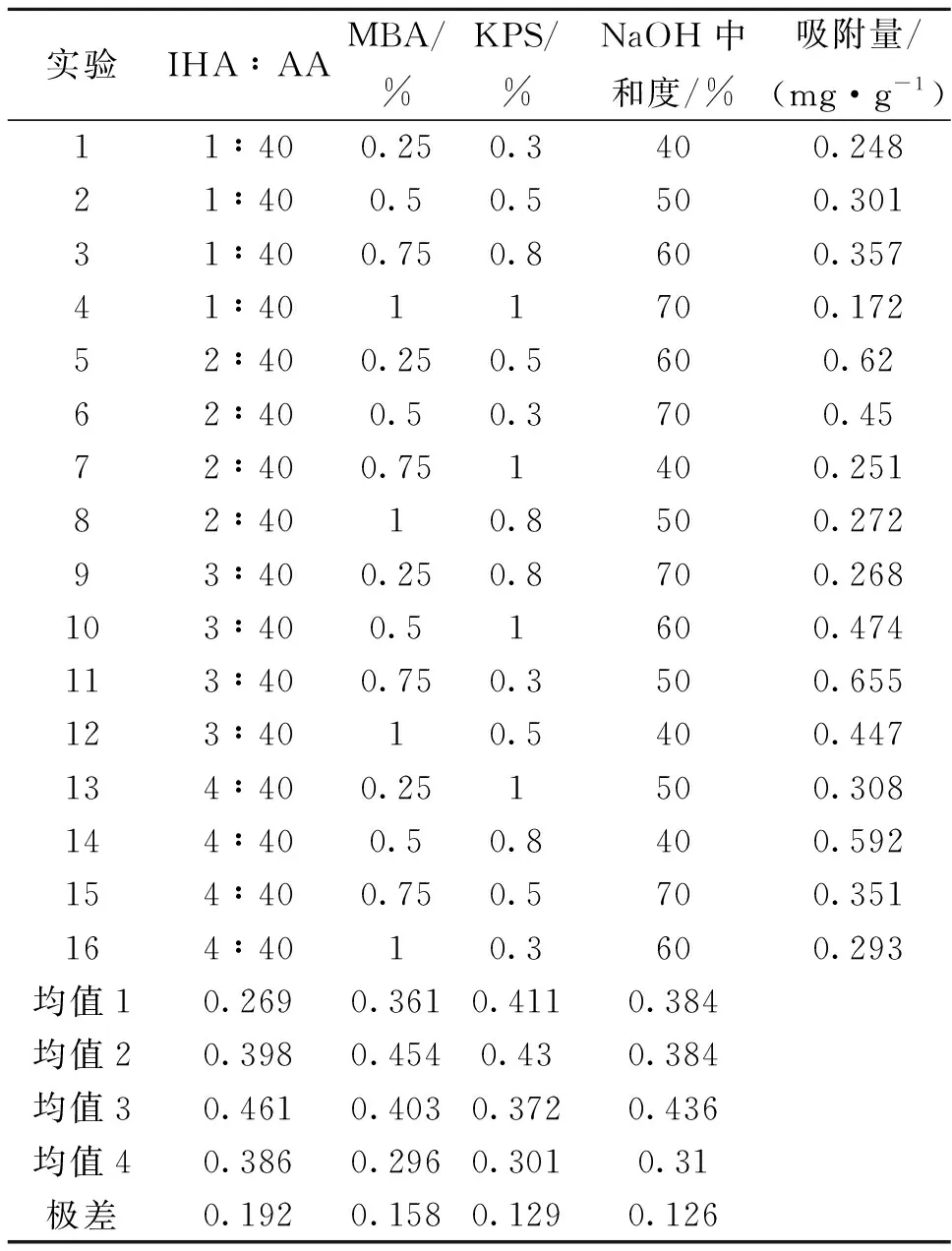
表 1 合成IHA-PAA的正交实验结果
由表1可知,在吸附树脂合成正交实验中,各实验条件下对Cr(Ⅵ)的吸附量介于0.172~0.655 mg/g。合成树脂吸附效果的影响因素由大到小依次为:单体比>MBA用量>KPS用量>NaOH中和度。

图 1 吸附量随单体配比的变化Fig.1 The change of adsorption capacitywith monomer ratio
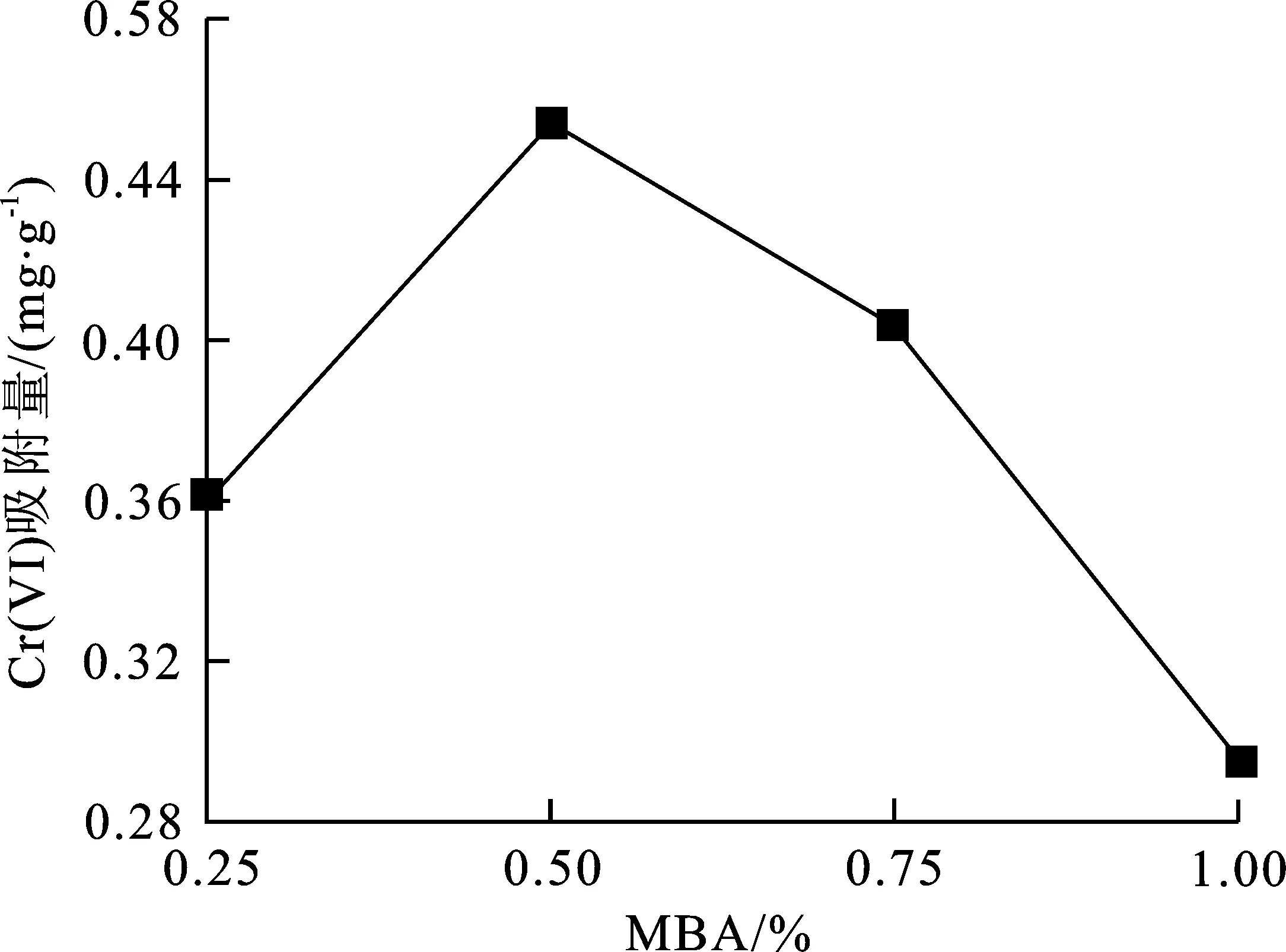
图 2 吸附量随MBA用量的变化曲线 Fig.2 The change of adsorption capacity with MBA
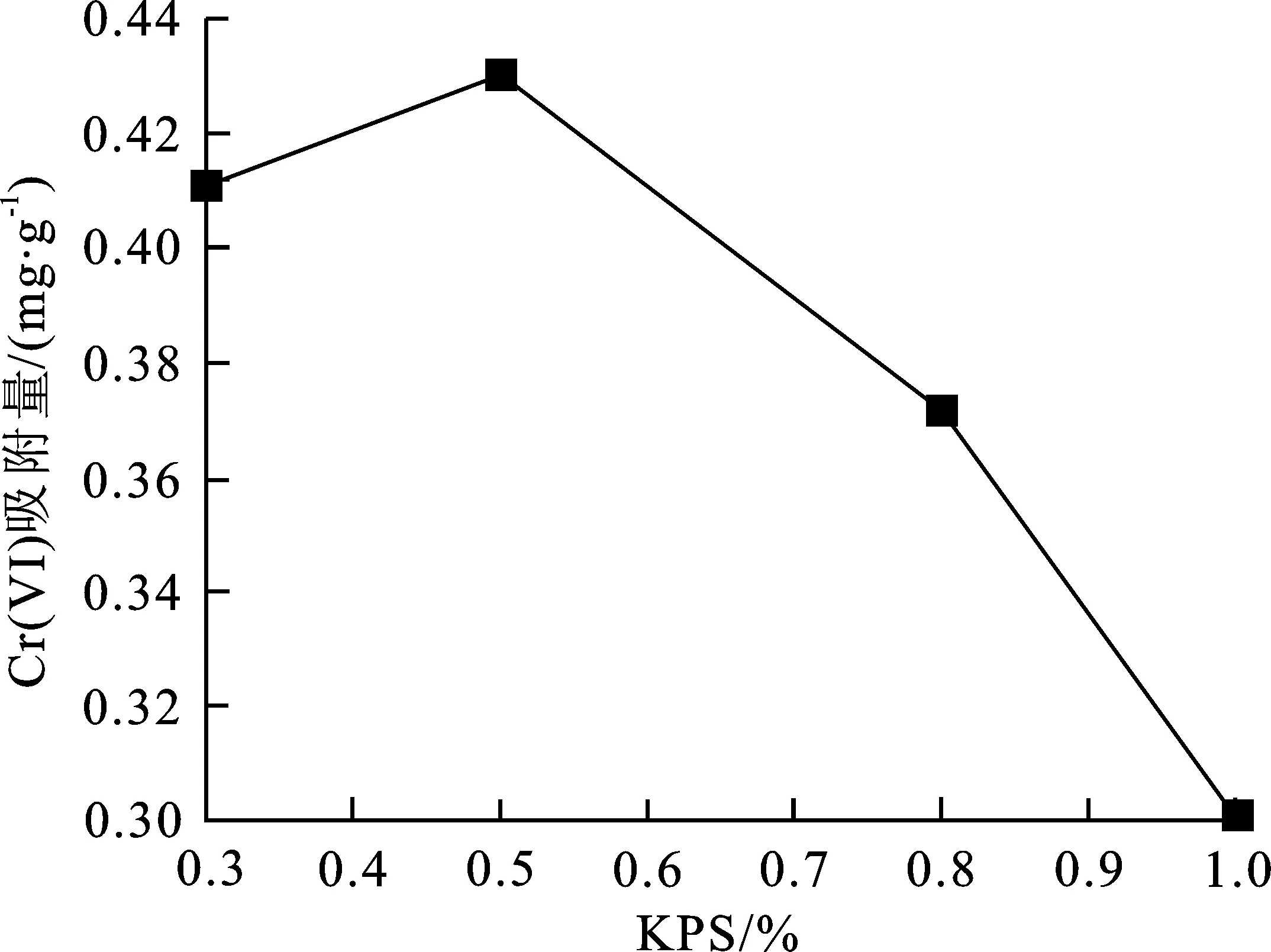
图 3 吸附量随KPS用量的变化曲线Fig.3 The change of adsorption capacity with KPS
由图1可知,IHA用量越多,活性官能团越多,对Cr(Ⅵ)的去除能力越好。但是,当IHA的含量过多时,IHA与丙烯酸接枝共聚度过高,共聚物延展性变差,单位体积内部空隙变小,导致内部活性吸附位点减少,吸附量降低。由图2可知,随着MBA用量的增加,树脂对Cr(Ⅵ)的吸附量先上升后降低。这是由于交联剂用量过大,合成树脂交联网络结构中交联点过多,树脂延展性差,内部网络空间过小,与Cr(Ⅵ)接触点位减少而造成的。由图3可知,当KPS用量过大时,导致其对Cr(Ⅵ)的吸附效果变差,这是由于其影响了接枝共聚的效率与合成树脂的三维结构与性能。由图4可知,当NaOH与丙烯酸中和度过高时,由于可溶物的溶解使得三维结构破坏,导致对Cr(Ⅵ)的吸附效果较差,吸附量降低。最终得到合成IHA-PAA的最佳条件:单体配比IHA∶AA为3∶40,MBA质量分数为0.5 %,KPS质量分数0.5 %,NaOH中和度为60 %。

图4 吸附量随NaOH中和度的变化Fig.4 The change of adsorption capacity with neutralization degree of NaOH
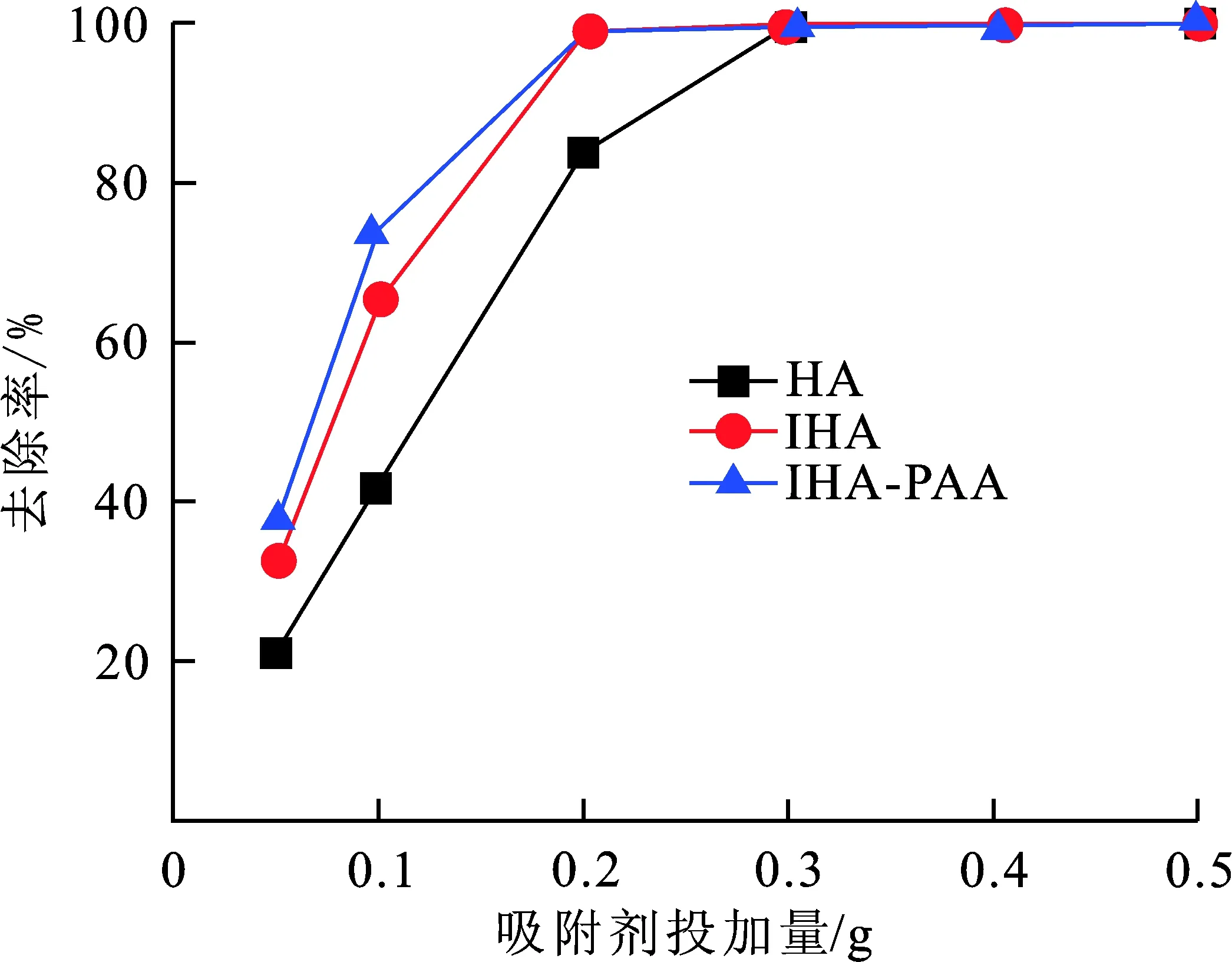
图 5 HA、IHA和IHA.PAA的吸附效果比较Fig.5 Comparison of the adsorption effect of HA-IHA and IHA-PAA
2.2 影响吸附因素
图5是相同Cr(VI)浓度下HA、IHA和IHA-PAA的吸附效果比较图。可以看出,3种吸附剂对Cr(VI)的吸附趋势是相似的;很明显,达到相同Cr(VI)去除率所需的HA-PAA吸附剂用量较少,表明HA-PAA吸附剂能力更强。
为保证吸附剂的吸附应用性能,对吸附过程pH、温度和吸附剂粒度的影响进行了实验分析。
2.2.1 pH值的影响 pH对IHA-PAA吸附效果的影响结果见图6。吸附量下降趋势为HA>IHA>IHA-PAA,说明IHA-PAA吸附量受pH变化影响最小,即耐酸碱性最强,IHA次之,HA受pH变化影响最大。可以看出,IHA-PAA的耐酸碱性最优,pH中性和偏酸性条件下IHA-PAA的吸附效果较好。
2.2.2 温度的影响 为测试温度对吸附Cr(VI)效果的影响,分别在15,25,35,45,55 ℃温度条件下进行实验,结果如图7。图7表明, IHA-PAA耐温性能更优,20~30 ℃时吸附效果好,适合常温使用。

图 6 pH对吸附Cr(VI) 效果的影响

图 7 温度对吸附Cr(VI) 效果的影响Fig.7 The effect of temperature on Cr(VI) adsorption
2.2.3 IHA-PAA 吸附剂粒径的影响 粒径大小会由于其表面结构及与水的接触程度不同对吸附速率具有一定的影响,IHA-PAA 吸附剂粒径对其吸附Cr(Ⅵ)效果如图8所示。可以看出, IHA-PAA粒径为60~80目吸附量达到峰值,对Cr(Ⅵ)的吸附量最大可达到0.749 mg/g。
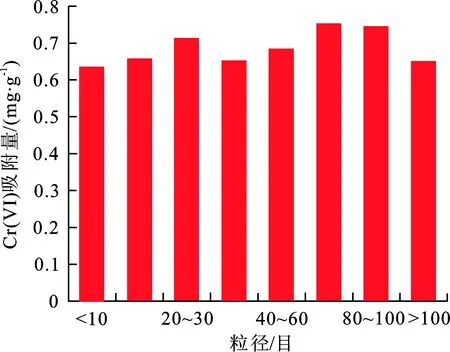
图 8 粒径对Cr(VI)吸附效果的影响Fig.8 The effect of particle size on Cr(VI) adsorption
2.3 红外光谱分析


图 9 HA、IHA和IHA-PAA红外光谱图Fig.9 FT-IR spectra of HA,IHA and IHA-PAA
2.4 扫描电镜分析
图10为HA、IHA和IHA-PAA的扫描电镜图。可以看出,HA表面比较光滑,改性IHA表面相对比较粗糙,而IHA-PAA表面粗糙程度尤其明显,且形成较多排列有序的簇状突起。簇状突起之间有较多明显的孔洞结构产生,有利于增大其有效吸附面积,提高吸附效率。

(a) HA(100 000×)

(b) IHA(100 000×)

(c) IHA-PAA(100 000×)图 10 HA 、IHA和IHA-PAA的SEM照片
2.5 等温吸附实验
采用Langmui等温吸附和Freundlich等温吸附对实验数据进行拟合分析,结果如图11,12和表2所示。

表 2 等温吸附方程的拟合常数
根据拟合结果可知,Langmuir吸附等温线的相关系数R2为0.897 3,qmax只有0.218 mg/g,且残差为2.975;而Freundlich吸附等温线的相关系数R2=0.9911,0<1/n<1(吸附朝着有利方向进行),且残差为0.049,远小于Langmuir吸附等温线残差。因此,Freundlich吸附等温线能够更好地描述IHA-PAA对Cr(Ⅵ)的吸附行为。因为IHA-PAA是一种非均匀共聚物,而Freundlich模型是一种经验模型,适用于非均质表面的吸附,用以表现吸附表面的不均匀表面能,因此Freundlich模型可以对其进行较好的拟合。
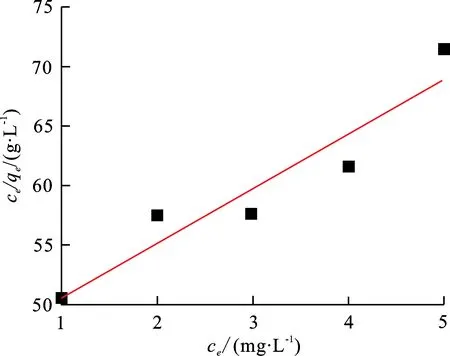
图 11 Langmuir吸附等温线Fig.11 Langmuir adsorption isotherm

图 12 Freundlich吸附等温线Fig.12 Freundlich adsorption isotherm
2.6 吸附动力学实验
吸附过程的动力学研究主要是用来描述吸附剂吸附溶质的速率快慢,通过动力学模型对数据进行拟合,从而探讨其吸附机理。采用拟一级动力学模型和拟二级动力学模型实验数据进行拟合,了解IHA-PAA吸附Cr(Ⅵ)的吸附动力学过程,结果如图13,14和表3所示。
根据拟合结果可知,低浓度条件下,一级动力学过程能够更好地描述IHA-PAA对Cr(Ⅵ)的吸附行为。说明IHA-PAA吸附Cr(Ⅵ)的速率与Cr(Ⅵ)溶液的浓度的一次方呈线性关系,是单因子决定反应速率的吸附行为。原因可能是物质传输步骤即膜扩散是吸附过程的限速步骤。溶液浓度较高(4~5 mg/L)时,符合拟二级动力学吸附过程,说明吸附过程除液膜扩散、颗粒内扩散等外,主要受化学作用所控制,涉及吸附质与吸附剂之间的电子共用或电子转移,即化学吸附是限速步骤。

图 13 不同浓度的一级动力学曲线Fig.13 The first-order kinetic curves at different concentration

图 14 不同浓度的二级动力学曲线Fig.14 Second-order kinetic curves at different concentration
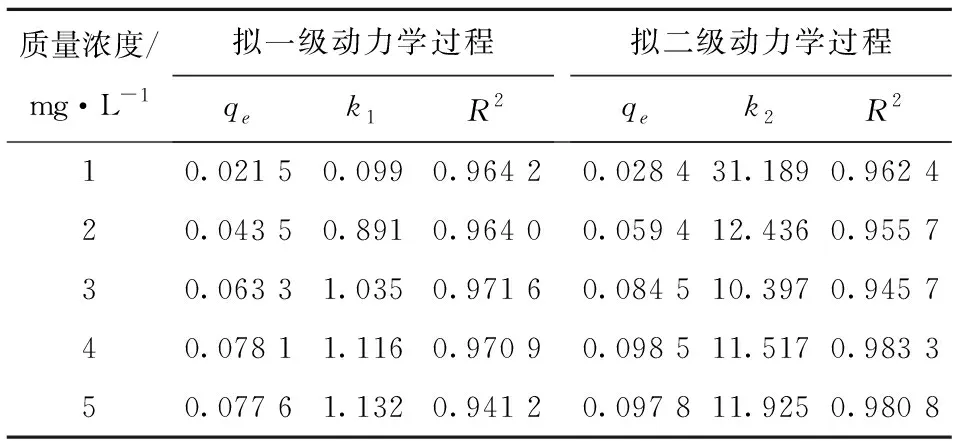
质量浓度/mg·L-1拟一级动力学过程qek1R2拟二级动力学过程qek2R210.021 50.0990.964 20.028 431.1890.962 4 20.043 50.8910.964 00.059 412.4360.955 7 30.063 31.0350.971 60.084 510.3970.945 7 40.078 11.1160.970 90.098 511.5170.983 3 50.077 61.1320.941 20.097 811.9250.980 8
3 结 论
(1) 在最佳合成条件,即单体配比IHA∶AA为3∶40,MBA用量为0.5 %,KPS用量为0.5 %,NaOH中和度为60 %,制备的粒径60~80目IHA-PAA对Cr(Ⅵ)的吸附量可达0.749 mg/g。
(2) IHA-PAA亲水基团增多,表面粗糙形成簇状突起,且产生孔洞结构,比表面积和孔容增大,吸附性能显著提高。
(3) HA-PAA对Cr(Ⅵ)吸附过程适合用Freundlich吸附等温过程拟合。低浓度条件下膜扩散是IHA-PAA对Cr(Ⅵ)吸附过程的限速步骤,高浓度条件下化学吸附是限速步骤。
