后腹腔镜下肾切除术治疗肾肿瘤的效果分析
2019-08-28周昌东田玉新杨新平王英迪张奇夫
周昌东 田玉新 杨新平 王英迪 孙 凯 林 洋 张奇夫
肾肿瘤是泌尿外科常见肿瘤之一,其发病率占全身实体性肿瘤的3%,我国近几年的肾肿瘤发病率有不断上升的趋势[1-3]。肾肿瘤按照发病部位可分为中央型及外周型肾肿瘤,其中多数为外周型肾肿瘤。肾肿瘤的具体发病机制还不明确,可能与遗传因素与基因表达有关[4]。随着医学技术的提高,肾肿瘤的生存率明显提高[5-6]。长期以来对肾肿瘤多采用患肾根治性切除术为主,但是对患者的创伤比较大[7-8]。保留肾单位肾肿瘤切除术是指1种局部彻底切除肾肿瘤组织,并且尽可能多地保留正常肾组织的手术方式,也具有创伤小、视野清晰、疗效确切、出血少等优势[9]。当前随着术中肾缺血性损伤预防方法的改善,使保留肾单位手术得到了广泛应用[10]。随着腹腔镜技术经过不断改进,其在泌尿外科领域取得了很大发展,已经部分取代了传统开放手术[11]。有研究表明腹腔镜下肾部分切除术能达到与腹腔镜下肾根治性切除术相仿的生存率外,最大限度的保留了肾功能[12]。特别是随着后腹腔镜技术的成熟,其已经应用于治疗大体积(直径>7 cm)的肾肿瘤,也取得了比较好的效果[13]。但是男性的泌尿男殖系统器官多位于盆腔底部或腹膜后,实施的难度比较大[14]。本研究采用回顾性对比研究方法,探讨了后腹腔镜下肾切除术治疗肾肿瘤的效果。现报告如下。
1 资料与方法
1.1 研究对象
采用回顾性、总结研究方法,2015年2月到2017年9月选择在我院诊治的肾肿瘤患者78例作为研究对象,纳入标准:我院伦理委员会批准了此次研究;血尿素氮、肌酐均处于正常范围内;术前检查及术后病理证实为T1期肾肿瘤;单侧发病与单发病灶;具有手术治疗指征;肾肿瘤直径3~9 cm。排除标准:有远处转移而行姑息性切除的病例;病理证实为肾盂癌等非肾细胞癌的病例;妊娠与哺乳期妇女;先天性心肝肾异常患者;凝血功能障碍,有全身出血性疾病患者。根据治疗方法的不同分为观察组40例与对照组38例,两组患者的肿瘤部位、肿瘤类型等对比差异无统计学意义(P>0.05)。见表1。

表1 两组一般资料对比
1.2 手术方法
观察组:给予后腹腔镜下肾切除术治疗,患者术前禁食、禁饮,术前晚及术日晨行清洁灌肠各1次。患者在气管插管全麻下取健侧卧位,升高腰桥,靠软沙发垫上,常规消毒铺巾。在腋中线髂嵴上方约2 cm处横行作一个1.5~2 cm的切口,切开肌肉组织直到腹膜后间隙,扩张腹膜后间隙。在腋前线与肋弓下2 cm交界处、腋后线十二肋缘下1 cm做一长约5 cm的切口,置入吸引器、腹腔镜、分离钳、超声刀等手术设备。用超声刀充分分离腰大肌前间隙,游离找到肾蒂,用切开肾动脉鞘膜,显露肾动脉。夹闭并剪断肾动脉后,找到肾静脉并游离、夹闭、剪断肾静脉。手术行区域性淋巴结清扫,剥离淋巴脂肪组织。将肾脂肪囊游离至输尿管,钛夹夹闭后切断输尿管,留置腹膜后引流管,缝合切口。
对照组:采用常规根治切除术,选择气管内插管静脉麻醉,患者取健侧卧位。选择患侧腰部11肋间或12肋下斜切口,显露肾周筋膜,游离胸膜、肾脏上极、中部和下极。游离输尿管至腹主动脉分叉处并进行结扎切断,分离肾动静脉,显露肾蒂,完整切除患肾。
所有患者术后密切监测患者的生命体征,常规使用抗生素3~5 d。
1.3 观察指标
①记录两组的术后肠道恢复时间、引流管放置时间、住院时间、手术时间、术中出血量等指标。②记录两组术后14 d发生的膈肌损伤、切口感染、肾血管出血、皮下气肿、皮下积液等并发症情况。③肾功能:在术后1 d与术后14 d空腹抽取全血3~4 ml,室温静置30 min,抗凝后离心(1500 rpm/min 离心5 min,离心半径为10 cm)分离上层血清,采用全自动生化分析仪(日本日立公司7100型)检测血肌酐含量。④随访至今,记录两组的中位生存时间,以月计算,因本病死亡为终点事件,失访及存活为截尾数据。
1.4 统计方法
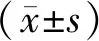
2 结果
2.1 围手术指标对比
所有患者都顺利完成手术,对照组的手术时间、术中出血量显著多于观察组(P<0.05),两组术后肠道恢复时间、引流管放置时间、住院时间对比差异无统计学意义(P>0.05)。见表2。
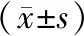
表2 两组围手术指标对比
2.2 术后并发症发生情况对比
观察组与对照组术后14 d并发症主要为切口感染、肾血管出血、膈肌损伤、皮下气肿、皮下积液,总发生率分别为10.0%和18.4%,均行保守治疗后好转,对比差异无统计学意义(P>0.05)。见表3。

表3 两组术后并发症发生情况对比/例
2.3 肾功能变化对比
观察组与对照组术后14 d的血SCr都显著高于术后1 d(P<0.05),观察组术后14 d的血SCr高于对照组(P<0.05)。见表4。
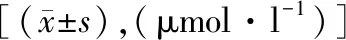
表4 两组手术后不同时间点肾功能变化情况
2.4 随访生存时间对比
所有患者随访至今,观察组的中位生存时间为(25.32±3.14)个月,对照组为(24.59±3.98)个月,两组对比差异无统计学意义(t=0.453,P=0.387)。
3 讨论
肾肿瘤是起源于肾实质泌尿小管上皮系统的肿瘤,在泌尿系统中的发病率仅次于膀胱肿瘤。肾肿瘤的常见病理组织学类型透明细胞癌,其次为嫌色细胞癌、乳头状肾细胞癌等[15]。
外科手术是治疗肾肿瘤的首选方法,研究表明开放肾切除根治术的术后疗效优于行单纯肾肿瘤切除术,但是传统开放肾切除术一般采用大切口,术中需切断肋胁部诸层肌肉,对患者的创伤比较大[16]。当前随着腹腔镜手术器械的完善及操作技能的发展,腹腔镜肾切除术已得到了广泛的开展,成为肾肿瘤治疗的标准术式[17]。有研究表明,在没有行保留肾单位肾肿瘤切除术的手术指证下,肿瘤直径<7 cm的肾肿瘤是目前公认的腹腔镜肾切除术的手术适应症[18]。
本研究显示所有患者都顺利完成手术,对照组的手术时间、术中出血量显著多于观察组,两组术后术后肠道恢复时间、引流管放置时间、住院时间对比差异无统计学意义;观察组与对照组术后14 d并发症总发生率分别为10.0%和18.4%,对比差异无统计学意义,表明后腹腔镜下肾切除术治疗不同类型的肾肿瘤都有比较好的效果,安全性好。随着球囊扩张技术的发展,使得后腹腔镜肾根治性切除术成为了可能,其在临床上的应用具有切口小、术后恢复快、出血少、疼痛轻、住院时间短等优点[19]。但是由于后腹腔空间小,缺乏良好的解剖标志等原因,在临床上的应用也具有更多的并发症[20]。在预防并发症中,仔细辨认解剖标志,在肾周筋膜外将肾脏轮廓游离出来[21];需要建立良好的后腹腔间隙,一般选取腋后线肋缘下2 cm处切口,分离左肾静脉时认清解剖层次结构,使用超声刀切割组织时不要损伤腹膜[22]。术后严密观测生命体征,如果有活动性出血,应果断行剖腹探查。
本研究显示观察组与对照组术后14 d的血SCr都显著高于术后1 d,观察组术后14 d的血SCr高于对照组,表明经后腹腔途径能促进肾功能的恢复。在肾肿瘤患者中,由于病侧肾脏全部切除后可导致有效肾单位减少,存在正常侧肾功能衰竭的风险,从而导致血Scr升高[23]。经后腹腔途径进行手术操作,尽管操作空间相对较小、缺乏清晰的解剖标志,手术中若损伤腹膜,增加手术难度[24]。但是但这种途径可迅速进入手术野,分离组织少,避免了腹腔污染和肿瘤种植,有利于肾功能的恢复[25]。有研究表明,在肾肿瘤切除术中,肾脏缺血都会产生潜在性的肾功能损害,为减少热缺血对肾功能的损害,可采用局部降温的方法以延长肾脏耐受热缺血损伤的时间,从而保护患肾功能[26]。本研究显示两组的中位生存时间相近,说明不同类型肾肿瘤患者的预后生存情况类似。不过本组研究纳入的病人总数仍然偏少,病例抽样是非随机性的,机制的探讨还不够,可能存在各种偏倚,将在下一步的研究中进行深入分析。
总之,后腹腔镜下肾切除术治疗肾肿瘤具有很好的可行性与安全性,提高患者的生存期间,减少对患者的创伤,促进患者术后肾功能恢复更快。
