Compass三维剂量验证系统在鼻咽癌容积旋转调强放射治疗计划剂量验证中的应用*
2019-08-27吴广鑫蔡勇君陈济鸿柏朋刚王艺辉
吴广鑫 蔡勇君 陈济鸿 柏朋刚 王艺辉*
容积旋转调强放射治疗(volumetric modulated arc therapy,VMAT)是近年来发展起来的一种新的调强放射治疗(intensity modulated radiation therapy,IMRT)[1-2]技术,该技术对治疗计划系统(treatment planning system,TPS)、网络系统以及直线加速器的各项参数提出了更高的要求,对剂量精准提出了更高的标准。鼻咽癌采取VMAT时,因其靶区复杂、危及器官(organ at risk,OAR)较多、剂量梯度较大等因素更加要求放射治疗剂量的精确。
Compass三维剂量验证系统是一种先进的验证设备,能够提供基于患者的各个靶区和OAR等感兴趣区域(region of interesting,ROI)的二维和三维剂量信息,为各ROI理论和实际的剂量差异提供更多的信息[3]。目前Compass的临床应用研究主要集中在食管癌[4]、宫颈癌[5]、前列腺癌[6]以及直肠癌[7]等肿瘤方面,对鼻咽癌的研究相对较少。基于以上原因,本研究回顾性分析17例鼻咽癌单弧VMAT计划的剂量验证数据,分析各ROI理论和实际照射剂量差异的原因,为鼻咽癌VMAT技术剂量的精准实施提供数据支持。
1 资料与方法
1.1 临床资料
选取解放军联勤保障部队第909医院收治的17例无转移鼻咽癌患者,其中男性12例,女性5例;年龄41~69岁,平均年龄(53.70±6.93)岁。根据中国鼻咽癌分期2017版本[8-9](AJCC第八版)进行分期。①T分期:T2、T3及T4分别为4例、8例和5例;②N分期:N1、N2和N3分别为6例、5例和6例;③临床分期:Ⅱ期4例,Ⅲ期6例,Ⅳa期7例。所有患者均行单弧VMAT放射治疗计划。
1.2 仪器设备
采用SOMATOM Definition双源64排CT模拟机(德国西门子公司),IBA Compass 3.1b三维剂量验证系统,PTW Unidose电离室及固体水;Synergy直线加速器(瑞典医科达公司)及Monaco 5.11治疗计划系统。
1.3 靶区及OAR的勾画和剂量设定
依据2010鼻咽癌调强放射治疗靶区及剂量设计指引专家共识[10]原发肿瘤及咽后淋巴结的肿瘤靶区GTVnx-P、临床靶区CTV1-P以及计划靶区CTV2-P的处方剂量分别为7128 cGy、6600 cGy和5600 cGy;双侧颈部转移淋巴结GTVnd-R/L-P和预防照射区CTVnd-R/L-P的处方剂量分别为6600 cGy和5600 cGy。OAR包括脊髓、脑干、视交叉、左右腮腺、视神经、晶体、颞叶、垂体及下颌骨等。OAR限量值:脊髓<45 Gy,脑干<54 Gy,腮腺D50<35 Gy,眼晶状体<7 Gy,视交叉<54 Gy,颞颌关节<70 Gy,颞叶<60 Gy,眼球<30 Gy。
1.4 WMAT计划设计
17例单弧VMAT计划的优化参数为:蒙特卡罗(Monte carlo,MC)算法,能量为6 MV的X射线,治疗床及准直角度均为0°,最大控制点数设定范围100~120[11]。MC算法不确定度模式1%,机架旋转角度为顺时针180°~360°,最小子野宽度1 cm,区域分割为30°,计算网格3 mm,优化模式为OAR优先(constrained)模式。
1.5 验证流程
按照厂商标准将Compass的MatriXX和角度传感器分别固定在直线加速机头和机架上,依据建模的数据加2 cm的固体水于Matrixx表面做剂量建成,依次进行初次本底测量、预照射、再次本底测量、几何位置和绝对剂量校准以及机架角度校正等步骤,以上步骤均符合标准后通过放射治疗网络管理系统Mosaiq执行相应的VMAT计划。
1.6 验证结果评价指标
采用3 mm、3%、阈值为1的γ通过率标准对各ROI分别计算治疗计划系统和COMPASS自身计算剂量的γ通过率比较(treatment planning systemcomputer dose,TPS-CD)和治疗计划系统和实测重建剂量的γ通过率比较(treatment planning system-reconstructed dose,TPS-RD)的γ通过率。通过剂量体积直方图(dose volume histogram,DVH)读取各ROI在TPS及RD上的D1%和D99%平均剂量Dmean等数据,并分别计算TPS-RD之间差值的绝对值和百分比,D1%和D99%分别表示靶区1%和99%体积受到的照射剂量。
1.7 统计学方法
采用SPSS17.0软件对数据进行统计分析,所有数据均以均数±标准差()记录。对TPS-CD和TPS-RD的γ通过率比较,TPS-RD的D1%、D99%及Dmean等剂量学比较均采用配对t检验,以P<0.05为差异有统计学意义。
表1 靶区和OAR的γ通过率比较(±s)
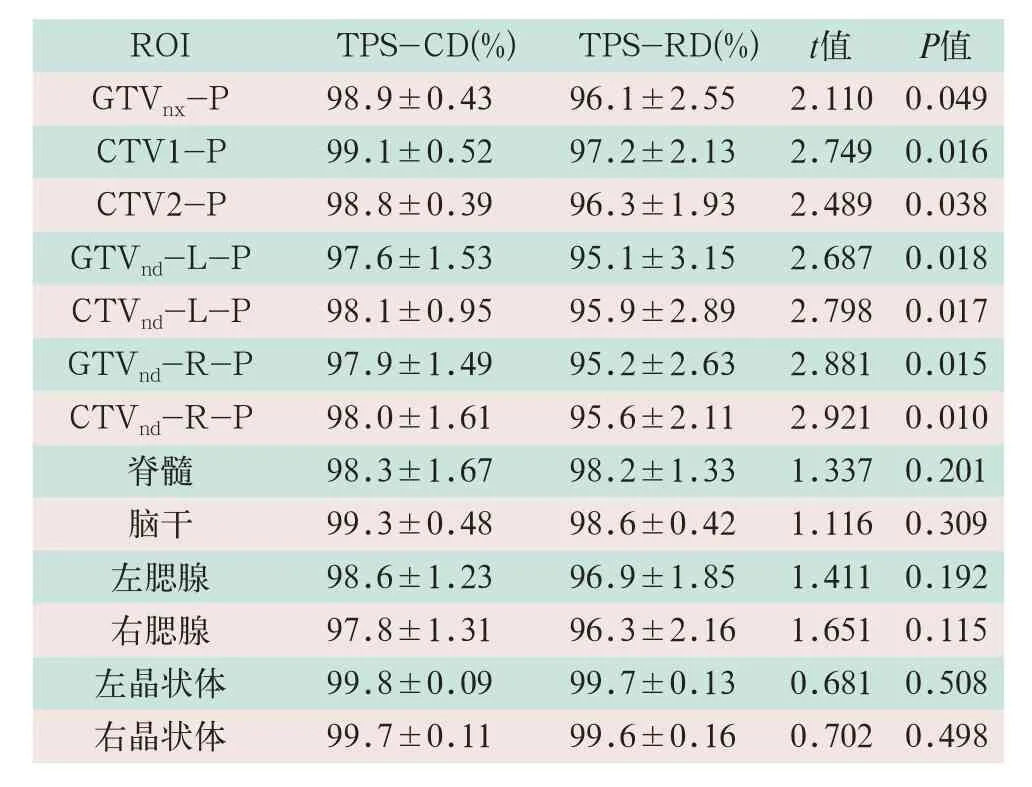
表1 靶区和OAR的γ通过率比较(±s)
注:表中ROI为感兴趣区域;TPS-CD为治疗计划系统和COMPASS自身计算剂量的γ通过率比较:TPS-RD为治疗计划系统和实测重建剂量的γ通过率比较
ROI TPS-CD(%) TPS-RD(%) t值 P值GTVnx-P 98.9±0.43 96.1±2.55 2.110 0.049 CTV1-P 99.1±0.52 97.2±2.13 2.749 0.016 CTV2-P 98.8±0.39 96.3±1.93 2.489 0.038 GTVnd-L-P 97.6±1.53 95.1±3.15 2.687 0.018 CTVnd-L-P 98.1±0.95 95.9±2.89 2.798 0.017 GTVnd-R-P 97.9±1.49 95.2±2.63 2.881 0.015 CTVnd-R-P 98.0±1.61 95.6±2.11 2.921 0.010脊髓 98.3±1.67 98.2±1.33 1.337 0.201脑干 99.3±0.48 98.6±0.42 1.116 0.309左腮腺 98.6±1.23 96.9±1.85 1.411 0.192右腮腺 97.8±1.31 96.3±2.16 1.651 0.115左晶状体 99.8±0.09 99.7±0.13 0.681 0.508右晶状体 99.7±0.11 99.6±0.16 0.702 0.498
表2 靶区和OAR的TPS-RD绝对剂量比较(±s)
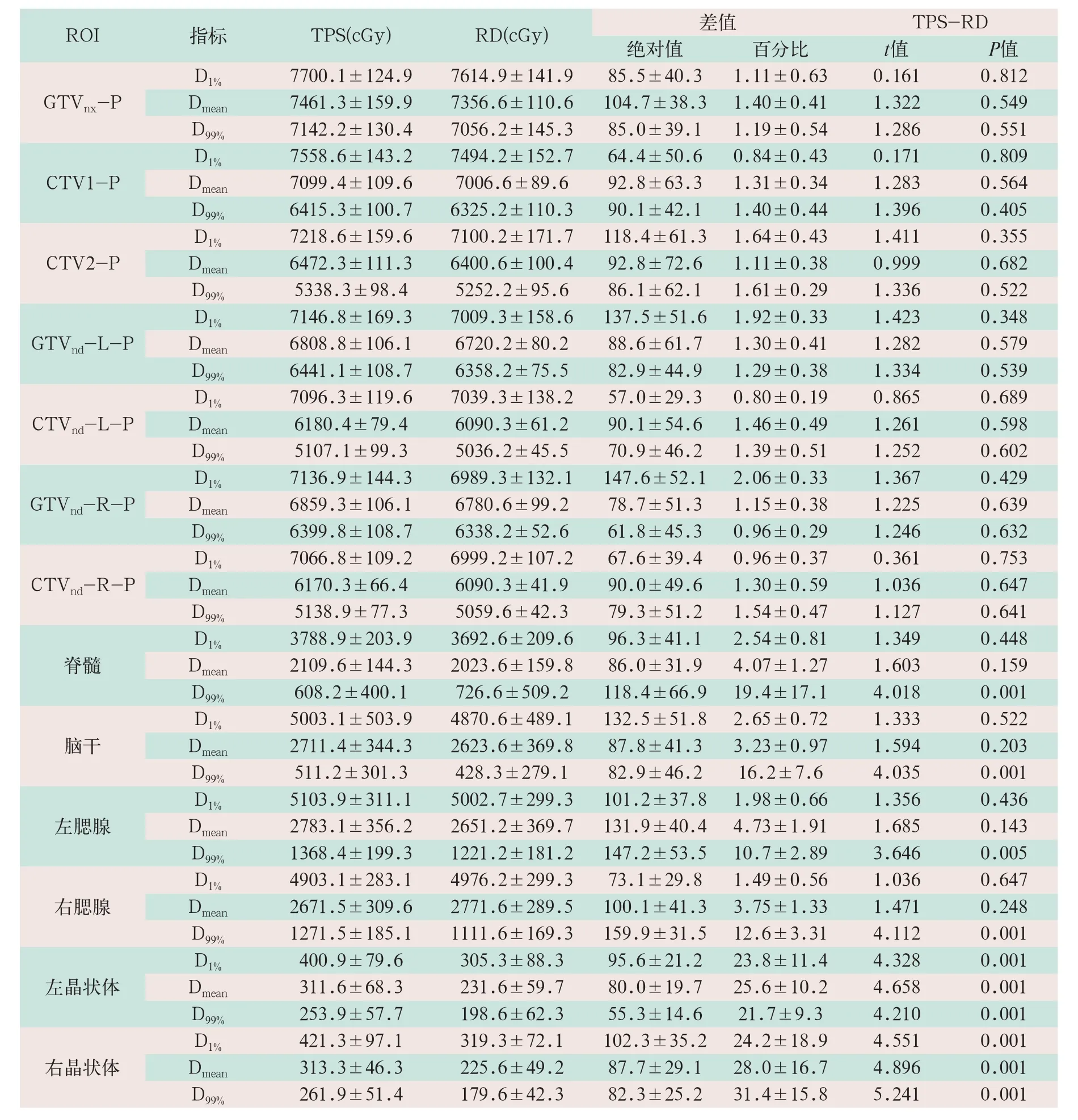
表2 靶区和OAR的TPS-RD绝对剂量比较(±s)
注:表中ROI为感兴趣区域;TPS为治疗计划系统;RD为实测重建剂量的绝对值;TPS-RD为治疗计划系统和实测重建剂量的绝对剂量比较
ROI 指标 TPS(cGy) RD(cGy) 差值 TPS-RD绝对值 百分比 t值 P值GTVnx-P D1% 7700.1±124.9 7614.9±141.9 85.5±40.3 1.11±0.63 0.161 0.812 Dmean 7461.3±159.9 7356.6±110.6 104.7±38.3 1.40±0.41 1.322 0.549 D99% 7142.2±130.4 7056.2±145.3 85.0±39.1 1.19±0.54 1.286 0.551 CTV1-P D1% 7558.6±143.2 7494.2±152.7 64.4±50.6 0.84±0.43 0.171 0.809 Dmean 7099.4±109.6 7006.6±89.6 92.8±63.3 1.31±0.34 1.283 0.564 D99% 6415.3±100.7 6325.2±110.3 90.1±42.1 1.40±0.44 1.396 0.405 CTV2-P D1% 7218.6±159.6 7100.2±171.7 118.4±61.3 1.64±0.43 1.411 0.355 Dmean 6472.3±111.3 6400.6±100.4 92.8±72.6 1.11±0.38 0.999 0.682 D99% 5338.3±98.4 5252.2±95.6 86.1±62.1 1.61±0.29 1.336 0.522 GTVnd-L-P D1% 7146.8±169.3 7009.3±158.6 137.5±51.6 1.92±0.33 1.423 0.348 Dmean 6808.8±106.1 6720.2±80.2 88.6±61.7 1.30±0.41 1.282 0.579 D99% 6441.1±108.7 6358.2±75.5 82.9±44.9 1.29±0.38 1.334 0.539 CTVnd-L-P D1% 7096.3±119.6 7039.3±138.2 57.0±29.3 0.80±0.19 0.865 0.689 Dmean 6180.4±79.4 6090.3±61.2 90.1±54.6 1.46±0.49 1.261 0.598 D99% 5107.1±99.3 5036.2±45.5 70.9±46.2 1.39±0.51 1.252 0.602 GTVnd-R-P D1% 7136.9±144.3 6989.3±132.1 147.6±52.1 2.06±0.33 1.367 0.429 Dmean 6859.3±106.1 6780.6±99.2 78.7±51.3 1.15±0.38 1.225 0.639 D99% 6399.8±108.7 6338.2±52.6 61.8±45.3 0.96±0.29 1.246 0.632 CTVnd-R-P D1% 7066.8±109.2 6999.2±107.2 67.6±39.4 0.96±0.37 0.361 0.753 Dmean 6170.3±66.4 6090.3±41.9 90.0±49.6 1.30±0.59 1.036 0.647 D99% 5138.9±77.3 5059.6±42.3 79.3±51.2 1.54±0.47 1.127 0.641脊髓D1% 3788.9±203.9 3692.6±209.6 96.3±41.1 2.54±0.81 1.349 0.448 Dmean 2109.6±144.3 2023.6±159.8 86.0±31.9 4.07±1.27 1.603 0.159 D99% 608.2±400.1 726.6±509.2 118.4±66.9 19.4±17.1 4.018 0.001脑干D1% 5003.1±503.9 4870.6±489.1 132.5±51.8 2.65±0.72 1.333 0.522 Dmean 2711.4±344.3 2623.6±369.8 87.8±41.3 3.23±0.97 1.594 0.203 D99% 511.2±301.3 428.3±279.1 82.9±46.2 16.2±7.6 4.035 0.001左腮腺D1% 5103.9±311.1 5002.7±299.3 101.2±37.8 1.98±0.66 1.356 0.436 Dmean 2783.1±356.2 2651.2±369.7 131.9±40.4 4.73±1.91 1.685 0.143 D99% 1368.4±199.3 1221.2±181.2 147.2±53.5 10.7±2.89 3.646 0.005右腮腺D1% 4903.1±283.1 4976.2±299.3 73.1±29.8 1.49±0.56 1.036 0.647 Dmean 2671.5±309.6 2771.6±289.5 100.1±41.3 3.75±1.33 1.471 0.248 D99% 1271.5±185.1 1111.6±169.3 159.9±31.5 12.6±3.31 4.112 0.001左晶状体D1% 400.9±79.6 305.3±88.3 95.6±21.2 23.8±11.4 4.328 0.001 Dmean 311.6±68.3 231.6±59.7 80.0±19.7 25.6±10.2 4.658 0.001 D99% 253.9±57.7 198.6±62.3 55.3±14.6 21.7±9.3 4.210 0.001 D1% 421.3±97.1 319.3±72.1 102.3±35.2 24.2±18.9 4.551 0.001 Dmean 313.3±46.3 225.6±49.2 87.7±29.1 28.0±16.7 4.896 0.001 D99% 261.9±51.4 179.6±42.3 82.3±25.2 31.4±15.8 5.241 0.001右晶状体
2 结果
2.1 靶区和OAR的γ通过率比较
γ通过率TPS-CD均>97.5%,TPS-RD均>95%,且TPS-CD均大于TPS-RD。两者靶区的γ通过率比较差异均具有统计学意义(t=2.110,t=2.749,t=2.489,t=2.687,t=2.798,t=2.881,t=2.921;P<0.05),OAR比较则差异无统计学意义,见表1。
2.2 靶区和OAR的TPS-RD绝对剂量比较
TPS-RD的靶区D1%、Dmean及D99%三项指标绝对剂量差异均无统计学意义;左右晶状体三项指标绝对剂量差异均有明显统计学意义(t=4.328,t=4.658,t=4.210,t=4.511,t=4.896,t=5.241;P<0.05);脊髓、脑干、左右腮腺等OAR的D99%差异有明显统计学意义(t=4.018,t=4.035,t=3.646,t=4.112;P<0.05);Dmean和D1%差异均无统计学意义,见表2。
3 讨论
近20年来,放射治疗技术发展日新月异,剂量精确性要求越来越高,验证方法已由传统的二维发展为三维。三维剂量验证优势明显,不仅可以探测剂量传递中或者TPS的错误,还可以在患者图像中立体显示剂量偏差分布,因此作为三维剂量验证设备之一的Compass已经得到了广泛的运用[12,3]。该系统由探测器和软件两部分组成,探测器是由1020个平行电离室组成的MatriXX矩阵,测量有效面积为24.2 cm×24.2 cm,灵敏度体积为0.07 cm3,间距7.62 mm。软件部分由Beam Commissioning、Detector Commissioning以及Patient 3D Dosimetry组成。①Beam Commissioning模块的功能是拟合直线加速器剂量学模型,包括百分深度剂量、离轴比曲线和因子及输出因子等因素;②Detector Commissioning模块的功能是在验证之前标定MatriXX矩阵的几何位置和电离室的绝对剂量;③Patient 3D Dosimetry模块可利用其自带的卷积/超分割算法(collasped cone convolution,CCC)对TPS的原始计划进行独立计算,即基于TPS数据重新计算剂量,也就是CD,此外还可将MatriXX矩阵固定于机头上,实际照射后采集注量图和角度信息后基于CCC算法重建出三维剂量分布,也就是RD。
本研究中,Compass三维验证系统和Monaco在使用之前都必须与相应的直线加速器模型拟合,建模和数据拟合的过程中必然会产生误差,且Monaco使用的MC算法与Compass的CCC算法也存在误差,两种误差最终体现出来的是TPS-CD之间的γ通过率,各ROI在TPS-CD的γ通过率都在97.5%以上,表明上述两种误差带来的影响较小。各ROI在TPS-RD的γ通过率均低于TPS-CD,这是因为影响TPS-RD的γ通过率原因除了与TPS-CD共同因素之外还有验证时Compass摆位精度、直线加速器MLC走位与机架旋转精度、剂量标定与剂量率的准确性等因素。靶区相关ROI的两组γ通过率比较具有统计学意义,这是因为靶区所在空间为高剂量区域且剂量梯度落差大,较多的参考点无法在半径为3 mm的球体空间匹配到剂量相同的点,双侧颈部淋巴转移区及其预防照射区的γ通过率低于原发肿瘤相关靶区,考虑是由于其所处空间毗邻皮肤,因剂量建成的原因导致一定的剂量误差[13]。OAR相关ROI的两组γ通过率比较无统计学意义,是因为其所在空间为低剂量区且剂量梯度落差小,基于上述原因有较高的γ通过率。
本研究对TPS-RD绝对剂量进行了统计对比,虽然绝对剂量对比体现的只有局部,临床实际应用以体现全局对比的γ通过率验证为主,但仍可为剂量的精准实施进一步提供数据支持。通过表2可见靶区D1%、Dmean及D99%三项指标绝对剂量差均<200 cGy,百分差均<2.5%,且差异均无统计学意义,提示TPS的理论剂量和实际的重建剂量高度吻合。晶状体三项指标绝对剂量差异均有明显统计学意义,除晶状体外的OAR的D99%差异有统计学意义,Dmean和D1%差异均无统计学意义,所有OAR有统计学差异的指标均为低剂量区,但其绝对剂量差均<200 cGy,临床实际意义不大,临床应用中舍弃低剂量区绝对剂量的对比。本研究仅为17例患者资料,可能存在统计学偏差,且此类研究受所选患者的TNM分期、靶区勾画和计划制定的主客观差异、直线加速器的型号和性能以及TPS的型号等因素影响较大。基于以上原因,本研究所得验证数据可能与类似研究有一定的差距,故未做横向对比。
4 结语
通过本研究的分析,在使用Compass三维验证系统时,应综合考虑靶区复杂程度、ROI的体积及所处位置以及剂量梯度等因素,并以γ通过率验证为主、绝对剂量验证进一步提供数据支持。
