立体定向放射治疗计划不同剂量区间三维γ通过率分析
2022-01-07刘颖孙海涛邓青萍袁玲张红利徐瑶瑶张晓鹏王鑫石兴源
刘颖,孙海涛,邓青萍,袁玲,张红利,徐瑶瑶,张晓鹏,王鑫,石兴源
1.广州医科大学附属第五医院放射治疗科,广东广州510700;2.中山市中医院医学影像放疗室,广东中山528400;3.惠州市中心人民医院设备科,广东惠州516001
前 言
随着放射治疗(以下简称放疗)技术的发展,放疗在肿瘤治疗中的地位不断提升,放射治疗技术从最初的适形放射治疗,发展为调强放射治疗(IMRT[1])和容积调强放射治疗(VMAT)。立体定向放射治疗(SBRT)是比调强放射治疗精度要求更高和技术更复杂的放射治疗技术。IMRT治疗技术分为静态和动态调强两种,目前广泛使用的动态调强特点是保持机架角固定,多叶光栅(MLC)走位时同时出束,且不断调节射束强度[2],VMAT技术在IMRT技术上,加入机架角的旋转,因此IMRT 和VMAT 治疗计划执行前,需验证放疗计划剂量准确性,以确保MLC 的走位、射束强度等所有机械参数准确执行。SBRT 技术在VMAT 技术上,加入床角的旋转,即采用非共面照射技术[3],因此计划复杂度更高。IMRT 和VMAT 计划多采用FF(Flattening Filter)模式,而SBRT 计划采用FFF(Flattening Filter Free)模式,FFF 模式下,未使用均整块处理射束,使得出射的射束强度中间高,周围低[4],因此射线的特点与FF 有较大区别[5]。与FF 相比,FFF模式[6]具有高剂量率、机头散射低、漏射少、射野外剂量小等优势,这些优势使得FFF 模式下,靶区外剂量跌落更迅速,细小的误差都会导致较大的剂量差别,因此剂量验证的要求更高。SBRT 计划执行过程的可靠性受床旋转稳定性、机架旋转稳定性、旋转速度、剂量率稳定性、MLC 到位精度的准确性[7]等多种因素的影响。为保证SBRT 计划能够可靠执行,需在病人治疗前进行严格的治疗计划验证。目前能用于计划验证的设备较多,如ARCCHECK(Sun nuclear)[8]、OCTAVIUS(PTW)[9]、Delta4(Scandidos)[10]、基于EPID 的设备[11]等。这些设备都是以γ 通过率为计划验证[12]通过与否的指标,但目前绝大多数工作者只关注总的通过率,而未深入分析γ 通过率的特点。
IMRT 和VMAT 一般用于治疗靶区相对较大,单次剂量小的肿瘤,低剂量区和高剂量区的比例较均衡,SBRT 计划一般常用于治疗肿瘤较小的靶区,靶区处方剂量高,剂量跌落快,低剂量区的比例远大于高剂量区[13]。目前用γ通过率为指标,验证放疗计划实际执行时的剂量分布与TPS 计算的剂量分布是否一致,而根据γ值计算定义,低剂量区的γ值一般低于高剂量区的γ值,γ值越低,γ通过率越高,低剂量区的γ通过率高于高剂量区。因此,SBRT 计划中,低剂量区的γ通过率会掩盖高剂量区的γ通过率。在验证SBRT 计划时,靶区通过率容易被低剂量区的通过率所掩盖,且单次剂量越高,低剂量区剂量的变化越容易被过度归一[14],使得低剂量区的通过率越高,越容易掩盖靶区的通过率。为探究SBRT 计划剂量验证通过率的特征,先分析不同阈值下γ通过率的变化,然后再分析不同的剂量区间内γ通过率的特征,最后,为探究γ通过率对不同剂量区间内剂量改变的敏感性,以5%为梯度,修改不同剂量区间内的剂量,并重新计算剂量γ通过率,计算出敏感度。
1 材料与方法
SBRT 计划验证过程为将患者放疗计划移植到均匀水模体上,然后计算放射治疗计划系统(TPS)计算的水模体上三维剂量分布(Dt)与计划验证设备重建出的实际剂量分布(Dp)间的γ通过率。本实验中采用PTW 公司的OCTAVIUS 圆柱形均匀水模体,并用其配套的Verisoft 软件重建出经过OCTAVIUS 的实际剂量分布,最后在Matlab 中计算Verisoft 重建出的三维剂量(Dp)与TPS 计算的三维剂量(Dt)间的γ通过率,图1为验证过程示意图。

图1 三维计划验证过程Fig.1 Three-dimensional plan verification
1.1 三维计划验证过程
本实验所用直线加速器为美国Variance 公司的Trilogy(配备60 对多页光栅)[15],使用的TPS 系统为Eclipse13.6 治疗计划系统。三维验证设备为德国PTW 公司的OVTAVIUS 圆柱形均匀水模体、1600SRS[16]二维电离室矩阵及分析软件Verisoft。其中1600SRS 二维电离室矩阵由1 381 个液体电离室组成,电离室大小为0.003 cm3,电离室探测范围为15 cm×15 cm,中心6.5 cm×6.5 cm 区域内的电离室较密集,电离室间距为2.5 mm,外围电离室间距为5.0 mm。Verisoft 软件可将探测板采集到的二维剂量分布重建为三维剂量Dp,并可将重建的剂量以DICOM 格式导出。在验证前,需标定验证设备,使用的标定工具为比利时IBA 公司的指型电离室FC65G及DOSE1剂量仪,小水箱,及IBA公司的固体水一套。
PTW 三维计划验证时,首先用CT 扫描OVTAVIUS 模体,将此模体的CT 图像导入TPS 中,然后将患者计划移植到OVTAVIUS 模体CT 集上,得到患者验证计划,将此验证计划传入四维集成治疗控制台(4-D Intergrated Treatment Console, 4DCT)上,对准OVTAVIUS 模体中心与直线加速器等中心后,在直线加速器上执行患者验证计划,并同时使用1600SRS 二维电离室矩阵采集OVTAVIUS 模体中心层面的剂量分布,在Verisoft 软件中将1600SRS 采集到的二维剂量分布重建为三维剂量分布(Dp),并计算Dt与Dp的γ通过率,流程示意图见图2。

图2 不同阈值下计算γ通过率的区域示意图Fig.2 Regional diagrams of gamma passing rate calculated under different thresholds
由于SBRT 计划精度要求高,在剂量计算时,计算网格大小设置为1 mm[17],选用精度更高的AXB剂量计算算法[18]。剂量验证前,先刻度验证设备,刻度时,在治疗床上放置5 块固体水,将指型电离室插入固体水预留的插孔中,用指型电离室和IBA剂量仪测量出标准条件(SSD=100,射野大小(10×10)cm2,水下5 cm)下直线加速器出束200 MU 的剂量仪度数,再将剂量仪读数转换为绝对剂量。此绝对剂量用于刻度1600SRS 探测板,刻度过程为:首先匹配1600SRS 探测板中心电离室与加速器绝对剂量,将OCTAVIUS 模体置于治疗床上,调节好1600SRS 探测板,使探测板水平放置,在探测板上放置机架角置于0°,射野大小为(10×10)cm2,剂量率300 MU/min,出200 MU 射束。再导入1600SRS 探测板校准文件,匹配所有电离室与绝对剂量。在4DTC 上执行患者验证计划,用1600SRS 探测器采集SBRT 患者验证计划在OCTAVIUS中心层面的二维剂量分布,并根据此二维剂量分布,在Verisoft 软件中重建出患者验证计划在OCTAVIUS 中的三维剂量分布。SBRT 计划是非共面射野,但在实际执行过程中,仍保持床角0°[19],不同床角的射野分开保存,重建时在Verisoft 软件中输入对应的床角,以此重建出三维非共面的剂量分布。最后在Matlab中计算Verisoft重建出的三维剂量(Dp)与TPS计算的三维剂量(Dt)间的γ通过率。
1.2 γ通过率
γ值是对比TPS 计算的剂量分布和验证设备重建或采集的剂量分布一致性度量函数,也是目前最常用 于剂量 验证的 指 标[20],γ值的 计算公 式 如下所示:

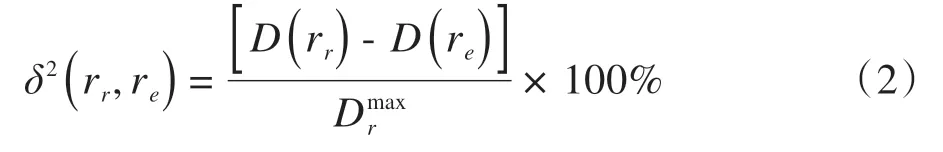
计算局部γ值时的计算公式如下所示:
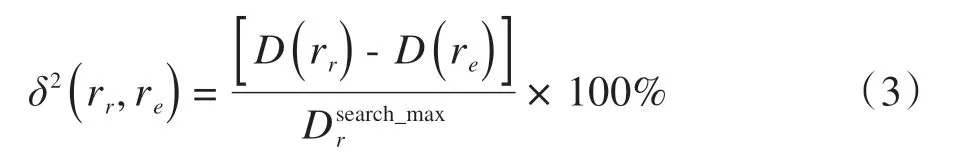
当γ小于1 时,认为参考图像与测量图像的两点间γ检测通过,将所有的γ值小于1 的点的总数目除以计算γ值的点的总数目,即为γ通过率,本文中分析全局γ通过率,计算γ值的点的总数目由阈值决定,阈值越小,计算γ值的点的总数目越多。
1.3 敏感度
为探究不同剂量区间内,γ通过率检测区间剂量改变的敏感性,用式(4)计算γ检测的敏感度:

其中,γ0指区间剂量未改变时的γ通过率,γc指区间剂量修改后的γ通过率。
1.4 实验过程
选取广州医科大学附属第五医院放射治疗科于2019年7月31日 至2021年3月31日执行的38 例SBRT 计划,并移植到OCTAVIUS 模体中生成验证计划,重建出验证计划实际执行时的三维剂量分布Dp,并将Dp 以DICOM 形式导出,将Dp 导入Matlab R2019a 中[21],根据γ验证定义,编写γ通过率函数,在Matlab 中首先计算不同阈值下Dp 与Dt 间的γ通过率,选择的阈值以10%为梯度递增,并以10%阈值的γ通过率作为基准值1,分析其他阈值的γ通过率与基准值1间是否有显著性差异,此过程可分析不同阈值对γ通过率的影响,过程如图2 所示。根据剂量跌落原理分析,离靶区越远,剂量跌落越慢,因此离靶区远的低剂量区域大于离靶区近的高剂量区域。
为分析不同剂量区间内γ通过率,将Dp 以10%分解成不同的剂量区间,分解示意图如图3 所示,计算不同剂量区间内γ通过率。随后对不同区间内的剂量以5%为梯度,增加不同剂量区间内的剂量,并计算区间剂量增加后剂量分布Dp'与Dt 间的γ通过率,并计算γ通过率探测不同剂量区间的剂量变化的敏感度,随后以11%~100%为基准值2,分析不同剂量区间的γ通过率与基准值2之间是否存在显著性差异。实验过程流程图如图4 所示,将Verisoft 导出的重建的三维剂量分布Dp与TPS导出的验证计划剂量分布Dt 导入Matlab,在Matlab 中分别计算不同阈值下和不同剂量区间的γ通过率,再单独修改某一剂量区间的剂量,再重新计算Dp'与Dt 间的γ通过率,并计算γ验证的敏感度。
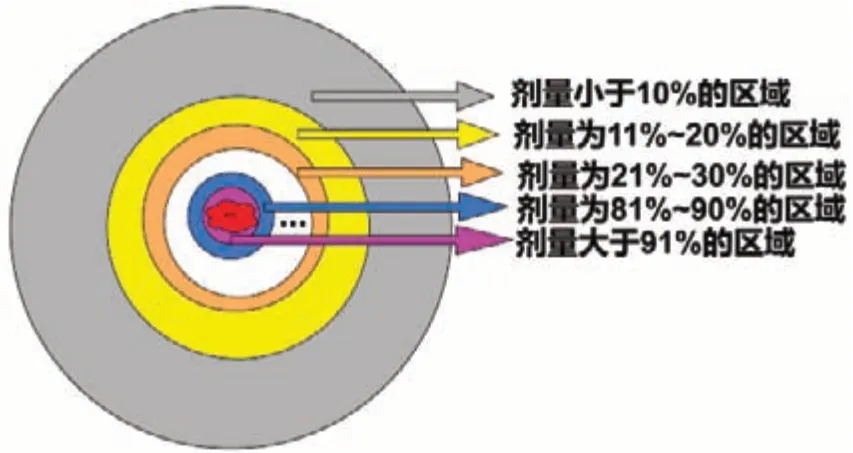
图3 不同剂量区间示意图Fig.3 Diagram of different dose ranges

图4 实验过程流程图Fig.4 Experimental flowchart
2 结果
2.1 不同阈值对γ通过率的影响
38 例SBRT 患者不同阈值γ通过率均值如表1 所示,3%/3 mm 标准下,当阈值大于40%后,γ通过率小于90%,在2%/3 mm 标准下,只有10%阈值的γ通过率大于90%,其他阈值下的γ通过率小于90%。2%/2 mm和3%/2 mm 标准下,所有阈值的通过率均小于90%。当搜索区域为2 mm 时,γ通过率普遍偏低,造成此结果的可能因素包括:首先,在执行验证计划时,摆放模体的等中心与TPS 扫描时的模体等中心间存在误差;其次,由于未进行插值处理,且剂量计算网格大小为1.25 mm,所以当搜索域为2 mm 时,对于测量图像中的某点,只能在参考图像中找到一个点来计算γ值,因此会降低γ通过率。图5 为不同阈值γ通过率箱线图,从图中可看出,3%/3 mm、3%/2 mm、2%/3 mm及2%/2 mm 标准下,阈值大于41%后的通过率波动较大。γ通过率均值曲线图分别如图6 所示,从图6中可看出,不同γ标准下,γ通过率随着阈值的增大逐步减小,到阈值为50%后,γ通过率普遍较低,变化较小,在临床治疗过程中,将剂量大于50%的称为照射区,此结果说明照射区内的剂量通过率普遍较低,在照射区外,尤其是低剂量区内的剂量通过率较高。以10%阈值的通过率作为基准1,分析不同阈值的γ通过率与基准值1间是否存在显著差异,首先分析数据分布特征,由于数据不服从正态分布,故采用非参检验,检验结果显示所有不同阈值下的γ通过率与基准值1间非参检验P值都为0,即都存在显著性差异。
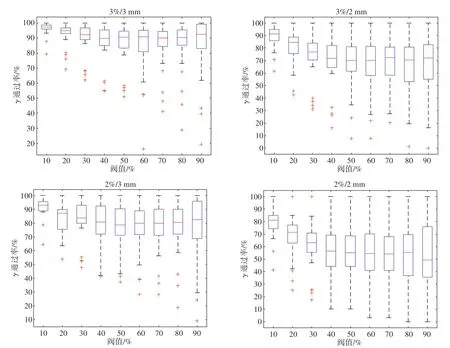
图5 不同γ标准下不同阈值的剂量验证γ通过率箱线图Fig.5 Boxplots of gamma passing rates in dose verification under different thresholds and at different criteria
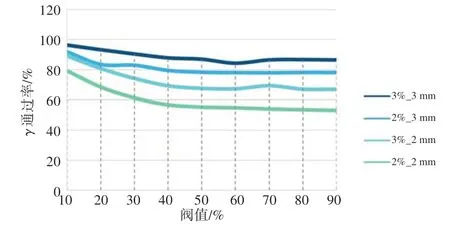
图6 不同阈值的γ通过率均值曲线图Fig.6 Histogram of mean gamma passing rate under different thresholds

表1 不同γ标准下不同阈值的γ通过率的均值和方差(%)Tab.1 Mean and variance of gamma passing rates under different thresholds and at different criteria (%)
2.2 不同剂量区间的γ通过率
38例SBRT患者不同剂量区间γ通过率均值曲线图如图7 所示。从图7 可看出,γ通过率均值成下降趋势,且到51%以上γ通过率均值保持基本不变。为进一步分析,图8 为不同剂量区间的γ通过率的箱线图,从图8可看出,若以10%阈值的γ通过率作为基准数据,则11%~20%剂量区间的γ通过率高于基准数据,且波动性更小。剂量大于41%的所有区间的γ通过率均不同程度低于基准数据,且波动性较大,这可能与靶区大小有关。从表2 可看出,搜索范围越小时,γ通过率越低,但低剂量区的受影响程度远低于高剂量区。由于本实验中,并未对参考剂量和测量剂量进行插值和配准处理,得到的是最原始的剂量分布的γ通过率,因此结果会比PTW 配置的Verisoft计算出的结果低。表2 显示所有γ标准下剂量大于51%的区间通过率均低于90%,临床上将50%的处方剂量包绕的区域定义为照射区,由于最大剂量一般大于处方剂量,因此51%最大值包绕的区域在照射区以内,即说明照射区以内的平均γ通过率小于90%,在3%/3 mm 标准下,10%阈值下γ通过率均值为96.4%,11%~20%和21%~30%剂量区间的通过率均值分别为98.44%和95.84%,均大于95%,31%~40%和41%~50%剂量区间的通过率均值分别为93.52%和90.15%,均大于90%,而照射区内,剂量通过率的均值均低于90%,且波动性极大。2%/3 mm 标准下,10%阈值下γ通过率均值为92.09%,而只有11%~20%和21%~30%的γ通过率高于90%,其余区间的通过率均低于90%。4 种标准下,γ通过率随着剂量增加,各区间内的γ通过率呈下降趋势,且高剂量区的通过率明显低于低剂量区。由于数据不服从正态分布,将10%~100%的数据作为基准数据,经非参检验后,其结果显示P值都为0,即都存在显著性差异。
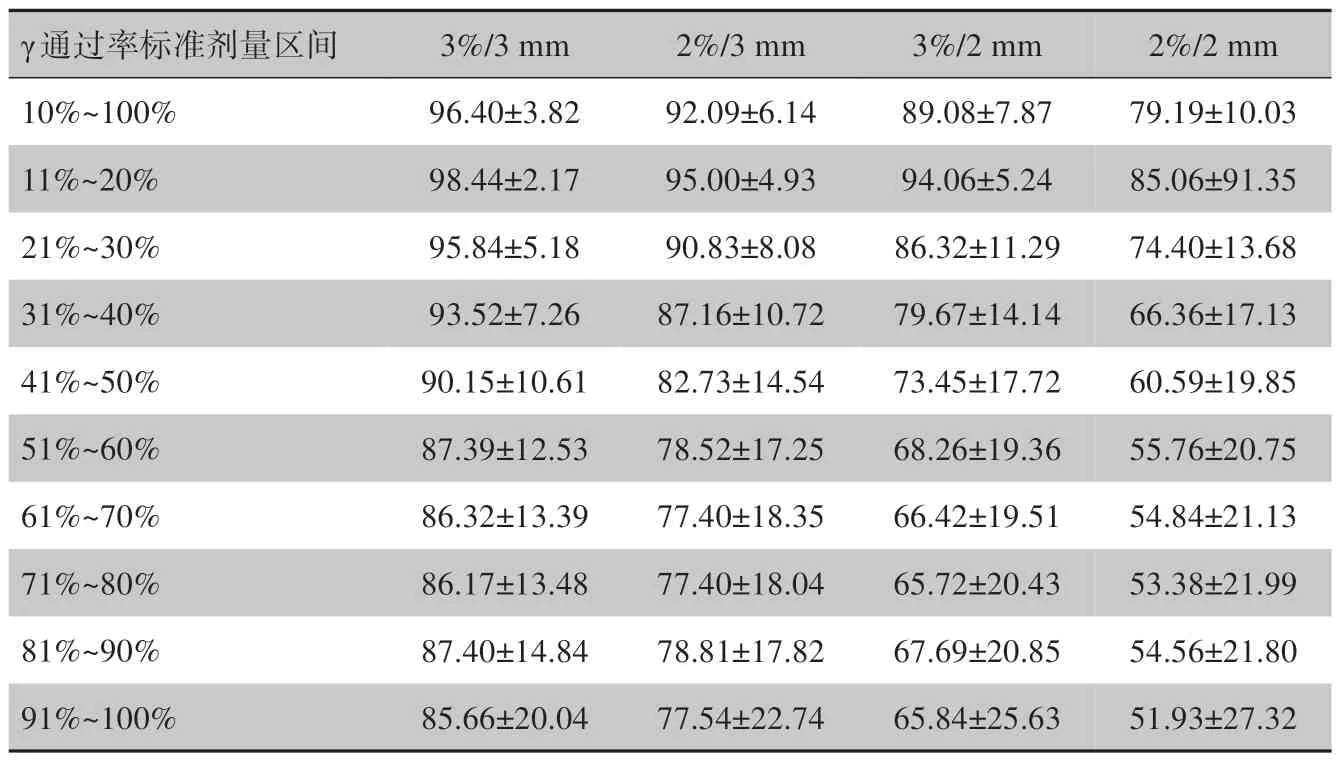
表2 不同γ标准下γ通过率的均值和方差Tab.2 Mean and variance of gamma passing rate at different criteria
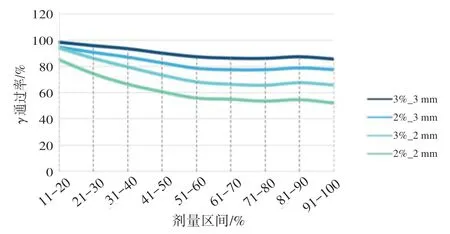
图7 不同剂量区间γ通过率均值曲线图Fig.7 Mean gamma passing rates in different dose ranges
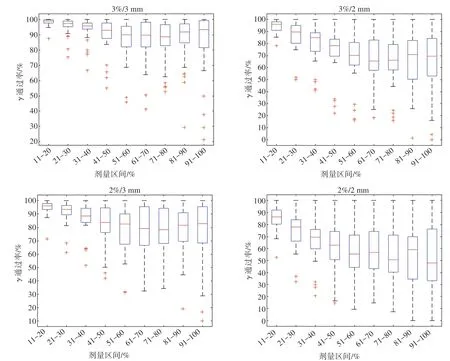
图8 不同剂量区间的γ通过率箱线图Fig.8 Boxplots of gamma passing rate in different dose ranges
2.3 不同剂量区间内γ通过率对剂量改变的敏感性
为进一步研究不同区间内,γ通过率对剂量改变的敏感性,以5%的梯度增加不同区间内的剂量,然后计算区间剂量增加后的10%~100%范围内的γ通过率,再根据敏感度计算公式,得出不同剂量区间剂量改变时γ通过率检测的敏感度。从阈值和区间剂量γ通过率的趋势分析,不同标准下的γ通过率的变化趋势相似,因此在探究剂量改变对γ通过率影响时,只分析了3%/2 mm 标准下γ通过率对剂量改变的敏感度。以5%为梯度增加特定剂量区间内的剂量,增加到50%止。图9为不同剂量区间内剂量增加后γ通过率变化的曲线图,从图中可看出11%~20%剂量区间内剂量增加对γ通过率的影响较大,21%~30%区间内剂量增加也会产生影响,但影响程度远小于11%~20%;31%~40%区间内剂量增加对γ通过率稍有影响,大于41%剂量区间对γ通过率的影响很小。图10 为不同剂量区间内剂量增加后γ通过率变化的均值箱线图,从图10 可看出,增加11%~20%剂量区间的剂量时,γ通过率变化较大,波动也较大,21%~30%区间的剂量变化对γ通过率的影响小于11%~20%,剂量大于61%的所有剂量区间内剂量的增加对γ通过率的影响都较小。图11 为不同剂量区间内剂量增加后γ通过率变化箱线图,从图中可看出,11%~20%区间内,随剂量的增加,γ通过率先快速降低,后又升高,剂量增加对γ通过率的影响非常明显。21%~30%区间γ通过率随区间剂量增加呈现先下降后基本保持不变的规律,当剂量增加30%以上后,γ通过率基本保持不变。31%~40%剂量区间内,剂量增加对γ通过率的影响较小,在增加20%之内,γ通过率稍有降低,当剂量增加大于20%后,γ通过率基本保持不变。剂量大于41%的所有区间内,剂量增加对γ通过率的影响都较小。
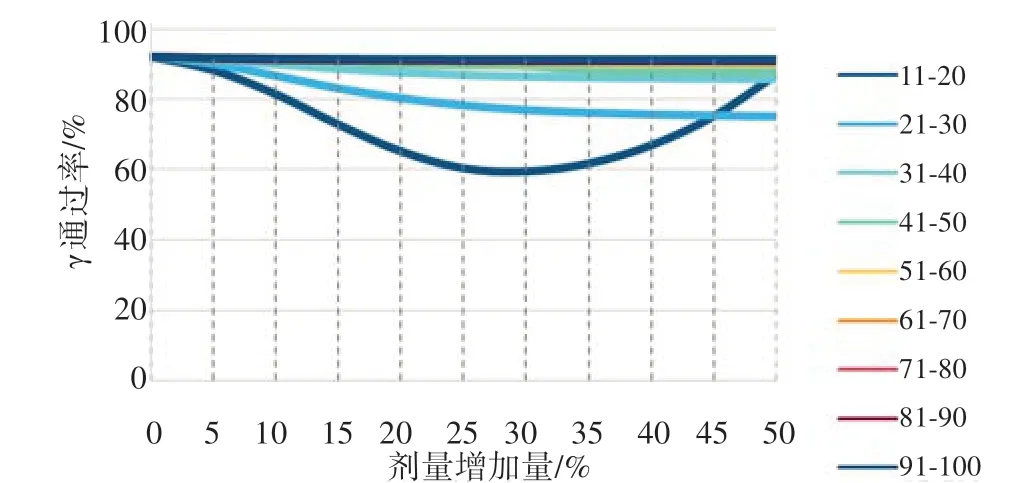
图9 不同剂量区间内剂量增加后γ通过率曲线图Fig.9 Mean gamma passing rates in different dose range after dose increase
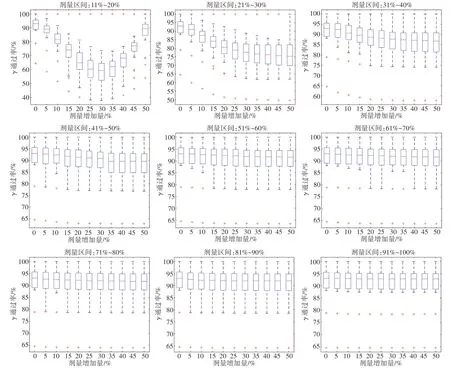
图10 不同剂量区间内剂量增加后γ通过率箱线图Fig.10 Boxplots of gamma passing rate in different dose ranges after dose increase

图11 不同剂量区间内剂量增加后γ通过率均值箱线图Fig.11 Boxplots of mean gamma passing rate in different dose ranges after dose increase
为进一步分析不同剂量区间内剂量增加对γ通过率的影响,计算γ对剂量增加的敏感度。按照敏感度计算公式,得到γ通过率对不同剂量区间剂量增加的敏感度,并分析剂量增加后的γ通过率与原γ通过率是否存在显著性差异。图12 为γ通过率对不同剂量区间剂量增加敏感度箱线图,从图中可看出γ通过率对低剂量区的剂量改变较敏感,尤其是11%~20%剂量区间内剂量的增加敏感,对21%~30%和31%~40%区间内的敏感度稍弱,但对剂量大于51%的剂量区间内剂量的增加基本不敏感。

图12 γ通过率对不同剂量区间剂量增加敏感度箱线图Fig.12 Sensitive of gamma passing rate to the dose increase in different dose ranges
3 讨论
在临床工作中,SBRT 技术是常用于无法手术或不愿接受手术治疗的肿瘤患者的有效治疗手段之一,而SBRT技术比调强技术更复杂,因此SBRT计划剂量验证应比调强计划剂量验证要求更高。从实验结果可看出,γ通过率对41%以上剂量区间内的剂量改变不敏感,因此验证SBRT 计划剂量时,临床工作者不应只看γ通过率,而应透彻了解γ通过率的计算过程及特点,当得到不同的γ通过率时,应分析γ值低的原因,并评估其可能造成的影响。从实验结果可看出,高剂量区的剂量改变对γ通过率的影响较小。
除本实验中考虑的影响因素外,还有其他因素会影响γ通过率。首先,目前所有的放疗计划剂量验证都是将病人的治疗计划移植到均匀水模体中生成验证计划,但是从剂量计算算法来看,病人体内的剂量计算除蒙特卡罗算法外,大多数的算法都是根据CT值,将水吸收剂量转换为相应组织吸收剂量,剂量计算时,非均匀性校准一直是剂量计算中的重点和难点。因此,应该使用相应的剂量验证设备,能验证将病人的治疗计划移植到非均匀模体上,并验证采集的非均匀模体的剂量及重建剂量与TPS 计算的剂量的γ通过率。其次,计算剂量差异时,在参考图像的搜索范围,当搜索范围越大时,可对比的点数越多,可能会降低γ值,从而提高γ通过率。第三,是否对剂量分布进行插值处理,当进行插值处理时,应分析对参考图像或测量图像,还是两者都进行了插值处理,若只对参考图像进行插值处理,则相当于测量点可在参考图像中寻找的对比点更多,理论上会提高γ通过率,若对测量图像进行插值处理,则相当于需计算γ值点的总数增多,而低剂量区的点增加量远多于高剂量区,理论上也会提高γ通过率,因此,应充分了解验证设备是否进行了插值处理,用的是何种插值算法,插值给γ通过率会造成哪些影响。第四,配准的影响,在做剂量验证时,首先要将参考图像和测量图像配准后,才能完成γ值的计算,当配准精度不够时,可能会降低γ通过率。
SBRT 计划常用于治疗靶区较小的病灶,且靶区内的剂量远高于靶区外剂量,因此,常会得到较高的全局γ通过率,因为全局γ计算时,将剂量差异归一到全局最大值,势必会减小剂量差异影响,此时靶区外的点的γ值都偏低,且SBRT计划中靶区小,靶区外的点远远多于靶区内的点,因此会拉高全局γ通过率。因此,对于SBRT计划,应关注不同剂量区间的γ通过率,再结合靶区特点,分析γ值高的点与靶区间的距离,以及该点是否属于重要器官或并联器官,并判断此点γ值偏高的影响。其次,靶区剂量越高时,对低剂量区的剂量改变越不敏感,若在靶区外有重要器官如脊髓、脑干等,应关注此结构对应的局部γ通过率。因此验证SBRT 计划γ通过率时,不能只单独看全局γ通过率,同时也要关注不同剂量区间的γ通过率。根据本文的实验结果,作者认为可以给每个剂量区间加入不同的权重,并得到最后的γ通过率,或者在做计划验证时,将γ通过率与解剖结构联系起来,给不同的结构相应的权重,得到加权后的γ通过率,用此γ通过率判断SBRT计划验证是否通过。
