低分子肝素治疗胎儿生长受限的临床疗效分析
2019-08-26沙梦晗陈素华亢庆玲张洋余楠李伟乌剑利肖娟
沙梦晗 陈素华 亢庆玲 张洋 余楠 李伟 乌剑利 肖娟
摘要:目的 分析低分子肝素治療胎儿生长受限的临床疗效。方法 选取2012年1月~2018年12月我院收治的60例胎儿生长受限(FGR)孕妇作为研究对象。根据治疗方案不同,分为对照组和实验组,各30例。对照组采用复方氨基酸及低分子右旋糖酐等治疗,实验组在对照组治疗的基础上给予低分子肝素,比较两组治疗前后孕周、胎儿生长指标、脐血流指标、羊水指标,实验组治疗前后D-D二聚体、血小板(PLT)、部分凝血活酶时间(APTT)、凝血酶原时间(PT)。结果 两组在治疗前后孕周差值比较,差异无统计学意义(P>0.05);两组胎儿生长指标、S/D比值、羊水指数、羊水最大前后径比较,差异无统计学意义(P>0.05);实验组治疗后APTT时间延长,与治疗前比较,差异有统计学意义(P<0.05),D-D二聚体、PLT、PT与治疗前比较,差异无统计学意义(P>0.05)。结论 低分子肝素对胎儿生长受限与传统治疗相比并没有明显优势,临床使用尚存在争议。
关键词:低分子肝素;胎儿生长受限;胎儿生长指标
中图分类号:R714.5 文献标识码:A DOI:10.3969/j.issn.1006-1959.2019.14.020
文章编号:1006-1959(2019)14-0061-04
Abstract:Objective To analyze the clinical efficacy of low molecular weight heparin in the treatment of fetal growth restriction.Methods 60 pregnant women with fetal growth restriction (FGR) admitted to our hospital from January 2012 to December 2018 were selected as subjects. According to different treatment options, they were divided into control group and experimental group, 30 cases each. The control group was treated with compound amino acid and low molecular weight dextran. The experimental group was given low molecular weight heparin on the basis of the control group. The gestational weeks before and after treatment, fetal growth index, umbilical blood flow index and amniotic fluid index were compared before and after treatment. DD dimer, platelet (PLT), partial thromboplastin time (APTT), prothrombin time (PT).Results There was no significant difference in gestational age difference between the two groups before and after treatment (P>0.05),there were no significant differences in fetal growth index, S/D ratio, amniotic fluid index, and amniotic fluid maximum anteroposterior diameter between the two groups (P>0.05). The APTT time in the experimental group was prolonged. Compared with before treatment, the difference was statistically significant (P<0.05). There was no significant difference between D-D dimer, PLT and PT before treatment (P>0.05).Conclusion Low molecular weight heparin has no obvious advantages compared with traditional treatment for fetal growth restriction. The clinical use is still controversial.
Key words:Low molecular weight heparin;Fetal growth restriction;Fetal growth index
胎儿生长受限(fetal growth restriction,FGR),也称宫内生长受限(intrauterine growth restriction,IUGR),是指胎儿应有的生长潜力受损,估测的胎儿体重小于同孕龄体重第10百分位数的SGA(小于孕龄儿)。FGR是一种常见的妊娠并发症,与多种不良围产期结局有关,导致新生儿围产期发病率和死亡率升高[1],出生后面临许多短期和(或)长期的问题,包括围产期窒息、胎粪吸入、生长发育迟缓及神经发育异常等[2]。临床上普遍采用休息吸氧、补充氨基酸、滴注右旋糖酐等方法,但其治疗效果不确切,目前对于FGR治疗尚未形成临床上广泛认可规范,因此如何更有效地早期干预FGR仍需进一步研究。近年来有研究将低分子肝素用于治疗FGR,但疗效评价不一[3]。本研究回顾性分析我院FGR患者传统治疗组和加用低分子肝素组的临床资料,评估低分子肝素治疗FGR的可行性,现报道如下。
1资料与方法
1.1一般资料 选取2012年1月~2018年12月于华中科技大学同济医学院附属同济医院收治的60例FGR孕妇为研究对象,根据治疗方案的不同,分为对照组和实验组,每组30例。实验组孕妇年龄21~40岁,平均年龄(29.43±4.74)岁,孕周27~35周,平均孕周(32.20±2.17)周;对照组年龄22~37岁,平均年龄(28.17±4.12)岁,孕周29~35周,平均孕周(32.14±1.75)周。FGR诊断标准:胎儿估测体重或腹围低于对应孕周正常值第10百分位数以下。纳入符合FGR诊断标准,无双胎妊娠,排除胎儿畸形和染色体异常等因素所致的内因性匀称型病例,无肝素使用禁忌证。
1.2方法 两组患者均加强营养、卧位休息、间断吸氧,并对母胎情况进行严密监护。对照组在上述治疗的基础上给予每日静滴氨基酸注射液(广东利泰药业有限公司,国药准字H20068041)250 ml及复方右旋糖酐40注射液(山东华鲁制药有限公司,国药准字H20068041)500 ml治疗。实验组在对照组治疗方案的基础上,给予皮下注射低分子肝素4000 IU/d(赛诺菲<北京>制药有限公司,国药准字J20150059)。7 d为1疗程,治疗1~2个疗程。
1.3观察指标 比较两组孕周差值(治疗开始和结束时监测实际孕周与超声孕周,计算其差值即孕周差值);治疗前后胎儿生长指标:头围、腹围、胎头双顶径、股骨长度;脐血流指标(S/D比值)、羊水指数、羊水最大前后径;凝血指标:D-D二聚体、血小板计数(PLT)、凝血酶原时间(PT)、部分凝血活酶时间(APTT)。
1.4统计学方法 采用SPSS 23.0软件对数据进行统计学分析,经过正态性检验及方差齐性检验后,计数资料用(x±s)表示,采用两独立样本t检验,P<0.05表示差异有统计学意义。
2结果
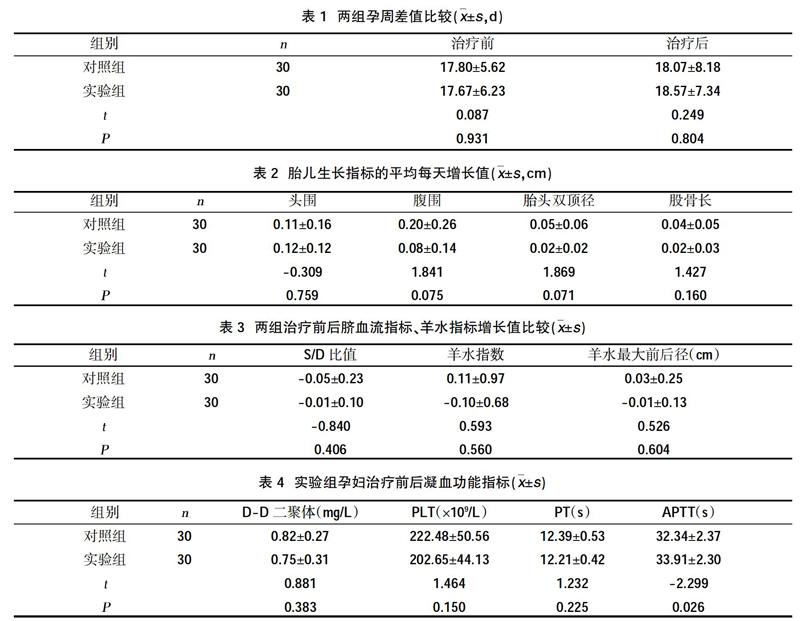
2.1两组治疗前后孕周差值的比较 两组孕妇治疗前后孕周差值比较,差异无统计学意义(P>0.05),见表1。
2.2两组治疗前后胎儿生长指标比较 两组治疗前后,胎儿头围、腹围、胎头双顶径、股骨长等胎儿生长指标的平均每天增长值比较,差异均无统计学意义(P>0.05),见表2。
2.3两组治疗前后脐血流指标、羊水指标增长值比较 两组孕妇治疗前后,S/D比值、羊水指数及羊水最大前后径的增长值比较,差异无统计学意义(P>0.05),见表3。
2.4实验组孕妇治疗前后凝血功能指标比较 肝素组孕妇治疗前后的D-D二聚体、PLT、PT比较,差异无統计学意义(P>0.05)。APTT治疗后时间延长,与治疗前比较,差异有统计学意义(P<0.05),见表4。
3讨论
FGR病因复杂不明,可以概括为母体、胎盘和胎儿三个方面。患有母体疾病如妊娠期糖尿病、肾功能不全、自身免疫性疾病、妊娠相关高血压疾病等,药物滥用如吸烟、饮酒,致畸物暴露以及宫内感染等,其FGR风险增加[4]。胎盘因素则是由于胎盘各种病变导致子宫胎盘血流量减少,胎儿供血不足。基因或染色体异常、结构异常也与胎儿生长受限有关,其中以三体综合征最为常见[5]。导致FGR的原因近1/3为遗传因素,2/3与胎儿生长环境有关[6]。ACOG最新临床指南提出,虽然FGR的主要病理生理机制不同,但它们大多指向共同的结果:子宫-胎盘灌注不足,胎儿营养供应减少[5]。研究发现[7,8],在胎儿生长受限患者中,胎盘绒毛内血管床减少,绒毛间血栓,胎盘绒毛膜炎,导致绒毛血管间的物质转运受阻,子宫-胎盘供血不足,从而影响胎儿的宫内生长发育。
正确识别FGR是对其进行有效治疗的前提和基础。FGR是生长潜力受损的小于孕龄儿(small for gestation age,SGA),但并非所有SGA均为FGR,且并非所有FGR均为SGA,二者不能完全等同。一项研究提出了胎儿生长受限的新定义,该定义不仅仅基于低于某一百分位数的出生体重,还包括与生长相关的其他胎儿和新生儿变量,以便更好地正确识别胎儿生长受限[9],这可能为今后的临床工作开展一项新思路。
目前对FGR的预防和治疗还很有限,临床重点在于寻找病因、改善胎盘循环、加强胎儿监测、改善新生儿结局。对临床怀疑FGR的孕妇应尽可能找出可能的致病原因。因母体因素引起的FGR,应及时治疗原发病,戒烟戒酒,使FGR的风险降到最低。JOGC临床指南指出对于有高危因素的孕妇,建议孕早期起服用低剂量阿司匹林[10],最近一项荟萃分析的结果也支持了这项指南:孕早期服用阿司匹林可适度降低高危妇女发生FGR的风险[11]。对于无法找到病因的FGR孕妇,尽管现在临床上采用多种治疗,但目前缺乏充分的证据支持卧床休息、常规吸氧、增加饮食对治疗FGR有效,尚未证实补充孕激素、静脉补充营养和注射低分子肝素对治疗FGR有效[1]。因此,肝素因其抗凝、抗炎、补体激活、促血管生成[12]等特性用于胎儿生长受限的应用研究。本次研究就低分子肝素治疗FGR是否有效进行探索。
研究表明[13-16],低分子肝素可改善胎盘血流,促进胎儿生长,可能有助于治疗胎儿生长受限,这四项研究中的FGR孕妇数量在46~104例,其中一项研究设计了对照组、实验组和健康组三个组别[16]。在设计的治疗方法上,其中两项实验为常规治疗加复方丹参液对比常规治疗加LMWH[13,16],一项实验为常规治疗与LMWH对比[15],另外一项实验为常规治疗与常规加低分子肝素进行比较[14]。四项研究的观察指标为胎儿生长情况、羊水指数、脐动脉血流情况、新生儿结局及凝血功能等指标中几项不等,观察结局为所有指标均显示肝素组的结局显著优于对照组。
然而,几项多中心随机对照试验的研究结果存在差异。除了一项研究是以胎儿生长受限作为单独的观察结果[17],其他的随机对照试验都是以妊娠并发症(包括FGR)的复合结局为观测指标[18-21],其中胎儿生长受限为研究的主要或次要观察结果。其中一项研究表明,低分子肝素有效降低了胎盘介导的妊娠并发症(包括FGR),但与对照组相比,肝素组孕妇分娩时的孕龄和新生儿体重没有明显差别[20],而其他四项随机对照试验得出结论[17-19,21]:与对照组相比,未观察到低分子肝素对胎儿生长受限的积极作用。另外一项多中心试验数据的荟萃分析显示低分子肝素并没有显著降低复发性胎盘介导的妊娠复合结局风险[22]。然而,试验质量对这些结果也有影响,单中心和多中心试验之间存在异质性;仅考虑来自多中心试验的数据时,低分子肝素没有明显的效果。还有研究发现,与单用阿司匹林相比,低分子肝素加阿司匹林的胎盘介导的妊娠并发症(包括FGR)没有差异[23]。
本次研究中,两组孕妇治疗前后孕周差值、各项胎儿生长指标平均增长值、羊水指标以及S/D比值平均增长值比较,差异均无统计学意义(P>0.05),表明低分子肝素对FGR的治疗无明显效果,但由于研究规模小,无法排除低分子肝素对FGR轻微有益或有害的影响。另外低分子肝素不会穿过胎盘,具有良好的母体安全性[24],肝素组治疗前后的凝血指标结果(P>0.05)基本支持了这一点。目前发表的许多研究结果不一致,可能与研究对象孕周、肝素类型、对照药物以及给药剂量和方式不同有关,与实验人群的异质性、纳入和排除标准不同等也有关系。另外,胎儿生长受限有多种病因和复杂的病理生理机制,可能导致研究的选择偏倚。因此,低分子肝素对于胎儿生长受限是否有效,需要更多可靠的临床数据,更多高质量的临床研究来进一步探讨。另外更好地了解疾病的机制将有望为更有效的干预措施提供背景,以预防胎儿生长受限的发生和改善预后,这也是今后研究胎儿生长受限的重要方向。
参考文献:
[1]Audette MC,Kingdom JC.Screening for fetal growth restriction and placental insufficiency[J]. Semin Fetal Neonatal Med,2018,23(2):119-125.
[2]Sharma D,Farahbakhsh N,Shastri S,et al.Intrauterine growth restriction-part 2[J].The Journal of Maternal-Fetal & Neonatal Medicine,2016,29(24):4037-4048.
[3]Skeith L.Low-molecular-weight heparin for the prevention and treatment of placenta-mediated pregnancy complications:The tides have shifted[J].Thromb Res,2018(170):207-208.
[4]Vayssière C,Sentilhes L,Ego A,et al.Fetal growth restriction and intra-uterine growth restriction: guidelines for clinical practice from the French College of Gynaecologists and Obstetricians[J].Eur J Obstet Gynecol Reprod Biol,2015(193):10-18.
[5]Bulletin AP.Fetal Growth Restriction[J].Obstetrics & Gynecology,2019,133(2):e97-e109.
[6]Sharma D,Shastri S,Farahbakhsh N,et al.Intrauterine growth restriction-part 1[J].J Matern Fetal Neonatal Med,2016,29(24):3977-3987.
[7]劉伯宁.胎儿宫内发育迟缓的胎盘病理变化[J].中国实用妇科与产科杂志,2002,18(1):19-20.
[8]Zhang S,Regnault TR,Barker PL,et al.Placental adaptations in growth restriction[J].Nutrients,2015,7(1):360-389.
[9]Beune IM,Bloomfield FH,Ganzevoort W,et al.Consensus Based Definition of Growth Restriction in the Newborn[J].J Pediatr,2018(196):71-76,e1.
[10]Lausman A,McCarthy FP,Walker M,et al.Screening,diagnosis,and management of intrauterine growth restriction[J].J Obstet Gynaecol Can,2012,34(1):17-28.
[11]Roberge S,Nicolaides K,Demers S,et al.The role of aspirin dose on the prevention of preeclampsia and fetal growth restriction:systematic review and meta-analysis[J].Am J Obstet Gynecol,2017,216(2):110-120.e6.
[12]Groom KM,David AL.The role of aspirin,heparin,and other interventions in the prevention and treatment of fetal growth restriction[J].Am J Obstet Gynecol,2018,218(2S):S829-S840.
[13]张佩玲.低分子肝素治疗胎儿生长受限的临床应用[J].中国当代医药,2014,21(7):55-59.
[14]梅耀玲.低分子肝素治疗胎儿生长受限的临床效果分析[J].中外医学研究,2019,17(2):8-10.
[15]王玉霞.应用低分子肝素治疗胎儿生长受限的效果观察[J].临床研究,2018,26(9):84-85.
[16]邓小梅,欧璐,向冬梅,等.低分子肝素治疗胎儿生长受限的临床效果及对新生儿结局的影响[J].中国现代医生,2015,53(17):43-45.
[17]Hansen AT,Sandager P,Ramsing M,et al.Tinzaparin for the treatment of foetal growth retardation:An open-labelled randomized clinical trial[J].Thromb Res,2018(170):38-44.
[18]Groom KM,Mccowan LM,Mackay LK,et al.Enoxaparin for the prevention of preeclampsia and intrauterine growth restriction in women with a history:a randomized trial[J].Am J Obstet Gynecol, 2017,216(3):296.e1-296.e14.
[19]Martinelli I,Ruggenenti P,Cetin I,et al.Heparin in pregnant women with previous placenta-mediated pregnancy complications:a prospective,randomized,multicenter,controlled clinical trial[J].Blood,2012,119(14):3269-3275.
[20]Rey E,Garneau P,David M,et al.Dalteparin for the prevention of recurrence of placental-mediated complications of pregnancy in women without thrombophilia:a pilot randomized controlled trial[J].J Thromb Haemost,2009,7(1):58-64.
[21]Rodger MA,Hague WM,Kingdom J,et al.Antepartum dalteparin versus no antepartum dalteparin for the prevention of pregnancy complications in pregnant women with thrombophilia(TIPPS):a multinational open-label randomised trial[J].The Lancet,2014,384(9955):1673-1683.
[22]Rodger MA,Gris JC,de Vries JIP,et al.Low-molecular-weight heparin and recurrent placenta-mediated pregnancy complications:a meta-analysis of individual patient data from randomised controlled trials[J].The Lancet,2016,388(10060):2629-2641.
[23]Haddad B,Winer N,Chitrit Y,et al.Enoxaparin and Aspirin Compared With Aspirin Alone to Prevent Placenta-Mediated Pregnancy Complications:A Randomized Controlled Trial[J].Obstet Gynecol,2016,128(5):1053-1063.
[24]Omri A,Delaloye J,Andersen H,et al.Low molecular weight heparin Novo(LHN-1)does not cross the placenta during the second trimester of pregnancy[J].Thromb Haemost,1989,61(1):55-56.
收稿日期:2019-3-31;修回日期:2019-4-11
編辑/肖婷婷
