管式气氛炉联用HPLCICPMS测定黑木耳中的三价铬和六价铬
2019-08-26李冰茹王北洪何昭颖马智宏
李冰茹,刘 静,王北洪,李 杨,何昭颖,马智宏
(北京农业质量标准与检测技术研究中心,农业部农产品质量安全风险评估实验室,北京 100097)
铬(Cr)主要以Cr(Ⅲ)和Cr(Ⅵ)的形式在植物或动物体内存在,形态决定其是必需元素还是有害元素,其三价态作为葡萄糖耐受因子成分参与体内糖、脂类、蛋白质和核酸的代谢,但较高剂量的Cr(Ⅲ)仍表现出细胞毒性反应[1-2];六价态会破坏DNA,具有强致癌效应[3]。因此,痕量铬的含量和化学形态对人类的健康有着重要的影响[3-4]。
样品前处理是检测铬形态的技术前提,直接影响检测结果的精度和准度。科学合理的前处理方法可以有效提高消解效率[5-6]。超声萃取[4]、微波萃取[5]等方法被用于测定胶囊、营养品、面粉中、保健食品[7-9]的Cr(Ⅲ)或Cr(Ⅵ),有着较好的稳定性和检出率。王晓波等[10]以及任凤莲等[11]采用浊点萃取方法、8-羟基喹啉(8-HQ)为鳌合剂分离出Cr(Ⅲ),通过计算总铬和Cr(Ⅲ)的含量间接推算出Cr(Ⅵ)含量,但是该方法在酸提取时需要浸泡6 h,用时较长。章剑扬等[12]利用EDTA二钠盐和硝酸铵溶液为提取液,采用加速溶剂萃取技术(ASE)对茶叶中2种价态铬进行提取,具有自动化程度高和同时测定2种价态的优点。席永清等[13]研究了在光盘上制备固相萃取柱的方法,设计了由5层结构组成的离心式微流控光盘,应用于Cr(Ⅲ)与Cr(Ⅵ)的分离,ICP-MS法检测总铬与未被固相萃取柱吸附的Cr(Ⅵ)含量,从而计算溶液中Cr(Ⅲ)含量。张毅等[14]以自制的PTFE微柱,对需要测定的Cr(Ⅲ)离子进行富集,取得理想检测效果。上述前处理方法有的耗时较长,有的装置复杂。因此温和简便的前处理分离测定以及避免使用还原性试剂是铬形态分析方法研究的关键。为此,本文建立以管式炉通入高纯氦气的前处理方法与高效液相色谱-电感耦合等离子体质谱联用[15-19]测定铬元素形态的新方法。通入高纯氦气是因为使用传统的马弗炉是在有氧情况下进行炭化,高温下氧的存在增加了Cr(Ⅲ)和Cr(Ⅵ)的转化[20],而管式气氛炉在无氧条件下高纯氦气作为保护气,高温下消解样品中的有机物,能够保持样品中Cr(Ⅲ)和Cr(Ⅵ)不发生转化,因此本实验采用高温管式炉无氧条件下高纯氦气保护对黑木耳样品进行处理。
近年的文献[21-22]及农业部风险评估专项监测发现:黑木耳中铬含量较高[23],但是黑木耳中铬形态含量的研究却少见报道,因此对其中的Cr(Ⅲ)和Cr(Ⅵ)测定有一定的营养安全意义。本实验以干制的黑木耳为例,在高温下高纯氦气保护下进行炭化,且保证炭化中铬的价态不发生转变,然后用流动相的乙二胺四乙酸二钠(EDTA-2Na)溶液络合,形成稳定的Cr(Ⅲ)-EDTA,通过高效液相色谱柱分离,利用ICP-MS检测Cr(Ⅲ)和Cr(Ⅵ)。
1 材料与方法
1.1 材料与仪器
木耳 北京各大超市及批发市场,袋装或散装;硝酸 优级纯,德国默克公司;Cr(Ⅲ)和Cr(Ⅵ)标准溶液 1000 mg/L,北京市环境保护所;EDTA-2Na 分析纯,北京化工有限公司;氨水 优级纯,北京市通广精细化工公司;质谱调谐液 美国Perkin Elmer公司。
NexIon 350 ICP-MS 美国PerkinElmer公司;GSL-1100X管式气氛炉 合肥科晶材料有限公司;Flexar液相泵 美国PerkinElmer公司;超声清洗机 江苏昆山超声仪器公司;粉碎机 德国IKA集团;超纯水 中扬超纯水系统;石英坩埚 无锡市鑫石陶瓷有限公司。
1.2 实验方法
1.2.1 样品前处理 黑木耳样品粉碎后过40目筛,过筛称取0.2000 g放入管式气氛炉中进行炭化,在10 min内匀速升温到450 ℃并保持2 h,然后冷却至室温,用pH7.0的流动相且含0.5 mmol/L EDTA-2Na溶液定容至50 mL;将定容好的样品超声15 min,温度37 ℃,超声功率700 W,在放置60 ℃的水浴中静置60 min,使EDTA-2Na与Cr(Ⅲ)充分络合,取出冷却室温,过0.45 μm微孔滤膜,待上机测定。同时做空白试验和加标回收。
1.2.2 前处理条件单因素实验
1.2.2.1 样品炭化温度 黑木耳样品粉碎后过40目筛,过筛称取0.2000 g放入管式炉中,在10 min内匀速升温,分别升温至200、300、350、400、450、500、600、650、700 ℃等并保持2 h,然后冷却至室温,其他步骤参照1.2.1,根据测定的铬含量选择最佳炭化温度。
1.2.2.2 样品炭化时间 黑木耳样品粉碎后过40目筛,过筛称取0.2000 g放入管式炉中,在10 min内匀速升温至450 ℃,分别保持1.0、1.5、2.0、2.5、3.0、3.5、4.0 h炭化时间,然后冷却至室温,根据测定的铬含量选择最佳炭化时间。
1.2.2.3 超声反应时间 按照1.2.1方法,将定容好的样品在0、5、10、15、20、30 min时间下进行超声实验,超声条件为温度37 ℃,功率700 W,根据测定的铬含量确定最佳超声时间。
1.2.2.4 络合温度和络合时间 按照1.2.1方法,将定容好的样品在15 min,温度37 ℃,功率700 W条件下进行超声实验后,分别在30、40、50、60、70、80 ℃温度下分别静置20、30、60、90、120 min进行交叉实验,根据测定的Cr(Ⅲ)含量选择EDTA-2Na与Cr(Ⅲ)的最佳络合反应时间与温度。EDTA-2Na与Cr(Ⅲ)充分络合,取出冷却室温,过0.45 μm微孔滤膜,待测。
1.2.3 标准曲线的绘制 将Cr(Ⅲ)和Cr(Ⅵ)标准溶液用pH=7的流动相且含0.5 mmol/L EDTA-2Na的溶液稀释至0.1 mg/L,作为标准储备液,然后再用流动相配成浓度为0、0.4、1.0、2.0、4.0、10.0、20.0 μg/L的Cr(Ⅲ)、Cr(Ⅵ)标准溶液系列,采用外标法,保留时间定性,峰面积定量。
1.2.4 加标回收实验 对干木耳做加标回收试验,其中Cr(VI)的添加水平分别为0.5、2.5和10.0 mg/kg,Cr(Ⅲ)的添加水平分别为5.0、10.0和20.0 mg/kg,按1.2.1步骤进行测定。
1.3 仪器条件
色谱条件为:Hamilton PRP-X100阴离子交换柱(250 mm×4.6 mm,10 μm),流动相为60 mmol/L硝酸铵(pH=7.0,稀氨水调节),流速为1.0 mL/min,进样量为50 μL,柱温25 ℃。
CP-MS工作参数为:RF功率1550 W,载气流量1.14 mL/min,采用碰撞反应模式,反应气体为He,氦气流量为2.0 mL/min、Rpq值为0.25,测量同位素:52Cr,主要技术参数参见表1。

表1 ICP-MS的碰撞模式下主要技术参数Table 1 The parameters of ICP-MS with KED mode
1.4 数据处理
本实验利用Excel(10.1.0.7566)进行数据统计分析。
2 结果与分析
2.1 样品处理条件分析
2.1.1 炭化温度及时间 黑木耳在不同温度下的炭化效果如图1所示,400 ℃以下样品不能较好炭化,尤其是部分大分子有机物质未能彻底炭化,导致一些结合态的铬不能完全释放出来,提取效率偏低;当温度高于600 ℃以后,铬与炭高温下反生反应,生成难熔的炭化铬化合物,造成提取样本含量偏低。因此,综合考虑炭化温度选择450 ℃,效果最佳。
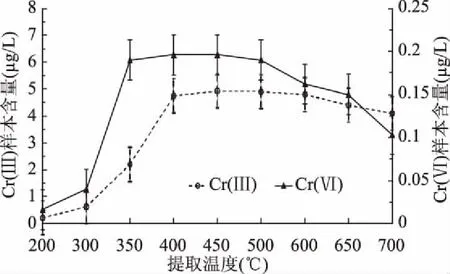
图1 炭化温度对提取样本含量影响Fig.1 Effect of different carbonization temperatures on the content of extrated samples
黑木耳在不同时间的炭化效果如图2所示,当炭化时间低于2.0 h时,样品中的有机物还没有彻底炭化,结合态的铬还没有完全释放出来,会造成提取出的样本含量结果偏低;随着时间增长,铬可能因挥发也会导致提取样本含量偏低,因此选择炭化的时间为2.0 h。
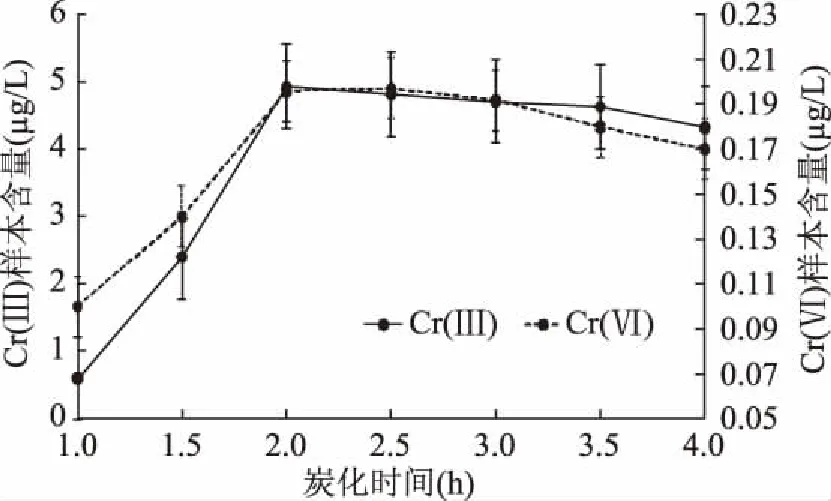
图2 炭化时间对提取样本含量的影响Fig.2 Effect of different carbonization time on the content of extrated samples
2.1.2 超声反应时间 超声反应时间对于铬含量的检测有着明显影响,按照1.2.2步骤检测后的结果如图3所示。由图3可见,随着超声时间的逐步增加,0~15 min内铬的含量明显升高,这是因为超声能够防止炭对Cr(Ⅲ)和Cr(Ⅵ)吸附。15 min之后趋于稳定,故选择超声时间为15 min。

图3 超声时间对络合反应的影响Fig.3 Effects of the ultrasonic time on the complexation reaction
2.1.3 Cr(Ⅲ)-EDTA络合温度和时间 如图4所示,在50 ℃时络合达到相对最优效果,因此50 ℃作为Cr(Ⅲ)-EDTA的络合温度。图5分析络合时间对于Cr(Ⅵ)的含量和Cr(Ⅲ)的含量的影响,发现随着时间增加Cr(Ⅵ)的含量无明显变化,Cr(Ⅲ)的含量呈现较大变化,由20至60 min时明显上升,后又趋于平稳,如图5所示。因此选择60 min作为Cr(Ⅲ)-EDTA络合时间。
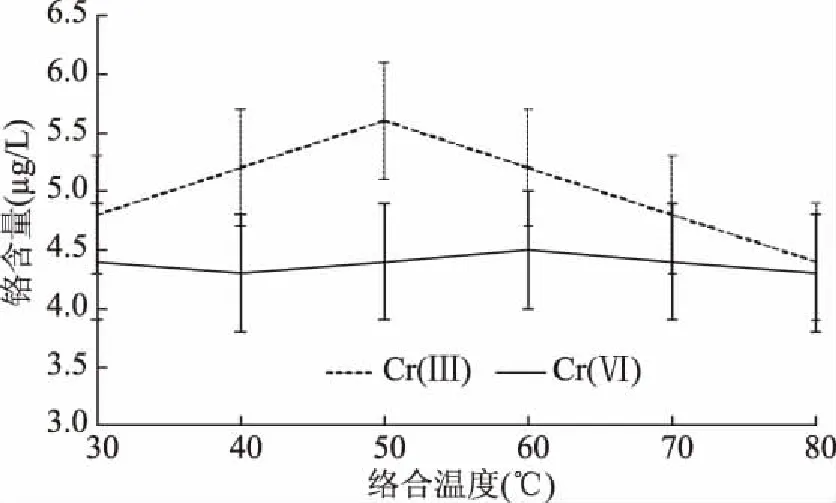
图4 络合温度对Cr(Ⅲ)和Cr(Ⅵ)含量的影响Fig.4 Effects of the complexation temperature on the concentration of Cr(Ⅲ)and Cr(Ⅵ)

图5 Cr(Ⅲ)-EDTA络合反应时间对铬含量的影响Fig.5 Effects of Cr(Ⅲ)-EDTA complexation time on the concentration of Cr
2.2 检测条件优化
2.2.1 流动相的选择 本实验采用阴离子色谱柱分离Cr(Ⅲ)和Cr(Ⅵ)。铬的两种价态Cr(Ⅲ)和Cr(Ⅵ)在不同的pH环境下稳定性有很大差异。当6
2.2.2 质谱干扰的消除 KED模式能够很好的消除其他杂质干扰,从图6在KED模式下检测52Cr得到的Cr(Ⅲ)和Cr(Ⅵ)的色谱图可以看出,色谱图中只有Cr(Ⅲ)和Cr(Ⅵ)的峰,其峰识别线(图中带三角标识的短线)清晰地标识了元素类别。

图6 KED模式下的Cr(Ⅲ)和Cr(Ⅵ)色谱图Fig.6 Chromatogram of Cr(Ⅲ)and Cr(Ⅵ)under KED model
2.2.3 线性关系 Cr(Ⅲ)的线性方程为y=1530.7x-120.16,R2=0.9998;Cr(Ⅵ)的线性方程为y=18582x-804,R2=0.9999。在0.1~50 μg/L范围内,线性关系良好,R2均达到0.9998以上,检出限分别为Cr(Ⅲ)0.2 μg/L、Cr(Ⅵ)0.1 μg/L。
2.2.4 空白试验 为了验证铬的形态在炭化过程中未发生Cr(Ⅲ)和Cr(Ⅵ)的转化,将Cr(Ⅲ)或Cr(Ⅵ)标样按照实验方法进行炭化、定容、检测,谱图如图7所示。图7中A是空白谱图,既没有Cr(III)的衍生峰,也没有Cr(Ⅵ)的衍生峰。图7中B是添加Cr(Ⅲ)标样的谱图,图中有两个峰识别线(带三角标识的短线),其中Cr(Ⅲ)具有非常明显的衍生峰,而Cr(Ⅵ)则没有峰。这说明利用管式气氛炉通入惰性气体进行保护炭化,能够防止传统马弗炉有氧情况下进行炭化,导致Cr(Ⅲ)向Cr(Ⅵ)转化现象的发生。

图7 空白色谱图和加标Cr(Ⅲ)色谱图Fig.7 Blank chromatogram and recovery of Cr(Ⅲ)chromatogram
2.2.5 回收率与精密度 加标实验结果如表2所示:Cr(Ⅲ)和Cr(Ⅵ)的回收率范围分别为80.0%~91.0%和80.2%~92.3%,RSD分别为2.0%~3.4%和1.5%~3.7%,证明本实验方法可用于干黑木耳中Cr(Ⅲ)和Cr(Ⅵ)的检测。

表2 Cr(Ⅲ)和Cr(Ⅵ)加标回收率Table 2 Recovery rate of Cr(Ⅲ)and Cr(Ⅵ)
2.3 实际样品测定
随机从市场上选择10份干黑木耳样品进行测试,结果见表3。样品中Cr(Ⅲ)含量在0.12~4.30 mg/kg之间,均未检出Cr(Ⅵ)。我国的食品标准GB2762-2017食品安全国家标准食品中污染物限量中蔬菜总铬限量值0.5 mg/kg,90%以上的样品超标。色谱如图8所示,其中一个样本的色谱图中Cr(Ⅵ)有峰标识线而无明显的衍生峰。

表3 干黑木耳样品中Cr(Ⅲ)和Cr(Ⅵ)的实际检测值Table 3 Contents of Cr(Ⅲ)and Cr(Ⅵ)in Auricularia auricula samples

图8 实测样品色谱图Fig.8 Chromatogram of measured sample
3 结论
本文建立了管式气氛炉无氧炭化-高效液相色谱-电感耦合等离子体质谱(HPLC-ICP-MS)检测干黑木耳中Cr(III)和Cr(VI)的方法。对样品在惰性气体保护下450 ℃进行2 h炭化处理后,加50 mL络合液超声处理,其优化条件为超声提取时间15 min,络合温度为60 ℃,络合时间为60 min。在惰性气体的保护下,样本在炭化过程中不发生氧化还原反应,保证样本中被检测元素的价态不发生转化。Cr(Ⅲ)和Cr(Ⅵ)的平均回收率范围分别为80.0%~91.0%和80.2%~92.3%,RSD分别为2.0%~3.4%和1.5%~3.7%。该方法操作简单,炭化过程无需添加酸碱试剂,不改变铬的价态,稳定好且回收率高,可推广用于农产品及其含多糖与胶质较高样品的铬不同价态的测定。
