超声引导下连续腰交感神经节阻滞对顽固性下肢疼痛患者疼痛介质及疼痛程度的影响
2019-08-26袁景和宋卫军白宝艳
袁景和, 宋卫军, 艾 芳, 白宝艳
(延安大学附属医院, 1. 疼痛科; 2. B超室, 陕西 延安, 716000)
顽固性下肢疼痛是常见的疼痛类型,多由周围及中枢神经损伤、障碍等所致,主要表现为持续与反复的下肢疼痛、皮肤温度下降,严重损害患者身心健康和日常生活[1]。目前,促神经修复等药物治疗是顽固性下肢疼痛常用的治疗方法,可有效缓解患者的疼痛症状,但仍有部分患者疗效欠佳[2]。近年来,神经阻滞技术逐渐被应用于临床镇痛中,通过阻滞相应的神经达到良好的镇静、镇痛作用[3]。本研究对顽固性下肢疼痛患者行超声引导下连续腰交感神经节(LSG)阻滞,观察其对患者疼痛介质及程度的影响,现报告如下。
1 资料与方法
1.1 一般资料
选取2016年6月—2018年6月本院顽固性下肢疼痛患者100例,依据随机数字表法分为药物组与阻滞组,每组50例。纳入标准: ① 经临床症状、实验室、病史、影像学等检查诊断为下肢神经病理病变所致顽固性下肢疼痛[4]; ② 局部冷、麻、凉感并有不同程度疼痛; ③ 年龄>18岁、无精神病病史; ④ 知情同意。排除标准: ① 近1个月有抗炎、激素、免疫等治疗史; ② 妊娠期、哺乳期女性; ③ 有心、肝、肾等严重性疾病; ④ 手术、外伤等其他原因所致下肢疼痛。本研究经伦理委员会审批通过, 2组性别、病因、年龄、体质量指数、病程比较,差异无统计学意义(P>0.05), 见表1。
1.2 方法
药物组给予0.3 g加巴喷丁(江苏恒瑞医药股份有限公司,国药准字H20050271, 0.3 g×10粒)+0.5 mg甲钴胺(亚宝药业集团股份有限公司,国药准字H20041767, 0.5 mg×20片)口服治疗, 3次/d, 共7 d。
阻滞组给予超声引导下连续LSG阻滞治疗,取侧卧位,消毒铺巾后通过便携式彩色二维超声仪(7.5 MHz凸阵探头,深7~10 cm, MicroMAXX, SOnoSite公司)探查腰椎情况,包括横截面(在L1、L2横突上将超声探头与脊柱方位垂直放置以获取低位胸椎和上位腰椎区域影像,腰大肌内部低回声区域为椎体,向外偏移为腰方肌,上端肌肉为竖脊肌)、纵截面(超声探头距离脊柱中线3~4 cm, 城垛样影像为L1、L2、L3横突),先对L1、L2定位并获取其横截面图像,以15 cm、21G腰穿刺针45 °下从探头外端、偏向L2进针4.5 cm达骨质后向L2椎体外部进针2.5 cm至LSG, 回抽无血无液后缓慢注射1%利多卡因(山东华鲁制药有限公司,国药准字H37022147, 0.1 g×5 mL) 5 mL, 确认分布均匀(L2椎体和竖脊间有不规则低回声、周边有高回声晕围绕)后,植入深3 cm的一次性硬膜外导管,回抽无血、无液后固定导管,无菌敷料覆盖,保存导管7 d, 此后以一次性电子输注泵输注1%利多卡因5 mL, 1次/d, 共7 d。
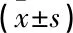
表1 2组一般资料比较
1.3 指标观察
比较2组疼痛介质、疼痛程度、皮肤温度、不良反应。① 疼痛介质。治疗前、治疗第7天后抽取外周血3 mL并分离血清(3 000 转/min, 10 min)后,采用酶联免疫吸附法检测降钙素基因相关肽(CGRP)、β-内啡肽(β-EP)、5-羟色胺(5-HT)。② 疼痛程度。治疗前和治疗第1、7天采用视觉模拟评分法(VAS)[5]评估,总分10分,得分越高表示疼痛程度越高。③ 皮肤温度。治疗前和治疗第1、7天采用医用红外线测温仪监测下肢胫皮肤温度,测3次取平均值。④ 不良反应,如恶心、呕吐、嗜睡、头晕等。
1.4 统计学方法
采用SPSS 22.0软件,计数资料采用率表示,行χ2检验,等级资料采用秩和检验,计量资料采用均数±标准差表示,采用独立样本t检验,同组间差异采用配对t检验,P<0.05为差异有统计学意义。
2 结 果
2.1 2组CGRP、β-EP、5-HT比较
药物组与阻滞组治疗前CGRP、β-EP、5-HT比较,差异无统计学意义(P>0.05); 2组治疗后CGRP、β-EP、5-HT低于治疗前,阻滞组治疗后CGRP、β-EP、5-HT低于药物组,差异有统计学意义(P<0.05), 见表2。
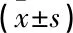
表2 2组CGRP、β-EP、5-HT比较
CGRP: 降钙素基因相关肽; β-EP: β-内啡肽; 5-HT: 5-羟色胺。与治疗前比较, *P<0.05; 与阻滞组比较, #P<0.05。
2.2 2组VAS评分比较
2组治疗前VAS评分比较,差异无统计学意义(P>0.05); 2组治疗第1、7天VAS评分低于治疗前,阻滞组治疗第1、7天VAS评分低于药物组,差异有统计学意义(P<0.05)。见表3。
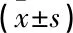
表3 2组VAS评分比较 分
与治疗前比较, *P<0.05; 与阻滞组比较, #P<0.05。
2.3 2组皮肤温度比较
2组治疗前皮肤温度比较,差异无统计学意义(P>0.05); 2组治疗1、7 d后皮肤温度高于治疗前,阻滞组治疗1、7 d后皮肤温度高于药物组,差异有统计学意义(P<0.05), 见表4。
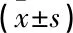
表4 2组皮肤温度比较 ℃
与治疗前比较, *P<0.05; 与阻滞组比较, #P<0.05。
2.4 2组不良反应比较
药物组与阻滞组不良反应发生率比较,差异无统计学意义(P>0.05), 见表5。
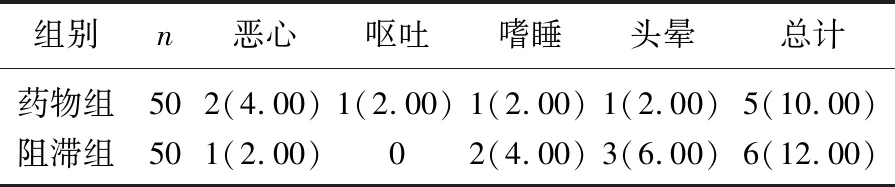
表5 2组不良反应比较[n(%)]
3 讨 论
神经病理病变所致顽固性下肢疼痛的机制尚未明确,主要与LSG参与疼痛介质产生与释放的调节功能紊乱有关,其常用的治疗方法为药物治疗,如促神经修复等药物[6-7]。加巴喷丁是常用的抗惊厥药物,对疱疹感染等所致神经痛具有良好的镇痛作用,而甲钴胺是一种内源性的辅酶B12神经药物,具有修复受损神经组织、促进轴索内输送和轴索再生及髓鞘形成、防止轴突变性等作用,且易于进入神经元细胞器并参与脑细胞和脊髓神经元胸腺嘧啶核苷的合成,在神经痛治疗中也具有良好的疗效[8-9]。有研究[10-11]报道,通过注射布比卡因等局麻药阻滞LSG可有效阻滞其疼痛传导,使对应区域的痛觉缓解,在治疗因LSG病变所致的顽固性疼痛中具有良好的疗效。CGRP是一类在脊髓水平发挥致痛作用的神经肽, β-EP是一种可激活LSG来促进痛觉信号传递、放大疼痛感受的疼痛介质, 5-HT则是能作用于神经根并增强LSG痛觉敏感性的因子, CGRP、β-EP、5-HT在LSG疼痛传递中具有重要的作用[12-13]。
本研究结果显示,药物组与阻滞组治疗后CGRP、β-EP、5-HT和治疗第1、7天VAS评分明显低于治疗前,阻滞组治疗后CGRP、β-EP、5-HT和治疗第1、7天VAS评分显著低于药物组,药物组和阻滞组治疗第1、7天皮肤温度显著高于治疗前,阻滞组治疗第1、7天皮肤温度显著高于药物组,表明超声引导下连续LSG阻滞能够有效减少顽固性下肢疼痛患者疼痛介质释放,有利于改善患者疼痛程度及皮肤温度。这可能是由于加巴喷丁的镇痛作用及甲钴胺促进神经修复的作用能够有效修复和改善LSG的疼痛调节功能[8-9], 使LSG参与的CGRP、β-EP、5-HT等疼痛介质释放减少[12-13], 从而缓解患者的下肢疼痛及皮肤温度异常。本研究超声引导下连续LSG阻滞治疗中,可能是由于超声临床上常用的影像学方法,具有操作简单、快捷、准确等优点,经超声引导下行穿刺,可清晰有效地显示机体组织内结构状况下精确穿刺目标组织并注射相应的药物,并阻滞所有的利多卡因为酰胺类局麻药,对中枢神经系统有明显的兴奋和抑制双相作用[10-11]。因此,本研究能够在超声引导下准确有效地对LSG行连续阻滞治疗,并通过利多卡因对LSG产生直接调节作用,尤其是可能有效调节了LSG参与疼痛介质产生与释放的调节功能,抑制了LSG对CGRP、β-EP、5-HT等疼痛介质释放的刺激作用[12-13], 进而降低了下肢疼痛信号的传递,更有效地改善了患者的疼痛程度及皮肤温度。本研究中,药物组与阻滞组不良反应发生率比较无显著差异,表明超声引导下连续LSG阻滞治疗顽固性下肢疼痛的安全性好。这可能是由于连续LSG阻滞中采用了超声引导的方式,能够准确有效地引导穿刺针穿刺至LSG处并准确注射利多卡因[14-15], 使利多卡因主要局限于LSG处,故未显著增加患者不良反应。
综上所述,超声引导下连续LSG阻滞可有效减少顽固性下肢疼痛患者疼痛介质释放,有利于改善患者疼痛程度及皮肤温度,且安全性好。
