高效液相色谱法同时测定博落回注射液中血根碱和白屈菜红碱的含量
2019-08-22赵有轩张传津张志民章安源
赵有轩,张传津,张志民,章安源
(山东省兽药质量检验所,济南250022)
博落回注射液主要含有血根碱和白屈菜红碱等生物碱,具有抗菌消炎、润肠止泻的功能,主要用于仔猪黄白痢的防治[1-3]。博落回注射液现收载于《兽药质量标准》(2017 年版[4])中药卷中,质量控制主要是采用薄层色谱法对其中的血根碱和白屈菜红碱进行鉴别,结合紫外-可见分光光度法测定吸光度值作限度检查,未对这两种有效成分进行含量测定。该制剂为罂粟科博落回(Macleaya cordata(Willd.)R.Br.)的果实经提取分离制成的生物碱硫酸盐水溶液。因博落回果原料稀缺,制剂工艺相对复杂,导致该产品质量参差不齐。为有效控制该产品质量,本文经过探索尝试,建立了高效液相色谱法同时测定博落回注射液中血根碱和白屈菜红碱含量的方法[4-11]。结果显示:本方法具有操作简单、分离迅速、灵敏度高等特点,可以用于博落回注射液中血根碱和白屈菜红碱的测定。
1 材料与试药
1.1 仪器 Agilent 1260高效液相色谱仪,配PDA检测器(安捷伦,美国);U-3900紫外分光光度计(日立,日本);BP211D分析天平 (赛多利斯,德国);PB-10酸度计(赛多利斯,德国);Milli-Q Advantage A10超纯水系统(密理博,美国)。
1.2 药品与试剂 盐酸血根碱,批号:510001-201101,含量:99.3%,来源:中国食品药品检定研究院;白屈菜红碱,批号:111718-200501,含量:100%,来源:中国药品生物制品检定所。甲醇,乙腈均为色谱纯;三乙胺、磷酸和盐酸均为分析纯;水为超纯水。
2 方法与结果
2.1 色谱条件 色谱柱:Waters Symmetry C18(4.6 mm × 250 mm,5 μm);流速:1.0 mL/min;流动相:乙腈-0.2%三乙胺溶液(磷酸调节pH至2.5),二极管阵列检测器,检测波长:270 nm;柱温:35 ℃;进样体积:10 μL。
2.2 溶液的制备
2.2.1 对照品贮备液制备 称取盐酸血根碱100 mg,置于10 mL容量 瓶中,称取白屈菜红碱100 mg,置于另一10 mL容量瓶中,分别加甲醇-1.0%盐酸溶液(50 ∶50)溶解,稀释至刻度,即分别得血根碱和白屈菜红碱对照品贮备液。
2.2.2 供试品溶液制备 博落回注射液三批,分别为:批号-2018122411,来源:山东华尔康兽药有限公司;批号-20180901,来源:山东圣旺药业股份有限公司;批号-20180201,来源:山西省芮城科龙兽药有限公司。分别精密量取博落回注射液5 mL,加甲醇-1.0%盐酸溶液(50 ∶50)稀释至100 mL,摇匀,即得。
2.3 专属性试验色谱图 在上述色谱条件下,确定阴性对照色谱图,血根碱和白屈菜红碱的色谱图以及博落回注射液色谱图,如下图1,图2,图3所示。
2.4 线性关系考察 吸取上述对照品溶液逐级稀释,分别制成 0.5、1、5、10、100 μg/mL 的血根碱溶液和 0.25、0.5、2.5、5、50 μg/mL 的白屈菜红碱溶液,分别取10 μL进样,以峰面积Y为纵坐标,血根碱、白屈菜红碱浓度X(μg/mL)为横坐标建立标准曲线。血根碱的回归方程为Y=33.932X-2.512,R2=1.000;白屈菜红碱的回归方程为 Y =69.419X-7.380,R2=1.000,相关系数良好。 (见图 4、图5)
2.5 添加回收试验 精密量取博落回注射液1 mL,置20 mL容量瓶中,分别加2 mL血根碱对照品贮备液和1 mL白屈菜红碱对照品贮备液,加甲醇-1.0%盐酸溶液(50 ∶50)稀释至刻度,取10 μL上机检测,血根碱的回收率在95% ~100%之间,见表1;白屈菜红碱的回收率在97% ~99%之间,见表2,均满足准确度的要求。
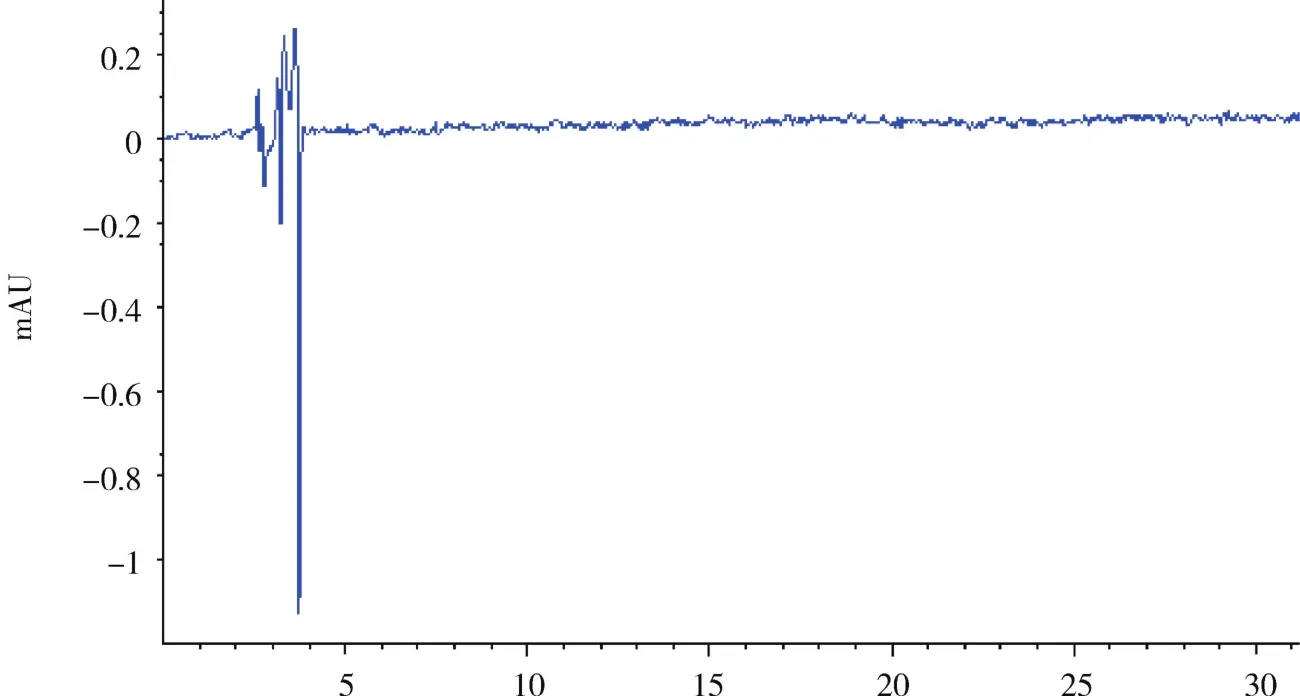
图1 阴性对照色谱图Fig 1 Chromatogram of negative control
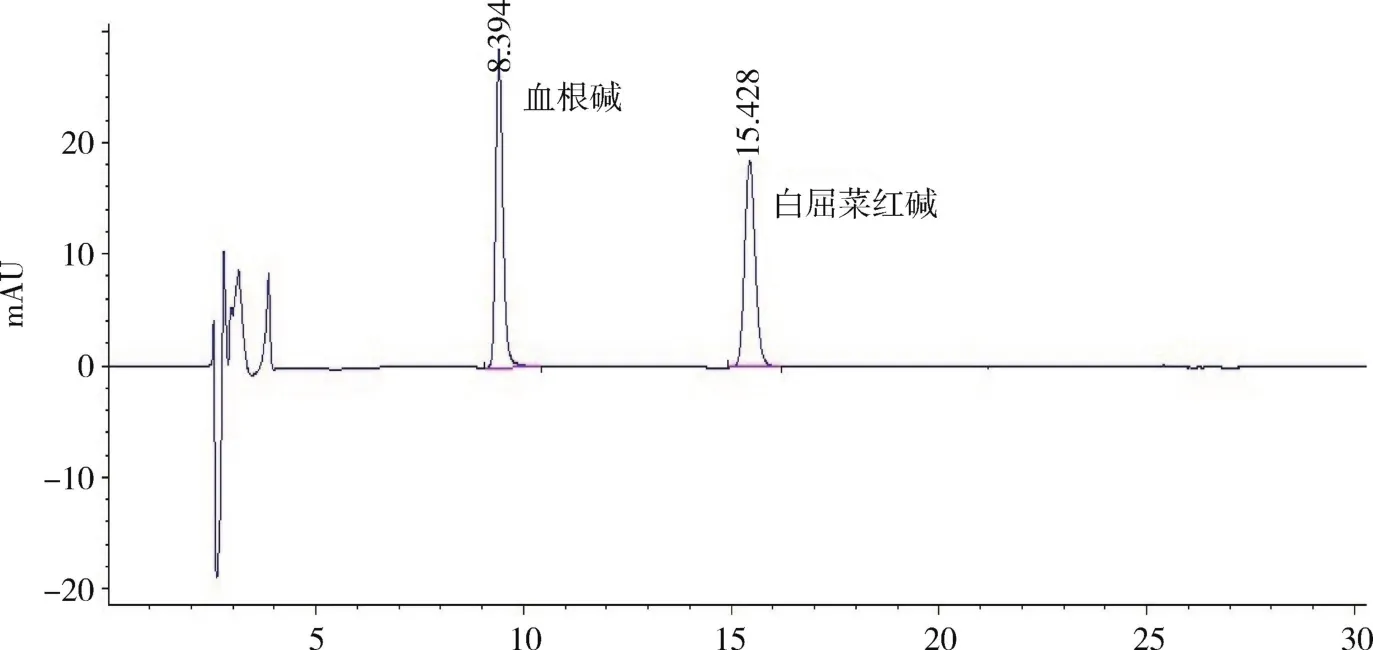
图2 对照品中血根碱和白屈菜红碱色谱图Fig 2 Chromatogram of sanguinarine and chelerythrine in reference solution
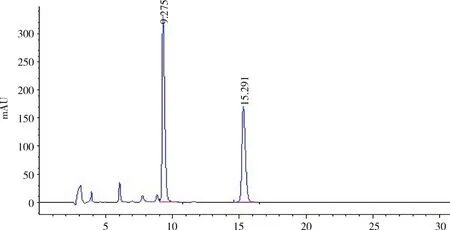
图3 博落回注射液中的血根碱和白屈菜红碱色谱图Fig 3 Chromatogram of sanguinarine and chelerythrine in Macleaya Cordata injection

图4 血根碱线性曲线Fig 4 Standard curve of sanguinarine
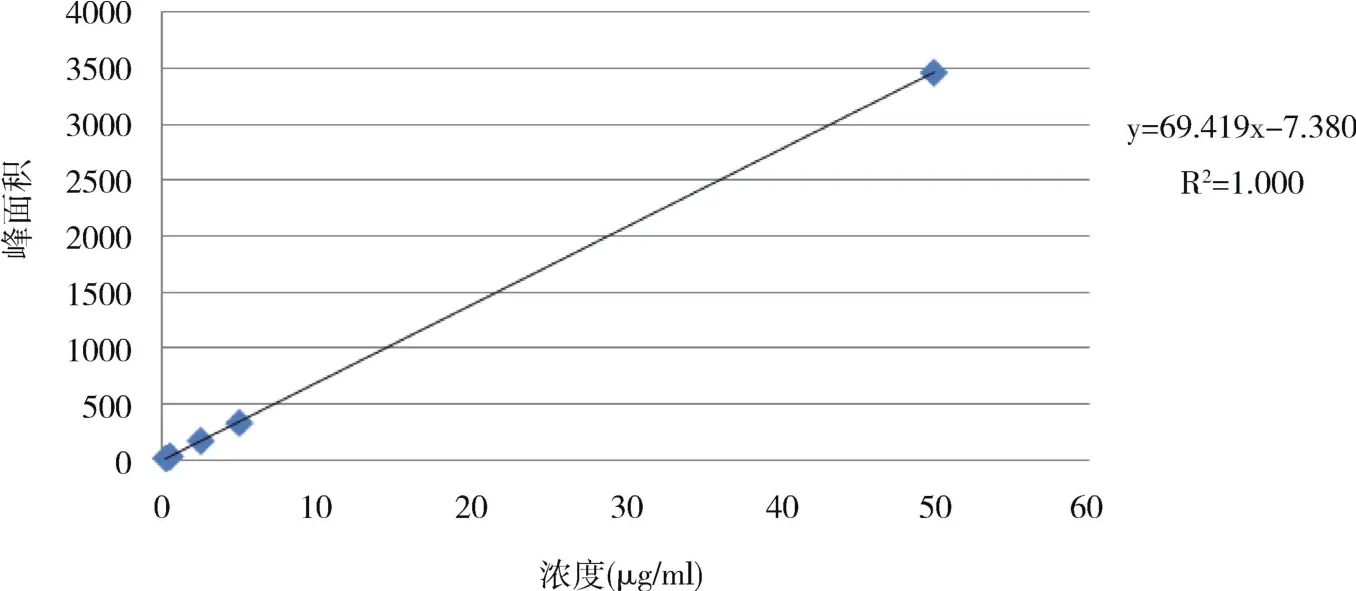
图5 白屈菜红碱线性曲线Fig 5 Standard curve of chelerythrine

表1 血根碱添加回收结果Tab 1 Results of recovery for sanguinarine
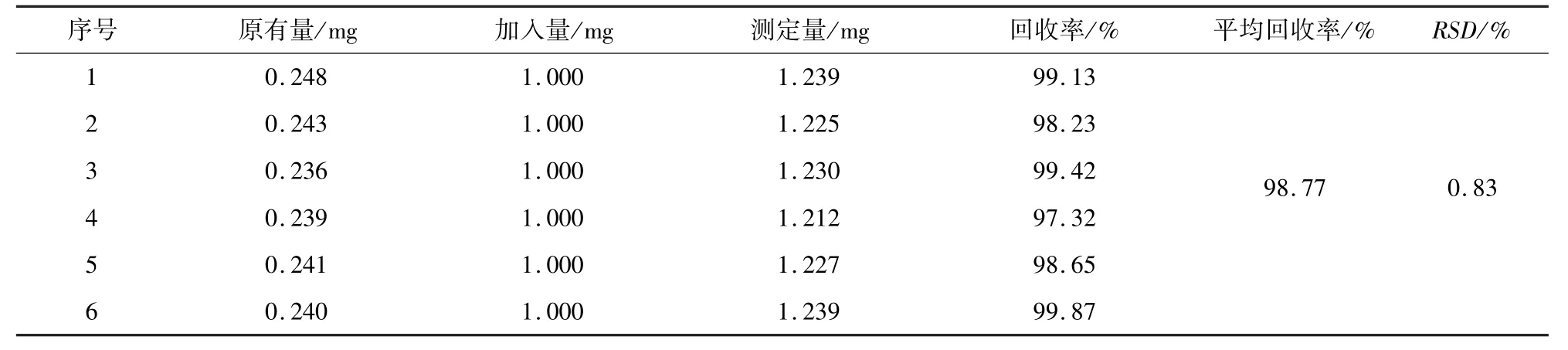
表2 白屈菜红碱添加回收结果Tab 2 Results of recovery for chelerythrine
2.6 精密度试验 取2.2.1项下对照品溶液,按照2.1项下色谱条件进样,连续进6针,计算血根碱和白屈菜红碱峰面积的 RSD,其中血根碱为0.56%,白屈菜红碱为0.22,精密度良好。 如表3,表4所示。
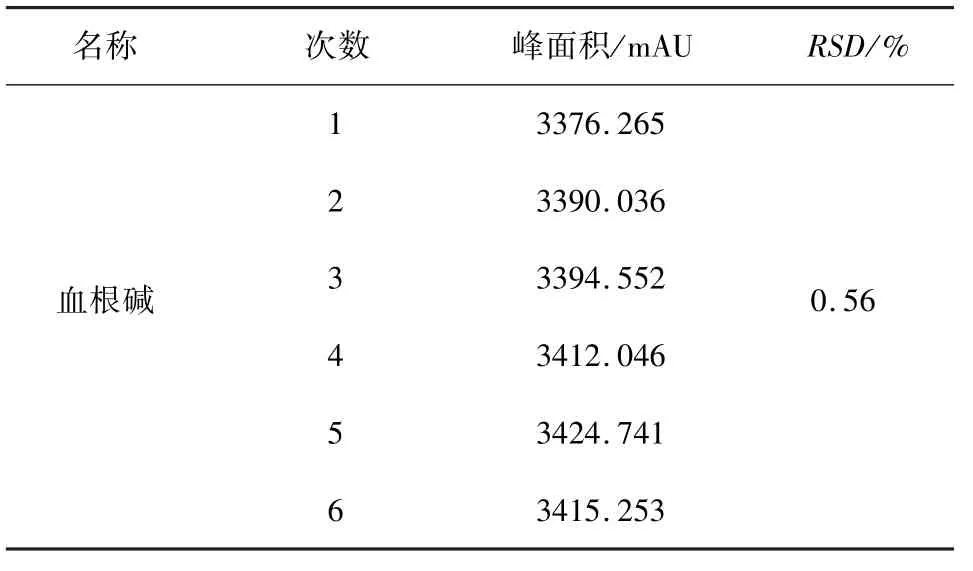
表3 博落回注射液中血根碱精密度试验(n=6)Tab 3 Precision test of sanguinarine in Macleaya Cordata injection (n=6)
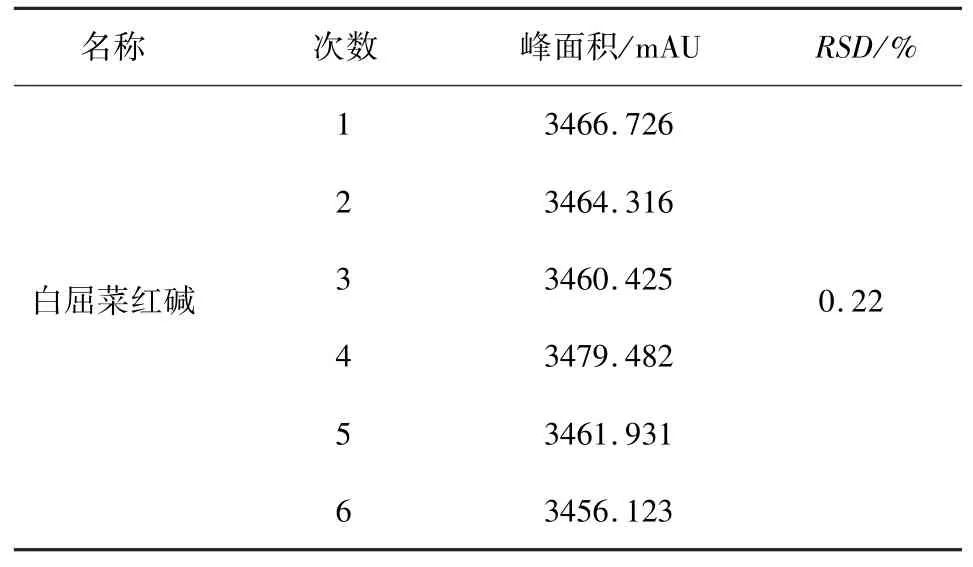
表4 博落回注射液中血白屈菜红碱精密度试验(n=6)Tab 4 Precision test of chelerythrine Macleaya Cordata injection (n=6)
2.7 稳定性试验 取2.2.1项下对照品溶液,按照2.1 项下色谱条件分别在0、2、4、8、12、24 h 下进样,测定不同时间下的峰面积,RSD(n=5),其中血根碱0.52%,白屈菜红碱0.23%,表明对照品溶液在24 h内稳定性良好。
2.8 样品测定 取2.2.2项下的3批博落回注射液,按照2.1项下的色谱条件进样,测定峰面积,计算血根碱和白屈菜红碱的含量,三批的血根碱含量分别是 97.65、100.32、100.96 μg/mL,白屈菜红碱含量分别是 50.99、49.03、48.53 μg/mL。
3 讨论与结论
3.1 流动相的选择 按照《兽药质量标准》(2003年版[3])上博落回提取物的液相标准选择梯度洗脱,流动相 A:乙腈,流动相 B:0.2%三乙胺(磷酸调节pH至2.5),发现在白屈菜红碱位置处基线漂移严重,影响了白屈菜红碱的峰形,根据参考文献[6],改成等度洗脱,流动相乙腈 -0.2%三乙胺(磷酸调节pH至2.5),洗脱效果良好。
3.2 pH的选择 根据《兽药质量标准》(2003年版[3])和参考文献[6],选择 pH2.0,2.5,3.0 几个值进行筛选,发现pH在2.0时,血根碱峰有拖尾,pH在3.0时,基线不平稳,而pH在2.5时,分离效果好,峰形最好,基线平稳,可达到最佳分离效果。
3.3 波长选择 分别取血根碱和白屈菜红碱对照品溶液,经紫外-可见分光光度计法测定吸收波长,显示血根碱在270和330 nm处有最大吸收,白屈菜红碱在270和320 nm处有最大吸收,在270 nm下同时测定血根碱和白屈菜红碱,结果显示在270 nm下有较高吸收值,且分离度良好。所以选择270 nm作为检测波长。
《兽药质量标准》(2017年版[4])上只有鉴别的方法,能定性,但是无法定量。根据本方法建立的液相方法可以快速测定血根碱和白屈菜红碱,省去了薄层鉴别的繁琐处理过程,达到快速测定含量的目的。相对于参考文献[6,8],优化了液相色谱条件,为了增加对照品的溶解性,改变了稀释剂,经过一系列优化和探索,回收率和精密度均有明显变好,峰形较之前有明显改善。
综上所述,本方法具有操作简单、分离迅速、灵敏度高等特点,可用于博落回注射液中血根碱和白屈菜红碱的测定。
