急性成人胸腰段脊柱脊髓损伤后路手术加速康复外科实施流程专家共识
2019-08-18郑博隆张志成高杰孙维郭航董补怀高子军黄大耿李静郑林宏闫航孟浩蔡思逸贺宝荣郝定均刘浩杨惠林孙宇李淳德沈建雄孙天胜邱贵兴
郑博隆 张志成 高杰 孙维 郭航 董补怀 高子军 黄大耿 李静 郑林宏 闫航孟浩 蔡思逸 贺宝荣* 郝定均* 刘浩 杨惠林 孙宇 李淳德 沈建雄* 孙天胜* 邱贵兴*
(西安交通大学附属红会医院1.脊柱外科,4.麻醉科,西安 710054;中国人民解放军总医院第七医学中心2.骨科,3.麻醉科,北京 100700;5.中国医学科学院北京协和医学院北京协和医院骨科,北京 100730;6.四川大学华西医院骨科,成都 610041;7.苏州大学附属第一医院骨科,江苏苏州 215006;8.北京大学第三医院骨科,北京 100191;9.北京大学第一医院骨科,北京 100034)
加速康复外科(enhanced recovery after surgery,ERAS)是基于循证医学证据通过多学科协作对围手术期各项措施进行优化,有效减少围手术期的创伤应激和术后并发症,加速患者康复[1]。急性成人胸腰段脊柱脊髓损伤后路手术是脊柱外科常见的手术之一,但如何将ERAS理念应用于这类脊柱损伤的治疗也困扰着广大脊柱外科医师。经全国脊柱外科专家组多次讨论,参考《成人急性胸腰段脊柱脊髓损伤循证临床诊疗指南》[2],在循证医学的基础上,针对急性成人胸腰段脊柱脊髓损伤后路手术ERAS 实施流程达成共识,供脊柱外科医师在临床工作中参考。该流程的实施需要脊柱外科医师、麻醉医师、病房护士、手术室护士、康复医师等多学科团队共同配合完成。为方便临床具体操作,制定了不同成员在不同围手术期阶段的任务表单,详见表1~5。
1 急性成人胸腰段脊柱脊髓损伤后路手术定义
本文探讨的范围是急性成人胸腰段新鲜骨折,合并或不合并脊髓损伤。骨折节段包括T10~L2 椎体,受伤至手术的时间不超过2 周,儿童及骨质疏松性椎体骨折不在本文讨论范围内。同时,本实施流程仅讨论后路手术的相关问题,不涉及前路手术。
2 急性成人胸腰段脊柱脊髓损伤的诊断
通过患者的外伤史、临床体征和影像学检查(常规行X 线、CT 和MRI 检查)明确诊断,胸腰段脊柱脊髓损伤的诊断内容包括2 部分:①骨折的部位和类型;②神经损伤的部位、程度和平面。
骨折部位和类型推荐采用最新AO分型对其进行分类,存在骨折脱位或旋转移位为C 型,存在张力带损伤为B型,不存在张力带损伤的单纯骨折为A型。
神经损伤推荐使用美国脊髓损伤协会(American Spinal Injury Association,ASIA)标准评估患者的神经功能状态。神经损伤的部位分为脊髓损伤、马尾神经损伤、神经根损伤。损伤程度分为不完全损伤与完全损伤,区别在于是否存在鞍区S4~S5感觉或运动功能保留;同时ASIA 残损分级分为A~E 级,其中A 级为完全损伤,E 级为无损伤,其余B、C、D 级为不完全损伤。神经损伤平面指身体两侧有正常感觉和运动功能的最低脊髓神经分布节段;感觉平面指身体两侧有正常感觉功能的最低脊髓神经分布节段;运动平面指身体两侧有正常运动功能的最低脊髓神经分布节段,应根据肌力至少为3级的那块关键肌来确定,要求该平面以上节段支配的关键肌肌力必须是5级。
以T12 爆裂骨折伴不完全脊髓损伤(AISA D 级)为例,完整的诊断应为“①T12 骨折A3 型;②不完全脊髓损伤(AISA D级、神经平面L1)”。
3 急性成人胸腰段脊柱脊髓损伤后路手术的目的及围手术期ERAS进程的主要问题
急性成人胸腰段脊柱脊髓损伤后路手术的目的是恢复脊柱序列,重建脊柱稳定性,解除神经压迫,为神经功能恢复创造条件。
围手术期ERAS进程的主要问题包括:①减少由于创伤和外科手术对患者生理和心理造成的双重打击[3];②促进急性胸腰段脊柱脊髓损伤术后神经功能的康复;③预防和处理神经损伤相关并发症。
4 术前评估和管理
患者的全面评估是ERAS 个体化实施的前提。评估应贯穿整个围手术期的ERAS流程中。
4.1 损伤严重程度评估和合并伤评估
急性创伤的患者常伴有全身合并伤,因此对患者进行损伤严重程度的评估是接诊的第一步。损伤严重程度评分(injury severity score,ISS)是1974 年由Baker等[4]首先提出,其计算方法为身体3个最严重损伤区域的最高简明损伤定级标准值的平方和。而之后的新损伤严重程度评分(new injury severity score,NISS)是由Osler等[5]建立的评分体系,较ISS的改进是不考虑解剖部位的限制,而只观察损伤严重程度的影响,即3个最高简明损伤定级标准值的平方和。研究显示NISS 在患者死亡风险的预测方面优于ISS[6],因此推荐使用NISS。
对于合并伤评估,严重的胸腰段脊柱脊髓损伤常合并胸腹伤,青壮年居多,休克的发生率较高。合并严重胸腹联合伤时可继发机体的生理紊乱,若纠正不及时,特别是合并感染时易导致多器官功能障碍综合征(multiple organ dysfunction syndrome,MODS),因为严重创伤是形成MODS 的基本原因[7]。所以应当反复多次查体,避免延误诊断。例如,胸椎骨折合并血气胸或血胸时,对于危及生命的血气胸患者应协同胸外科医师或直接让胸外科医师处理,放置胸腔闭式引流,伴多根多处肋骨骨折的患者需行肋骨固定术。待胸部情况稳定,可耐受手术时及早手术。对于单纯血胸的患者如果不危及生命,可在脊柱手术的同时放置胸腔闭式引流管,缩短治疗周期,加速康复[8]。当然,需要密切关注患者的肺功能、血红蛋白、白蛋白等,同时避免长时间引流管的放置导致的感染、肺不张等情况的发生。
4.2 脊柱外科手术基本评估和管理
4.2.1 美国麻醉医师协会(American Society of Anesthesiologists,ASA)分级评估:根据ASA 分级对患者全身健康情况与疾病严重程度进行评估,初步判断患者对围手术期应激反应的耐受力[9]。
4.2.2 心肺功能评估:推荐美国纽约心脏病学会(New York Heart Association,NYHA)心功能分级和代谢当量(metabolic equivalent of task,MET)评估患者的心功能。超过60岁的患者常规行心脏超声检查评估。常规行双肺CT检查判断是否合并呼吸系统疾病。对怀疑存在呼吸功能异常者通过肺功能检查和动脉血气分析判断有无通气和/或换气功能障碍。
4.2.3 凝血功能评估:通过病史采集、体格检查及术前实验室凝血功能检查可发现患者是否存在可能增加围手术期出血的相关疾病。
4.2.4 血糖评估:建议空腹血糖控制在5.6~10.0 mmol/L,随机血糖控制在12.0 mmol/L 以内[10]。术前应将原有降糖方案过渡至胰岛素。糖尿病患者手术当日停用口服降糖药和非胰岛素注射剂,停药期间监测血糖,使用常规胰岛素控制血糖。
4.2.5 高血压评估:术前了解患者高血压病因、病程、程度和靶器官受累情况。建议择期手术前中青年患者血压控制<130/85 mmHg,老年患者<140/90 mmHg为宜。合并糖尿病的高血压患者血压控制<130/80 mmHg[11]。必要时术前请心内科会诊并指导治疗。
4.2.6 营养评估:根据营养风险筛查2002(nutrition risk screening 2002,NRS2002)进行评估,总分>3 分者请营养科介入,通过营养支持保证术前白蛋白>35 g/L。
4.2.7 术后恶心呕吐风险评估(postoperative nausea and vomiting,PONV):对于女性、不吸烟、晕动症或既往有恶心呕吐病史,及术后应用阿片类药物的患者,注意识别并采取相应的防治措施[12]。
4.2.8 术后谵妄易感因素评估:高龄、认知功能障碍、合并多种内科疾病、摄入量减少、生理功能储备减少、多种药物应用、酗酒为术后谵妄的易感因素[13],应识别此类患者并采取相应预防措施。
4.2.9 静脉血栓风险评估:对于肥胖、瘫痪、静脉曲张、高龄、脑梗死、血栓病史及家族史、D-二聚体水平增高等有深静脉血栓及肺栓塞高危因素的患者可采用Wells 血栓风险评分进行评估[14,15]。
4.3 急性成人胸腰段脊柱脊髓损伤后路手术专项评估和管理
4.3.1 骨折损伤类型评估:推荐采用最新的AO分型[16]对骨折的损伤类型进行分型,使用胸腰段损伤分类和严重程度评分(thoracolumbar injury classification and severity score,TLICS)[17]来确定患者的治疗方案。TLICS评分≤3分,建议保守治疗;TLICS=4分,可选择手术或保守治疗;TLICS≥5分,建议手术治疗。
推荐根据神经功能状态和后方韧带复合体完整程度来选择手术入路,同时载荷分享评分(load sharing classification,LSC)[18]也可作为手术入路选择的参考。无神经损伤,无论后方韧带复合体断裂与否,推荐进行后路手术;合并神经损伤患者,无后方韧带复合体断裂时可选择前路手术,伴后方韧带复合体断裂时可行后前路手术,为减少手术创伤,也可经后路手术行前方减压。
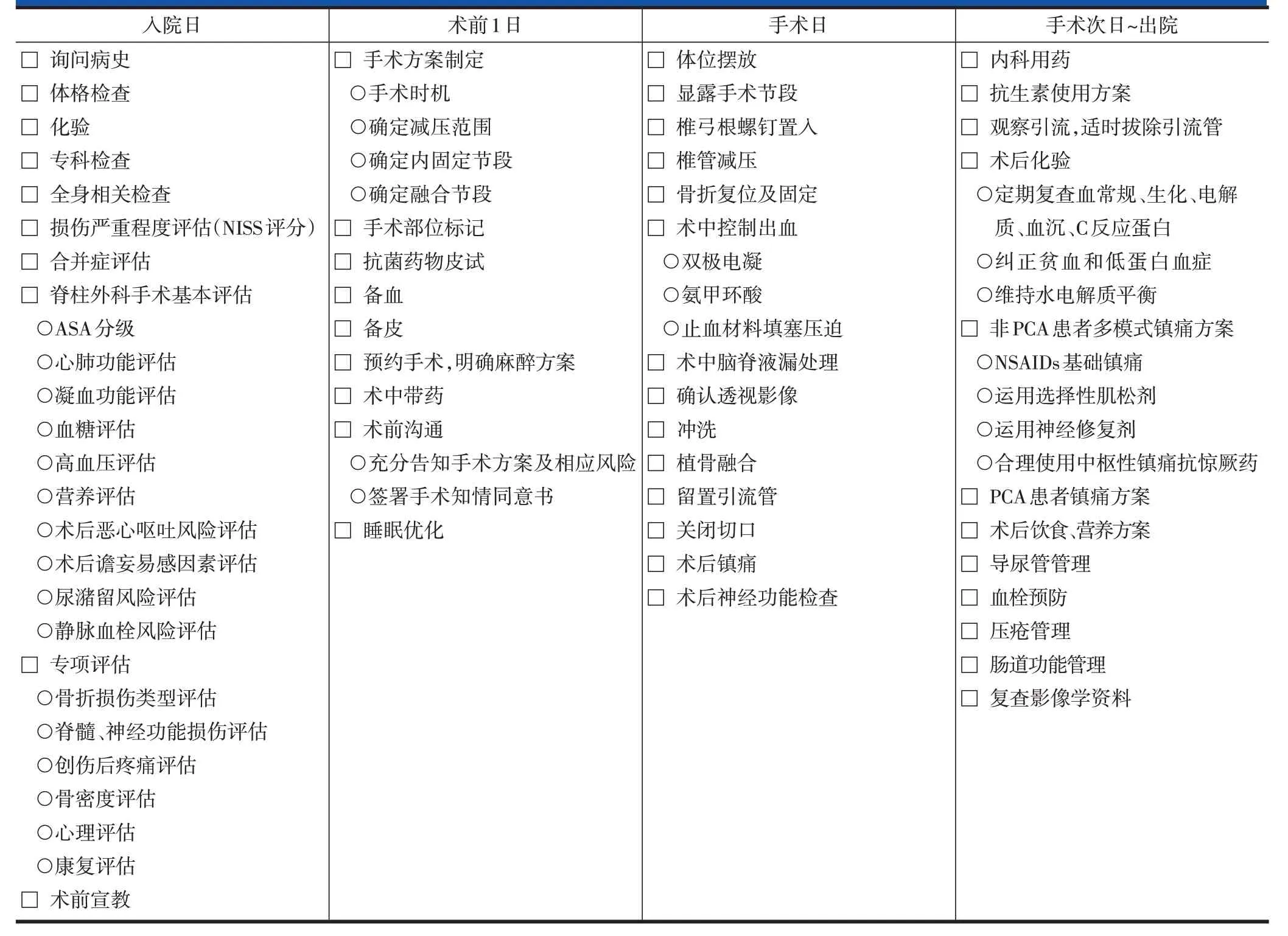
表1 急性成人胸腰段脊柱脊髓损伤后路手术的ERAS实施流程——外科医师表单
4.3.2 脊髓、神经功能损伤评估:胸腰段脊柱脊髓损伤神经功能评估首先需要判断神经损伤的部位,分为脊髓损伤、马尾神经损伤、神经根损伤等;其次推荐使用ASIA评估患者的神经功能状态[19]。
应用ASIA标准对患者进行神经功能评估时推荐使用以下顺序:①确定左右两侧的感觉平面;②确定左右两侧的运动平面;③确定神经平面;④确定损伤程度;⑤确定ASIA 残损分级;⑥确定部分保留带(zone of partial preservation,ZPP)。
感觉平面、运动平面及神经平面的确定见前所述。ASIA分级A级为在骶段S4~S5无任何感觉和运动功能保留;B级为损伤平面以下包括S4~S5自主活动消失,但感觉功能保留;C 级为损伤平面以下感觉存在,且至少一半以上的关键肌肌力<3级;D级为损伤平面以下感觉存在,且至少一半的关键肌肌力≥3级;E级为自主活动和感觉功能正常。其中A级为完全损伤,E级为无损伤,其余B、C、D级为不完全损伤。
ZPP的概念越来越受到重视,因为脊髓损伤后部分保留带是脊髓功能恢复的重要预测因素,有重要临床意义。以往关于ZPP 的定义只是适用于完全脊髓损伤,而在脊髓损伤神经功能分类标准2019 更新版中重新定义了ZPP,不再以ASIA分级为基础,而是以鞍区S4~S5 无任何感觉(肛门深部压觉、鞍区轻触觉、鞍区针刺觉)或运动功能保留(肛门自主收缩)为基础。定义ZPP一般使用的是关键肌确定损伤平面,但如果无鞍区运动功能保留,且运动平面以下存在3个节段以上的非关键肌运动功能保留,也可使用非关键肌确定损伤平面。
4.3.3 创伤后疼痛和功能评估:可采用视觉模拟评分(visual analogue score,VAS)、Oswestry 功能障碍指数(Oswestry disability index,ODI)等对腰背痛及日常功能进行评估。
4.3.4 骨密度评估:对于绝经后妇女和65岁以上男性,需在围手术期进行骨密度测量,合并骨质疏松(T 值<-2.5 SD)的患者,不在本共识的讨论范围内。
4.3.5 患者心理评估:胸腰段脊柱脊髓损伤不仅导致患者疼痛和残疾,由于生活质量下降和长期卧床亦会给患者带来心理问题。建议采用患者健康状况问卷-9(patient health questionnaire-9,PHQ-9)[20]和广泛性焦虑自评量表-7(generalized anxiety disorder-7,GAD-7)进行评估,必要时请心理科或精神科医师进行干预。
4.3.6 康复评估:所有患者都应进行康复评估,目的是了解患者的功能状态和预后,制定个体化的康复方案。术前评估的重点是脊柱脊髓功能(ASIA 分级)、泌尿功能、支具和矫形器。术后阶段性评估内容包括:①脊柱脊髓功能评定:ASIA 分级;②疼痛评估:VAS 评分[21]、ODI;③日常生活活动能力(activity of daily living,ADL)评定:未合并脊髓损伤者使用改良Barthel 指数(modified Barthel index,MBI),合并脊髓损伤者使用脊髓损伤独立性测量(spinal cord lesion independence measure,SCIM)[22];④生活质量(Quality of life,QOL)评估:健康调查量表(36-item short form health survey,SF-36)[23]、欧洲五维健康量表(European five-dimensional health scale,EQ-5D)。
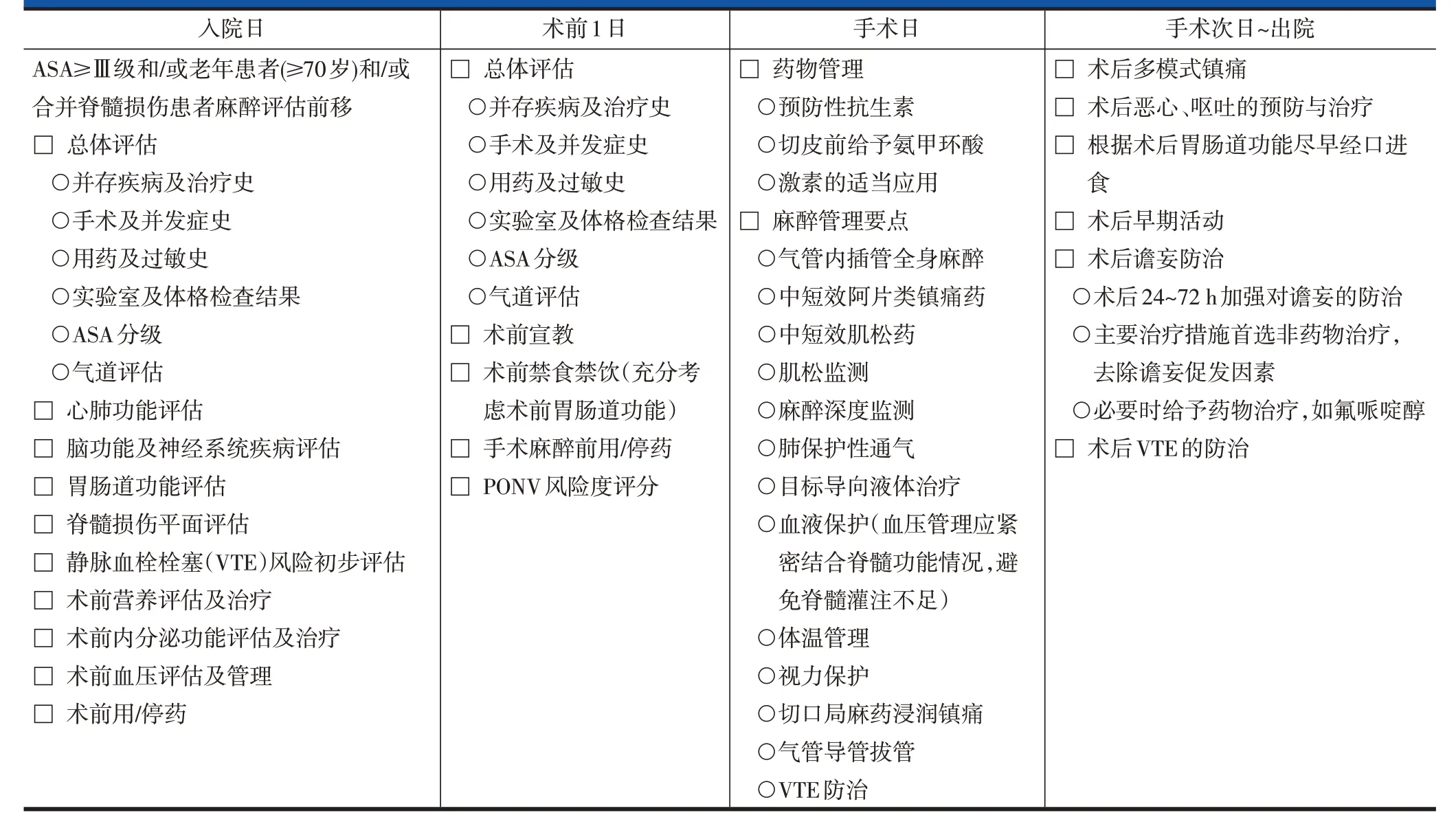
表2 急性成人胸腰段脊柱脊髓损伤后路手术的ERAS实施流程——麻醉医师表单
5 术前宣教
急性成人胸腰段脊柱脊髓损伤患者围手术期ERAS 倡导由外科医师、麻醉医师、病房与手术室护士、康复医师组成的多学科协作诊疗,应从患者入院后的综合宣教开始。
入院后应向患者讲解胸腰段脊柱脊髓损伤后疼痛产生机理和出现神经损伤的原因,安抚患者因创伤造成的心理打击,同时指导患者进行有效咳嗽排痰、床上排便训练,预防相关并发症的发生。
术前宣教的一个重点是使患者更好地了解神经损伤的预后,更客观地明确神经功能可能的恢复状况和康复目标,因为胸腰段脊柱脊髓损伤中神经损伤不同的损伤类型和损伤程度预后截然不同。T11、T12骨折合并的神经损伤为腰段脊髓损伤,T12、L1骨折合并的神经损伤为圆锥损伤,L2 骨折合并的神经损伤多为马尾神经损伤,而脊髓损伤和马尾神经损伤的功能恢复及对患者生活质量的影响不同;同时,仅有10%~20%ASIA 分级A 级患者术后可重新获得运动功能,ASIA 分级B 级的患者中20%~25%在术后1 年后可恢复行走能力,而对于运动不全损伤(ASIA C 级和D 级)的患者,神经功能可获得更好的恢复。因此,术前应与患者充分沟通,告知神经损伤的预后,明确手术获得的收益是否与患者的预期一致。
术前宣教的另一个重点是使患者了解神经损伤后潜在的早期和晚期并发症,及相应的应对措施,并获取患者及家属的理解和配合,尽量减少并发症带来的不利影响。例如,胸腰段脊髓损伤后泌尿系的并发症为膀胱功能障碍,可出现尿失禁或尿潴留、泌尿系感染及上尿路损害,甚至引起肾功能衰竭导致死亡;而间歇导尿是解决膀胱功能障碍和减少泌尿系感染的重要措施。因此,对于伴有神经损伤的胸腰段脊柱脊髓损伤患者,术前宣教中也应重点介绍脊髓损伤后易出现的泌尿系感染、压疮、下肢深静脉血栓等相关并发症及其应对措施。
同时,康复医师应在术前与患者及家属进行充分沟通。不合并脊髓损伤者应按照脊柱后路融合术的流程,告知术后翻身、起床等转移方法及肢体功能锻炼方法。合并脊髓损伤者应按照截瘫康复流程,告知患者家属术后体位摆放的要求、支具穿脱方法、转移方法、肢体主、被动功能锻炼方法、呼吸功能训练、膀胱功能训练、矫形器使用方法等,同时注重心理疏导。

表3 急性成人胸腰段脊柱脊髓损伤后路手术的ERAS实施流程——病房护士表单
6 麻醉要点
胸腰椎骨折因解剖位置特殊,手术创伤较大,围手术期并发症多,麻醉处理有其特殊性。麻醉医师除常规麻醉任务外还需协助骨科医师积极处理存在脊髓损伤患者的植物神经功能紊乱和抢救脊髓功能。优化围手术期麻醉管理策略有利于减少全身应激,提高围手术期安全性和舒适性,降低围手术期并发症。胸腰段脊柱脊髓损伤后路手术中患者均取俯卧位,通常选择全身麻醉,麻醉前可使用糖皮质激素,有助于预防术后恶心呕吐、抑制气道高反应性、预防过敏反应、减轻全身炎症反应。
对于术前不合并胃肠功能紊乱,如胃排空障碍、消化道梗阻的患者,术前禁食6 h,禁饮2 h;术前2 h可服用清饮(≤400 ml)。对于术前存在脊髓损伤后神经源性胃肠道功能障碍患者,应根据胃肠道功能情况审慎应用ERAS倡导的术前禁食水原则,麻醉实施前应予足够的胃排空时间,降低返流误吸风险[24]。
胸腰椎骨折患者术前可能合并血容量不足、自主反射亢进综合征和离子平衡紊乱等,术中应采取有针对性的管理措施。除建立常规无创监测外,中心静脉压力监测和有创动脉压力监测可精准指导循环、呼吸、代谢的管理。麻醉深度监测以脑电双频指数(bispectral index,BIS)控制在40~60 为标准,避免血压骤然波动引起脊髓血流紊乱。
术中循环管理方面,提倡以目标导向性液体治疗(goal-directed therapy,GDT)的理念及措施指导液体治疗[25]。术中维持出入量平衡,避免输液过度引起的心功能不全和外周组织水肿,避免输液不足引起的隐匿性低血容量和组织低灌注。在麻醉诱导和体位搬动过程中需严密观察血流动力学变化,必要时辅助应用血管活性药物,推荐适当使用α肾上腺素受体激动剂,如苯肾上腺素或低剂量去甲肾上腺素等缩血管药物,避免血压剧烈波动增加心脑血管并发症或影响脊髓血供,建议维持术中血压波动不超过术前水平的20%[26]。术前存在脊髓损伤患者不建议常规控制性降压,避免脊髓低灌注,建议维持平均动脉压在80~90 mmHg[27,28]。对于术中预计出血量达到总血容量10%或>400 ml时,建议采用自体血回输[29,30]。
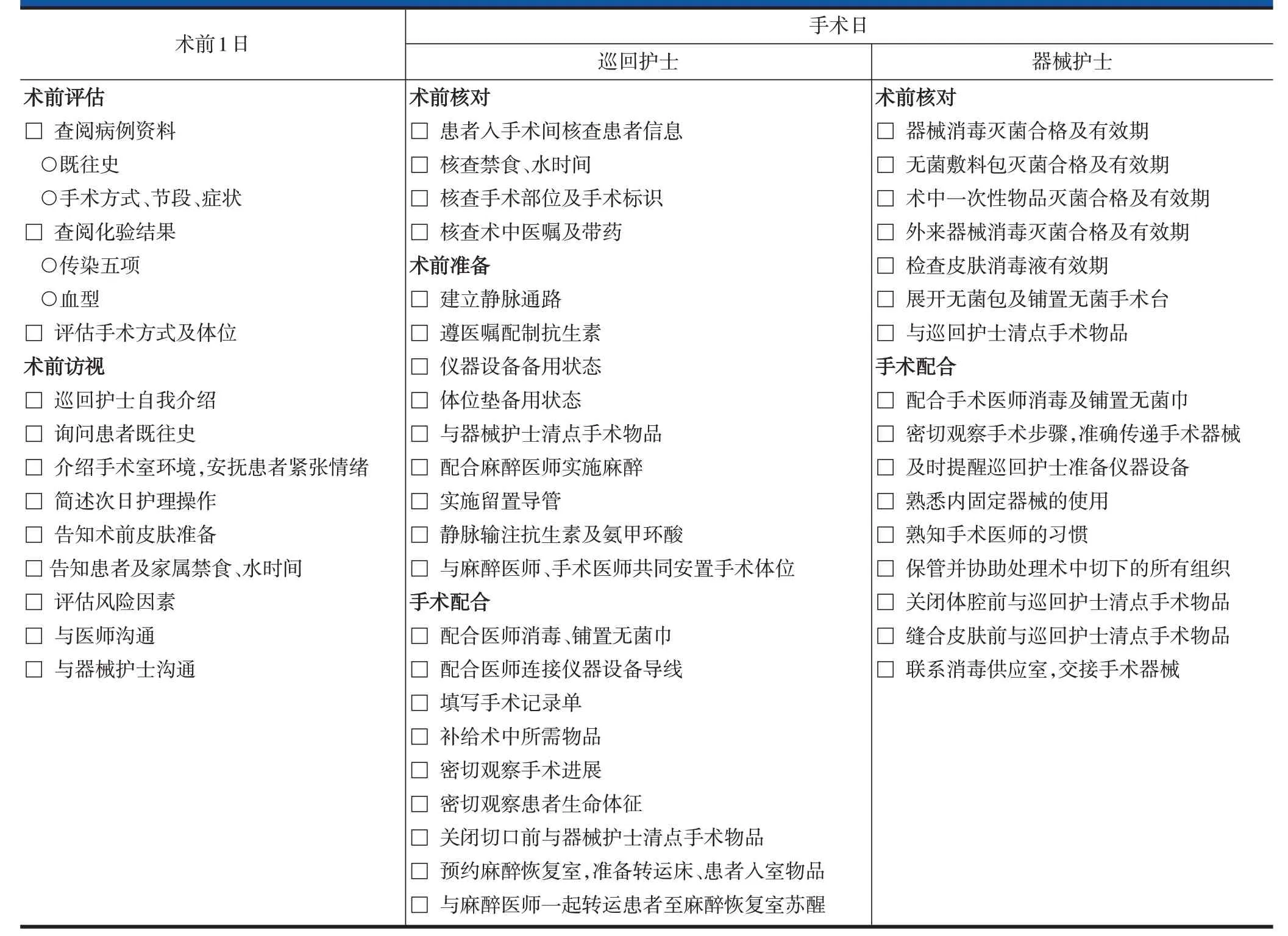
表4 急性成人胸腰段脊柱脊髓损伤后路手术的ERAS实施流程——手术室护士表单
术中采取肺保护性通气策略可避免加重术前存在的肺损伤,有效降低术后肺部并发症发生率,同时注意加强体温管理。推荐多模式预防术后恶心呕吐。
7 手术时机
《成人急性胸腰段脊柱脊髓损伤循证临床诊疗指南》[2]Ⅰ级证据表明,在不完全脊髓损伤呈进行性加重时,应行急诊手术治疗。在条件允许的情况下,推荐合并脊髓及马尾神经损伤患者尽可能在48 h内行手术治疗[31,32]。对于不合并脊髓及马尾神经损伤的患者,在条件允许的情况下,尽早手术治疗,因为一项Ⅰ级证据表明对无神经损伤的胸腰段脊柱脊髓损伤患者行早期手术可实现早期功能锻炼,减少并发症,缩短住院时间[33]。
8 手术要点
急性成人胸腰段脊柱脊髓损伤后路手术的主要目的是恢复脊柱序列,解除神经压迫,重建脊柱稳定性。手术入路的选择应根据患者后方韧带复合体和神经功能状态、医疗设备及技术条件,从简单到复杂,尽可能在单一入路下完成手术。本共识主要聚焦后路手术。
8.1 正确的体位摆放
正确的体位摆放有利于术中体位复位、减少术中出血和术后并发症。关注点包括:①体位摆放应方便术中体位复位,对于骨折脱位的患者,应尽量通过体位复位使骨折断端接近解剖复位;②建议使用俯卧位垫悬空胸部和腹部或使用碳纤维床,避免腹部压力增加引起术中出血增多;③俯卧位时应注意骨性凸起处使用琼脂垫保护以防压疮,同时保证男性生殖器避免受压。术中尽可能使颈椎保持中立位,若头是偏向一侧,俯卧时间超过1 h后,应将头偏向另外一侧,每隔1 h更换1次,可起到保护患者颈椎的作用。
8.2 手术减压固定融合的原则
后路手术包括减压、固定和融合,但应根据患者情况进行个体化治疗。对于无神经损伤且椎管内存在骨性占位的胸腰椎骨折患者,可不行椎管切开减压;对于合并神经损伤者,推荐行椎管切开减压。多数胸腰段骨折可用短节段固定,对于骨折脱位者,推荐行长节段固定,对于椎弓根结构完整的伤椎,可行伤椎椎弓根螺钉固定。胸腰段爆裂骨折行后路复位椎弓根内固定者可不行植骨融合,而对于需要通过长节段固定获得稳定的患者,推荐长节段内固定加选择性短节段融合术。这部分的具体操作细节可参考《成人急性胸腰段脊柱脊髓损伤循证临床诊疗指南》[2]。
8.3 术中出血控制
胸腰段后路手术术中出血来源主要是骨折断端出血和神经减压时椎管内硬膜外出血。骨折断端出血可使用骨蜡封堵,而硬膜外出血应使用双极电凝进行止血,临近神经根周围应将双极电凝的功率控制在15 W 之内[34],同时使用明胶海绵等止血材料填塞。对于无法使用电凝止血的部位,可使用明胶海绵和棉片压迫止血。建议切皮前给予冲击量氨甲环酸10~20 mg/kg,根据情况术中以1 mg/kg/h 的速度持续泵入,能有效减少术中出血[35],而且不增加血栓风险。
8.4 术中脑脊液漏的处理
如果术中发生脑脊液漏,应当立即仔细修补硬脊膜,对硬脊膜进行严密的缝合,可联合使用纤维蛋白胶封闭或人工硬脊膜补片修补,也可使用纤维肌肉瓣或脂肪组织进行填塞覆盖[36],放置引流管,并一定要严密缝合筋膜层。
8.5 切口闭合原则
分层缝合是关闭切口的原则。筋膜层的严密缝合可有效减少脑脊液漏的发生,减少切口渗液和感染的风险。筋膜层缝合要求头尾端不留死角。皮下组织层活动度大,缝合时尽量对合,减少脂肪液化和瘢痕的形成。皮肤层缝合建议采用可吸收倒刺线行皮内缝合,保证在皮缘对合的同时减少张力,这样有利于皮缘的血供,缩短愈合时间。
9 围手术期血液管理
围手术期血液管理目标主要为预防和治疗贫血。对于择期手术患者,手术前后应行贫血筛查并及时治疗贫血。当血红蛋白男性<130 g/L、女性<120 g/L时,因明确贫血原因,针对不同病因行相关治疗。对于术前血红蛋白<100 g/L患者,建议备血,术中根据情况行输血治疗,无需常规采用术中自体血回输,但对于预计出血量超过总血容量的15%时,建议采用自体血回输。
10 术后引流管的管理
对于伤口引流管,建议术后2~3 d 拔除,拔管指征为24 h引流量<50 ml。
对于合并脑脊液漏患者,研究表明早期(≤3 d)拔除引流管不会增加术后伤口不愈合及其他并发症发生率[37],因此建议早期拔除引流管并行加压包扎。但如果术者对筋膜层缝合不确定,可适当延长引流管
放置时间,拔管前行引流管夹闭试验[38],但禁用负压引流,防止低颅压、颅内血肿、蛛网膜下腔出血等。术后可采用头低脚高的体位,减轻脑脊液对破口压力,有利于硬脊膜裂口愈合。在维持水电解质平衡、适当补充蛋白的前提下,润肠通便、减少咳嗽可减少腹压引起的脑脊液压力增高,有利于硬脊膜愈合。
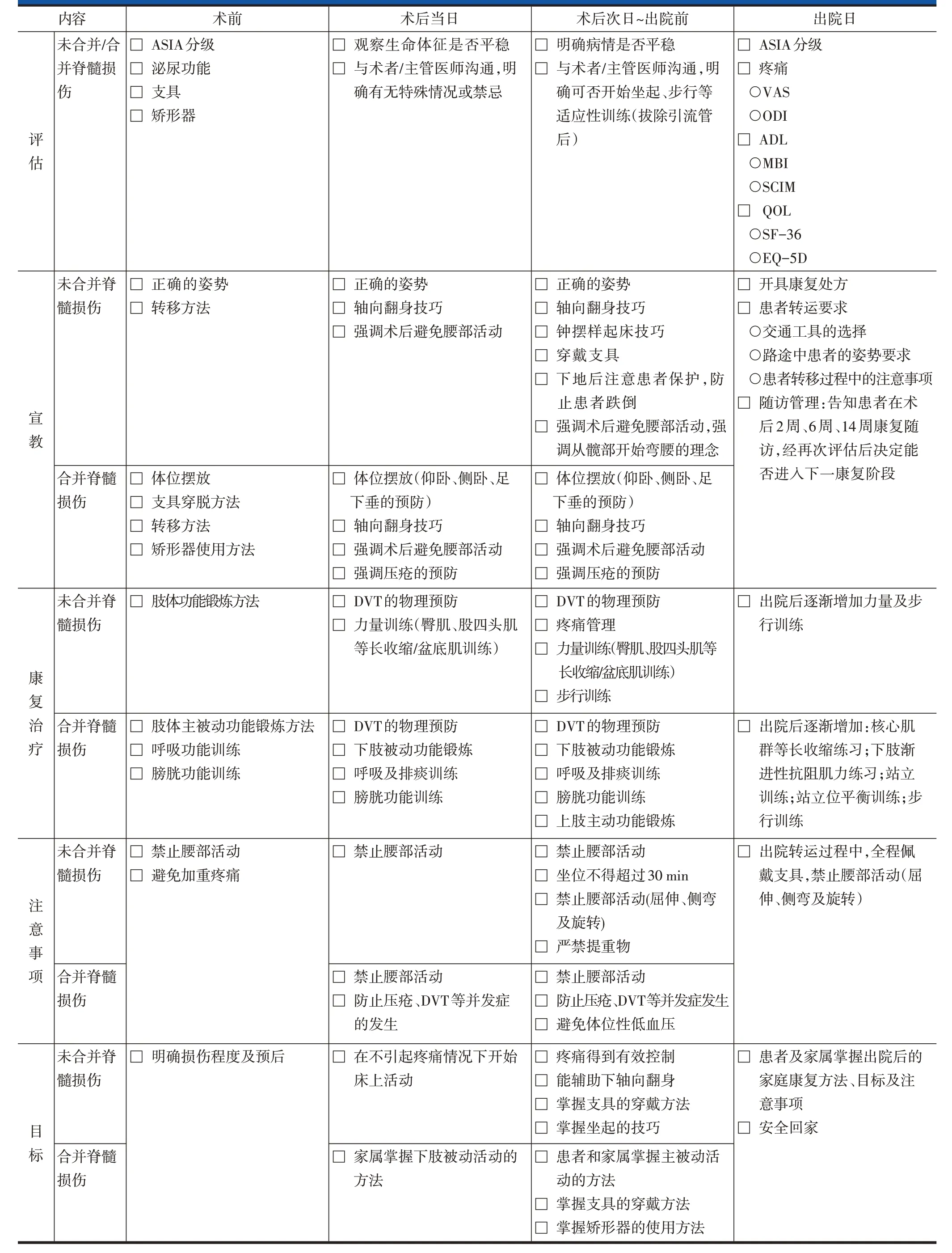
表5 急性成人胸腰段脊柱脊髓损伤后路手术的ERAS实施流程——康复医师表单
11 围手术期疼痛管理
控制围手术期疼痛是减少患者卧床及住院时间,加速康复的重要方法。胸腰段脊柱脊髓损伤患者围手术期疼痛包括骨折局部疼痛、切口周围疼痛及神经性疼痛。其中神经性疼痛相比其他疼痛程度更严重,因此需制定更加完善的围手术期疼痛控制方案:提倡超前镇痛和多模式镇痛,重视神经性疼痛。
创伤患者入院时常表现为疼痛,因此入院后即应开始镇痛。镇痛药以非甾体抗炎药(nonsteroidal anti-inflammatory drugs,NSAIDs)为基础,选择性COX-2抑制剂可发挥止痛及保护胃黏膜的作用。严重疼痛影响睡眠的患者可联合应用阿片类药物(盐酸曲马多、氨酚羟考酮等)和/或镇静催眠药,但应注意药物用量。术后患者可根据情况选择患者自控镇痛(patient controlled analgesia,PCA)或不使用镇痛泵。对于使用镇痛泵的患者,需注意预防恶心、呕吐;对于不使用镇痛泵的患者,根据疼痛评分,采用多模式镇痛,以NSAIDs 为基础用药,加用盐酸乙哌立松和中枢性镇痛、抗惊厥药(如普瑞巴林等),尽量减少阿片类药物的应用,以减少如恶心呕吐、肠麻痹等并发症发生。
12 围手术期尿管的管理
为促进胸腰段脊柱脊髓损伤后路手术患者早期下地活动,提倡在安全的前提下尽早拔除导尿管。导尿管的拔除分为以下2种情况:①对于无神经损伤的患者,女性在麻醉清醒后拔除导尿管,男性在术后第二天清晨拔除导尿管;对于有尿潴留高危因素的患者,可适当延长拔管时间[39]。②对于合并神经损伤的患者,泌尿系干预的目的主要是预防膀胱过度膨胀、泌尿系感染及上尿路损害,清洁间歇导尿的近期和远期效果都是安全的,无菌间歇导尿更有助于减少泌尿系感染和菌尿的发生。
急性胸腰段脊髓损伤造成排尿功能障碍时,应立即采取留置导尿,每1~2周更换;当患者合并尿道损伤等留置导尿禁忌证时,可行耻骨上膀胱造瘘[40]。当出入量平衡时,可停止留置导尿,开始间歇导尿,每4~6 h导尿1次。当存在尿道狭窄、膀胱颈部梗阻、尿道或膀胱损伤(尿道出血、血尿)、膀胱容量<200 ml时应推迟间歇导尿,待上述情况处理后可继续间歇导尿[41]。间歇导尿后,若残留尿量<l00 ml,应行系统膀胱训练,锻炼反射性排尿,同时应定期行尿常规、细菌培养检查,一旦发生感染,可根据已知敏感药物进行治疗。
13 并发症的预防和处理
13.1 血栓的预防
深静脉血栓是脊髓损伤后的常见并发症,常在脊髓损伤后2 周内发生,脱落后常引起致命肺栓塞,是这一时期死亡的主要原因之一。由于伤后瘫痪、活动减少、尤其是交感神经系统损伤导致血管调节机能受损引起静脉血流淤滞,最常见于小腿,但大腿和腹股沟处的深静脉血栓更为危险。
对于不合并神经损伤、双下肢运动功能正常的患者,如患者条件允许,术后24 h即可下地活动。术后采用基础预防结合物理预防(弹力袜)的方式预防下肢深静脉血栓,术后第二日开始行下肢适应性训练预防血栓,对于不能下地患者使用下肢静脉泵、主动或被动活动等综合性方法预防血栓。对于合并神经损伤、无法下地活动的患者,建议在使用机械性预防外应用低分子肝素[42]。无论是否合并脊髓损伤,均应定期行双下肢静脉B超检查,并监测D-二聚体。
13.2 压疮的管理
首先做好患者和家属宣教,使其了解保护皮肤完整的重要性,定时检查压疮的好发部位,应从以下方面管理:①加强皮肤护理,至少每2 h 翻身1 次,早期合理应用减压床垫等设备,保持受压皮肤清洁干燥,避免温度过高;②防止各种原因引起的皮肤损伤;③压疮一旦发生,应定期换药,改善全身营养状态,借助各种理疗方法促进压疮愈合;④对长期不愈合、伴有骨关节感染、窦道形成的Ⅲ、Ⅳ度压疮建议手术治疗。
13.3 肠道功能管理
尽早评估患者直肠功能,观察粪便性状、排便次数和频率,判断直肠功能障碍的类型(反射性直肠和迟缓性直肠)。反射性直肠由S2 以上的脊髓损伤造成,迟缓性直肠由S2 以下的脊髓损伤及马尾神经损伤造成。反射性直肠因排便反射存在,可通过反射自主排便,建议使用手指刺激和轻叩中腹的方法促进排便;迟缓性直肠无排便反射,脊髓损伤早期可使用栓剂,必要时行手工排便。
14 术后康复锻炼
根据是否合并脊髓损伤,选择相应的康复流程。
14.1 不合并脊髓损伤的康复
对于稳定型骨折,根据患者切口情况及留置管道拔除情况,强调康复早期介入、早期离床。对于不稳定型骨折,根据术者建议佩戴支具离床[43]。术后早期以深静脉血栓预防、呼吸功能训练、转移训练及四肢的主动活动练习为主;逐渐增加核心肌群的等长收缩练习及步行训练。
14.2 合并脊髓损伤的康复
根据ASIA 分级制定相应的康复方案。术后早期,注意体位摆放及床上转移训练,防止压疮;注意保持踝关节功能位,防止足下垂;呼吸及排痰训练;膀胱功能训练;下肢被动活动练习,避免因挛缩造成关节活动受限;鼓励患者进行上肢的主动活动及力量训练,为下地时支撑辅助器械做准备。待患者一般情况稳定后,佩戴支具进行起床训练,注意循序渐进,避免体位性低血压;增加核心肌群等长收缩练习及下肢渐进性抗阻肌力练习,并根据ASIA 分级选择相应矫形器,逐渐增加站立训练、站立位平衡训练及步行训练。必要时辅以功能性电刺激、减重步行训练等[44-47]。
专家组成员(按姓氏笔画)
丁 琛 马亚群 王思亮 王诗军 毛海青 刘西芳 刘 浩 刘 楠 闫 航 孙天胜 孙 宇
孙浩林 孙 维 杜 培 李 放 李 莉 李淳德 李 静 杨惠林 邱贵兴 邹叶芳 沈建雄
宋琳琳 张志成 张 蕾 陈 峰 苑 垒 周非非 周谋望 郑林宏 郑博隆 孟 浩 郝定均
洪 瑛 贺宝荣 高子军 高 杰 殷国勇 郭 航 唐 帅 越 雷 黄大耿 韩 彬 嵇富海
蔡思逸 董补怀
说明:本共识为《脊柱手术加速康复外科实施流程专家共识》系列共识之一,为方便读者阅读,系列共识中的部分段落有重复,不属于学术不端范围,特此说明。
