利培酮缓释片的体外释放度及其在家兔体内的药动学研究Δ
2019-08-15王敏王倩李春霞沈雁孙益新
王敏,王倩,李春霞,沈雁,孙益新
(1.南京医科大学附属儿童医院药学部,南京210000;2.中国药科大学药学院药剂系,南京 210009)
有序介孔二氧化硅材料是一类孔径在2~50 nm范围内且孔道结构有序的多孔材料,其不仅具有适宜的孔径和有序的孔道结构,还具有较高的比表面积、稳定的骨架结构和易于修饰的内表,因此其应用范围较为广泛[1-2],主要应用于药物控制释放、催化、生物传感以及癌症的治疗[3],其较为重要的一个应用即作为药物载体。部分特异性和溶解性较差的药物,患者需要服用大剂量的药物才能达到足够的治疗效果,大剂量的药物又是引发药品不良反应的首要原因,特别是对于治疗窗窄或有细胞毒性的化疗药物。所以,寻求合适的载体来增加特异性和溶解度较差药物的靶向性和溶解度显得尤为重要。2001年,Vallet-Regí首次提出将介孔二氧化硅作为缓控释系统中药物的载体[4],由于介孔二氧化硅材料拥有分子级别的孔道直径、较大的比表面积、狭窄的孔径分布、有序的孔道结构以及良好的生物相容性,适用于作为药物的骨架型载体,将药物载入到孔道内部,延长药物释放时间,提高药效的持久性;此外,还可对介孔二氧化硅进行修饰,以达到靶向效果,将药物准确地运送到靶细胞和病变部位[5]。介孔二氧化硅的制备方法包括水热合成法[6]、溶胶-凝胶法、微波合成法、相转变法以及在非水体系中的合成等。
利培酮(Risperidone)为苯并异 唑衍生物,是多巴胺D2受体及5-羟色胺2A受体有力的拮抗药,水溶性差,适用于急慢性精神分裂症及其阳性症状和阴性症状的治疗[7]。与典型的抗精神病药物氯丙嗪、氟哌啶醇等相比,利培酮的临床疗效好、不良反应小,能显著提高患者的生活质量[8]。利培酮口服吸收很快,1~2 h就可达到血药浓度峰值,半衰期为3 h,在肝代谢酶细胞色素P450(CYP)2D6的作用下可转化为9-羟基利培酮;9-羟基利培酮是利培酮的主要代谢产物,药理活性是利培酮的70%,二者共同构成抗精神病药的活性成分。目前利培酮的上市制剂有薄膜包衣片、胶囊剂、口服溶液剂、分散片、口腔崩解片、口腔速溶膜、微球注射剂(缓释),主要以口服固体制剂(速释)为主,该类制剂主要用于精神病急性发作时用药。现有速释制剂用于患者急性发作时,具有良好的效果,但针对精神病类疾病长期性、间断性发病,患者需要长期频繁服药,因此近年来研究者们利用各种新剂型和新技术,力图不断提高制剂的缓控释性能,意在改善精神病患者的精神状态,减少甚至避免患者病症的急性剧烈发作,从而提高患者生存质量。虽然缓控释注射微球可以较好地提高制剂的缓控释性能,但是其使用不如口服制剂便捷,注射给药时有时还需要熟练注射操作的专业人员协助。因此课题组研制了一种新型的以介孔二氧化硅为骨架的利培酮缓释片。
本文建立了利培酮和9-羟基利培酮血药浓度的高效液相色谱(HPLC)检测方法,并以家兔为模型动物,以市售利培酮片(商品名:维思通)为参比制剂,经介孔二氧化硅负载的利培酮缓释片为受试制剂,探讨二者在家兔体内的药动学特征。以介孔二氧化硅为骨架的利培酮缓释片的释药机制图见图1。
1 材料
1.1 仪器
U-3000 HPLC系统,配有四元泵、在线脱气机、自动进样器、UV检器和Chromeleon工作站(美国Themo公司);UV-3200紫外分光光度计(上海美谱达仪器有限公司);78X-6A片剂四用测定仪、YPD-200C片剂硬度测定仪(上海黄海药检仪器有限公司);DP-30A单冲压片机(上海天祥健台制药机械有限公司);KDC-140HR高速冷冻离心机(安徽中科中佳科学仪器有限公司);PHS-3C pH计(上海雷磁仪器厂)。
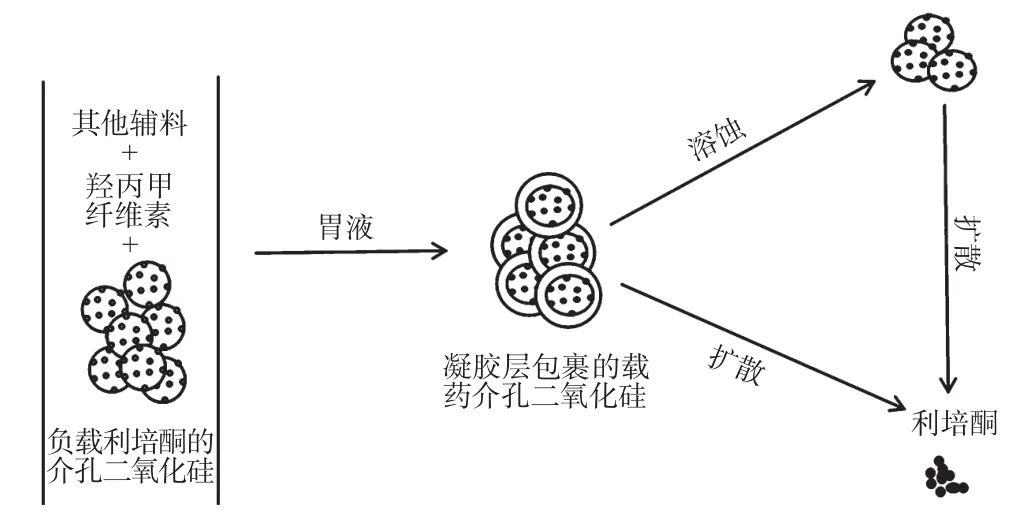
图1 以介孔二氧化硅为骨架的利培酮缓释片的释药机制图Fig 1 Release mechanism of Risperidone sustained-release tablets with mesoporous silica as matrix
1.2 药品与试剂
利培酮原料药(武汉贝尔卡生物医药有限公司,批号:20140722,纯度:99.0%);利培酮对照品(批号:100570-201704,纯度:99.9%)和氯氮平(内标)对照品(批号:100323-201002,纯度:99.8%)均购自中国食品药品检定研究院;9-羟基利培酮原料药(济南伟都精细化工有限公司,批号:11082301,纯度:99.2%);利培酮片(商品名:维思通,西安扬森制药有限公司,批号:C14202188122,规格:2 mg);CEOLUSTMKG802微晶纤维素(MCC,日本旭化成株式会社);Tablettose®80乳糖(德国美剂乐集团);介孔二氧化硅[中南大学提供,批号:170401,比表面积:680 m2/g,孔容积:3.4 cm3/g,平均孔径:9.0 nm(7~12 nm)];硬脂酸镁(SH-YM-L)、玉米淀粉(SH-L)、羟丙甲纤维素(HPMC K4M)均购自安徽山河药用辅料股份有限公司;肝素钠[中国医药(集团)上海化学试剂公司,分析纯];乙腈和甲醇为色谱级,浓盐酸、乙醚、乙酸铵、乙酸、氢氧化钠等均为分析纯。
1.3 动物
新西兰家兔,普通级,♀♂各半,约2.5 kg,购自南京市江宁区青龙山动物繁殖场,实验动物生产许可证号:SCXK(苏)2017-0001。
2 方法与结果
2.1 载药介孔二氧化硅的制备及载药率测定
2.1.1 载药介孔二氧化硅的制备 按前期研究[9]方法,采用振荡法对介孔二氧化硅进行载药。精密称取利培酮 2.0 g,加入甲醇15 mL,超声(频率:30 kHz,功率:250 W,时间:3~5 min)溶解,加入介孔二氧化硅7.0 g,搅拌,超声(频率:25 kHz,功率:200W,时间:20 min)后放置在平板振荡器上,振荡频率40 r/min,用红外灯1 W/m2照射4 h,放入真空干燥箱,温度为30℃,干燥10 h,最终制得载药介孔二氧化硅。
2.1.2 载药率测定 按前期研究[9]方法测定载药量。精密称取3份等量载药介孔二氧化硅,各0.01 g,置于10 mL离心管中,加甲醇7 mL,超声(频率:30 kHz,功率:250 W,时间:10 min),离心(13 360×g)10 min,收集上清液;所得沉淀再按上述方法处理2次,合并上清液,加甲醇定容至100 mL,于236 nm波长处测定吸光度值,计算利培酮含量,并按照下面的公式计算载药率:载药率=载体中药物质量/载体和药物总质量×100%。结果,载药介孔二氧化硅的载药率为20.0%(n=3)。
2.2 利培酮缓释片的制备
采用粉末直接压片法制备利培酮缓释片。采用等量递加法将已过40目筛的载药介孔二氧化硅30 g、HPMC K4M 300 g、MCC 170 g、乳糖100 g 依次进行混合,再用过筛法(20目筛)充分混匀,加入润滑剂硬脂酸镁5 g,选用7号冲头,控制片剂硬度为7 kg/cm2,片质量为200 mg,压片,即得利培酮缓释片,每片含利培酮2 mg。分别制备3批利培酮缓释片,批号分别为090101、090102、090103。
2.3 利培酮缓释片的体外释放度测定
2.3.1 体外释放度的测定 将片剂放入转篮中,加释放介质0.1 mol/L盐酸900 mL,设定转速为100 r/min,温度为(37±0.5)℃,启动溶出仪,于 5、15、30、60、90 min以及 2、3、4、6、8、10、12 h定时取样,同时补充等量同温度空白介质以保持释放液体积恒定。所取样液经0.45 μm微孔滤膜过滤,取续滤液,作为供试品溶液,于236 nm波长处测溶液的吸光度,并计算累积释放度(Q)。比较市售利培酮片、3批利培酮缓释片及其物理混合物(利培酮、介孔二氧化硅以载药比例物理混合,其他处方与利培酮缓释片均一致,直接压片法制得片剂)的体外释放曲线,结果见图2。
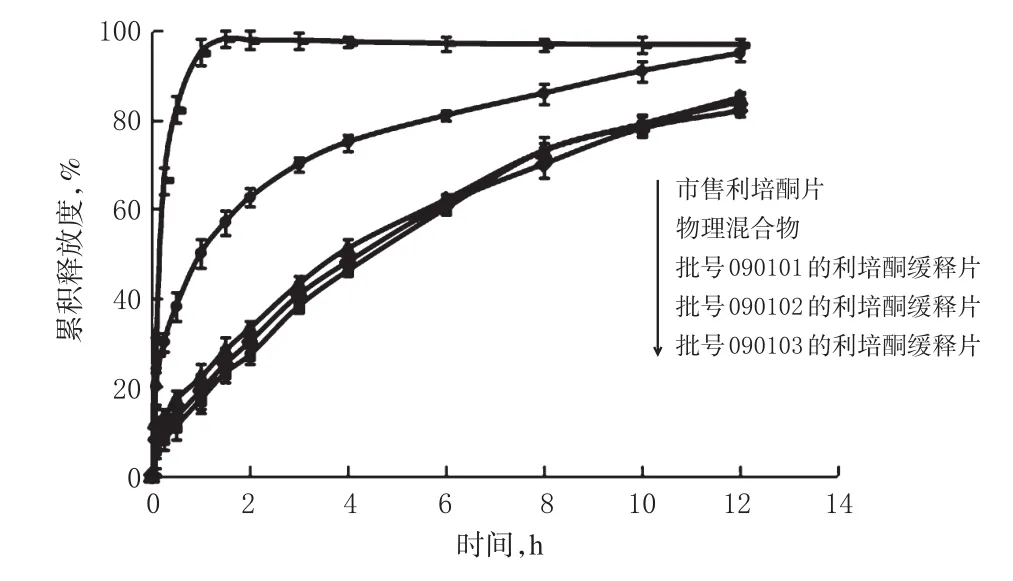
图2 市售利培酮片、利培酮缓释片及其物理混合物的体外释放曲线(n=6)Fig 2 Release curve in vitro of commercially available Risperidone tablets,Risperidone sustained-release tablets and physical mixtures(n=6)
由图2可以看出,与市售利培酮片和物理混合物比较,利培酮缓释片的释放速度明显减慢。市售利培酮片、物理混合物以及批号分别为090101、090102、090103的利培酮缓释片的12 h释放度(Q12h)分别为97%、95%、82%、84%、85%,利培酮缓释片的平均Q12h为83.7%。同时采用相似因子(f2)法比较3批利培酮缓释片的体外释放曲线发现,f2均大于50,表明3批间体外释放稳定,无明显差异。
2.3.2 体外释放机制 按零级释放、一级释放、Higuchi方程、Hixson-Crowell方程和Ritger-Pappas方程对“2.3.1”项下利培酮缓释片的体外释放数据进行拟合,结果见表1。
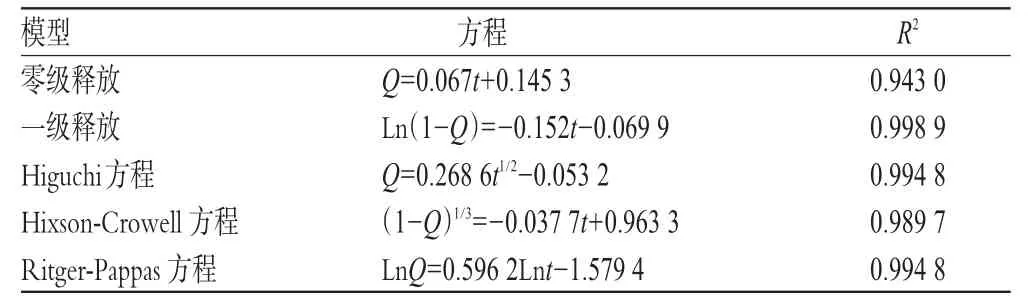
表1 利培酮缓释片的释药模型拟合结果Tab 1 Release model fitting of Risperidone sustainedrelease tablets
由表1可以看出,利培酮缓释片在0.1 mol/L盐酸中的释放更接近于一级释放,表明药物体外释放速率与药物浓度成正比。Higuchi方程反映的是扩散机制,Hixson-Crowell方程反映的是溶蚀机制,从拟合结果看,Higuchi方程扩散机制优于Hixson-Crowell方程溶蚀机制,说明利培酮缓释片的释药机制是扩散与溶蚀相结合的,扩散为主、溶蚀为辅,与Ritger-Pappas方程拟合结果一致(Ritger-Pappas中n=0.596 2,即 0.45<n<0.89,提示药物释放机制为扩散与骨架溶蚀机制相结合)。
2.4 利培酮血药浓度的测定
参考文献[10]建立测定家兔体内利培酮血药浓度的方法。
2.4.1 色谱条件 色谱柱:Agilent Zorbax Eclipse Plus C18(250 mm×4.6 mm,5 μm);流动相:0.1 mol/L醋酸铵溶液(用氨试液调节pH 至5.0)-甲醇-乙腈(30∶50∶20,V/V/V);检测波长:279 nm;柱温:25 ℃;流速:1 mL/min;进样量:20 μL。
2.4.2 贮备液的制备 将利培酮对照品、9-羟基利培酮原料药和氯氮平对照品经105℃干燥2 h,分别准确称样用甲醇配制成质量浓度分别为100 μg/mL的利培酮贮备液、100 μg/mL的9-羟基利培酮贮备液和20 μg/mL氯氮平贮备液,保存于4℃冰箱备用。
2.4.3 血浆样品处理 精密吸取血浆样品0.5 mL于10 mL离心管中,加入氯氮平贮备液50 μL,轻轻摇匀,加入2 mol/L氢氧化钠溶液0.5 mL,摇匀后加入无水乙醚4 mL,涡旋振荡5 min,离心(1 484×g)4 min,取上层乙醚层3 mL,真空浓缩(1 500 r/min,40℃,35 min,下同)至干,然后加入1 mol/L盐酸溶液0.2 mL涡旋振荡3 min,真空浓缩至干,残渣用100 μL流动相溶解,离心(1 484×g)10 min后精密量取上清液进样分析。
2.4.4 专属性考察 取利培酮贮备液、9-羟基利培酮贮备液、氯氮平贮备液和利培酮贮备液+9-羟基利培酮贮备液+氯氮平贮备液+空白血浆按“2.4.1”项下色谱条件进样分析,记录色谱图。结果,利培酮、9-羟基利培酮和氯氮平的保留时间分别为4.2、3.7和8.4 min,理论板数以利培酮计均大于3 000,利培酮和9-羟基利培酮的分离度为3.16,利培酮和氯氮平的分离度为17.36。高效液相色谱图见图3。
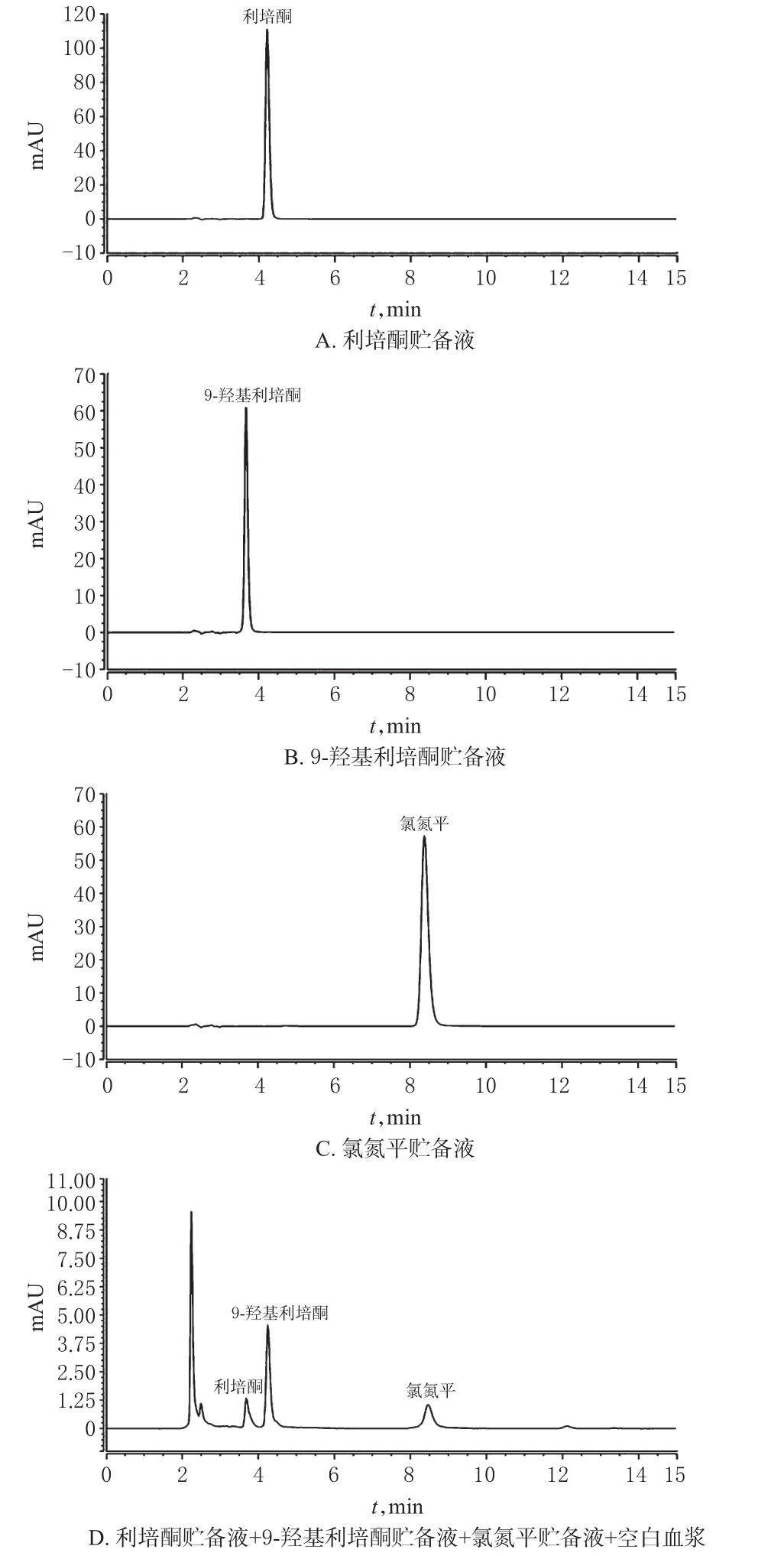
图3 高效液相色谱图Fig 3 HPLC chromatograms
2.4.5 线性关系考察 分别精密吸取一定体积的利培酮贮备液和9-羟基利培酮贮备液,用甲醇稀释成质量浓度为10、100、200、400、600、800、1 000、1 200 ng/mL的系列标准溶液。分别取上述系列标准溶液各50 μL,置于离心管中,精密吸取空白血浆0.5 mL,按“2.4.3”项下方法处理后,进样分析。以利培酮或9-羟基利培酮与氯氮平的峰面积比(y)对利培酮或9-羟基利培酮的质量浓度(x)进行线性回归分析。得利培酮的回归方程为y=0.109x+0.073 6(r=0.999 1),在 1~120 ng/mL质量浓度范围内线性关系良好,定量下限为1 ng/mL;9-羟基利培酮的回归方程为y=0.084 4x-0.074(r=0.999 3),在1~120 ng/mL质量浓度范围内线性关系良好,定量下限为1 ng/mL。
2.4.6 回收率试验 (1)方法回收率。取0.5 mL空白血浆,加入利培酮贮备液和9-羟基利培酮贮备液,配制低、中、高质量浓度(利培酮和9-羟基利培酮质量浓度分别均为20、60、100 ng/mL)的血浆样品,按“2.4.3”项下方法处理后进样分析,记录峰面积,代入回归方程计算含量和方法回收率。结果显示,利培酮低、中、高质量浓度血浆样品的方法回收率分别为101.0%、98.4%、99.3%,RSD分别为1.50%、0.46%、2.02%(n=3);9-羟基利培酮低、中、高质量浓度血浆样品的方法回收率分别为102.8%、98.8%、98.8%,RSD分别为0.85%、0.39%、1.39%(n=3)。(2)提取回收率。取0.5 mL空白血浆,加入利培酮贮备液和9-羟基利培酮贮备液,配制低、中、高质量浓度(利培酮和9-羟基利培酮质量浓度分别均为20、60、100 ng/mL)的血浆样品,按“2.4.3”项下方法处理,进样测定,记录峰面积A1。取空白血浆按“2.4.2”项下方法处理后加入相应质量浓度的利培酮贮备液和9-羟基利培酮贮备液,进样测定,记录峰面积A2。以A1/A2×100%计算提取回收率。结果显示,利培酮低、中、高质量浓度血浆样品的提取回收率分别为87.6%、83.9%、89.7%,RSD分别为5.39%、2.57%、3.25%(n=3);9-羟基利培酮低、中、高质量浓度血浆样品的提取回收率分别为89.0%、88.9%、88.2%,RSD分别为1.48%、3.56%、2.00%(n=3)。
2.4.7 精密度试验 取空白血浆0.5 mL,加入利培酮贮备液和9-羟基利培酮贮备液,配制低、中、高质量浓度(利培酮和9-羟基利培酮质量浓度分别均为20、60、100 ng/mL)的血浆样品,按“2.4.3”项下的方法处理后进样分析,测定峰面积,代入回归方程计算含量。同日内测定5次,考察日内精密度;每日测定1次、连续测定5 d,考察日间精密度。结果,利培酮日内RSD为0.67%(n=5),日间RSD为2.81%(n=5);9-羟基利培酮日内RSD为0.98%(n=5),日间RSD为3.27%(n=5)。
2.4.8 稳定性试验 取空白血浆0.5 mL,加入利培酮贮备液和9-羟基利培酮贮备液,配制低、中、高质量浓度(利培酮和9-羟基利培酮质量浓度分别均为20、60、100 ng/mL)的血浆样品,考察血浆样品经历反复冻融(-20℃冷冻-室温解冻)3次、室温放置10 h、-20℃存放15 d以及处理后的血浆样品室温放置24 h的稳定性,每一种稳定性在低、中、高质量浓度水平进行3次测定。结果,冻融、冰冻、室温处理后血浆样品中利培酮和9-羟基利培酮的测定值与标示值的RE均<15%,说明分析测试过程中样品较为稳定。
2.5 药动学研究
2.5.1 实验设计 家兔12只,♀♂各半,平均体质量为2.5 kg,用抛硬币的方法分为2组,一组灌胃利培酮缓释片,另一组灌胃市售利培酮片,给药量均为1片(按利培酮计为2 mg),均用5 mL温水送服,服药2 h后方可再饮水,3 h后再进食。
2.5.2 血浆样品的制备 给药后 0、0.5、1、2、3、4、6、8、10、12、24、36、48 h取样,每次耳缘静脉取血1 mL,所取血样置于2 mL肝素钠离心管中,离心(5 939×g)5 min,得血浆样品。
2.5.3 血药浓度及药动学参数结果 采用药动学软件Kinetica 4.4的非房室模型(NCA)分析,对实验数据进行处理,市售利培酮片和利培酮缓释片在家兔体内的药-时曲线详见图4,药动学参数见表2。
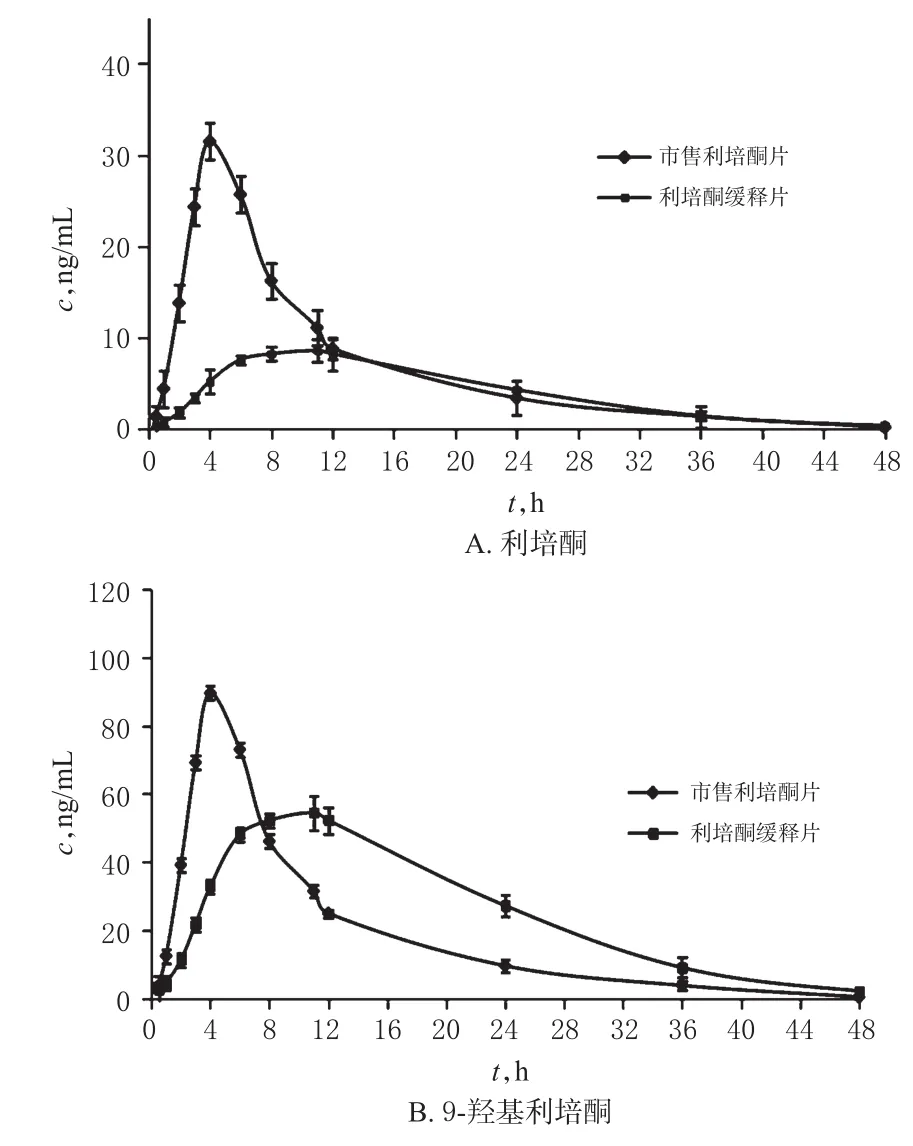
图4 市售利培酮片和利培酮缓释片在家兔体内的药-时曲线Fig 4 Blood concentration-time curves of commercially available Risperidone tablets and Risperidone sustained-release tablets in rabbits
表2 市售利培酮片和利培酮缓释片在家兔体内的药动学参数(±s,n=6)Tab 2 Pharmacokinetic parameters of commercially available Risperidone tablets and Risperidone sustained-release tablets in rabbits(±s,n=6)
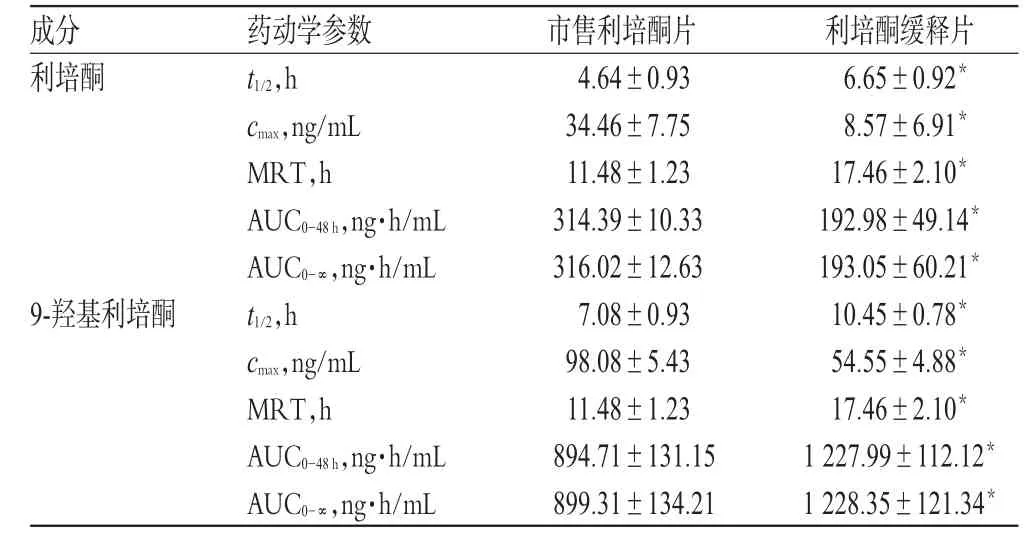
表2 市售利培酮片和利培酮缓释片在家兔体内的药动学参数(±s,n=6)Tab 2 Pharmacokinetic parameters of commercially available Risperidone tablets and Risperidone sustained-release tablets in rabbits(±s,n=6)
注:与市售利培酮片比较,*P<0.05Note:vs.commercially available Risperidone tablets,*P<0.05
成分利培酮9-羟基利培酮利培酮缓释片6.65±0.92*8.57±6.91*17.46±2.10*192.98±49.14*193.05±60.21*10.45±0.78*54.55±4.88*17.46±2.10*1 227.99±112.12*1 228.35±121.34*药动学参数t1/2,h cmax,ng/mL MRT,h AUC0-48 h,ng·h/mL AUC0-∞,ng·h/mL t1/2,h cmax,ng/mL MRT,h AUC0-48 h,ng·h/mL AUC0-∞,ng·h/mL市售利培酮片4.64±0.93 34.46±7.75 11.48±1.23 314.39±10.33 316.02±12.63 7.08±0.93 98.08±5.43 11.48±1.23 894.71±131.15 899.31±134.21
表4的统计结果通过SPSS 19软件进行双侧t检验显示,与市售利培酮片比较,利培酮缓释片在家兔体内的t1/2和MRT明显延长、cmax明显降低、以利培酮计的AUC明显降低、以9-羟基利培酮计的AUC明显增加(P<0.05)。
3 讨论
3.1 体外释放行为
由于利培酮为pH依赖性药物,其在pH<8时,随着pH的增大溶解度减小;pH≥8时几乎不溶[11]。因此实验前期对利培酮缓释片在0.1 mol/L盐酸和pH 4.0、5.0、6.8、7.4的磷酸盐缓冲液(PBS)条件下的释放度进行了研究。结果发现,pH 4.0、5.0、6.8、7.4的PBS用于处方筛选,其区分力较差,因而选择0.1 mol/L盐酸作为释放介质。为了更好地模拟体内过程后期应补测利培酮缓释片在模拟胃液中的释放情况。
3.2 实验动物选择
虽然家兔是食草动物,在进行口服胃肠道给药的生物利用度实验时,药物在其胃肠道的吸收和代谢行为可能与人体有一些差异,但目前仍有较多以家兔为模型动物的药动学实验,例如Spogli R等[12]以家兔为模型动物,考察负载在二氢氧化镁上的白藜芦醇固体分散体的药动学;El-Say KM等[13]在评价卡维地洛固体脂质纳米粒药动学时,采用家兔为动物模型;BaiA等[14]在家兔中测试了氨磺必利-纳米脂质体胶囊的药动学,发现基于纳米脂质体的胶囊改善了氨磺必利的口服生物利用度,因而以家兔为动物模型,对于口服药物药动学评价有一定的指导意义。
3.3 给药剂量选择
利培酮缓释片规格为2 mg,若掰开服用,会改变片剂的结构,使释药形式发生改变,对药物的释药行为影响较大。同时在前期实验中,参考市售利培酮片药品说明书,在新西兰家兔上进行了利培酮剂量为0.31~5.00 mg/kg(以mg/m2计,为人体最大推荐剂量的0.4~6倍)的致畸作用研究,与阴性对照组比较,未发现畸形发生率增大,即家兔对于利培酮耐受剂量不大于5 mg/kg。本实验中,利培酮缓释片和市售利培酮片的规格均为2 mg,药动学实验中给药量为2 mg,既便于给药,又在家兔耐受范围内,且实验过程家兔没有异常情况出现。
本研究结果表明,利培酮经介孔二氧化硅负载后体内外均具有缓释作用,可延长药效发挥的时间。
