铝热还原钛氧化物直接合金化机理研究
2019-08-14尚德礼
尚德礼
(鞍钢集团钢铁研究院海洋装备用金属材料及其应用国家重点实验室,辽宁 鞍山114009)
钢的直接合金化就是指用含有合金元素的氧化物作为合金化剂,炼钢过程直接将含有合金元素的氧化物加入钢液,通过合金化剂配加的还原剂,或用钢液中已存在的脱氧元素将合金元素还原出来,达到合金化的目的。传统上冶炼含钛钢时主要采用添加钛铁的方式进行合金化,主要原因是钛铁在钢液中的溶解速度较快,同时具有较高的收得率。但是制备钛铁需要消耗大量的能源,且造成环境污染,因此钛铁合金化成本较高。由于钛氧化物较钛铁在价格上存在优势,有学者就钛氧化物直接合金化的可行性进行了热力学分析[1],但并没有进行深入研究,仅就反应速度进行动力学分析,直接合金化的具体形式也并未提及;加之钛氧化物稳定性较强,不易被还原,且还原出的金属钛又易被氧化,在反应机理不甚明确的条件下,简单的工业应用难度较大,因此鲜有该方面的应用报道。随着用户对含钛钢需求的增大,考虑到节能环保及成本问题,用钛氧化物直接合金化技术来替代采用钛铁合金化技术是必要的。本文以TiO2和金属铝为直接合金化剂原料,分析了钛氧化物直接合金化可行性机理,并对影响条件行了探讨。
1 还原钛氧化物的热力学机制
铝热还原钛氧化物的体系中,钛元素可能出现的化合价有0、+2、+3、+4价,对应四种价态的纯净物存在方式为:金属钛、TiO、Ti2O3以及TiO2。铝还原钛氧化物过程可能出现的相关关键热力学方程如下[2]:

将以上各式的标准吉布斯能与温度的关系制成曲线,图1为铝还原氧化钛的标准吉布斯能变化情况。

图1 铝还原氧化钛的标准吉布斯能变化情况
由图1看出,用铝作还原剂时,在炼钢温度条件下,铝均能将钛矿中的TiO2还原成金属钛,进而可对钢液进行钛合金化。该体系中所有反应都是具备自发倾向的反应,但随着温度的升高,其自由能也随之增高,所以温度升高不利于反应的进行,降低温度有利于提高金属钛的收得率。因此在直接合金化时,控制钢液温度,不仅有利于提高钛收得率,还可以防止因钢液温度过高而导致的耐材损毁、钢液二次氧化等问题。
2 还原钛氧化物的动力学变化机制
从热力学分析可知,在炼钢温度条件下铝完全可以还原TiO2实现钛直接合金化,因此在平衡态时铝可以还原钛氧化物。但是炼钢时,合金化过程时间不允许过长,否则会引起一系列问题,如连铸断浇、钢水温降过大等。由于动力学条件等制约,铝能否还原钛氧化物或还原率水平是多少还需通过理论验证。
首先了解TiO2+4/3Al=Ti+2/3Al2O3反应的宏观过程,铝还原TiO2反应示意图如图2所示。
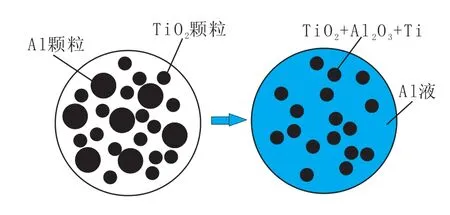
图2 铝还原TiO2反应示意图
反应过程如下:
(1)细铝粉与细小的TiO2均匀混合组成均匀混合物;
(2)混合物加入钢液后,随着温度升高到大于铝的熔点(660.4℃),混合物中的铝颗粒开始熔化,铝液扩散到TiO2颗粒表面;
(3)铝液与TiO2表面发生化学反应,生成了Ti和Al2O3,该反应微观过程可采用未反应核模型理论描述。
图3为TiO2与Al反应的未反应核模型。用该模型可计算铝还原氧化钛的这一多相反应的速度。模型假定氧化钛为致密的球体,反应TiO2+4/3Al=Ti+2/3Al2O3只发生在产物层与未反应核的界面上,而且已达到反应平衡。总的反应速度受铝液与氧化钛之间的外扩散,铝在反应产物层中的内扩散和界面化学反应控制,速率方程[3]为:

图3 TiO2与Al反应的未反应核模型

式中,J为速率;De为扩散系数;ro为初始TiO2球体半径;r为反应后TiO2球体半径;C1为球体外表面的浓度;C为反应界面上的浓度;k为反应的速率常数;K为反应的平衡常数;C平为反应的平衡浓度;Co为初始浓度;β为外扩散的传质系数。
代入 r=ro(1-R)1/3,则式(10)变为:
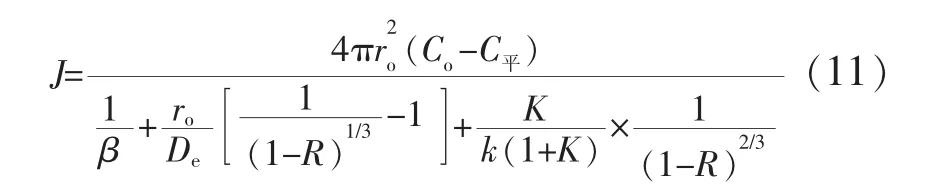
式中,R为氧化钛的还原率,即氧化钛颗粒质量去除氧量后与原颗粒质量之比,%。
据未反应核的质量衡算可得:

式中,n为氧化钛摩尔量;τ为时间;ρo为氧化钛中的氧密度,kg/m3;为氧化钛中的氧密度,mol/m3,而为氧的摩尔质量,再带入r=ro(1-R)1/3,则(12)式变为:


由于铝的还原性高于钛,因此界面反应速度较快,另外铝在边界层的外扩散速度要远高于铝在致密的还原产物(氧化铝)中的扩散速度,即De<<k,De<<β。则整个反应过程由还原层的内扩散所控制。而式(15)可简化为:
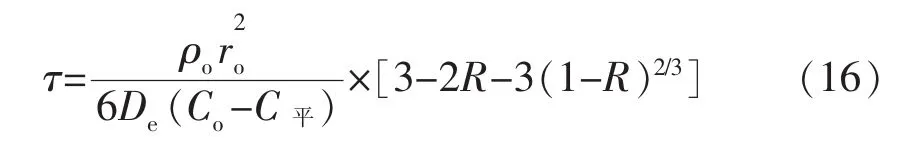
根据 TiO2密度(4.26 g/cm3)可计算出 ρo,Al在产物层中的有效扩散系数De取决于产物层的致密度。1 500℃时,Al在 CaO44%-Al2O312%-SiO244%三元渣中的扩散系数为 7×10-7cm2/s[4],Al在固相产物层中的扩散系数肯定小于此值。但Al在固态致密的钢中扩散系数可达到1×10-8cm2/s[5],Al在固相产物层中的扩散系数肯定又大于此值。 假定 De=0.7×10-7cm2/s、C平=0,按式(16)计算,使 10 μm 的 TiO2全部转变成 Al2O3的时间仅为1.27 s。也就是在铝粉和氧化钛粉混合物加入钢液瞬间,钛就会被铝还原。实际应用中,可采用粒径为10 μm的钛氧化物细粉为原料制备合金化剂,也可以通过增加或减少钛氧化物细粉粒径调整反应速度。
铝粉和氧化钛粉混合物加入钢液后,反应瞬间完成,由于金属钛密度为4.54 g/cm3,氧化钛密度为 4.26 g/cm3,金属铝密度为 2.7 g/cm3,氧化铝密度为3.97 g/cm3,显然金属钛的密度最大,因此还原反应发生后,被还原出的金属钛会下沉到混合物的底部,即金属钛可以直接与钢液接触,显著增强了合金化效果。
钛氧化物直接合金化的效果还取决于钢液的条件及熔渣状况。由于直接合金化剂反应速度极快,因此在实际生产中,直接合金化剂的加入时机可参照钛铁合金合金化时机,必须满足如下条件:精炼钢水快要结束前,钢水氧含量小于0.002 5%,钢水中的Al控制在0.025%以上,这时加入直接合金化剂可保证提高并稳定钛的回收率。直接合金化时,钢水温度的控制应低于钛铁合金化时的钢水温度,一方面防止钢水温度过高加速金属钛氧化,另一方面钢水温度过高不利于还原反应进行。钢包渣氧化性及碱度也应严格控制,生产实践表明,随着钢包渣氧化性的增加,钛收得率呈明显下降趋势;同时钢包渣中SiO2含量的增加也将导致钛收得率降低(钢渣存在Ti+SiO2=TiO2+Si的反应)。因此,要保证钛有较高的收得率,渣中(FeO+MnO)含量控制在5%以下,同时减少转炉下渣量,防止渣中SiO2含量增加,渣中SiO2含量应控制在10%以下。
3 结论
(1)热力学分析表明,在炼钢条件下,铝完全可以还原TiO2,被还原出的金属钛可对钢液实现钛直接合金化,该过程不仅降低钛铁消耗成本,还避免了制备钛铁造成的环境污染问题。
(2)动力学变化机制表明,粒径为10 μm的TiO2全部转变成Al2O3的时间小于1.27 s,铝粉和氧化钛粉混合物加入钢液瞬间氧化钛就会被铝还原,从而实现钛直接合金化。由于反应在瞬间完成,对整个冶炼体系环节不会造成不良后果。
(3)铝粉和氧化钛粉混合物加入钢液后,反应瞬间完成,由于金属钛密度分别大于氧化钛密度、金属铝密度和氧化铝密度,因此还原反应发生后金属钛会下沉到混合物的底部,即金属钛可以直接和钢液接触,显著增强了合金化效果。
