自蔓延高温合成TiC/Fe金属陶瓷结构复合材料的研究*
2019-07-30马调调
马调调
(榆林市天然气化工有限责任公司 陕西 榆林 718100)
自蔓延高温合成技术(Self-propagation High-temperature Synthesis,简称SHS)是前苏联科学家米尔亚诺夫于1967年首先提出的由粉末原料合成材料的一项新技术。材料的自蔓延高温合成是材料科学与工程领域活跃的研究方向之一。其基本特点是:利用外部提供必要的能量诱发高放热化学反应体系局部发生化学反应(点燃),形成化学反应前沿(燃烧波)。此后化学反应在自身放出热量的支持下继续进行,表现为燃烧波蔓延至整个反应体系(燃烧波速度为0.1~25 cm/s),最后合成所需材料(粉体和固结体)。其热化学反应通用方程式为:金属氧化物+铝(粉末)=氧化铝+金属+热能[1]。SHS是利用反应物之间高的化学反应热的自加热和自传导作用来合成材料的一种技术,当反应物一旦被点燃,便会自动向尚未反应的区域传播,直至反应完全,放热化学反应过程同时伴随相转变和结构变化[2]。它是燃烧、质量传递、传热与凝固相互叠加的复杂过程,包含着化学反应机理和过程、物理化学变化、组织和结构的转变、物质和热量的交换[3]。自蔓延有关理论涉及到SHS热化学、SHS反应过程与动力学、SHS燃烧学,人们对燃烧合成绝对温度、燃烧波特征、燃烧波传播方式(燃烧波方程)、SHS图及燃烧动力学等均进行了研究[4~8]。自蔓延高温合成技术以其无以比拟的优点自问世以来引起科学界的广泛关注,成为工程技术人员和科研工作者的研究焦点。
SHS技术目前己发展成为可同粉末冶金、烧结、熔铸、焊接、挤压、表面技术等互相结合而又自成体系的材料制备体系,成为一个包括多学科交叉的新学科分支[9~12]。自从Merzhanov发明自蔓延以来,得到了迅速的发展,研究对象也从当初的高反应热的硼化物、碳化物、硅化物发展到弱反应的氢化物、磷化物、硫化物等[13]。自蔓延高温合成技术以自蔓延方式实现粉末间的反应,工艺简单,工序减少,一经引燃启动过程后就不需对其进一步提供能量[14]。由于燃烧波通过试样时产生高温,可将易挥发杂质排除,使产品纯度增高。同时燃烧过程中有较大的热梯度和冷凝速度,能获得复杂的相或亚稳相及能在合成材料的同时使之致密化,易从一些原料直接转变为另一种产品,且可实现过程的机械化和自动化,可用于合成金属、陶瓷和复合材料等多种材料。
1 实验条件及实验方法
1.1 实验所用材料
实验用原料选用工业钛粉(纯度为99%,粒度小于45 μm)、石墨(平均粒径为1 μm)、还原铁粉(纯度为98.5%,平均粒径为20 μm)、Al粉(纯度98%,粒度小于50 μm)及纳米级稀土。
浇注金属材料为低合金钢,化学成分为: C 0.15%~0.35%,Si 0.30%~0.80%,Mn 11.00%~14.00%,Ni≤0.05%,Cr≤0.07%,P≤0.05%,S≤0.05%。
本实验选用Ti、C、Te和Al粉末混合、粘结剂选用松香,其中Ti粉为一级钛粉,粒度为400目,Al为分析纯化学试剂,粒度为200目,C为无定碳黑,他们的粉末特性见表1。SHS预制块的成分比例为(质量分数)Ti∶C∶Fe∶Al=3.2∶0.8∶3∶3,配制150 g,将粉末混合后研磨0.5~1 h,使粉末充分的混合。然后将松香用酒精溶开,并将适量的酒精倒入已配制好的粉末中。在本次实验中分别加入了1%和3%的稀土,试找出稀土在自蔓延反应中的作用。

表1 原料粉末的特性
1.2 差热实验
取混合粉末样品各70~100 mg,进行差热分析实验,实验参数如表2所示。

表2 差热实验参数表
2 热力学计算
2.1 自蔓延反应热力学
SHS热力学主要是计算SHS反应的放热量以及反应放热使体系能达到的最高温度,即反应绝热温度。用这些结果可以判断体系反应是否发生、反应的趋势、反应是否能够自维持以及反应的放热是否能使产物熔化或汽化等。反应热力学问题关系着反应进行方向和最终产物的相组成,因此从理论上建立反应热力学判据来判断在不同工艺条件下反应进行的方向和产物的相组成,不仅可以为实验研究提供有效的理论指导,同时也可以减少实验的盲目性,所以对反应热力学的研究不仅具有理论价值,而且具有实用性。
2.2 自蔓延反应体系绝热温度的计算
Merzhanov根据实验提出SHS燃烧波自维持的热力学判据,当绝热温度Tad>1 800 K时,燃烧波才能自维持下去,并且绝热温度的高低直接影响生成相的组态及反应机理。
在Tad>1 800 K,恒压条件下,对于反应体系有
A(s) +B(s) =AB(s)+ΔH
根据热力学第一定律
Cp=dH/dT
即
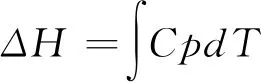
或

故反应期间放出的热量为

式中ΔHθ为产物在298K时的标准生成焓,Cp为产物热容。由于自蔓延反应过程相当快,可把该体系设成绝热体系,体系的热效应为ΔH=0。对于反应式:

查得数据[4]代入得
ΔHθ=2×(-1 675.27)+3×(-184.1)-3×
(-944.75)=-1 068.59 kJ/mol
又

由于直接将数据代入该式计算十分繁杂,现将其进行分步计算如下:
1)对于T<3 290 ℃,TiC为固态。

10-5T-2+18.83×10-2)dT+3ΔHm=730.77 kJ
对于T ≥3 290 ℃,TiC为液态。

×62.76=188.28Tad-619 441.2
2)对于T<800 ℃,Al2O3为固态。
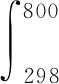

-48.367×105T-2)dT+2ΔHm=747.32 kJ
对于T≥800 ℃,Al2O3为液态。
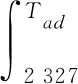
×144.863 =289.73Tad-674 192.4
又
-ΔHθ=ΔH1+ΔH2+ΔH3+ΔH4
即
1 068 590=730 772.98+188.28Tad-619 441.2
+747 319.55+289.73Tad-674 192.418 8.28
Tad+289.73Tad=884 131.08
得
Tad=1 850 K
解得Tad=1 850 K,它高于1 800 K,说明反应能够顺利进行。
2.3 体系绝热温度对自蔓延反应的意义
通过对反应绝热温度的计算可以进行以下分析:
1)反应绝热温度作为反应能否自我维持的重要判据。根据热力学原理,任何一个反应,只要自由能变化为负值,反应就能发生。
2)反应绝热温度作为工艺设计的依据。对某体系的Tad与熔点Tm进行比较,可以判断自蔓延过程中产物是否出现液相。这对于有效控制反应过程以及对产物实现致密化是十分有益的。即当Tad
2.4 绝热温度与反应起始温度的关系
由图1可以看出,随反应起始温度升高,体系绝热温度也升高。
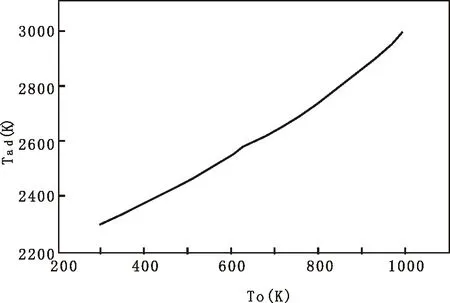
图1 绝热温度与反应起始温度的关系
2.5 制备预制块
2.5.1 预制块配料参数确定
在配制SHS粉料过程中,Ti粉和C粉是按化学反应计量式进行,即Ti,C原子百分含量(%)比为1∶1,质量分数比为4∶1。Al粉是作为溶剂加入的,如果直接利用Ti粉与C粉之间的自蔓延高温反应来制备TiC 烧结块很容易引起C的烧损,而且反应很难控制,反应温度高,实验条件要求高,所以采用Al作溶剂,在浇注过程中,预制块被加热到约660 ℃时即接近溶剂熔点时,自蔓延反应开始进行。在温度升高反应组元扩散到溶剂金属基体中形成熔点低于基体金属的合金的情况下,反应起步温度能进一步降低,由此可见Al的加入能降低Ti与C生成TiC反应的起始温度,当Al熔化后,熔融的Al因毛细作用在钛颗粒和碳颗粒表面铺展开,促使Ti在Al中进一步固溶,形成Al3Ti熔液。虽然C在Al中的固溶度很小,但仍有少量的C固溶到包覆着它的Al3Ti熔液中。固溶的钛原子和碳原子在Al3Ti熔液中相互扩散,经碰撞发生化学反应生成细小TiC粒子,并放出大量热,使得预制块的温升速度出现转折。温度的升高促使钛原子和碳原子的固溶和扩散速度加快,以至出现钛原子和碳原子在Al3Ti溶液中的大规模相互扩散,发生反应生成大量的陶瓷相TiC。在反应正常进行的前提下,其含量应给予控制,因含量过高,可产生过多对反应无益相。Fe粉是作为稀释剂加入的,其目的是在SHS合成反应过程中的高温使Fe粉熔化,使铁液包覆新生成陶瓷相TiC,达到TiC和铁液的自润湿,以利于母液铁水铸渗和TiC颗粒向母液铁水的分散。在不影响其他条件的前提下,其含量应尽量大。综合上述各种因素,选定SHS粉末配比为Al∶Te∶Ti∶C=3∶3∶0.8∶3.2
本次实验共配制了3种成分的粉末,分别是:按计算所得配比配制;在第一种配比的基础上加入3%的稀土;在第一种配比的基础上加入1%的稀土。
2.5.2 压制预制块
将配制好的粉末混合均匀以后,准备压制SHS预制块,预制块模具的尺寸为30 mm×30 mm×10 mm,模具形状如图2所示。

图2 预制块模具
将粉末放入模具后,采用油压机压制预制块,压力为8~10 MPa,压制后的预制块厚度为5~6 mm。并在预制块的中心留有一个小孔,以方便预制块放入浇注模型中的固定。压制完成后,把预制块放在通风处让其自然干燥1~2 d,使其达到一定的实验强度。
2.6 浇注实验
SHS反应过程中会产生大量的气体,如不能及时的排除,将会对铸造组织产生十分不利的影响,造成大量的气孔等铸造缺陷;同时考虑反应产物的密度与基体金属的密度存在很大的差异,所以将预制块置于试件顶端,以利于SHS反应中产生的气体及时的通过铸型的通气孔排除,让液态钢液与固体预制块充分接触,依靠液态金属液的高温来引燃固体反应物(预制块),发生反应生成增强陶瓷相(TiC),从而在铸件表面形成具有一定厚度的表面自生复合材料,且复合材料的组织和成分呈梯度分布与母材金属逐渐过渡,由外至内依次为复合层—过渡层—基体金属。本次实验将3种不同成分的预制块分别放置在3个不同的位置;型砂采用水玻璃沙,目的是增加砂型的透气性,利于反应过程中产生的大量气体的排出。在浇注之前,用喷灯对整个砂型进行充分的预热,预热8~10 min,以增加砂型的透气性,减少铸件产生的气孔。浇注实验完成后,将SHS反应的区域从铸件中分离出来,并为后期的铸态组织观察作好前期准备。

图3 浇注示意图
3 工艺参数的影响
3.1 工艺参数对Al-Ti-C体系燃烧过程的影响
3.1.1 预热温度对燃烧温度和燃烧速度的影响

图4 燃烧温度与预热温度的关系

图5 燃烧速度与预热温度的关系
由图4、图5可知,提高预热温度可以使燃烧温度和燃烧速度也随之提高,原因在于:一方面预热温度的提高增加了反应物的生成焓,使反应放出的热量有所增加;另一方面由于预热温度的提高使反应物间的扩散速率增加,基于以上2方面的原因必然使SHS反应的燃烧温度与燃烧速率增加。
3.1.2 预制块密实度对燃烧温度和燃烧速度的影响

(a)燃烧温度 (b)燃烧速度图6 预制块密实度对燃烧温度和燃烧速度的影响的关系图
由图6(a)可以看出,燃烧温度基本不随预制块密实度的变化而变化。这是由于预制块密度的增大虽然导致单位体积放热量的增加,但同时也使预制块的导热率增加,从而使燃烧前沿带走的热量也随之增加,两方面因素共同作用的结果是燃烧温度随预制块密实度的变化不明显。由图6(b)可以看出,燃烧速率随预制块密实度增加,有加快的趋势。这是由于预制块密度的增加减少了预制块内的孔隙度,增加了反应物间的接触,有利于扩散反应的进行,燃烧速度加快。
3.1.3 反应物颗粒尺寸对燃烧温度的影响
实验表明,增强体粒度对表面复合层质量的影响主要表现在金属母液的渗透、增强体颗粒的熔化及熔解的难易程度上。粒度大的颗粒在合金涂层中形成的孔隙较大,曲折度随之减小,流动阻力小,有利于金属母液向涂层中的渗透,可增加复合层的厚度;但是过大的粒度对合金颗粒的熔化和熔解极为不利,会影响增强体在复合层中分布的表面质量。同时,我们发现毛细作用产生的毛细管力可大大加强金属母液对增强体颗粒的浸润作用,对促进金属母液向预制块表层的渗透极为有利,因此较小的粒度可以加强毛细作用的效果,增加表面复合层厚度。然而,如前所述,粒度过小又会增大流动阻力影响金属液的渗透,降低复合层厚度,两者的作用是相互矛盾的。
3.1.3.1 碳粉的影响

图7 不同碳源时燃烧温度-时间关系曲线
碳粉不同时,由于碳粉粒度、成分及结构等的差异,燃烧温度也存在一定的差异。图7为碳粉分别为炭黑和石墨(4 μm)时的燃烧温度—时间关系曲线。由图7可知,石墨作为碳源时,燃烧温度Tc较高,且温度曲线光滑;而用碳黑作为碳源时,燃烧温度较低,温度变化曲线折曲较多,有时甚至出现双峰。据有关资料研究表明:在研究TiC的合成时,也同样得出石墨作为碳源时燃烧温度较高的结果。炭黑中含有较多的碳氢化合物杂质,一方面由于杂质多而造成碳量不足;另一方面这些杂质在SHS过程中呈气体挥发掉,从而会带走一部分热量,造成热量的损失,这样使得炭黑作为碳源时燃烧温度较低。另外,由于在挥发的过程中存在不均匀挥发,引起所测的温度曲线会出现多个突然的折弯变化。在实际的反应过程中,体系处于高温时间相差无几,于是,在含有细小碳粉的体系中,碳粉参加反应的比较多,反应的也就比较充分;相应地生成的TiC的量也就比较多,反应放热多,体系的反应温度较粒度大的也较高。
反应物粒度对燃烧温度的影响有2个方面:即影响燃烧反应的反应速度和反应转化率。从而降低了热产生的速度和热产生的大小,因此,降低了燃烧温度。对石墨来说,当粒度在一定范围内变化对燃烧温度影响较小,这可能与在反应过程中石墨沿平行结构层方向的裂开有关。图8是石墨粒度对燃烧温度的影响图。由图8可知,石墨对燃烧温度的影响只有在粒度增大到一定程度的时才会比较明显。

图8 石墨粒度对燃烧温度的影响
3.1.3.2 钛粉粒度的影响
图9为钛粉粒度对燃烧温度影响。钛粉粒度的大小对燃烧温度的影响相对较大,当钛粉粒度增大时,燃烧温度随着钛粉粒度的增大,燃烧温度降低。
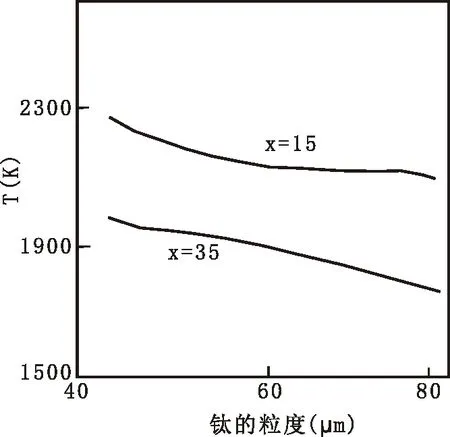
图9 钛粉粒度对燃烧温度的影响
3.1.3.3 铁粉含量对燃烧温度的影响
图10为体系燃烧温度随铁含量变化的情况。随着铁含量增高,体系燃烧温度Tad总体上呈降低趋势。Tad随铁含量增高而呈线性降低,在铁含量为55%~60%处出现一个温度平台,当Tad为1 808 K时,对应的是α-Te的熔点Tm。因此,含铁量60%时处于能否进行SHS反应过程的边界处。图10中还表示了SHS反应过程中实际燃烧温度Tc随铁含量的变化关系,Tc随含碳量的变化趋势是相同的。但由于实际SHS反应过程中的热量损失,实际燃烧温度要比理论值低几百度。当铁含量继续增高时,燃烧温度将降低至铁的熔点之下。由于钛的熔融温度比铁高,因此对TiC-Fe体系来说,当铁含量大于40%时,SHS过程中的液相主要是较低温度接触下共熔而产生的共熔相。以上燃烧温度随铁含量的变化关系说明在该体系的SHS反应过程中,铁是起稀释剂的作用的。

图10 铁粉含量对燃烧温度的影响
3.1.3.4 铝粉粒度及含量的影响
SHS反应体系反应开始于铝熔化之后,因而可以认为铝粉对燃烧温度的影响与铝粉粒度对铝粉熔化速度的影响密切相关。在燃烧波蔓延的过程中,由于大粒度的铝粉导致融化速率减慢,而燃烧进行很快,这样在燃烧带内势必造成一部分铝来不及熔化,使Al与TiO2、C间的接触面积减少,扩散进行更加困难,反应的完全程度受到影响,导致燃烧温度和燃烧速率降低。此外。由于部分未熔化的Al还在后续反应区内继续吸热、熔化、升温,这也使燃烧速率降低。
对于铝粉含量的影响首先从热力学角度分析,当铝粉含量增加时,提高了体系Al3Ti向TiC转变的临界温度,同时也降低了反应温度,使Al3Ti向TiC转变的可能性降低。其次从动力学的角度分析,铝粉量增加,体系内Ti、C含量减少,且相隔的距离增大。反应所需的扩散距离和时间延长,降低了反应生成TiC的速度,使那些在热力学有可能生成TiC的体系没能完全生成TiC。因此,就会出现随着铝粉含量的增加,生成TiC的量在减少、生成Al3Ti的量在增加。
分析铝量对生成TiC颗粒尺寸的影响时认为,生成TiC的过程实际是一个生核和长大的过程,温度高,生长的充分,颗粒尺寸就大。当铝量较少时,反应的温度高,体系停留在较高温度的时间就长,TiC颗粒长大较充分,颗粒尺寸也就大;相反铝量增大,反应温度低,TiC生长不充分,所颗粒以尺寸就小。因此,随着铝量的增加,生成TiC的颗粒尺寸在减小。
3.2 工艺因素对复合层结合质量的影响
3.2.1 预制块制作的影响
预制块制作的好坏直接影响到复合层的结合质量,要获得具有良好的融合界面的复合层,必须控制以下因素。
1)粘结剂。粘结剂的作用是将反应物颗粒粘结在一起,并使预制块具有一定的强度,以免在浇注过程中被钢水冲散。使预制块形成稳定的毛细管或孔隙,保证钢水很好地浸透预制块。可以不同程度地改善钢水与预制块间的浸润性。本实验采用松香加乙醇,于其属于会气化分解的有机粘结剂,铸件表面的气孔偏多。
2)熔剂。熔剂的作用是浇注初期包裹反应物颗粒使之不受氧化,受热熔化后能除去反应物颗粒表面的氧化膜,清洁表面,增加钢水的浸润性。醇基涂料要用有机溶剂作为分散剂(溶剂),其中最常用的是醇类,工业用乙醇(酒精),它无毒、无臭、易挥发、易燃,可满足性能要求,而且价格较低,供应情况较好。其乙醇的含量大于95%,以酿造厂生产的质量较好。
3)预制块的烘干工艺。试验表明,烘干可使预制块有一定的干强度,不被钢水冲散,并且减少浇注时产生的发气量和水分,但在烘干过程中,要注意温度不能过高,否则反应物的氧化和粘结剂的过烧都会使反应不能进行。本实验预制块的烘干温度在250 ℃左右,保温2 h左右。
4)预制块的厚度。由于铸渗表面复合层是依靠渗入涂料层的高温金属母液的热量熔化、溶解、稀释合金粉以及铸渗合金向内扩散并与基体金属母液发生反应,经冷却凝固而成的。因此,在其他条件相同的情况下,预制块的厚度对铸渗表面复合层的质量有很大的影响。预制块的厚度的影响和铸件的蓄热能力即金属母液包含的热量有关。从整个试样的截面积来看,在试样的厚壁处放置相对薄一些的预制块,其铸渗效果要较在试样的薄壁处放置相对厚一些的预制块好得多。这是由于壁厚处金属母液蕴含相对多的热量可以使母材保持较长的熔融液相状态。于是,金属液就可以渗透得较彻底一些,铸渗合金也达到很好的扩散效果,从而提高复合层的厚度和增强体颗粒的分布状况。因此,预制块的厚度应和对应的铸件壁厚相适应。
3.2.2 铸造工艺对复合层质量的影响
1)浇注温度。浇注温度对铸渗质量的影响最为显著。这是由于浇注温度越高,母材金属液的粘度越小,流动性也就越好,金属液保存的热量液也由于温度的增高而增加,于是金属液保持液态的时间就愈长,从而利于金属液向复合层的渗透和预制块表面层的熔融及分解,利于气体和夹杂物的排出,同时提高表面复合层的厚度以及改善增强体颗粒的分布情况;反之,浇注温度低,则金属液的流动性变差,渗透能力降低,易产生气孔、夹渣等缺陷。此外金属液的温度低,母材保持液态的时间较短,预制块得不到充分的热量,很难引发SHS 反应,或反应不完全,出现夹渣、内气孔难以熔化的TiC 颗粒,使界面融合差,甚至不融合导致复合层厚度降低;浇注温度过高,则易冲散预制块或者不能形成复合层。应在保证预制块完整不被冲散的前提下,尽量提高浇注温度,使反应充分进行,延长生成物熔融态的时间,延长界面扩散熔融时间,以提高复合层的致密度及融和层厚度。
2)铸型和预制块的预热。其预热可使钢水在铸型中的液态停留时间延长,有利于钢水的渗透和SHS 反应的充分进行。预热温度以180~220 ℃为宜,太低达不到预热效果,太高会使粘结剂、熔剂失效而导致反应物的氧化。本实验预热温度为200 ℃。
3)造型。本实验采用水玻璃砂干型,具有良好的透气性,有易于钢水充型过程中的气体排放。
4 组织及性能分析
4.1 实验方法
用切割机切割铸件,用砂轮机打磨成平面,然后用280~1 000目的SiC砂纸依次打磨试样,磨至试件表面无明显划痕再用5 μm、2.5 μm的金刚石研磨粉在抛光机上依次对试样进行抛光,用绒布将试样打磨干净,用3%的稀硝酸酒精对试样进行腐蚀。在金相显微镜下观察材料复合层组织形貌并分析其形成的原因。
4.2 表面复合材料的组织观察分析
按计算结果配比SHS粉末获得的铸件表面复合层如图11(a)所示。由图11(a)可知:复合材料层由TiC、Al2O3和Fe三相组成,TiC 呈近球状均匀分布,Al2O3颗粒比较粗大,呈不规则状,而铁相则作为粘结相将TiC颗粒粘结起来,形成典型的TiC/Fe金属陶瓷结构的复合材料。同时由于Fe的密度大于TiC及Al2O3,所以复合材料的组织和成分呈梯度分布并与母材金属逐渐过渡, 由上而下依次为复合层—过渡层—基体金属。由图11(b)可知,TiC颗粒细小呈均匀的分布,说明反应比较充分。由图11(b)、(c)、(d)可以明显地看出从复合层―过渡层―基体,TiC颗粒的大小是不同的,越靠近基体TiC颗粒就越大,且复合材料层与基体呈阶梯状逐渐过渡,而且界面不明显,说明复合材料的结合性能非常好。

(a) (b) (c) (d)
图11复合表面的显微组织
4.31 500~1 800 ℃激冷产物的组织分析
由于在此温度范围内反应温度己经很高,燃烧极为剧烈且很难被熄灭,由资料分析[9]可知,反应产物仅由Al2O3和TiC两相组成,表明反应已经进行完全。图12(a)、(b)是此温度范围激冷产物的组织照片。由图12可知,产物中生成了大量的TiC颗粒,TiC颗粒有所长大,反应生成的Al2O3是以大块状的基体而存在,细小的TiC颗粒分布于其上。

(a) (b)
图121500~1800℃激冷产物的组织结构(×400)
由图12可知:反应前Al颗粒、C颗粒和Ti颗粒仅呈现简单的机械接触;随着温度的升高,Ti被空气中O2氧化形成TiO2颗粒;当达到Al熔点(800 ℃)以后Al发生熔化,熔融Al沿混合物间隙发生漫渗及毛细作用,于是增大了Al与TiO2、C颗粒的接触面积。由干Al与TiO2不润湿Al与TiO2反应仅限于局部反应是微弱的,宏观上表现出放热很小,当体系温度达到920 ℃后,Al与TiO2的润湿性得以改善,Al液进一步在TiO2颗粒表面延展,TiO2颗粒完全被Al液包覆,且由于温度升高,Ti、Al、O原子的扩散能力大大提高。Al-TiO2还原反应开始大量进行,随着Al-TiO2还原反应的进行,反应放出的大量热使体系温度迅速上升,大量单Ti不断被还原出来。因此,当体系温度继续升高达到1 000 ℃以后,Ti、C反应开始大量进行,Al、Ti反应受到抑制。C颗粒周围的富态层进一步增厚,并且由于C原子的溶解及扩散也加速,Ti、C反应得以在富态层内发生。C颗粒周围进行的微观过程是:C不断溶解并向外扩散,Ti也不断从外部输运过来,于是在C颗粒周围富钛层内靠近C颗粒表面处,Ti、C原子不断结合生成TiC颗粒并长大。
4.4 复合材料层和过渡层组织的分析
图13为铸态复合材料层和远离复合层铸钢基体组织。其钢基体组织为在奥氏体基体上分布一定数量白色的铁素体及碳化物,如图13(a)所示。复合层组织为在珠光体基体上分布大量TiC颗粒,其形状近似球形,尺寸细小且分布均匀,与基体的界面清晰、干净,如图13(b)所示。对于Ti-C-Fe三元系合金,可能产生的化合物有TiC,Fe3C和Fe2Ti,但在复合层组织未发现Fe3C和Fe2Ti,其原因可能是作为稀释剂Fe粉熔化和铸渗铁水总是迟于自蔓延高温反应,反应大量消耗了Ti、C,使溶液中Ti、C含量较低,从动力学上使生成Fe3C和Fe2Ti可能性降低。

(a) 复合层组织 (b) 过渡层组织
图13铸态组织的结构(×100)
5 稀土对复合层组织的影响
5.1 稀土的加入对复合层组织的影响
随着材料科学的发展,稀土在很多合金材料的开发和利用上得到广泛应用。它的作用主要如下:可净化钢液,如脱氧和脱硫,除去钢中的气体,并使成分趋于均匀,减少枝晶偏析;能改变夹杂物形状,使夹杂物变的细小并弥散分布于晶内;减缓了奥氏体的分解,使钢的淬透性和淬硬性得到提高;可使某些合金钢的铁素体、珠光体及奥氏体晶粒细化,有阻碍奥氏体晶粒长大和细化碳化物的作用;稀土元素加入钢中能有效地提高铸钢的流动性,降低铸造应力,抑制和消除热裂纹,能细化铸钢的一次结晶,抑制和消除柱状晶的形成。因此稀土能有效的改善铸钢的工艺性能。凝固“组织控制”——稀土在钢中的形成较高熔点的化合物,在钢液凝固前析出,呈细小的质点分布在钢液中,作为非均质形核中心,降低钢夜结晶的过冷度,因而可细化钢的凝固组织,减少偏析,实现凝固组织控制。
在本实验中,由于反应混合物中加入1%的稀土铈氧化物和3%的稀土铈氧化物,试图找出稀土加入量对反应复合层组织的影响。图14为3种不同含量稀土成分的预制块的断面图。

无稀土 1%稀土 3%稀土图14 不同含量稀土成分的预制块的断面图
由图14可知,稀土的加入量对反应的过程中的结合层的结合力有着非常密切的关系,虽然稀土的加入会对铸造组织晶粒起到细化的作用,使得增强颗粒(TiC)得到细化,复合层组织更加细密,如图15(a)所示。现将没有加入稀土的复合层组织(如图15(b)所示)与其对比观察,可见细化结果非常明显。

图15 有无稀土元素的复合层组织对比(×400)
从图14中我们可以看出,随着稀土加入量的增大也使复合层与基体之间的结合情况越来越不理想。未加入稀土的预制块在发生自蔓延反应之后,复合层与基体两者之间结合得很完美,从而在铸件表面形成具有一定厚度的表面自生复合材料;可以清晰地看见复合材料的组织和成分呈梯度分布与母材金属逐渐过渡,由上至下依次为复合层—过渡层—基体金属。加入1%稀土的断面图中我们也能看见在铸件表面形成具有一定厚度的表面自生复合材料,隐约能看见复合材料的组织和成分呈梯度分布向母材金属逐渐过渡,但是其结合的情况与未加入稀土相比较而言就大不相同,无论从复合层的厚度还是致密度都远远不如未加入稀土的好。相对未加入稀土和加入1%的相比较而言,加入3%的复合材料过渡层几乎在断面图中很难能找到,可以看见预制块与基体之间存在一条明显的分界线,也就是说预制块与高温的钢液未能发生自蔓延反应,但是高温的钢也使预制块产生了烧结。
5.2 表面复合材料的硬度

表3 复合材料硬度值(HRC)
本研究采用低碳合金钢作为基体,其铸态组织为马氏体和贝氏体的混合组织,硬度较低。当在基体内原位生成TiC增强相时,硬度得到进一步提高。从表面到基体,用硬度计每隔一定距离测量其硬度值。表3是Al-Ti-C体系制备所得表面复合材料的硬度的变化。
表3所示硬度分别为基体、复合层平面横向硬度值。可看出复合材料层的硬度较基体有很大的提高。
6 复合层组织存在的缺陷
微孔存在的原因:气孔是反应铸渗复合材料中的主要缺陷。反应铸渗过程中,气体的产生主要来源有以下几个方面:预制块自身孔隙携带气体;粉末颗粒表面吸附气体;杂质相和其他反应物的气化,气体不能及时逸出,留在铸渗层内,就形成气孔;材料在燃烧过程中产生一些挥发气体及少量CO,难以完全排出,从而在材料内形成孔隙;燃烧过程中有Al蒸发,在材料内部形成背压产生的抗力将阻碍材料的致密化;在燃烧后施加压力不足,使材料连成脆性骨架。有资料显示,目前解决材料组织疏较有效的方法是施加压力。且随着加压压力的增大,材料的致密度增加。
7 结论
1)从实验可知,在SHS反应铸造方法中利用高温钢液制备铸造钢基合成TiC/Fe表面复合材料方法是可行的,反应合成表面复合层的TiC颗粒呈理想孤立球状分布,Al2O3呈光亮的不规则形状围绕在TiC颗粒周围形成典型的TiC/Fe金属陶瓷结构复合材料。
2)表面复合材料结合处无明显结合面,结合紧密,从基体到复合层逐渐呈梯度过渡。
3)稀土的加入使高温自蔓延反应组织晶粒得到细化,加入量过高,会抑制自蔓延反应的反应强度和剧烈程度,使表面复合层与基体结合疏松,结合厚度减小。
4)TiC/Fe表面复合材料硬度远远高于基体,且从基体到复合层也呈现梯度分布。
通过实验基本上得出了稀土的加入及加入量对SHS反应组织形态影响的因素,预制块的压实度对SHS反应强烈程度的影响,总体上完成了本次实验的任务,对本课题的后续研究做了基础性的贡献。
笔者相信,随着反应铸造工艺的不断完善及其基础研究的不断深入,各种高性能的原位MMCS必将在航空航天、汽车制造和仪器仪表等工业中,得到广泛的应用,并取得较大的经济效益和社会效益。
