2015至2017年黄石地区慢性乙型病毒性肝炎合并非酒精性脂肪性肝病的临床与病理分析
2019-07-28袁水英费新应刘文涛邵志林
沈 震 袁水英 费新应 刘文涛 邵志林
鄂东医疗集团市中医医院(市传染病医院)肝病科 (湖北 黄石, 435000)
最新的流行病学统计,我国现有HBV感染者约9 000万,其中慢性乙型肝类(CHB)患者约有2 000万[1]。随着人民生活水平的不断提高和“缺少锻炼”为主生活方式的流行,CHB合并非酒精性脂肪性肝病(NAFLD)的发病率也呈不断上升趋势。因此,CHB与NAFLD之间的关系得到越来越多的重视。本研究对黄石地区2015~2017年合并NAFLD患者的临床和病理进行了分析,旨在为临床决策提供线索。
1.资料与方法
1.1 研究对象 选取2017年3月至2018年9月黄石市中医医院肝病科门诊及住院病人,行肝组织穿刺以及实验室检查的CHB合并NAFLD患者176例为研究对象。回顾性分析研究,根据有无合并(NAFLD)及程度分为CHB组,CHB合并NAFLD轻度组,CHB合并NAFLD中重度组。研究通过医院伦理委员会通过,患者签署知情同意书。
1.2 纳入标准 ①CHB的诊断标准参照2015年中华医学会肝病学分会和中华医学会感染病学分会联合制定的《慢性乙型肝炎防治指南》的标准[2]。②NAFLD诊断标准参考2010年中华医学会肝脏病学分会脂肪肝和酒精性肝病学组修订的《非酒精性脂肪性肝病诊疗指南》的临床诊断标准[3]。
1.3 排除标准 ①合并有甲型肝炎、丙型肝炎、戊型肝炎等其他嗜肝病毒感染者。②合并有酒精性肝病、药物性肝病、自身免疫性肝病、代谢性肝病及造血系统和胆道疾病。③因过度肥胖、肋间隙过窄、腹水等因素致FibroScan检测失败者。④存在肝脏或者其他器官肿瘤患者。⑤肝脏穿刺失败或未能准确读取肝组织病理学结果的患者。⑥器官、骨髓移植术后。
1.4 实验室检查 肝脏生化指标主要包括 ALT、AST、GGT、TG、TC等,采用全自动生化分析仪(Hitachi,7020 型,Hitachi 公司,日本)。甲型肝炎、丙型肝炎、戊型肝炎等免疫学指标采用全自动酶标仪检测(Thermo 公司,美国),若样本检测孔的吸光度值高于空白对照孔吸光度的值2.1 倍,结果即为阳性,否则为阴性。血清HBV DNA检测采用实时定量PCR检测仪(LightCycler 480,Roche 公司,瑞士),检测区间为 500~1×108IU/ml。
1.5 肝组织学检查及评判标准 采用16G巴德一次性全自动活组织检查针行经皮肝穿刺获取 1.0~2.0 cm长的肝组织标本,至少包含6个以上汇管区,用4%甲醛固定,常规石蜡切片,同时进行HE和Masson染色。固定两位有经验的病理医师进行读片。参考NAS积分(0~8分):①肝细胞脂肪变:0分 (<5%);1分 (5%~33%);2分(34%~66%);3分(>66%)。②小叶内炎症(20 倍镜计数坏死灶):0分(无);1分(<2个);2分(2~4个);3分(>4个)。③肝细胞气球样变:0分,无;1分,少见;2分,多见。④Knodell(HAI)评分系统:汇管周围坏死(0~10分);肝小叶内变性和灶性坏死(0~4分);汇管区炎症(0~4分);肝纤维化(0~4分)。

2 结果
2.1 3组患者性别、年龄和BMI情况比较 见表1。
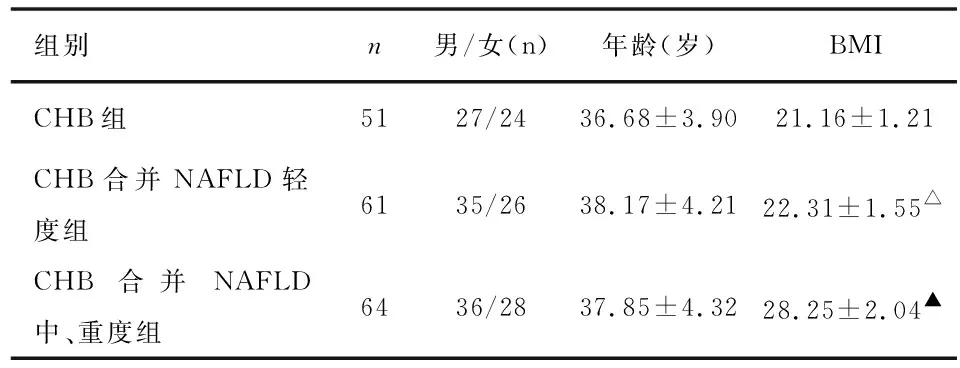
表1 3组患者性别、年龄和BMI情况比较
2.2 3组患者肝功能和血脂情况比较 见表2。
表2 3组患者肝功能和血脂情况比较
2.3 3组患者HBV DNA和肝脏病理组织学评分比较 见表3。
表3 3组患者HBV DNA和肝脏病理组织学评分比较分)
3 讨论
据国内外的报道,CHB患者合并NAFLD的发病率约为16.3%~37.6%[5,6]。有研究表明,HBV合并NAFLD发病与宿主的年龄、性别、肥胖、BMI、TC、TG等代谢因素相关[7],而少数研究则提出,HBV能通过增加LXRa转录活性上调SREBP-1以及上调PPAR-1,致肝细胞内脂肪累积而最终导致脂肪肝[8,9]。有鉴于此,理顺两者的相互关系,对于指导临床决策和判断预后,具有一定的积极意义。
在Machado等[6]的荟萃分析中,4 100例HBV患者中NAFLD的发病率为29.6%,其中6项研究显示NAFLD与严重的肝组织炎症无关[OR=0.69,95%CI(0.35~1.39),P=0.305],5项研究显示有无NAFLD与肝纤维化等级无关[SMD 0.22,95%CI(-0.84~0.41),P=0.495],2项研究的分析显示有无NAFLD患者的HAI评分没有差异[SMD 9.04,95%CI(-0.29,0.37),P=0.823]。但也有研究表明,循环中甘油三酯浓度的改变可能是诱导肝脏发生炎症反应的重要的机制,CHB如果合并NASH,会加重肝脏炎症和纤维化的进程。
从组织病理学分析,脂肪变性是NAFLD常见的组织学特征,主要表现为肝腺泡3区为主不同程度的大泡性、小泡性和大、小泡混合性脂肪变性。此外,大泡性肝细胞脂肪变性、小叶炎症和窦周纤维化是NASH的组织学特征,CHB的组织学特征是弥漫性界面炎和明显的汇管区炎症。这些都为更准确地判断CHB合并NAFLD患者的病情和临床决策提供了组织学依据[10]。
本研究发现,CHB合并NAFLD的患者并不少见,入组病例在相同的转氨酶水平下比较后发现,合并肝脂肪变的CHB组患者无论是BMI或是TC、TG水平均明显高于单纯CHB组(P<0.05)。值得注意的是,单纯CHB、CHB合并NAFLD轻度者HBV DNA水平差异无统计学意义(P>0.05),但均显著高于CHB合并NAFLD中重度者,差异有统计学意义(P<0.05),和文献[6]报道一致,这提示即使HBV DNA水平达到了抗病毒治疗的标准,肝脏的炎症活动仍然可能是因为肝脂肪变引起的,需要充分衡量抗病毒治疗的必要性以及针对脂肪肝进行相应的规范治疗,包括了饮食控制和体育锻炼,以及保肝降酶治疗。在组织学上比较,3组患者的肝纤维化评分水平差异无统计学意义(P>0.05)。虽然,脂肪变的CHB患者均具有典型的肝脂肪变和肝脏气球样变,但对于单纯CHB及CHB合并NAFLD轻度组,肝脏炎症主要表现为汇管区周围及汇管区炎,故其炎症和纤维化仍然考虑和HBV活动有关,需要抗病毒治疗;而对于CHB合并NAFLD中重度者,肝脏炎症主要表现为小叶炎症,汇管周围肌汇管区炎较轻,故转氨酶的升高主要与肝脂肪变有关。
由此看来,肝脏脂肪变的程度,并不加重CHB患者的肝纤维化程度,肝脂肪变轻度的CHB患者肝功能的异常主要和HBV活动有关,而肝脂肪变中重度的CHB患者肝功能异常则可能和脂肪肝有关,脂肪肝与HBV DNA水平的关系仍需进一步研究。
