复方苦参注射液治疗慢性乙型肝炎有效性和安全性的系统评价和Meta分析*
2019-07-28梁士兵田紫煜李玉琦杨思红曹卉娟刘建平
梁士兵 田紫煜 李玉琦 杨思红 曹卉娟 刘建平△
1.山西中医药大学基础医学院 (山西 太原, 030000) 2.北京中医药大学循证医学中心
乙型肝炎是由乙型肝炎病毒(HBV)感染肝脏而引起的病毒感染性疾病,其可损伤肝脏并引起其他急性或慢性疾病。慢性乙型肝炎(CHB)的定义为乙肝表面抗原持续阳性6个月或以上。CHB是全球性重要公共卫生问题。据世界卫生组织报告,全球约20亿人曾感染HBV,其中2.4亿人为慢性HBV感染者,而每年约有65万人死于HBV感染所致的肝功能衰竭、肝硬化和肝细胞癌[1~3]。中国作为乙型肝炎高感染率国家, HBV感染者约9000万例, 居于全球之冠[4]。现有CHB患者约2800万例, 每年因肝硬化、肝癌等乙肝相关并发症死亡的患者高达26.3万例[5~6]。
目前,中国CHB防治指南(2015更新版)共推荐了7种治疗CHB的抗病毒药物,包括2种干扰素和5种核苷(酸)类似物[7]。美国和韩国肝病学会所推荐药物与之相同[8]。尽管治疗CHB的药物种类较多,但至今尚无特效药物。复方苦参注射液(CKI)属纯中药制剂,主要由苦参和白土苓2种中药精制而成,收载于卫生部药品标准(第14册),常用于抗肿瘤,且疗效突出、副反应少[9]。
本研究首次基于以往相关随机对照试验(RCTs),对CKI治疗CHB的有效性与安全性进行了系统评价,为临床医生规范用药提供循证证据。
1 资料与方法
1.1 文献纳入与排除标准 纳入标准:①研究类型:RCTs,语言限定为中文和英文。②研究对象:被明确诊断为CHB的患者,无年龄、性别及种族限制。③干预措施:试验组患者采用CKI,或者在对照组患者用药基础上加用CKI;对照组患者采用除CKI外的其他常用药物。如果两组患者同时接受一般辅助疗法,则辅助疗法应完全相同。④结局指标应至少包含以下之一:主要结局指标:全因死亡率;乙型肝炎相关死亡率(由肝硬化或肝细胞癌等肝脏疾病或失代偿引起);乙型肝炎相关疾病的发病率(或肝脏失代偿,如肝硬化或肝细胞癌);生命质量;严重不良事件。次要结局指标:HBeAg阴转率;HBV DNA阴转率;ALT复常率或治疗前后ALT水平变化;一般(非严重)不良事件。排除标准:①无法获取全文的文献;②涉嫌抄袭的文献;③对同一研究发表的多篇文献,则对多篇文献中可用信息进行综合。
1.2 文献检索策略 系统检索知网、万方、维普、SinoMed、PubMed和 Web of science数据库。检索年限为建库到2019年6月15日。为更全面获取文献,中文数据库检索词设定为苦参注射液、乙肝、肝炎、HBV,英文数据库检索词设定为Compound matrine injection和Compound Kushen injection。根据不同数据库情况,分别选择主题词、摘要等方式进行检索。以知网检索为例,其检索策略为:SU = ‘苦参注射液’AND SU = (‘乙肝’ + ‘肝炎’ +‘HBV’)。
1.3 文献筛选与资料提取 将检索所获取全部文献的题录导入NoteExpress 3.0软件。首先排除重复发表的文献,再根据纳入/排除标准,逐一阅读题目、摘要及全文,对文献进行筛选。使用Excel 2010建立资料提取表,对纳入文献进行资料提取。
1.4 偏倚风险评价标准 采用Cochrane协作网“偏倚风险”评价工具[10],包括:①随机序列的生成;②分配方法隐匿;③患者和实施者盲法;④结局评价者盲法;⑤不完整结局数据;⑥选择性结局报告;⑦其他偏倚。每一项均可被评为“低偏倚风险”、“高偏倚风险”或“偏倚风险不确定”。
1.5 统计学方法 应用RevMan 5.3软件对数据进行统计分析。对于二分类资料,采用相对危险度(RR)和95%置信区间(CI)表示;对于连续性资料,采用均数差(MD)和95%CI表示。通过I2值判断不同研究间的统计学异质性大小:当研究间统计学异质性较小时(I2≤25%),采用固定效应模型进行Meta分析;当研究间存在较大统计学异质性时(25%
2 结果
2.1 检索结果 通过系统检索共获取461篇文献。经查重、阅读题目和摘要,共排除442篇文献,对剩余19篇文献进行全文阅读筛选,最终纳入11篇中文文献(11项研究)[11~21]。筛选流程见图1。

图1 文献筛选流程图
2.2 纳入文献特征 见表1、图2。所有研究均在中国进行,且均为双臂RCT。表1显示了所有研究的详细特征。所有研究共涉及1123例受试者,试验组572例,对照组551例。受试者年龄范围为16~68岁,男女比例为1.04∶1,仅1项报告了受试者的疾病严重程度[21]。有8项研究仅文字描述试验组与对照组的基线可比[12~14,16~20],1项以表格比较了两组患者基线,其余2项未提及基线可比性信息[11,21]。
2.3 偏倚风险评估 所有研究均未报告随机序列生成方法、随机分配隐匿及盲法相关信息,但根据试验组和对照组患者的干预措施进行评估,认为11项研究不可能对受试者和医生实施了盲法,因此,所有文献的选择偏倚和测量偏倚均被评为“不清楚”,实施偏倚被评为“高风险”;所有研究均未提及研究方案及注册信息,仅1项报告了严重不良事件[13],其余文献均未报告预先设定的主要结局指标,因此,所有研究文献的报告偏倚均被评为“高风险”;所有文献中,4项无法判断是否存在受试者脱失[11~13,20],其失访偏倚被评为“不清楚”,其余7项则不存在受试者脱失[14~20,21],其失访偏倚则被评为“低风险”。所有研究文献中,9项研究的试验组和对照组基线具有可比性文献[12~20],因此将这9项研究的其他偏倚评为“低风险”,其余2项因未提及基线可比性相关信息而被评价为“不清楚”[11,21]。图2显示了纳入研究偏倚风险评估情况。

图2 纳入文献偏倚风险评估情况
2.4 结局指标
2.4.1 主要结局 所有研究均未报告全因死亡率、乙型肝炎相关死亡率、乙型肝炎相关疾病发病率和患者生存质量。仅1项报告了试验组和对照组均未发生严重不良事件,其余研究未提及相关信息。因此,本研究未能对CKI治疗或辅助治疗CHB的以上结局指标进行评价分析。
2.4.2 次要结局
2.4.2.1 HBeAg阴转率 11项研究中,有6项报告了HBeAg阴转率,其中1项比较类型为“CKIvs保肝药物”[12],5项为“CKI+对照措施vs对照措施”[11,13,16,18,21]。
“CKIvs保肝药物”的研究,其试验组和对照组HBeAg阴转受试者数分别为7例和2例,总样本量分别为21例和20例。结果显示两组无统计学差异[RR=3.33, 95%CI为(0.78, 14.17)]。经分析,5项“CKI+对照措施VS对照措施”的研究间统计学异质性小(I2=0),采用固定效应模型,结果显示两组有统计学差异[RR=1.91, 95%CI为(1.53, 2.40)]。根据对照药物类别不同,对5项研究进行亚组分析,1项为“CKI+保肝药物vs保肝药物”,试验组和对照组的HBeAg阴转受试者数分别为5例和2例,总样本量分别为30例和29例,结果显示2组无统计学差异(RR=2.42, 95%CI为(0.51, 11.48)][12];4项为“CKI+抗病毒药物vs抗病毒药物”,且研究间统计学异质性较小(I2=20%),采用固定效应模型,结果显示CKI联合抗病毒药物应用,优于单用抗病毒药物[RR=1.90, 95%CI为(1.51, 2.38)][13,16,18,21]。见图3。

图3 HBeAg阴转率:CKI+对照措施 vs 对照措施
2.4.2.2 HBV DNA阴转率 11项研究中,有7项研究报告了HBV DNA阴转率,其中1项为“CKIvs保肝药物”[12],6项为“CKI+抗病毒药物vs抗病毒药物”[13,14,16,18,19,21]。
1项“CKIvs保肝药物”的研究,其试验组和对照组的HBV DNA阴转受试者数分别为6例和1例,总样本量均各为36例。结果显示两组无统计学差异[RR=6.00, 95%CI为(0.76, 47.36)]。经分析,6项“CKI+抗病毒药物vs抗病毒药物”的研究间存在较大统计学异质性(I2=30%),采用随机效应模型,结果显示CKI联合抗病毒药物应用,优于单用抗病毒药物[RR=1.47, 95%CI为(1.27, 1.70)]。见图4。
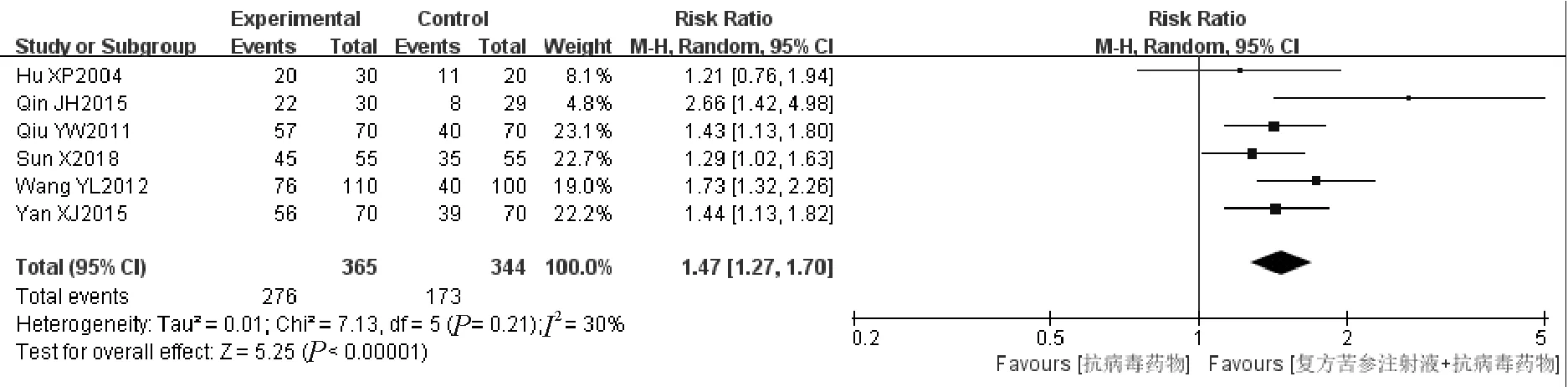
图4 HBV DNA阴转率:CKI + 抗病毒药物 vs 抗病毒药物
2.4.2.3 ALT复常率或治疗前后ALT水平变化 11项研究中,2项“CKI+抗病毒药物vs抗病毒药物”的研究报告了ALT复常率[13,18];7项报告了治疗前后ALT水平变化:其中1项为“CKI+保肝药物vs保肝药物”[11],6项为“CKI+抗病毒药物vs抗病毒药物”[14~17,19,20]。
经分析,2项报告了ALT复常率的研究间存在显著统计学异质性(I2=76%)。因此,未对这2项研究结果进行Meta分析。其中1项报告了CKI联合抗病毒药物,相比单用抗病毒药物,二者的ALT复常率分别为96.67% (29/30)、93.10% (27/29), 比较差异无统计学意义[15];另外1项报告了CKI联合抗病毒药物的ALT复常率显著高于抗病毒药物单用[20]。
7项报告了治疗前后ALT水平变化的研究间存在显著统计学异质性(I2=89%)。1项“CKI+保肝药物vs保肝药物”的研究,其结果显示两组无统计学差异[MD=-21.07 U/L,95%CI为(-45.05,2.91)];6项“CKI+抗病毒药物vs抗病毒药物”的研究间存在显著统计学异质性(I2=91%)。因此,根据治疗疗程不同。对6项“CKI+抗病毒药物vs抗病毒药物”的研究进行亚组分析:2项疗程为6周的研究间存在显著统计学异质性(I2=98%)[16,19],未进行Meta分析;3项疗程为8周的研究间存在较大统计学异质性减小(I2=63%)[14,15,20],采用随机效应模型,结果显示两组有统计学差异[MD=-29.34 U/L,95%CI为(-41.11, -17.56)];1项疗程为24周的研究,其试验组和对照组总样本量各为63例,结果显示2组有统计学差异[MD=-44.43 U/L,95%CI为(-62.02, -26.84)][17]。见图5。

图5 治疗前后ALT水平变化:CKI+抗病毒药物 vs 抗病毒药物
2.4.2.4 一般(非严重)不良事件 纳入研究中,有3项“CKI+抗病毒药物vs抗病毒药物”的研究报告了这一结局指标。其中1项报告了治疗期间两组患者均无一般不良事件[14]。另外2项报告了两组患者均发生了一般不良事件发生[18,19]:1项报告了两组不良反应类似,主要为流行性上呼吸道感染样症状、皮疹、脱发等,经对症处理均恢复,但未报告具体病例数[18];1项则报告了在治疗过程中,治疗组有8例、对照组有9例受试者发生间断胃肠不适,但2组比较差异无统计学意义(P>0.05)[19]。
2.5 其他统计分析 根据预先设定,对于纳入文献数量≥10篇的Meta分析需要进行倒漏斗图分析,文献数量≥8篇的Meta分析需要进行TSA分析。然而,本研究中没有达到以上要求的Meta分析,因此未进行相关分析。
3 讨论
3.1 主要发现 CKI与抗病毒药物(如拉米夫定、恩替卡韦、干扰素)联合应用,相比单用抗病毒药物治疗CHB,在增加HBeAg阴转人数、HBV DNA阴转人数及降低ALT水平上存在一定优势。而CKI单用、或与保肝药物(如甘草酸二铵注射液、还原型谷胱甘肽)联合应用治疗CHB,相比单用保肝药物,在增加HBeAg阴转人数、HBV DNA阴转人数或降低ALT水平上并无差别。由于仅极少数研究报告了不良事件信息,因此,现有证据尚不足以对CKI治疗CHB的安全性得出结论。
3.2 本研究局限性 首先,仅纳入了以中文和英文发表的文献,可能会遗漏其他语言发表的文献而导致证据收集不全;其次,未能对Meta分析进行倒漏斗图分析和TSA分析,无法排除小样本研究效应对研究结果的影响,也无法验证Meta分析结果稳定性。第三,所纳入RCT中,有9项均给予了试验组和对照组相同常规治疗,但由于无法获取常规疗法的具体操作信息,所以,本研究未能考虑常规疗法对CKI有效性和安全性的影响。基于以上几点,本研究证据仅能为CKI治疗CHB提供有限参考价值。
3.3 对今后开展相关RCT的建议 首先,应招募足够样本量,关注研究方法、规范试验设计(如正确实施随机、盲法等),参照国际公认的SPIRIT声明提前制定研究方案并注册[22];其次,本研究所纳入RCT只关注了HBeAg阴转率、HBV DNA阴转率等替代结局,而未关注更加以患者为中心的全因死亡率、乙型肝炎相关死亡率、乙型肝炎相关疾病的发病率、患者生命质量等结局,这与其他研究发现的问题几乎一致[23]。因此,建议今后开展的RCT除了关注替代结局外,还应更加以患者为中心,关注全因死亡率、乙型肝炎相关死亡率、乙型肝炎相关疾病的发病率、患者生命质量等;第三,应严格按照CONSORT声明[24]对RCT进行规范报告。
该证据表明,CKI对于CHB的治疗能够起到一定疗效,而对于CKI应用于CHB治疗的安全性,现有证据尚不足以得出结论。未来,需要更多严格设计、大样本量的高质量RCT来研究确认CKI治疗CHB的有效性和安全性。
