高炉渣基A型沸石的合成及对Pb2+离子的吸附
2019-07-17赵斯琴
刘 静,温 馨,赵斯琴,长 山
(1.内蒙古师范大学化学与环境科学学院,呼和浩特 010022;2.内蒙古自治区环境化学重点实验室,呼和浩特 010022)
1 引 言
内蒙古包钢高炉渣是炼铁过程中产生的主要固体废弃物,是一种复杂的硅酸盐,其主要化学成份为CaO 39.5320%、SiO234.6574%、MgO 6.9019%、SO32.4473% TiO21.2379%、Fe2O30.7749%等[1]。中国年产高炉渣约3.6亿吨,目前大部分以铺路材料和超细粉形式作为水泥原料[2],广泛应用于建筑领域。但是这些利用都是低附加值,且无法完全利用如此规模的高炉渣。Kuwahara等[3]将高炉渣酸浸过滤,得到富含Ca2+、Mg2+、Al3+滤液,取滤液通过共沉淀法可以合成类水滑石。而大量研究表明,酸浸后的滤渣是硅凝胶,可以作为沸石合成的硅源,并且实现高炉渣浸出液制备类水滑石,而浸出渣制备沸石,不再产生二次废弃物。
A型沸石是一种由硅氧四面体和铝氧四面体组成的立方型晶体,具有规则的空腔和骨架结构。A型沸石作为一种具有优异功能的非金属矿物材料,在工业中有广泛的应用。其显著特点是孔隙度高、比表面积大,从而表现出较强的离子交换性能、吸附性能、催化性能、耐酸性能、耐热性能、耐辐射性能等性能,因此被广泛用于去除废水中氨氮、氟、重金属离子、有机物和放射性物质等[4-7]。A型沸石的性能依赖于其骨架结构、结晶形貌和晶粒大小,而影响合成的因素有原料摩尔比[n(SiO2)/n(Al2O3)]、[n(H2O)/n(SiO2)]、结晶温度和水热时间[8-12]。
基于以上文献基础,本研究以内蒙古包钢高炉渣为原料,采用水热法成功合成了高炉渣基A型沸石,探讨原料配比、结晶温度和时间对合成高炉渣A型沸石结构和晶体形貌的影响,并表征微观结构,研究其对Pb2+离子的吸附性能。
2 实 验
2.1 主要的仪器试剂
高炉渣(包头钢铁厂,100目);盐酸;氢氧化钠;偏铝酸钠;硝酸铅(模拟废水)。
采用UItimaⅣ型X射线衍射仪表征样品相结构,以CuKα射线作为辐射源,管电压为40 kV,管电流为40 mA;样品的形貌分析以S-4800型场发射扫描电子显微镜测定,722N型可见分光光度计。
2.2 高炉渣基A型沸石的合成
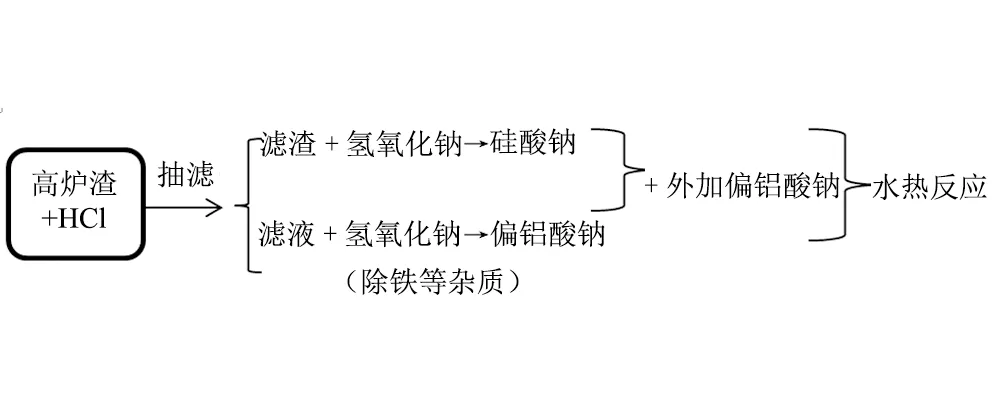
图1 合成高炉渣基A型沸石的实验流程 Fig.1 Experimental flow of zeolite Abased on blast furnace slag
实验流程如图1,称取10 g高炉渣,加入60 mL 3 mol·L-1HCl,充分搅拌30 min,抽滤,将得到的上层固体在电热鼓风干燥箱中80 ℃干燥以备硅源,滤液用3 mol· L-1NaOH溶液调节,使Al(OH)3完全沉淀,过滤并在鼓风干燥箱中50 ℃干燥以备铝源。配置50 mL 4.62 mol·L-1NaOH溶液,把上述氢氧化钠溶液分成两半,将上述得到的硅源固体加入一半的NaOH溶液中,过滤留下清液A,上述得到的铝源固体加入到另一半的NaOH溶液中,过滤留下清液B。把下清液B加入A溶液中,一滴一滴地加入50 mL 0.54 mol·L-1NaAlO2溶液,得到的混合液充分搅拌1 h。再转移至50 mL聚四氟乙烯高压釜中,水热温度为100 ℃,反应12 h,即可得到高炉渣基A型沸石。同法合成不同n(SiO2)/n(Al2O3)比分别为0.24、0.48、0.71、0.95的高炉渣基A型沸石,不同n(H2O)/n(SiO2)比分别为48、58、68、78、88、98的高炉渣基A型沸石,不同水热时间分别为8 h、12 h、16 h、20 h、24 h的高炉渣基A型沸石,不同水热温度分别为80 ℃、100 ℃、120 ℃、140 ℃的高炉渣基A型沸石,即得系列高炉渣基A型沸石。
2.3 吸附性能实验
2.3.1 Pb2+离子的标准曲线
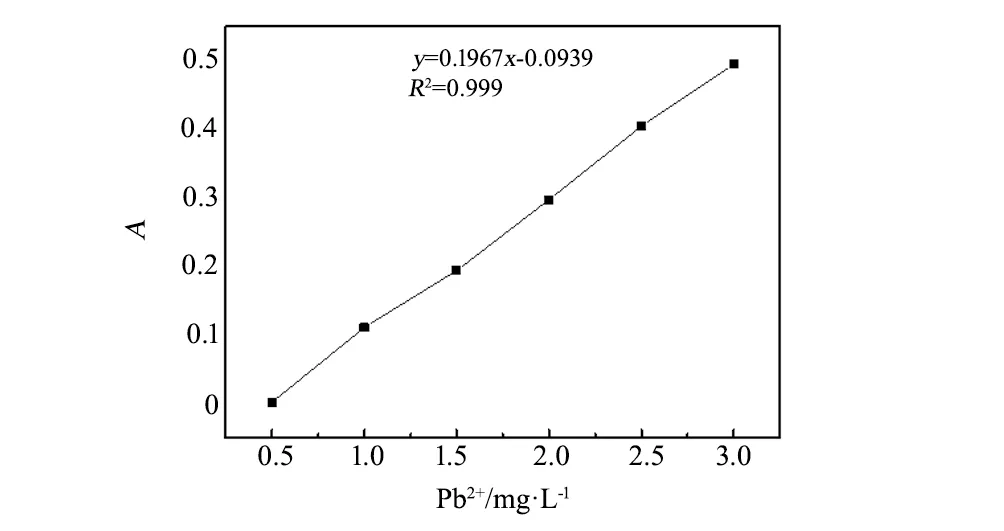
图2 Pb2+离子溶液的标准曲线 Fig.2 Standard curve of lead ions
分别取不同浓度的Pb2+离子溶液,并用722N型可见分光光度计测定各溶液的吸光度,波长为575 nm,以Pb2+离子溶液的浓度为横坐标轴(c),以吸光度为纵坐标轴(A),用线性回归求出标准曲线如图2。其标准曲线公式A=0.1967x-0.0939,R2=0.999,即Pb2+离子溶液的浓度与吸光度具有良好的线性关系[13]。
2.3.2 吸附性能实验
室温下,分别取25 mL(50 mg·L-1) Pb2+离子溶液于100 mL的锥形瓶中,高炉渣基A型沸石的加入量分别为10 mg、20 mg、30 mg、40 mg、50 mg、60 mg,于200 r·min-1多用振荡器上振荡60 min,然后静置,用针筒过滤器取澄清液,分别加入1 mL缓冲溶液,0.5 mL二甲基酚橙溶液于10 mL比色管中,定容,摇匀,装进比色皿中,于722N型可见分光光度计测定吸光度,并根据公式(1)和(2)计算吸附后Pb2+离子溶液的浓度、吸附率和吸附量。同理研究不同吸附时间对高炉渣基A型沸石吸附Pb2+离子的影响;不同Pb2+离子溶液浓度对高炉渣基A型沸石吸附Pb2+离子的影响;Pb2+离子溶液不同pH值对高炉渣基A型沸石吸附Pb2+离子的影响。
η=(C0-C')/C0×100%
(1)
q=(C0-C')×25/m
(2)
式中:C0-吸附前溶液中Pb2+离子溶液浓度(mg/L),C'-吸附后溶液中Pb2+离子溶液浓度 (mg/L),η-吸附率(%),q-吸附量(mg/g),m-吸附剂的用量(mg)。
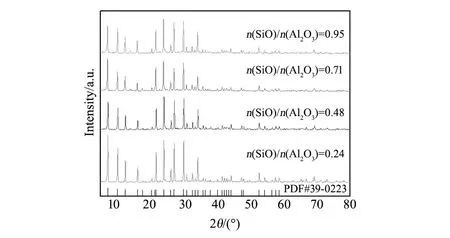
图3 不同n(SiO2)/n(Al2O3)比合成高炉渣基A型沸石的XRD图谱 Fig.3 XRD patterns of zeolite A based on blast furnace slag synthesized with different n(SiO2)/n(Al2O3)
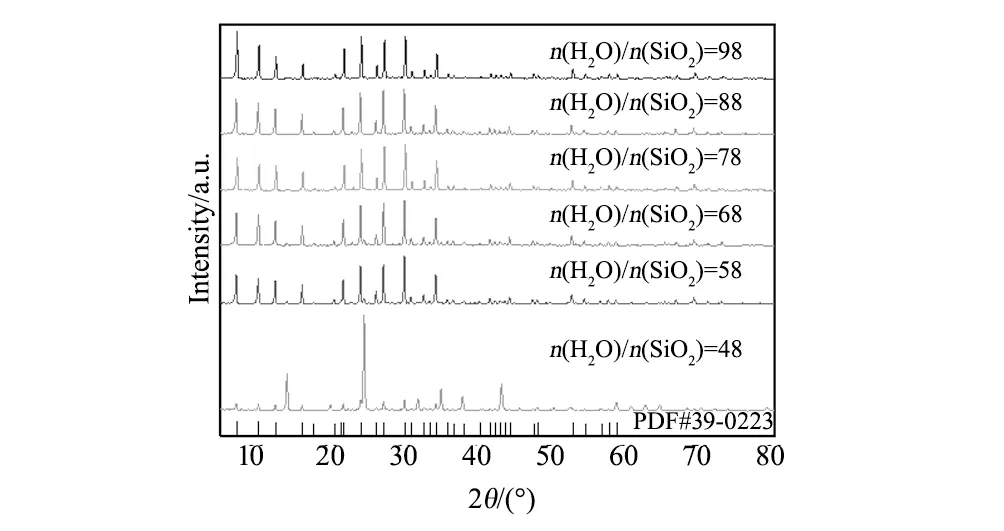
图4 不同n(H2O)/n(SiO2)比对合成高炉渣基A型沸石的XRD图谱 Fig.4 XRD patterns of zeolite A based on blast furnace slag synthesized with different n(H2O)/n(SiO2)
3 结果与讨论
3.1 高炉渣基A型沸石的合成
3.1.1 高炉渣基A型沸石XRD结果与讨论
文献可知,n(SiO2)/n(Al2O3)的比列在0~1范围之间,能够形成高炉渣基A型沸石[14-15],根据高炉渣内部SiO2的含量,当NaAlO2的加入量为2.312~9.248 g范围之间,硅源与铝源的比列恰好在0~1范围内。图3为水热温度为100 ℃、水热时间为12 h、不同n(SiO2)/n(Al2O3)比合成高炉渣基A型沸石的XRD图谱。由图3可知,当n(SiO2)/n(Al2O3)值分别为0.24、0.48、0.71、0.95所合成样品的XRD图谱与PDF标准卡比对,分别对应于A型沸石的特征衍射峰,可见所合成样品均为结晶度较好的高炉渣基A型沸石,其中n(SiO2)/n(Al2O3)的比例为0.24所合成高炉渣基A型沸石XRD图谱中衍射峰强度最强,即此时样品的结晶度最好,从而,本实验初步选择n(SiO2)/n(Al2O3)=0.24为最佳合成条件。
文献可知大多数沸石晶体的内孔中都存在着可流动的水分子,当加热或抽真空时,沸石可以脱水,而当晶体重新与水接触时又可以重新吸附水分子,水分子可以自由地进入沸石的空穴内[16-17],即合成A型沸石与外加水量有一定的关系。图4为n(SiO2)/n(Al2O3)值为0.24,水热温度100 ℃、水热时间12 h、不同n(H2O)/n(SiO2)的比例合成高炉渣基A型沸石的XRD图谱。由图4可知,n(H2O)/n(SiO2)值为48所合成高炉渣基A型沸石的衍射峰与标准A型沸石衍射峰相比,对应程度较差,说明高炉渣基A型沸石生长未完全;随着n(H2O)/n(SiO2)比例的增加,所合成高炉渣基A型沸石的衍射峰与标准卡片中A型沸石特征衍射峰对应逐渐吻合,结晶度也越来越好,可见,n(H2O)/n(SiO2)的比列越大,越有利于合成高结晶度的A型沸石。原因为,反应体系在一定温度条件下,高炉渣基A型沸石的合成是在以水为加热介质为进行[18], 水量多少影响着体系中的传热效果, 从而影响沸石晶体的生长,从而n(H2O)/n(SiO2)越大越有利于A型沸石晶体的生长。本实验初步确定n(H2O)/n(SiO2)=98为最佳合成条件。
图5为水热温度为100 ℃、n(SiO2)/n(Al2O3)值为0.24、n(H2O)/n(SiO2)值为98、不同水热时间所合成高炉渣基A型沸石的XRD图谱。由图5可知,所有时间条件所合成样品XRD图谱与PDF标准卡比对,均产生了A型沸石的特征衍射峰,即不同时间条件均合成出了A型沸石;同时随着结晶时间的延长,产物的结晶度呈现不规则变化的趋势;水热时间为8 h所合成高炉渣基A型沸石衍射峰的强度较弱,说明晶体结晶度不够,原因有可能为,此时晶体主要以成核向晶体快速生长的过渡期为主,因此晶体未完全进行晶化[19],而水热时间为12 h所合成高炉渣基A型沸石XRD图谱可知,样品无杂质,且衍射峰强度较强,表明样品晶化完全,继续增加晶化时间,所合成高炉渣基A型沸石的衍射峰强度变化不大,实验初步确定最佳水热时间为12 h。
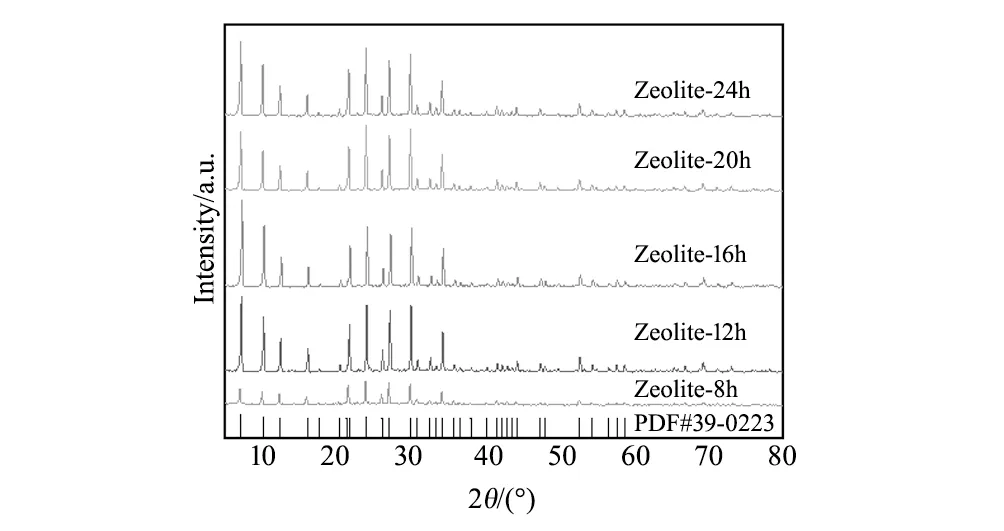
图5 不同水热时间合成高炉渣基A型沸石的XRD图谱 Fig.5 XRD patterns of zeolite A based on blast furnace slag synthesized at different hydrothermal time
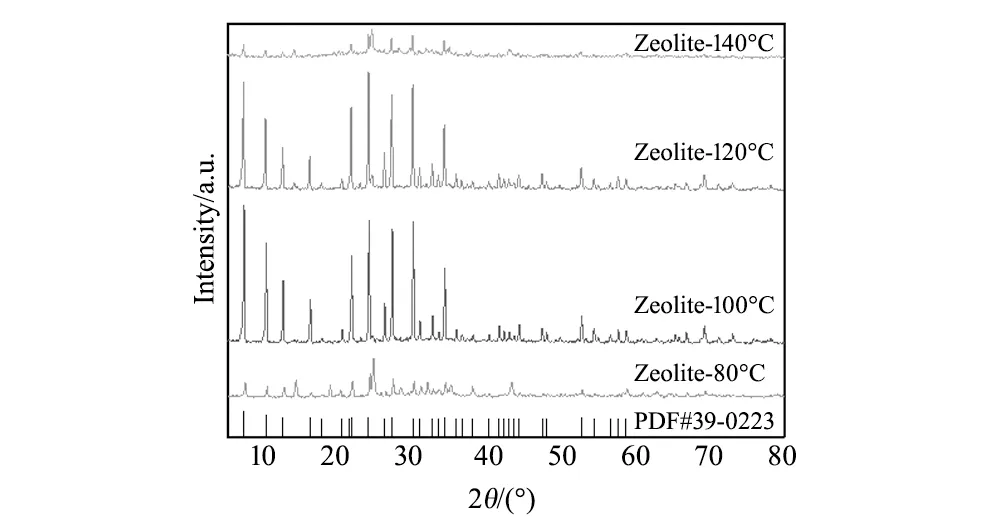
图6 不同水热温度合成高炉渣基A型沸石的XRD图谱 Fig.6 XRD patterns of zeolite A based on blast furnace slag synthesized at different hydrothermal temperatures
图6为n(SiO2)/n(Al2O3)值为0.24、n(H2O)/n(SiO2)值为98、水热时间为12 h、不同水热温度所合成高炉渣基A型沸石的XRD图谱。由图6可知,所有样品XRD图谱均对应于PDF标准卡中A型沸石特征衍射峰,即不同温度条件均合成出了高炉渣基A型沸石;其中,水热温度为80 ℃所合成高炉渣基A型沸石,衍射峰强度较弱,即A 型沸石的结晶度较低,而水热温度分别为 100 ℃和120 ℃时所合成高炉渣基A型沸石,峰型尖锐、无其它杂峰,即样品的结晶度较好,当继续增加水热温度为140 ℃时,XRD 谱图中A型沸石的衍射峰强度反而开始减弱。原因为,随着温度的升高,能够加快晶体晶化速度,但过高的反应温度反而破坏已形成晶体的结构,即温度升高带来动力学有利的同时降低了热力学条件,在一定的温度范围内过冷度的减小造成结晶的驱动力不足,限制了相同时间内结晶度的提高[20-23]。本实验初步确定100 ℃为最佳水热温度。

图7 不同 n(SiO2)/n(Al2O3)比合成高炉渣基A型沸石的SEM照片 (a)0.24;(b)0.48;(c)0.7;(d)0.95 Fig.7 SEM images of zeolite A based on blast furnace slag synthesized at different n(SiO2)/n(Al2O3) (a)0.24;(b)0.48;(c)0.71;(d)0.95
3.1.2 高炉渣基A型沸石的SEM结果与讨论
图7为不同n(SiO2)/n(Al2O3)比所合成高炉渣基A型沸石的SEM照片,放大倍数均为10000倍。由图7可知,当n(SiO2)/n(Al2O3)比分别为0.24和0.48时,所合成的样品具有标准A型沸石规则的立方晶体形貌,其它杂质较少,在合成过程中用氢氧化钠溶液已经除去铁等主要杂质。其中n(SiO2)/n(Al2O3)比为0.24时,能够观察到大小不同的立方体相互排列的形貌,证明所合成的样品为高炉渣基A型沸石;而当n(SiO2)/n(Al2O3)值分别为0.71和0.95时,所合成的样品少有立方体形的晶体形貌,同时形成了许多棒状的晶体形貌,证明此时晶体成型未完全。结合XRD结果,实验确定n(SiO2)/n(Al2O3)=0.24为最佳合成条件。
图8为不同n(H2O)/n(SiO2)比所合成高炉渣基A型沸石的SEM照片。由图8可知,n(H2O)/n(SiO2)值为48所合成样品图片中,只有少量立方体形的A型沸石;随着n(H2O)/n(SiO2)比例的逐渐增加,图片中A型沸石的比例逐渐增多,并具有规整的晶面;其中,n(H2O)/n(SiO2)值为98所合成高炉渣基A型沸石图片中,清晰地观察到许多大小不一,正六面体形的晶体形貌。结合XRD结果,实验确定n(H2O)/n(NaOH)=98为最佳合成条件。

图8 不同n(H2O)/n(SiO2)比对合成高炉渣基A型沸石的SEM照片 (a)48;(b)58;(c)68;(d)78;(e)88;(f)98 Fig.8 SEM images of zeolite Abased on blast furnace slag synthesized under different n(H2O)/n(SiO2) (a)48;(b)58;(c)68;(d)78;(e)88;(f)98
图9为不同水热时间所合成高炉渣基A型沸石SEM照片。由图9可知,水热时间为8~24 h范围之间,所合成的样品均能观察到完整的立方体形、大小不同的A型沸石;其中,水热时间为12 h所合成高炉渣基A型沸石图片中,清晰地观察到完整的大小不一排列的立方晶体的形貌。结合XRD结果,实验确定水热时间为12 h为最佳合成条件。
图10为不同水热温度所合成高炉渣基A型沸石的SEM照片。由图10可知,水热温度为80 ℃所合成样品图片中,能够观察到棒状和球状堆积而组合的形貌,可见该温度条件下未能形成A型沸石;水热温度为100 ℃所合成样品图片中,可以观察到大小不一,完整的立方体A型沸石;水热温度分别为120 ℃和140 ℃时所合成样品图片可知,该温度条件下虽然形成了A型沸石,但观察到样品结构比较松散,原因可能为,高炉渣合成A型沸石的形成与温度有一定的关系,温度过低,晶体成核过程所提供的能量过低,不足以使晶体由成核向快速生长转化;温度过高,容易使晶体稳定的结构坍塌而变得松散。结合XRD结果,实验确定水热温度100 ℃为最佳合成条件。

图9 不同水热时间合成高炉渣基A型沸石的SEM照片 (a)沸石-8 h;(b)沸石-12 h;(c)沸石-16 h;(d)沸石-20 h;(e)沸石-24 h Fig.9 SEM images of zeolite A based on blast furnace slag synthesized under different hydrothermal time(a)zeolite-8 h;(b)zeolite-12 h;(c)zeolite-16 h;(d)zeolite-20 h;(e)zeolite-24 h

图10 不同水热温度合成A型沸石的SEM照片 (a)沸石-80 ℃;(b)沸石-100 ℃;(c)沸石-120 ℃;(d)沸石-140 ℃ Fig.10 SEM images of zeolite A based on blast furnace slag synthesized under different hydrothermal temperatures (a)zeolite-80 ℃;(b)zeolite-100 ℃;(c)zeolite-120 ℃;(d)zeolite-140 ℃
3.2 高炉渣基A型沸石对Pb2+离子的吸附性能
3.2.1 高炉渣基A型沸石的加入量对Pb2+离子吸附的影响
为了研究加入量对高炉渣基A型沸石吸附Pb2+离子影响,在吸附时间为2 h,Pb2+离子溶液浓度为50 mg/L,不调节溶液pH的条件下,不同高炉渣基A型沸石加入量对吸附Pb2+离子影响如图11。由图11可知,高炉渣基A型沸石对Pb2+离子具有较强的吸附性能,而随着高炉渣基A型沸石投入量的逐渐增加,对Pb2+离子的吸附率呈先增加再减少的变化趋势,对Pb2+离子的吸附量呈逐渐减小的趋势,当吸附剂加入量为10 mg,吸附量最大,为117.29 mg/g,当吸附剂加入量为60 mg,吸附量最小,为19.64 mg/g;其中吸附剂投入量为30 mg时,对Pb2+离子的吸附率达到最高,为94.82%。原因为,高炉渣基A型沸石表面具有潜在的活性,内部含有-OH官能团,因此对Pb2+离子具有较高的吸附性能[24],随着高炉渣基A型沸石投加量的不断增加,高炉渣基A型沸石的吸附能力达到饱和而吸附率下降,所以本实验确定吸附剂的最佳质量为30 mg。
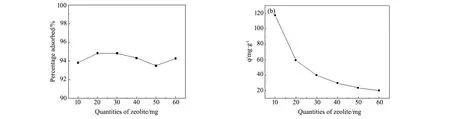
图11 加入量对高炉渣基A型沸石吸附Pb2+离子影响曲线图 (a)吸附率;(b)吸附量 Fig.11 Effect of the quantities of zeolite A based on blast furnace slag on adsorption properties of Pb2+ (a)adsorption rate;(b)adsorption quantity
3.2.2 吸附时间对高炉渣基A型沸石吸附Pb2+离子的影响
为了研究吸附时间对高炉渣基A型沸石吸附Pb2+离子影响,在高炉渣基A型沸石加入量为30 mg,Pb2+离子溶液浓度为50 mg/L,不调节溶液pH的条件下,不同吸附时间对吸附Pb2+离子影响如图12。由图12可知,当吸附时间为10 min时,高炉渣基A型沸石吸附率就达到94.75%,吸附量均在39 mg/g左右,与粉煤灰等矿物质合成A型沸石吸附Pb2+离子的吸附量相差不大[25-26],而延长吸附时间对吸附率和吸附量均没有明显的影响。这主要是因为在吸附初期Pb2+离子主要被吸附在高炉渣基A型沸石的外表面,外扩散阻力较低,吸附较快[27],伴随着吸附时间的延长,溶液中的Pb2+离子浓度逐渐降低,与此同时吸附质沿着沸石微孔向内部吸附扩散,由此吸附时间对高炉渣基A型沸石吸附Pb2+的影响不大。基于实验结果,确定最佳吸附时间为10 min。
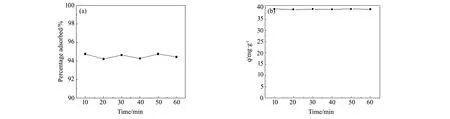
图12 吸附时间对高炉渣基A型沸石吸附Pb2+离子的影响曲线图 (a)吸附率;(b)吸附量 Fig.12 Effect of adsorption time on adsorption of Pb2+ by zeolite A based on blast furnace slag (a)adsorption rate;(b)adsorption quantity
3.2.3 吸附动力学的建立
在研究吸附动力学的过程中,最常用模型是准二级动力学模型。在固相吸附容量的基础上推导出了准二级动力学模型,可表示为:
(3)
(4)
式中k2为准二级模型的速率常数:q为t的吸附量:qe为平衡吸附量:t为吸附时间。
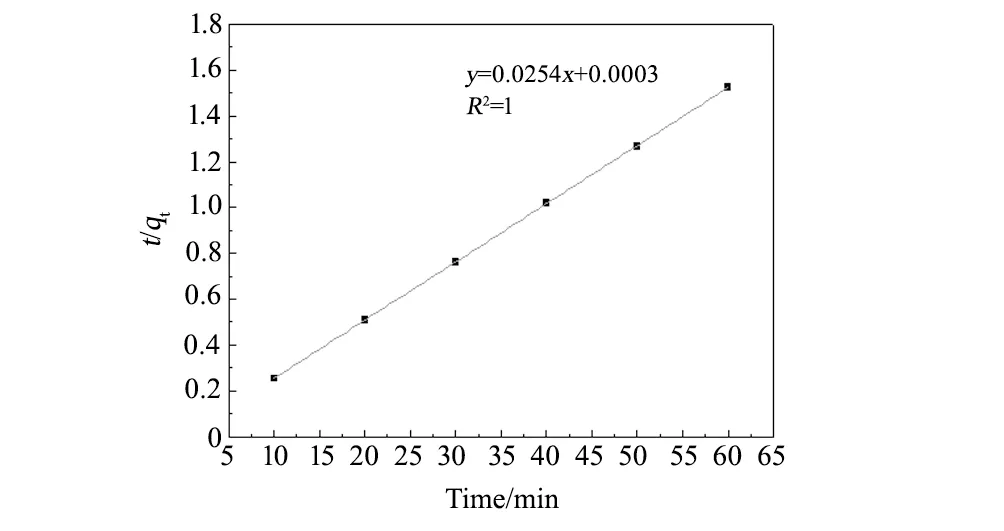
图13 高炉渣基A型沸石拟二级吸附动力学模型 Fig.13 Model of secondary adsorption kinetics of the zeolite A synthesized based on blast furnace slag
为研究高炉渣基A型沸石对Pb2+离子的吸附速率,对其进行线性拟合,结果如下:

表1 拟二级吸附动力学模型数据Table 1 Model data of secondary adsorption kinetics
表1为拟二级吸附动力学模型数据,由表1可知:拟二级动力学方程的拟合程度较好,R2等于1,并由图13高炉渣基A型沸石拟二级吸附动力学模型可知高炉渣基A型沸石拟二级动力学模型具有良好的线性关系。高炉渣基A型沸石对Pb2+离子的吸附过程能够很好地符合伪二级动力学方程,平衡时吸附量为39.37 mg/g。
3.2.4 Pb2+离子溶液浓度对高炉渣基A型沸石吸附Pb2+离子的影响
图14为Pb2+离子溶液初始浓度对高炉渣基A型沸石吸附Pb2+离子的影响曲线图。由图14可知,随着Pb2+离子溶液浓度的增加,高炉渣基A型沸石的吸附率呈现先增加再减少的趋势,当Pb2+离子溶液的浓度为80 mg·L-1时,吸附率可达96%以上,而吸附量呈线性增加。原因为,Pb2+离子溶液的浓度过低时,高炉渣基A型沸石表面的活性位点未全部反应,而随着Pb2+离子溶液浓度的增大,使得其表面的所有活性位点完全反应,从而使得吸附率先增加。再继续增加Pb2+离子溶液浓度,表面已经有吸附完全后的氢氧化铅沉淀覆盖在沸石外表面,并吸附位点较少,因此吸附率有所减弱。
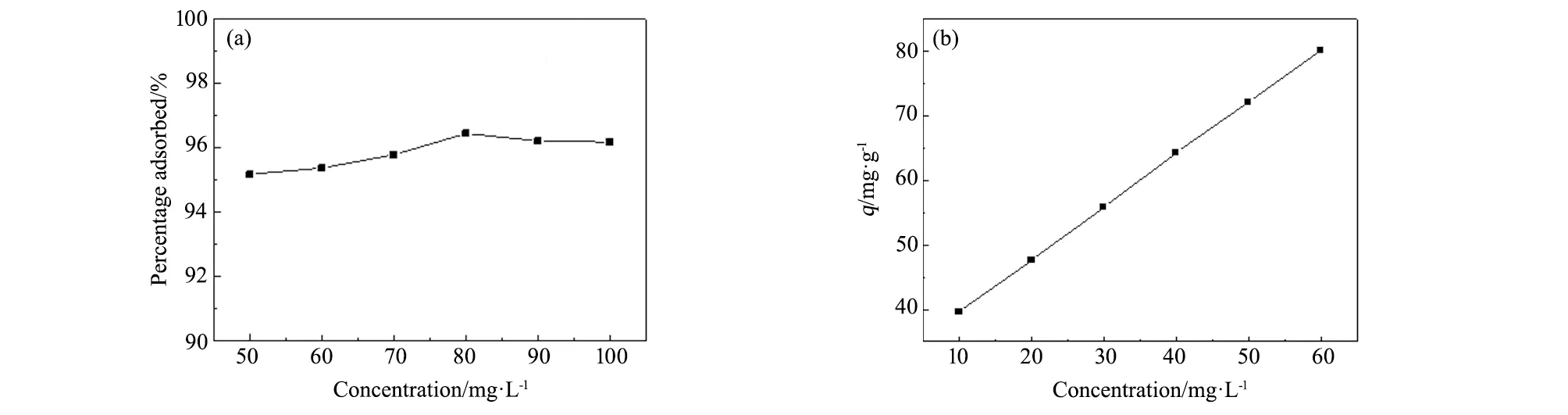
图14 Pb2+离子溶液初始浓度对高炉渣基A型沸石吸附Pb2+离子的影响曲线图 (a)吸附率;(b)吸附量 Fig.14 Effect of ion concentration of Pb2+ on the adsorption properties of the zeolite A synthesized based on blast furnace slag (a)adsorption rate;(b)adsorption quantity
3.2.5 吸附等温线的建立
描述吸附过程最常用的基础数据是吸附等温线,为了进一步研究高炉渣基A型沸石吸附Pb2+离子的行为,分别采用Langmuir和Freundlich吸附等温线对实验数据进行拟合。Langmuir吸附等温式的线性表达式为:
(5)
式中:k为Langmuir吸附平衡常数;Ce为吸附后溶液中溶质的平衡浓度,qe为吸附后吸附剂的平衡吸附量,q∞为吸附剂的极限吸附量。
Freundlich吸附等温方程的表达式为
(6)
按式(5)和式(6)进行线性回归分析,可得高炉渣基A型沸石的吸附等温线,如图15所示。计算得到的Langmuir和Freundlich吸附等温方程参数列于表2中。
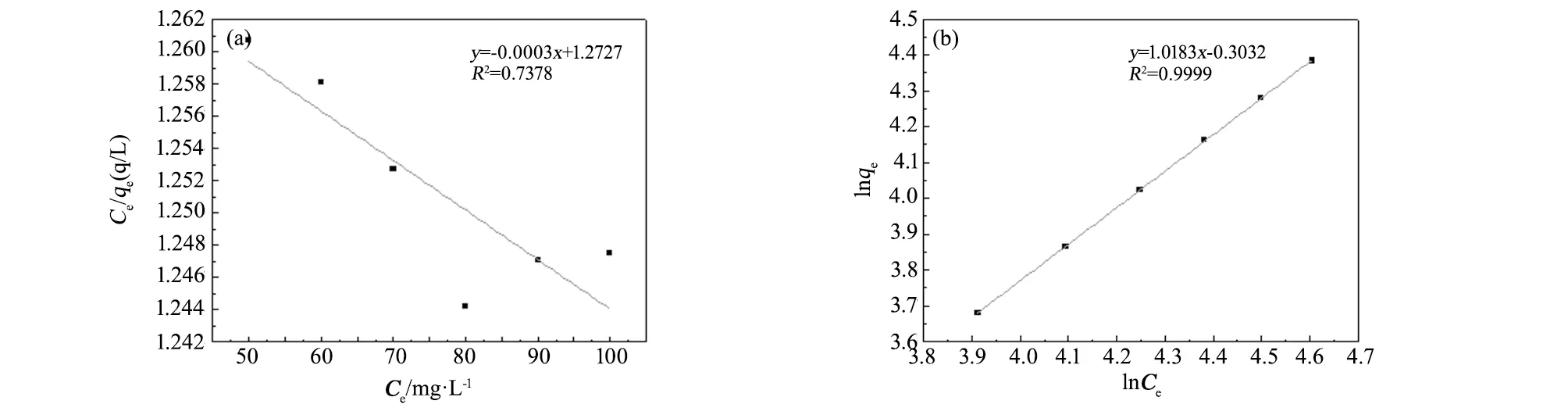
图15 高炉渣基A型沸石Langmuir吸附等温线和Freundlich吸附等温线 Fig.15 Adsorption isotherm of Langmuir adsorption isotherm and Freundlich adsorption isotherm by the zeolite A synthesized based on blast furnace slag

Langmuirq∞/mg·g-1kLR2FreundlichkFnR2 3333.32.36×10-40.73780.73840.98200.999 9
高炉渣基A型沸石Langmuir吸附等温式的线性相关系数R2=0.7378,Freundlich吸附等温式的线性相关系数R2=0.9999,说明高炉渣A型沸石对Pb2+离子的吸附符合Freundlich吸附等温方程,属于多分子层吸附,1/n介于0.1~2之间,说明吸附容易进行。
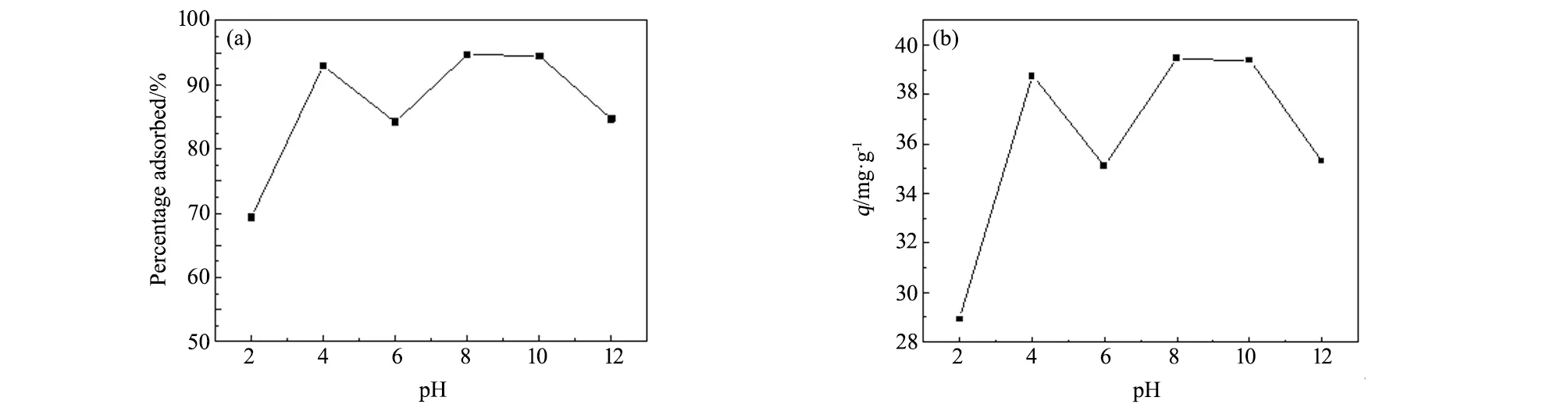
图16 溶液的pH对高炉渣基A型沸石吸附Pb2+离子的影响曲线图 (a)吸附率;(b)吸附量 Fig.16 Effect of pH on adsorption of Pb2+ ion by the zeolite A synthesized based on blast furnace slag (a)adsorption rate;(b)adsorption quantity
3.2.6 Pb2+离子溶液pH对高炉渣基A型沸石吸附Pb2+离子的影响
图16为溶液的pH对高炉渣基A型沸石吸附Pb2+离子的影响曲线图。由图16可知,高炉渣基A型沸石吸附Pb2+时,溶液的pH值对去除率有一定的影响, pH<4时,高炉渣基A型沸石对Pb2+离子的吸附率较小;pH值在4~10范围内,对Pb2+离子的吸附性能较高,其中pH=6时,有个明显的下调现象;pH>10时,对Pb2+离子的吸附率明显下降。原因有可能为,pH<4时,由于溶液中的H+浓度过高,占据了高炉渣基A型沸石的吸附位点,并与Pb2+离子形成了竞争吸附,因此Pb2+离子吸附率较低[28];pH=6时,Pb2+离子配合物的溶解度降低,因而产生沉淀效应使Pb2+离子吸附率减小;pH>10时,这主要是由于在碱性条件下,Pb2+离子部分形成氢氧化物沉淀[29-32],从而导致吸附性能减弱,吸附量与吸附率的变化规律一样。因此本实验条件下,最佳溶液pH值确定为中性。
4 结 论
采用内蒙古包头高炉渣为前驱体,利用水热法成功合成了高炉渣基A型沸石。高炉渣基A型沸石最佳合成条件为:n(SiO2)/n(Al2O3)=0.24 、n(H2O)/n(SiO2)=98、水热温度为100 ℃和水热时间为12 h。所合成的高炉渣基A型沸石对Pb2+离子具有较强的吸附性能,吸附率最高达94.82%,符合拟二级动力学模型,属于多分子层吸附,吸附容易进行,平衡吸附量为39.37 mg/g。
