1 128张免疫抑制剂处方超说明书用药情况及其不良反应风险分析Δ
2019-07-15张翠翠让莹子王雪莲马建龙
张翠翠,让莹子,王雪莲,刘 畅,马建龙,张 镭
(中日友好医院药学部,北京 100029)
超说明书用药是指药品使用的适应证、给药方法、适用人群、剂量或疗程不在药品监督管理部门批准的药品说明书之内的用法[1]。由于审批时间长,修改药品说明书需要大量时间和费用,加上在一些特殊人群(妊娠期、围产期妇女,儿童及老人)中很难进行临床试验等原因,超说明书用药为普遍存在的临床现象[2-5]。超说明书用药的风险远高于按照药品说明书用药,会引发药品安全性、有效性、医疗责任和伦理学等一系列问题[6]。免疫抑制剂可对患者体内具有免疫活性的细胞起到杀伤与免疫抑制作用,能够抑制T细胞与B细胞介导的免疫反应,在器官移植、风湿免疫性疾病及血液系统疾病等方面发挥重要作用[7]。但是,如果免疫抑制剂使用不当,将会带来感染、肝肾损伤等不良反应,甚至发生肿瘤等严重并发症。本研究对某三级甲等医院(以下简称“该院”)免疫抑制剂超说明书用药情况进行梳理,并对其不良反应风险进行分析,为临床合理超说明书用药提供参考,更好地规避超说明书用药的风险。
1 资料与方法
1.1 资料来源
从该院信息系统中抽取2016年7月至2018年6月门诊药房所有免疫抑制剂处方。
1.2 方法
根据国家食品药品监督管理总局批准的最新版药品说明书,从适应证、给药剂量、适应人群和给药途径等4个方面对每张处方中每个用药记录逐项判断其是否与药品说明书相符;若不相符,则认定其存在超说明书用药,记录超说明书用药的类型,并通过Excel软件对药品通用名、药品说明书用法和临床实际用法进行总结和整理。以涉及的具体药品通用名、不良反应为检索词,检索中国知网、维普数据库和万方数据库等中文数据库及PubMed等外文数据库,检索时限截至2018年6月,收集具体药品的超说明书用药的相关文献及指南、专家共识,并对报道的不良反应进行汇总、分析。通过Micromedex数据库的Thomson分级系统查询免疫抑制剂超说明书用药的收录情况,评价药物用法的循证医学证据。通过Micromedex数据库查询超说明书用药涉及药品的说明书中的不良反应,应用风险矩阵法对具体风险发生的可能性以及后果严重性进行不良反应风险评价[8]。本研究对药品说明书中记录的药品不良反应发生率进行描述,并对风险发生可能性水平标准进行调整,具体评分标准见表1。根据药品说明书中记载的不良反应发生率及后果严重性的结果,建立二维坐标体系,进行矩阵排序,得到各个风险因素的风险级别。具体风险级别对照表参照表2所列的澳大利亚-新西兰风险管理标准(AS/NZS 4360∶2004)[9],其中,“E”为极严重风险(extremelyrisk);“H”为高危险度风险(highrisk);“M”为中等危险度风险(moderaterisk);“L”为低危险度风险(lowrisk)。

表1 风险发生可能性和风险后果严重性分级评分标准Tab 1 Standard of occurrence probability and severity levels of risks

表2 AS/NZS 4360∶2004矩阵评估指数Tab 2 AS/NZS 4360: 2004 matrix assessment index
2 结果
2.1 免疫抑制剂超说明书用药情况
该院免疫抑制剂超说明书用药处方共计1 128张,类型主要为超适应证用药,主要涉及环孢素软胶囊、他克莫司胶囊、吗替麦考酚酯分散片及吗替麦考酚酯胶囊,见表3。

表3 免疫抑制剂超说明书用药情况Tab 3 off-label drug use of immunosuppressants
2.2 免疫抑制剂超说明书用药证据类型
1 128张免疫抑制剂超说明书用药处方均有循证医学证据,其中,有国外指南证据的处方占8.3%,有国内指南证据的处方占35.1%,有专家共识证据的处方占52.8%,有其他文献证据的处方占3.7%,见表4。
2.3 免疫抑制剂超说明书用药的有效性、推荐级别和证据等级分类
共25项免疫抑制剂超说明书用法,环孢素软胶囊超说明书用法中有4项被Micromedex数据库收录,他克莫司胶囊超说明书用法中有3项被Micromedex数据库收录,吗替麦考酚酯分散片超说明书用法中有4项被Micromedex数据库收录,见表5。
2.4 免疫抑制剂超说明书用药的不良反应风险矩阵评估指数
免疫抑制剂超说明书用药的不良反应风险矩阵评估指数显示,环孢素胶囊的肾毒性,吗替麦考酚酯胶囊/吗替麦考酚酯分散片的呼吸困难、淋巴瘤及非黑色素瘤和他克莫司胶囊的肾毒性、呼吸窘迫综合征的不良反应风险级别为E级,为极严重风险,需要严密关注,见表6。
3 讨论
3.1 免疫抑制剂超说明书用药及其证据分析
免疫抑制剂超说明书用药主要集中在以下几类疾病:自身免疫异性疾病,如系统性红斑狼疮、特发性炎性肌病、干燥综合征、贝赫切特综合征、多发性硬化、混合性结缔组织病、狼疮肾炎、重症肌无力及视神经脊髓炎;血液系统疾病,如原发性免疫性血小板减少症、再生障碍性贫血及骨髓增生异常综合征;肾脏相关疾病,如肾小球肾炎、肾病综合征。以上超说明书用药均有国内外指南或专家共识作为证据支持,证据强度较高,共有11项(占44.0%)被Micromedex数据库收录记载。在Micromedex数据库推荐、证据和有效性评价中,对于环孢素软胶囊超说明书用于再生障碍性贫血、他克莫司胶囊超说明书用于狼疮肾炎的评价较高,均为有效性等级,即证据支持有效(Class Ⅱa),推荐等级为大多数情况下推荐使用(Class Ⅱa),证据等级为结论冲突的随机对照试验的荟萃分析、小规模或研究方法有显著缺陷的随机对照试验及非随机研究(B类)。随着医学的发展、器官移植技术的进步,该院的肺移植手术也逐渐增多,肺移植术后的急、慢性排斥反应依然是影响患者预后的因素,而术后患者免疫抑制剂应用的正确与否,对患者的生存时间、生活质量均有直接影响。但目前免疫抑制剂超说明书用于肺移植术后只有一些零散的单中心研究和随机对照临床试验[10-15],并未形成相关指南或共识,证据级别较低。临床医师应根据患者的个体情况和免疫抑制剂的药物特点,合理制订免疫抑制方案。

表4 免疫抑制剂超说明书用药证据类型Tab 4 Evidence types of off-label use of immunosuppressants
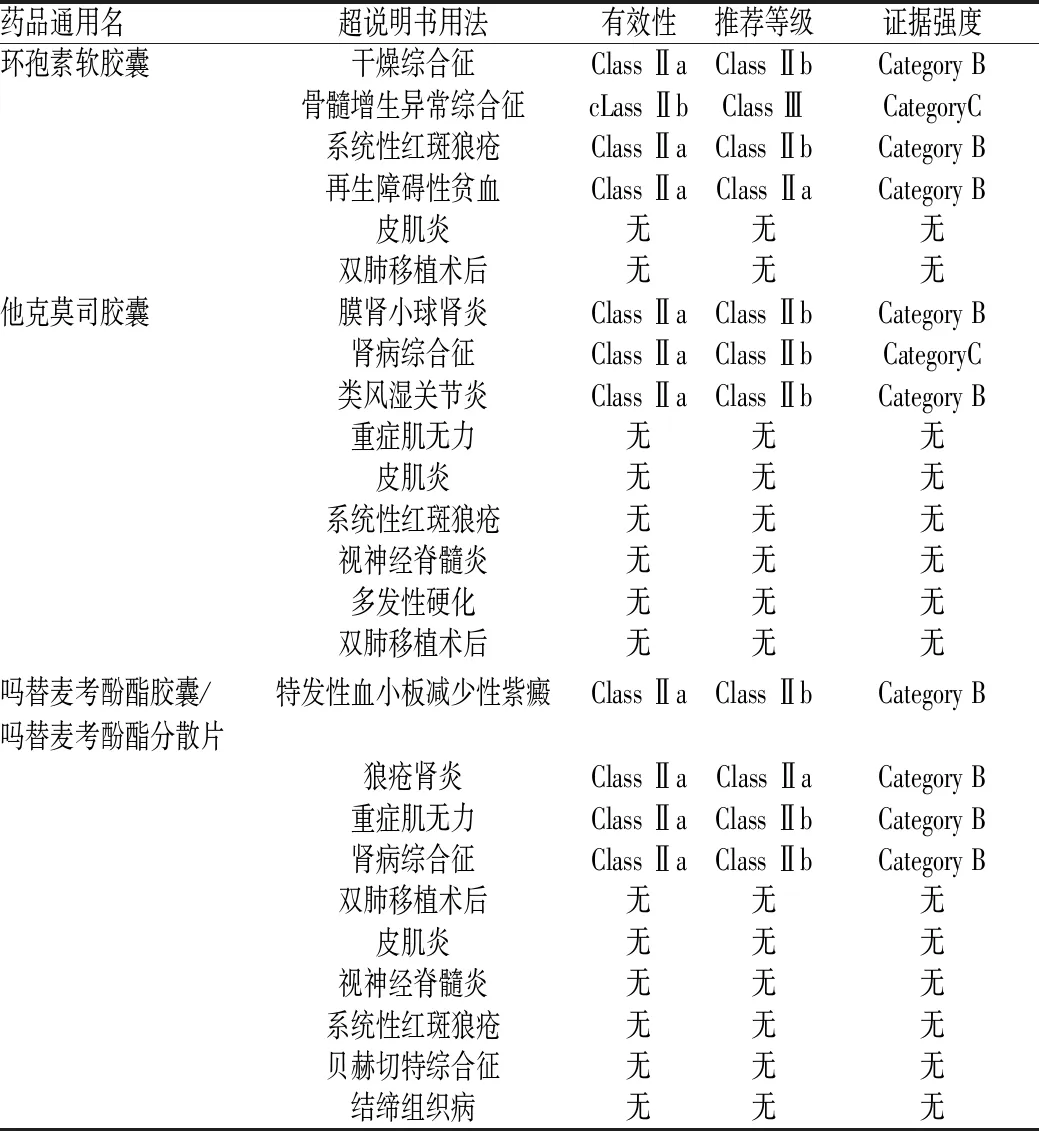
表5 免疫抑制剂超说明书用药的有效性、推荐级别和证据等级分类Tab 5 Efficacy, recommendation grade, evidence intensity of off-label use of immunosuppressants
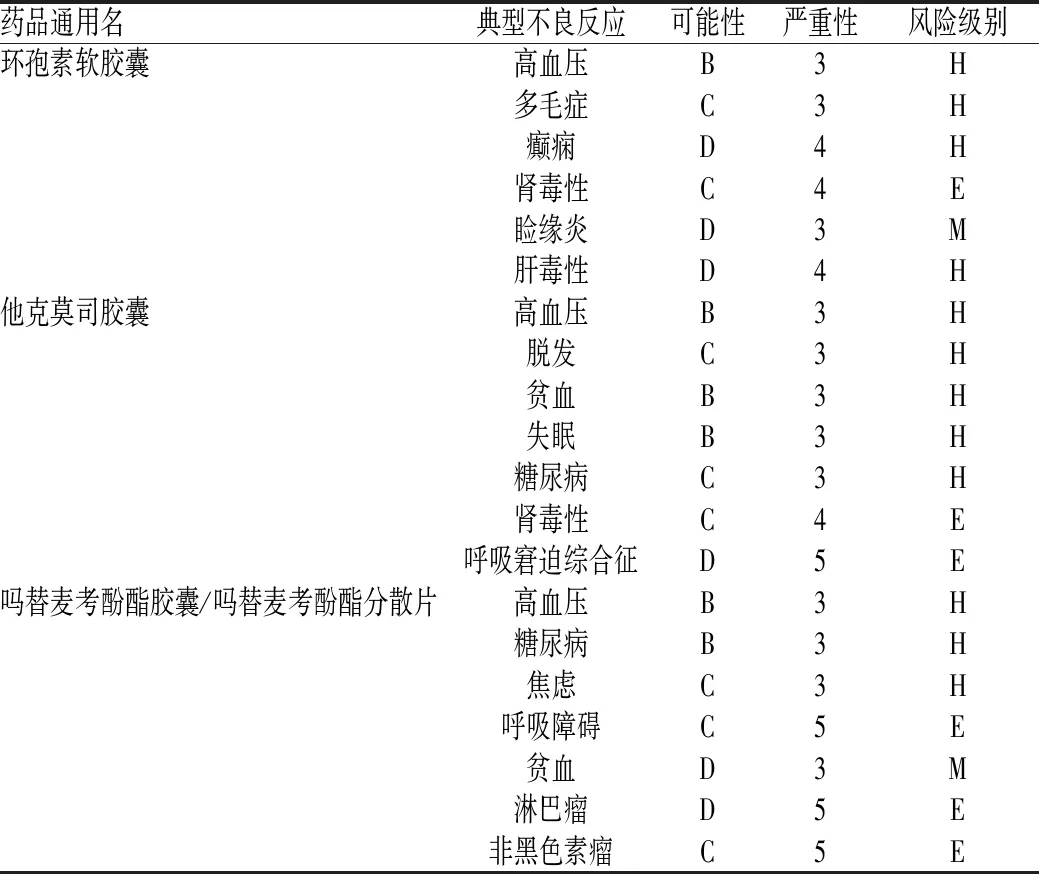
表6 免疫抑制剂超说明书用药的不良反应风险矩阵评估指数Tab 6 Matrix assessment index of adverse drug reactions of off-label use of immunosuppressants
3.2 免疫抑制剂超说明书用药不良反应风险分析
目前,药品不良反应严重程度的分级标准主要有世界卫生组织的四级标准、文献报道中经常使用的三级标准及美国的九级标准[16]等。以上分级标准在表述上存在着抽象、冗繁、不全面和操作性不佳等问题,且没有进行量化处理,使研究人员难以对某类或单个药物进行评价,从而不利于药品安全监管和医务人员对临床药物的选择。风险矩阵法是一种能够把危险发生的可能性和伤害的严重程度综合评估的风险大小定性的风险评估分析方法,常用1个二维的表格对风险进行半定量分析,其优点是操作简便、快捷,将风险可视化。吴长青等[8]肯定了风险矩阵法在药品不良反应评价中的作用。但风险矩阵法的缺点在于对风险的评估只是一个相对值的评价,无法定量地判定各个风险之间的差距,其评价结果只比较出风险因素间相对的风险程度高低。从本研究不良反应风险矩阵评估指数结果可以看出,吗替麦考酚酯胶囊7项不良反应中有3项风险级别为E级,为极严重风险;而其10项超说明书用法中,有6项未被Micromedex数据库收录,证据级别较低,建议临床谨慎超说明书使用吗替麦考酚酯胶囊,确需使用时,在用药过程中建议患者定期进行血药浓度监测,综合评估用药效果,严密监测其不良反应。
4 建议
超说明书用药在临床诊疗中普遍存在,即使有循证医学证据支持,也依然存在不良反应及法律等方面的风险。免疫抑制剂可能引发骨髓抑制、肝肾毒性等严重不良反应,其超说明书用药更应谨慎。本研究结果显示,该院95.6%的免疫抑制剂超说明书用药证据级别为国内外诊疗指南或专家共识,但仍有4.4%的超说明书用药证据级别较低,缺乏系统的循证医学证据支持,给患者用药安全带来了严重隐患。医院应建立超说明书用药评价小组,对其安全性、有效性进行系统评价,形成推荐意见及达成共识,最终形成院内指导意见应用于临床。目前国内并没有针对超说明书用药安全性评价的具体办法,需尽快建立超说明用药安全性评价体系。本研究尝试运用风险矩阵法,结合不良反应发生的概率与后果,对免疫抑制剂超说明书用药的不良反应风险进行了初步评估,评估结果可为医院规范超说明书用药安全性评价提供参考。
