甲巯咪唑与丙硫氧嘧啶对甲状腺功能亢进患者肝功能影响的系统评价*
2019-07-08刘敏苏娜秦舟徐珽
刘敏,苏娜,秦舟,徐珽
(1.四川大学华西医院药剂科,成都 610041;2.四川大学华西药学院,成都 610041)
甲状腺功能亢进(hyperthyroidism,甲亢)是内分泌科常见疾病,国内外指南均推荐以下3种方式治疗甲亢[1-2]:抗甲状腺药物(antithyroid drug,ATD)治疗、I131治疗和手术治疗。目前临床常用抗甲状腺药物是甲巯咪唑(methimazole,MMI)和丙硫氧嘧啶(propylthiouracil,PTU)[2],这两种药物均可诱导肝损伤等严重不良反应,严重时可危及生命[3]。目前的系统评价仅对肝损伤例数进行了评价[4],并未对各项肝生化指标异常情况进行深入评价,笔者在本研究系统全面评价甲巯咪唑和丙硫氧嘧啶对甲亢患者肝功能的影响,旨在为临床安全用药提供循证依据。
1 资料与方法
1.1检索方法 计算机检索CNKI、VIP、WANFANG、CBM、PUBMED、COCHRANE LIBRARY、EMBASE、MEDLINE等中英文数据库。中文检索词为“甲状腺功能亢进”“甲亢”“Graves病”“甲巯咪唑”“丙硫氧嘧啶”“肝功能”“肝损伤”“肝损害”“肝毒性”等。英文检索词为“Hyperthyroidism”“Graves Disease”“Methimazole”“Propylthiouracil”“liver function”“hepatotoxicity”“liver injury”“liver failure”等。检索时间为建库起至2017年10月,采用主题词和关键词相结合的方式检索并进行文献溯源。
1.2纳入标准
1.2.1研究类型 随机对照试验(randomized controlled trial,RCT)。
1.2.2研究对象 诊断为甲亢或毒性弥漫性甲状腺肿患者[1-2],不限年龄、性别和种族。
1.2.3干预措施 干预措施分别为使用甲巯咪唑治疗和使用丙硫氧嘧啶治疗,不限剂量和疗程。
1.2.4结局指标 主要结局指标为肝损伤例数,次要结局指标为肝生化指标异常例数以及治疗前后肝生化指标变化值,肝生化指标包括丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转移酶(AST)、碱性磷酸酶(alkaline phosphatase,ALP)、总胆红素(T-BiL)。肝损伤判断标准为:在排除其他病因、疾病或药物所致肝损伤的情况下,患者用药前肝功能正常,用药后肝生化指标至少有1项升高至正常值上限2倍以上;或者患者用药前肝功能轻度异常,用药后呈进行性加重[5]。
1.3排除标准 排除无相应结局指标以及数据不完整的研究。
1.4数据的提取与质量评价
1.4.1数据的提取 由2名研究者独立阅读题名和摘要,采用统一数据提取表进行数据提取,并进行交叉核对,出现争议时讨论解决。提取信息主要包括作者、发表时间、干预措施、患者例数、性别、年龄、疗程、结局指标等。
1.4.2质量评价 采用改良Jadad量表[6]对纳入研究的质量进行评价,评分为1~3分的研究为低质量研究,评分为4~7分的研究为高质量研究。评价的具体内容包括:①随机序列的产生;②分配隐藏;③盲法;④失访与退出。
1.5统计学方法 应用Cochrane协作网提供的Revman5.3.5版软件进行Meta分析。计数资料用相对危险度(relative risk,RR)作为效应量,计量资料用标准化均数差(standardized mean difference,SMD)作为效应量,均以95%置信区间(confidence intervals,CI)表示。采用卡方检验对纳入研究的异质性进行评价[7],各研究间异质性较小(P>0.1,I2<50%)则采用固定效应模型进行分析;反之则采用随机效应模型进行分析,并进一步行敏感性分析或亚组分析,最后可通过绘制倒漏斗图判断是否存在发表偏倚。
2 结果
2.1文献检索及质量评价结果 共检索到文献1067篇,其中中文文献416篇,英文文献651篇,用EndnoteX7软件去除重复文献332篇,阅读文题和摘要后初筛出60篇,阅读全文后有28项研究符合纳入或排除标准,最终纳入分析甲亢患者3181例,其中使用甲巯咪唑患者1752例,使用丙硫氧嘧啶患者1429例。甲巯咪唑组患者起始剂量多为30 mg·d-1,再逐渐减量至5~10 mg·d-1维持;丙硫氧嘧啶组患者起始剂量多为300 mg·d-1,再逐渐减量至50~100 mg·d-1维持。甲巯咪唑组患者年龄25.1~45.38岁,丙硫氧嘧啶患者年龄25.1~46.1岁,纳入研究的疗程为12周~24个月,见表1。纳入研究中有2项Jadad评分为1分[16,20],16项Jadad评分为2分[8-10,12-13,15,17,21,25,28-32,34-35],10项Jadad评分为4分[11,14,18-19,22-24,26-27,33],因而此次纳入的研究中有18项是低质量研究,10项是高质量研究。
2.2数据分析
2.2.1肝损伤例数 17项研究[8-11,14,16,18-20,23-25,29,31-34]报道了丙硫氧嘧啶组和甲巯咪唑组肝损伤例数。异质性检验显示,各研究间统计学差异较小(P=0.80,I2=0%),采用固定效应模型进行分析。森林图结果显示,丙硫氧嘧啶组肝损伤发生率更高[RR=2.73,95%CI(2.23,3.34),P<0.000 01](图1)。
2.2.2肝生化指标异常例数 18项研究报道了丙硫氧嘧啶组和甲巯咪唑组ALT异常例数,13项研究报道了AST异常例数,14项研究报道了ALP异常例数,18项研究报道了T-BiL异常例数。Meta分析结果表明,丙硫氧嘧啶组肝生化指标出现异常的例数高于甲巯咪唑组,结果见表2。
2.2.3ALT变化值 4项研究[22,27,30,35]报道了丙硫氧嘧啶组和甲巯咪唑组治疗前后ALT水平。异质性检验显示,各研究间统计学差异较小(P=0.53,I2=0%),采用固定效应模型进行分析。森林图结果显示,丙硫氧嘧啶组ALT值升高更明显[SMD=0.68,95%CI(0.46,0.90),P<0.000 01](图2)。
2.2.4AST变化值 4项研究[22,27,30,35]报道了丙硫氧嘧啶组和甲巯咪唑组治疗前后AST水平。异质性检验显示,各研究间统计学差异较小(P=0.85,I2=0%),采用固定效应模型进行分析。森林图结果显示,丙硫氧嘧啶组AST值升高更明显[SMD=0.38,95%CI(0.17,0.59),P=0.0005](图3)。
表1 纳入研究的信息和质量评价结果

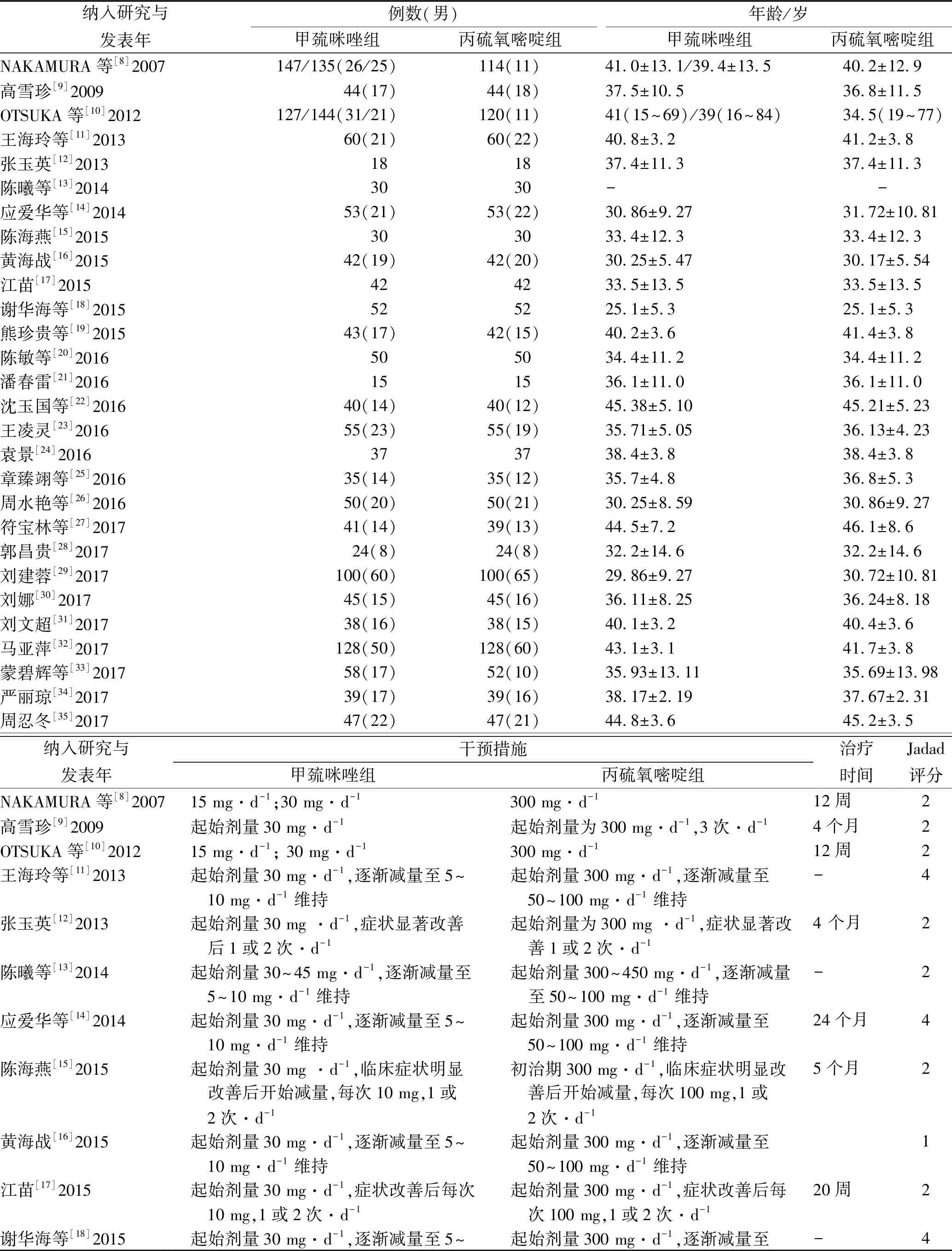
纳入研究与发表年例数(男)甲巯咪唑组丙硫氧嘧啶组年龄/岁甲巯咪唑组丙硫氧嘧啶组NAKAMURA等[8]2007147/135(26/25)114(11)41.0±13.1/39.4±13.540.2±12.9高雪珍[9]200944(17)44(18)37.5±10.536.8±11.5OTSUKA等[10]2012127/144(31/21)120(11)41(15~69)/39(16~84)34.5(19~77)王海玲等[11]201360(21)60(22)40.8±3.241.2±3.8张玉英[12]2013181837.4±11.337.4±11.3陈曦等[13]20143030--应爱华等[14]201453(21)53(22)30.86±9.2731.72±10.81陈海燕[15]2015303033.4±12.333.4±12.3黄海战[16]201542(19)42(20)30.25±5.4730.17±5.54江苗[17]2015424233.5±13.533.5±13.5谢华海等[18]2015525225.1±5.325.1±5.3熊珍贵等[19]201543(17)42(15)40.2±3.641.4±3.8陈敏等[20]2016505034.4±11.234.4±11.2潘春雷[21]2016151536.1±11.036.1±11.0沈玉国等[22]201640(14)40(12)45.38±5.1045.21±5.23王凌灵[23]201655(23)55(19)35.71±5.0536.13±4.23袁景[24]2016373738.4±3.838.4±3.8章臻翊等[25]201635(14)35(12)35.7±4.836.8±5.3周水艳等[26]201650(20)50(21)30.25±8.5930.86±9.27符宝林等[27]201741(14)39(13)44.5±7.246.1±8.6郭昌贵[28]201724(8)24(8)32.2±14.632.2±14.6刘建蓉[29]2017100(60)100(65)29.86±9.2730.72±10.81刘娜[30]201745(15)45(16)36.11±8.2536.24±8.18刘文超[31]201738(16)38(15)40.1±3.240.4±3.6马亚萍[32]2017128(50)128(60)43.1±3.141.7±3.8蒙碧辉等[33]201758(17)52(10)35.93±13.1135.69±13.98严丽琼[34]201739(17)39(16)38.17±2.1937.67±2.31周忍冬[35]201747(22)47(21)44.8±3.645.2±3.5纳入研究与发表年干预措施甲巯咪唑组丙硫氧嘧啶组治疗时间Jadad评分NAKAMURA等[8]200715 mg·d-1;30 mg·d-1300 mg·d-112周2高雪珍[9]2009起始剂量30 mg·d-1起始剂量为300 mg·d-1,3次·d-14个月2OTSUKA等[10]201215 mg·d-1; 30 mg·d-1300 mg·d-112周2王海玲等[11]2013起始剂量30 mg·d-1,逐渐减量至5~起始剂量300 mg·d-1,逐渐减量至-4 10 mg·d-1维持 50~100 mg·d-1维持张玉英[12]2013起始剂量30 mg ·d-1,症状显著改善起始剂量为300 mg ·d-1,症状显著改4 个月2 后1或2次·d-1 善1或2次·d-1陈曦等[13]2014起始剂量30~45 mg·d-1,逐渐减量至起始剂量300~450 mg·d-1,逐渐减量-2 5~10 mg·d-1维持 至50~100 mg·d-1维持应爱华等[14]2014起始剂量30 mg·d-1,逐渐减量至5~起始剂量300 mg·d-1,逐渐减量至24个月4 10 mg·d-1维持 50~100 mg·d-1维持陈海燕[15]2015起始剂量30 mg ·d-1,临床症状明显初治期300 mg·d-1,临床症状明显改5个月2 改善后开始减量,每次10 mg,1或 善后开始减量,每次100 mg,1或 2次·d-1 2次·d-1黄海战[16]2015起始剂量30 mg·d-1,逐渐减量至5~起始剂量300 mg·d-1,逐渐减量至1 10 mg·d-1维持 50~100 mg·d-1维持江苗[17]2015起始剂量30 mg·d-1,症状改善后每次起始剂量300 mg·d-1,症状改善后每20周2 10 mg,1或2次·d-1 次100 mg,1或2次·d-1谢华海等[18]2015起始剂量30 mg·d-1,逐渐减量至5~起始剂量300 mg·d-1,逐渐减量至-4
续表1 纳入研究的信息和质量评价结果
Tab.1Informationandqualityassessmentoftheincludedstudies


纳入研究与发表年干预措施甲巯咪唑组丙硫氧嘧啶组治疗时间Jadad评分 10 mg·d-1维持 50~100 mg·d-1维持熊珍贵等[19]2015起始剂量30 mg·d-1,逐渐减量至5~起始剂量300 mg·d-1,逐渐减量至-4 10 mg·d-1维持 50~100 mg·d-1维持陈敏等[20]2016起始剂量30 mg·d-1,逐渐减量至5~起始剂量300 mg·d-1,逐渐减量至6个月1 10 mg·d-1维持 50~100 mg·d-1维持潘春雷[21]2016起始剂量30 mg ·d-1,症状改善后每起始剂量300 mg·d-1,症状改善后每4个月2 次10 mg,1或2次·d-1 次100 mg,1或2次·d-1沈玉国等[22]2016起始剂量30 mg·d-1,逐渐减量至5~起始剂量300 mg·d-1,逐渐减量至12个月4 10 mg·d-1维持 50~100 mg·d-1维持王凌灵[23]2016起始剂量30 mg·d-1,逐渐减量至5~起始剂量300 mg·d-1,逐渐减量至-4 10 mg·d-1维持 50~100 mg·d-1维持袁景[24]2016起始剂量30~45 mg·d-1,症状好转后起始剂量300~450 mg·d-1,症状好转12个月4 5~10 mg·d-1维持 后50~100 mg·d-1维持章臻翊等[25]201630 mg·d-1,3次·d-1300 mg·d-1,3次·d-1-2周水艳等[26]2016起始剂量30 mg·d-1,逐渐减量至5~起始剂量300 mg·d-1,逐渐减量至24个月4 10 mg·d-1维持 50~100 mg·d-1维持符宝林等[27]2017起始剂量30 mg·d-1,逐渐减量至5~起始剂量300 mg·d-1,逐渐减量至12个月4 10 mg·d-1维持 50~150 mg·d-1维持郭昌贵[28]2017起始剂量 30 mg·d-1,症状改善后起始剂量300 mg·d-1,患者症状改善4个月2 20 mg,2次·d-1 后为100 mg,2次·d-1刘建蓉[29]2017起始剂量30 mg·d-1,逐渐减量至5~起始剂量300 mg·d-1,逐渐减量至24个月2 10 mg·d-1维持 50~100 mg·d-1维持刘娜[30]2017起始剂量30 mg·d-1,逐渐减量至5~起始剂量250 mg·d-1,逐渐减量至12个月2 10 mg·d-1维持 90 mg·d-1维持刘文超[31]2017起始剂量30 mg·d-1,逐渐减量至5~起始剂量300 mg·d-1,逐渐减量至-2 10 mg·d-1维持 50~100 mg·d-1维持马亚萍[32]2017起始剂量30 mg·d-1,逐渐减量至5~起始剂量300 mg·d-1,逐渐减量至2 10 mg·d-1维持 50~100 mg·d-1维持蒙碧辉等[33]2017起始剂量分别为15,20,30 mg,逐渐减起始剂量分别为150,200,300 mg,逐渐12周4 量至5~15 mg·d-1维持 减量至50~150 mg·d-1维持严丽琼[34]2017起始剂量30 mg·d-1,症状好转后5~起始剂量300 mg·d-1,症状好转后-2 10 mg维持 50~100 mg维持周忍冬[35]2017起始剂量30 mg·d-1,逐渐减量至5~起始剂量300 mg·d-1,逐渐减量至12个月2 10 mg·d-1维持 50~100 mg·d-1维持
2.2.5ALP变化值 3项研究[22,30,35]报道了丙硫氧嘧啶组和甲巯咪唑组治疗前后ALP水平。异质性检验显示,各研究间统计学差异较小(P=0.90,I2=0%),采用固定效应模型进行分析。森林图结果显示,丙硫氧嘧啶组ALP值升高更明显[SMD=0.47,95%CI(0.23,0.72),P=0.0002](图4)。
2.2.6T-BiL变化值 3项研究[22,30,35]报道了甲亢患者使用丙硫氧嘧啶和甲巯咪唑治疗前后T-BiL水平。异质性检验显示,各研究间统计学差异较小(P=0.45,I2=0%),采用固定效应模型进行分析。森林图结果显示,丙硫氧嘧啶组T-BiL值升高更明显[SMD=0.70,95%CI(0.45,0.95),P<0.000 01](图5)。
2.3发表偏倚 以肝损伤例数为指标,绘制倒漏斗图进行发表偏倚分析。倒漏斗图以各研究的RR值为横坐标、SE(log[RR])为纵坐标。结果显示,各研究散点左右分布大致对称,似倒漏斗状,因此本研究的发表偏倚较小(图6)。

图1 丙硫氧嘧啶组和甲巯咪唑组肝损伤例数森林图

指标纳入研究个数丙硫氧嘧啶组异常例数总例数甲巯咪唑组异常例数总例数异质性检验I2值/%RR(95%CI)PALT异常例数18[9,11-17,19,21-24,26,28,29,31,34]1637593376004.83(3.39,6.88)<0.000 01AST异常例数13[11,13-15,17,19,22-24,26,29,31,34]696161861703.62(2.24,5.84)<0.000 01ALP异常例数14[9,11,12,14,16,19,21-23,26,28,29,31,34]316201362102.24(1.22,4.13)0.009T-BiL异常例数18[9,11-17,19,21-24,26,28,29,31,34]5475934760351.51(1.02,2.22)0.04

图2 丙硫氧嘧啶组和甲巯咪唑组ALT变化值森林图

图3 丙硫氧嘧啶组和甲巯咪唑组AST变化值森林图

图4 丙硫氧嘧啶组和甲巯咪唑组ALP变化值森林图

图5 丙硫氧嘧啶组和甲巯咪唑组T-BiL变化值森林图

图6 肝损伤例数倒漏斗图
Fig.6Invertedfunnelplotofthenumberofpatientswithliverinjury
3 讨论
笔者在本研究中以肝损伤例数、肝生化指标异常例数以及治疗前后肝生化指标的变化值等为结局指标,对甲巯咪唑和丙硫氧嘧啶致肝功能损伤的情况进行分析。Meta分析结果表明,丙硫氧嘧啶所致肝损伤的风险高于甲巯咪唑。此外,有两项大型回顾性研究也进行了相关报道,但因纳入患者的基本情况差异较大,仅对其进行描述性分析。WANG等[3]研究结果显示,使用甲巯咪唑的34 361例患者中有122例发生肝损伤,使用丙硫氧嘧啶的24 941例患者有37例发生肝损伤。YANG等[36]报道中国某医院13年间90例因使用抗甲状腺药物出现重度肝损伤的患者,其中使用甲巯咪唑51例,使用丙硫氧嘧啶39例。这两项研究证据表明,丙硫氧嘧啶并不比甲巯咪唑更容易产生肝毒性,可能与纳入患者均为亚洲人群有关,尚需更多研究证据来证明。
本研究的局限性在于,纳入文献的质量不高,大多为中文文献,且未对患者的肝损伤程度做亚组分析,大多数患者为轻中度肝损伤,少数为重度肝损伤,也未对肝损伤类型做区分。本次纳入研究的患者使用甲巯咪唑和丙硫氧嘧啶的比例大致为1:1,与其在临床上的实际应用情况有偏差,且未考虑性别因素的影响。
本研究结果提示,丙硫氧嘧啶较甲巯咪唑更易诱发肝损伤,但两者发生肝损伤的程度均较轻。甲巯咪唑和丙硫氧嘧啶致肝损伤的机制尚未完全明确。研究表明,反应代谢物的形成和免疫介导的毒性作用是导致肝损伤的主要机制[37]。鉴于抗甲状腺药物的肝毒性,建议对使用抗甲状腺药物患者的肝功能进行定期监测,转氨酶或胆红素显著升高时可停药,以避免肝损伤进一步加重,必要时还可加用保肝利胆药[38],同时也提示肝功能异常甲亢患者在选用抗甲状腺治疗药物时需谨慎。
