果胶多糖水热法降解及其产物体外抗氧化性评价
2019-07-05姜美云赖晨欢范一民
姜美云,唐 硕,王 婷,赖晨欢,范一民,勇 强,*
(1.南京林业大学 林业资源高效加工利用协同创新中心,江苏 南京 210037;2.南京林业大学化学工程学院,江苏 南京 210037)
果胶是一种天然大分子酸性多糖,分子质量介于10~400 kDa之间,主要由半乳糖醛酸聚糖(homogalacturonan,HG)、鼠李半乳糖醛酸聚糖-I(rhamnogalacturonans I,RG-I)和鼠李半乳糖醛酸聚糖-II(rhamnogalacturonans II,RG-II)组成[1]。其中,HG主要是由D-半乳糖醛酸通过α-1,4糖苷键连接而成,且半乳糖醛酸残基易被乙酰化和甲酯化。RG-I主链是由鼠李糖和半乳糖醛酸交替组成的重复单位,并带有中性糖基侧链。RG-II主链为聚半乳糖醛酸,侧链含有4 种结构复杂的寡糖[2]。由于果胶结构复杂,分子质量大,溶解性差,导致其生物利用率低,限制了其生物活性的发挥。为提高果胶多糖的生物活性,降低果胶多糖分子质量可显著改善其生物活性和生物利用率[3]。目前,果胶多糖降解产物作为稳定剂、增稠剂、凝胶剂和抗氧化剂广泛应用于食品、化妆品、医药等行业[4-6]。因此,近年来果胶多糖限制性水解技术成为果胶多糖高值化利用的研究热点之一。
目前果胶多糖限制性水解的方法主要包括酶水解[7-8]、酸水解[9-11]和水热法[12-13]。酶水解法虽然条件温和,反应专一性高,但由于果胶结构复杂,导致酶法限制性水解果胶所需的果胶酶种类繁多,且成本高,不利于工业化生产。酸水解法条件剧烈,水解程度不易控制,水解产物中单糖含量较高,且半乳糖醛酸容易形成内酯[14],降低了果胶多糖的限制性水解效率。水热法是一种环保清洁的限制性水解方法,由于在水解过程中不添加外源酸,避免了设备腐蚀和环境污染等问题,利于工业化放大生产。在果胶多糖的水热法限制性水解过程中,果胶多糖中的部分酸性糖基以及乙酰基脱落,释放酸性糖和乙酸,从而作为水热过程中的弱酸催化剂,催化果胶多糖的限制性水解[15]。目前,水热法已经成功应用于多种多糖的限制性水解[16-18]。Miyazawa等[17]报道了以聚半乳糖醛酸为原料,通过水热法降解得到聚合度为2~10的低聚物;Saravana等[18]采用水热法降解制备低分子质量的褐藻糖胶,并发现水热降解后的褐藻糖胶抗氧化性、抗菌性、抗凝活性等生物活性提高。但果胶多糖的水热法可控降解报道较少。
本实验以商品果胶多糖为原料,采用水热法降解果胶多糖。通过单因素试验和正交试验考察水热处理温度、水热处理时间、pH值等因素对果胶多糖降解产物得率的影响;采用乙醇分级沉淀的方法分离制备出不同分子质量的果胶多糖降解产物,并通过化学抗氧化法评价其体外抗氧化性。研究结果可为制备不同分子质量的果胶多糖降解产物和开拓活性果胶多糖降解产物的应用提供理论依据。
1 材料与方法
1.1 材料与试剂
商品果胶 上海麦克林生化科技有限公司;半乳糖醛酸等单糖标准样品 美国Sigma-Aldrich公司;其他试剂均为分析纯 国药集团化学试剂有限公司。
1.2 仪器与设备
ICS-3000型高效液相离子交换色谱仪(配有脉冲安培检测器) 美国戴安公司;1200型高效液相色谱仪(配有示差检测器) 美国Agilent公司;油浴蒸煮罐35 mL。
1.3 方法
1.3.1 商品果胶的成分分析
1.3.1.1 糖基组成的测定
采用高效液相离子交换色谱法测定果胶多糖及其降解产物的糖基组成[19]。操作如下:称取10 mg绝干质量商品果胶或经冷冻干燥处理的果胶多糖降解产物于5 mL水解瓶中,加入2 mL去离子水,每10 min摇匀一次。待果胶充分溶解后,加入2 mL质量分数8%的硫酸溶液并置于高温灭菌锅中于121 ℃反应60 min。反应结束后,加入0.16 mL质量分数50%的NaOH溶液进行中和,并梯度稀释到100 倍,采用DINOXICS-3000型高效液相离子交换色谱仪进行定量分析(CarboPac PA10色谱柱和脉冲安培检测器)。其中,葡萄糖、半乳糖、阿拉伯糖和木糖的分析条件为:柱温30 ℃,流动相200 mmol/L NaOH,流速0.2 mL/min,进样量10 μL;鼠李糖和半乳糖醛酸的分析条件为:柱温30 ℃,流动相200 mmol/L NaOH和500 mmol/L CH3COONa,流速0.3 mL/min,进样量10 μL。
1.3.1.2 酯化度的测定
采用化学滴定法对果胶酯化度进行测定[20]。操作如下:称取0.5 g绝干质量果胶于烧杯中,分别加入95%乙醇溶液5.0 mL、氯化钠1.0 g、去离子水100 mL和酚酞试剂3 滴,充分摇匀至果胶溶解。采用0.1 mol/L NaOH溶液进行滴定直至体系变色,并记录消耗量(记为VA);然后,加入0.3 mol/L NaOH溶液25 mL,充分混合并静置30 min,随后加入0.3 mol/L盐酸溶液25 mL并充分摇匀,最后用0.1 mol/L NaOH溶液滴定直至体系颜色变为红色,并记录消耗量(记为VB)。果胶酯化度按公式(1)计算:
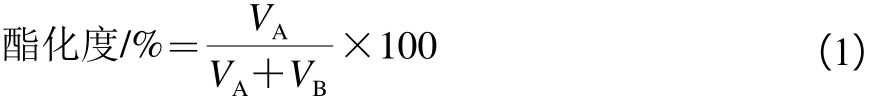
1.3.1.3 果胶多糖相对分子质量的测定
采用凝胶渗透色谱测定商品果胶及其水热降解产物的分子质量[21-22]。操作条件如下:Agilent 1200型高效液相色谱仪,Ultrahydrogel 120和Ultrahydrogel 250串联,柱温55 ℃,流动相0.6 mol/L KH2PO4溶液,流速0.6 mL/min,进样量10 μL,检测器为示差折光检测器。
1.3.2 水热法降解果胶多糖条件优化试验设计
1.3.2.1 单因素试验
于35 mL的油浴蒸煮罐中,加入25 mL料液比为1∶25(g/mL)的初始商品果胶,分别于不同水热处理条件下(水热处理温度分别为100、120、140、160 ℃和180 ℃,水热处理时间分别为5、20、35、50 min和65 min,pH值分别为2、4、6、8、10和12)进行果胶限制性水解反应,以研究水热处理温度、水热处理时间、pH值对果胶多糖降解产物得率的影响。
1.3.2.2 正交试验
在单因素试验结果的基础上,以商品果胶多糖降解产物得率为考察指标,选取水热处理温度、水热处理时间、pH值进行3因素3水平L9(33)正交试验,以确定水热法降解果胶多糖的最佳工艺条件,见表1。

表1 正交试验因素与水平Table 1 Code and level of independent variables used for orthogonal array design
1.3.3 果胶多糖降解产物得率的计算
为避免未水解果胶多糖对果胶多糖降解产物得率计算的影响,采用乙醇沉淀法[23]对果胶水热处理液进行预处理,操作如下:于商品果胶水热处理液中添加乙醇至乙醇终体积分数为20%,充分混匀后静置离心,以去除未水解的果胶多糖沉淀。果胶多糖降解产物仍溶解于上清液中,为计算果胶多糖降解产物得率,取10 mL的上清液,蒸发除去乙醇后加水定容至原体积。取5 mL上述样品溶液,加入5 mL质量分数8%硫酸于121 ℃反应1 h后,利用高效液相离子色谱测定酸解前后半乳糖醛酸的含量。果胶多糖降解产物得率和单糖得率(游离的半乳糖醛酸)按公式(2)、(3)计算:

式中:Ca为上清液酸解后半乳糖醛酸质量浓度/(g/L);Cb为上清液酸解前半乳糖醛酸质量浓度/(g/L);Cg为商品果胶酸解后半乳糖醛酸质量浓度/(g/L)。
1.3.4 不同分子质量果胶多糖降解产物的乙醇分级分离
将商品果胶于140 ℃和pH 6的条件下进行水热降解30 min,所得水热处理液用于不同分子质量果胶多糖降解产物的乙醇分级分离。当体系中乙醇溶液体积分数分别为50%、60%和70%时,离心分离所得沉淀经冷冻干燥、称质量计量后,分别标记为组分S1、S2、S3,并对各组分的分子质量和糖基组成进行测定。具体操作过程如图1所示。

图1 水热处理液经乙醇分级沉淀获得S1、S2和S3组分的操作步骤示意图Fig. 1 Flow chart of the ethanol fractionation of the hydrothermal hydrolsate
1.3.5 果胶多糖降解产物体外抗氧化性的测定
1.3.5.1 1,1-二苯基-2-三硝基苯肼(1,1-dipheny1-2-picryl-hydrazyl,DPPH)自由基清除能力的测定
于15 mL试管中依次加入2 mL不同质量浓度(0.5、1.0、1.5、2.0、2.5、3.0 g/L)的多糖溶液,加入2 mL DPPH溶液(0.2 mmol/L,溶于80%乙醇溶液中),混匀后在室温下避光反应30 min,于517 nm波长处测定吸光度,记为A0[24]。对照组为不同质量浓度多糖样品2 mL,分别加入2 mL无水乙醇,在517 nm波长处测定吸光度,记为A1。空白组为2 mL无水乙醇,加入2 mL DPPH溶液,在517 nm波长处测定吸光度,记为A2。以相同质量浓度的VC做阳性对照,每个样品重复实验2 次。DPPH自由基清除率按公式(4)计算:
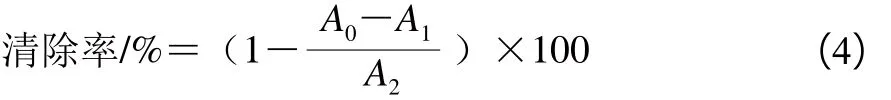
1.3.5.2 超氧阴离子自由基清除能力的测定
利用邻苯三酚的自氧化方法检测多糖对超氧阴离子自由基的清除作用。于15 mL试管中依次加入1 mL不同质量浓度(0.5、1.0、1.5、2.0、2.5、3.0 g/L)的多糖溶液,加入4.5 mL 0.05 mol/L(pH 8.2)的Tris-HCl缓冲液,然后在25 ℃水浴中预热20 min。取0.5 mL预热好的45 mmol/L邻苯三酚,加入到样品中,迅速混匀,5 min内于325 nm波长处测定吸光度,记为A0[25]。用蒸馏水代替邻苯三酚时测得的吸光度记为A1。空白组以蒸馏水代替多糖样品,吸光度记为A2。以相同质量浓度的VC做阳性对照,每个样品重复实验2 次。超氧阴离子自由基清除率按公式(5)计算:

1.4 数据统计分析
实验重复3 次,结果以 ±s表示,采用Excel软件对数据进行整理、Origin Pro 2017软件作图。采用SPSS 20.0软件对数据进行显著性分析和方差分析,P<0.05,差异显著。
2 结果与分析
2.1 商品果胶糖基成分分析
为分析果胶多糖中的糖基组成,本实验中采用高效液相离子交换色谱法分析商品果胶多糖完全水解产物,结果如表2所示。

表2 商品果胶的糖基组成分析Table 2 Glycosyl composition analysis of commercial pectin
由表2可知,商品果胶的主要成分是酸性糖半乳糖醛酸基,占果胶多糖干基的62.10%;中性糖基总质量分数为22.29%,包括葡萄糖基、半乳糖基、木糖基、鼠李糖基和阿拉伯糖基。Wang Xin等[26]报道了商品苹果果胶糖基组成,其中半乳糖醛酸质量分数为66.00%,中性糖质量分数为11.50%,与本实验中商品果胶的糖基组成基本一致。
2.2 水热法降解果胶多糖单因素试验结果
2.2.1 水热处理温度对果胶多糖降解产物得率的影响
在商品果胶料液比1∶25(g/mL)、pH 2.6(果胶溶液自然pH值)、水热处理35 min条件下,分别考察水热处理温度(100、120、140、160 ℃和180 ℃)对果胶多糖降解产物得率的影响,结果如图2所示。

图2 水热处理温度对果胶多糖降解产物得率的影响Fig. 2 Effect of hydrothermal treatment temperature on the degradation efficiency of pectic polysaccharide
由图2可知,当水热预处理温度在100~140 ℃范围内,随着温度的升高,果胶多糖降解产物得率呈现不断上升的趋势,由16.7%提高至42.0%,单糖得率从0.4%提高到5.5%。而当温度从140 ℃升高至180 ℃时,果胶多糖降解产物得率急剧下降,从42.0%下降至0.4%;而单糖得率呈现先上升后降低的趋势,并在160 ℃时,单糖得率达到最高(6.5%)。这可能是由于在较高的水热处理强度(140~160 ℃)下,部分果胶多糖彻底降解为单糖,使得单糖得率提高;而当水热处理温度进一步升高至180 ℃时,单糖得率急剧下降至0.1%,这是由于过高的预处理温度使得单糖进一步降解产生糠醛等衍生物[27];此外,半乳糖醛酸易形成内酯结构,导致糖得率显著下降[14]。Martínez等[28]报道了以橘皮废液为原料的水热法制备果胶多糖,其水热条件优化结果表明,水热处理最适温度同样为140 ℃。因此果胶多糖水热法降解的适宜温度为140 ℃左右。
2.2.2 水热处理时间对果胶多糖降解产物得率的影响
在商品果胶料液比1∶25(g/mL)、pH 2.6(果胶溶液自然pH值)、水热处理温度140 ℃条件下,分别考察水热处理时间(5、20、35、50、65 min)对果胶多糖降解产物得率的影响,结果如图3所示。
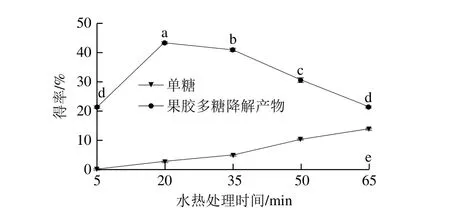
图3 水热处理时间对果胶多糖降解产物得率的影响Fig. 3 Effect of hydrothermal treatment time on the degradation efficiency of pectic polysaccharide
由图3可知,当水热处理时间由5 min延长至20 min时,果胶多糖降解产物得率由21.5%提高至43.3%;与此同时,单糖得率由0.3%增加至3.0%。然而,进一步延长水热处理时间至65 min时,果胶多糖降解产物得率呈现不断下降的趋势,由43.3%下降至21.7%;单糖得率却呈现不断上升的趋势,由3.0%提高至13.8%,说明水热处理时间过长易导致果胶多糖限制性降解产物进一步水解为单糖,从而降低果胶多糖降解产物得率。因此选择果胶多糖水热法降解的适宜时间为20 min左右。
2.2.3 pH值对果胶多糖降解产物得率的影响
在商品果胶料液比1∶25(g/mL)、水热处理温度140 ℃、水热处理20 min条件下,考察pH值(2、4、6、8、10、12)对果胶多糖降解产物得率的影响,结果如图4所示。
由图4所示,若控制pH值在2~12时,果胶多糖降解产物得率和单糖得率无明显变化,果胶多糖降解产物得率维持在41.1%~42.5%范围内,单糖得率维持在5.9%~7.5%范围内。说明水热处理的pH值对果胶多糖降解产物得率和单糖得率无显著影响。此外,实验结果表明,当水热处理pH值为2~12时,水热处理30 min后,体系的pH值均处于2.1~2.8。这说明在140 ℃水热处理过程中,果胶多糖的乙酰基和半乳糖醛酸基大量脱落[15],使整个处理体系的pH值急剧降低,从而削弱了pH值对果胶多糖降解得率的影响。
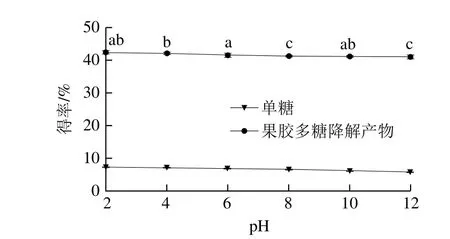
图4 pH值对果胶多糖降解产物得率的影响Fig. 4 Effect of pH on the degradation efficiency of pectic polysaccharide
2.3 水热降解法正交试验结果

表3 果胶多糖降解L9(33)的正交试验结果Table 3 Orthogonal array design L9 (33) with experimental results
按照正交试验优化得到的最佳工艺条件(表3),即水热处理温度140 ℃、水热处理时间30 min、pH 6,重复3 次平行实验进行验证,果胶多糖得率分别为45.8%、46.3%、46.5%,平均得率为46.2%,表明该方法稳定可靠。由表4可知,对果胶多糖降解得率的影响:水热处理温度>水热处理时间>pH值。
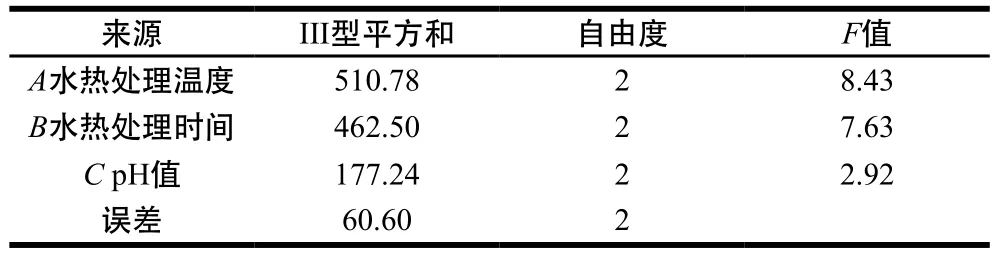
表4 方差分析与显著性分析结果Table 4 Analysis of variance of regression equation and significance test
2.4 不同分子质量范围果胶多糖降解产物的分离
采用乙醇分级沉淀法,将商品果胶多糖水热降解产物进行分离,分别于乙醇体积分数为50%、60%和70%下获得果胶多糖降解产物S1、S2和S3三个组分。采用凝胶排阻色谱分析商品果胶多糖和3 种果胶多糖降解产物的分子质量分布,结果如图5所示。
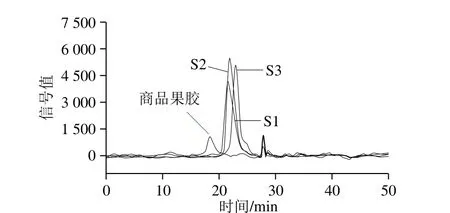
图5 果胶多糖活性降解产物中S1、S2和S3组分的分子质量分布Fig. 5 Molecular mass distribution of S1, S2 and S3
由图5可知,3 种果胶多糖降解产物的信号峰呈现典型的正态分布,表明此3 种组分经乙醇分级分离后分子质量相对均一。此外,经GPC Addon软件分析结果表明,随着乙醇体积分数逐渐增加,其沉淀分离所得的果胶多糖降解产物分子质量逐渐降低(表5)。与商品果胶相比,果胶多糖经过水热法降解后,分子质量大大降低。

表5 不同分子质量果胶多糖的性质分析Table 5 Properties of degradation products of pectic polysaccharide with different molecular masses
在此基础上,采用高效液相离子交换色谱法分析3 种果胶多糖降解产物的糖基组成,结果如表5所示。经乙醇分级沉淀技术分离制备的3 种组分S1、S2、S3糖基组成与商品果胶的糖基组成基本相似。并且这3 种降解产物占水热总糖的质量百分比分别为37.8%、19.2%和41.3%。综上所述,采用乙醇分级沉淀技术可实现果胶多糖降解产物的有效分离与制备,并通过高效液相离子交换色谱法分析还可实现不同分子质量果胶多糖降解产物的定量分析,为不同分子质量范围果胶多糖降解产物的抗氧化性研究提供技术支持。
2.5 不同分子质量果胶多糖降解产物的抗氧化活性
2.5.1 DPPH自由基清除能力
如图6所示,果胶多糖对DPPH自由基的清除能力与其聚合度和质量浓度的大小有关。当质量浓度为0.5~3.0 g/L时,商品果胶对DPPH自由基的清除率均低于15.0%;而果胶多糖降解产物S1、S2和S3组分对DPPH自由基的清除能力随质量浓度的增大而显著增强。当果胶多糖降解产物质量浓度为3.0 g/L时,S1、S2和S3组分的DPPH自由基清除率分别达49.8%、45.1%和39.8%,分别是商品果胶清除率的4.0、3.6 倍和3.2 倍。这一研究结果与李健军[29]的研究结果一致。综上所述,采用水热法降解果胶多糖可显著提高其清除DPPH自由基的能力。
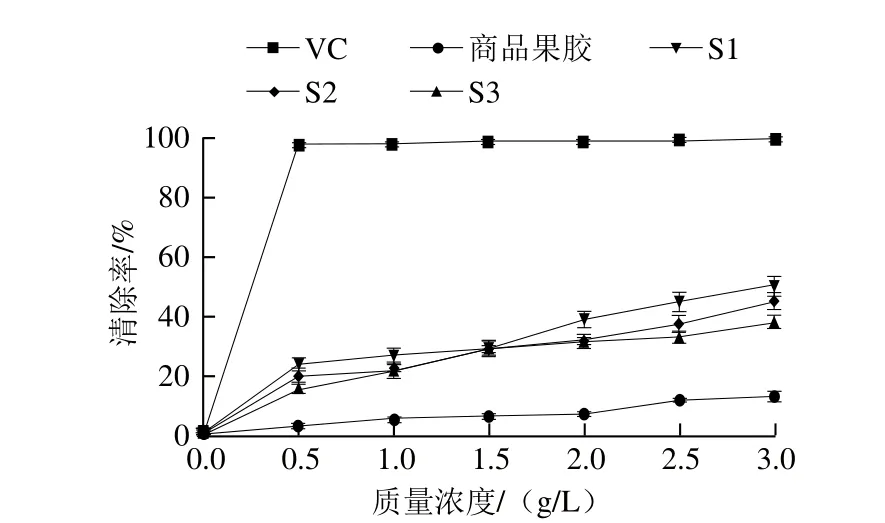
图6 不同分子质量的果胶多糖降解产物对DPPH自由基的清除作用Fig. 6 DPPH radical scavenging effects of peptic oligosaccharides with different molecular masses on
2.5.2 超氧阴离子自由基清除能力

图7 不同分子质量的果胶多糖降解产物对超氧阴离子自由基的清除作用Fig. 7 Superoxide anion scavenging effects of pectic oligosaccharides with different molecular masses
如图7所示,商品果胶与其水热降解产物均具有清除超氧阴离子自由基的能力。在质量浓度0.5~3.0 g/L范围内,随着质量浓度的不断增大,商品果胶超氧阴离子自由基清除率从69.2%下降到5.5%。S1、S2、S3组分对超氧阴离子自由基的清除能力随分子质量的增大而减小,可能是因为商品果胶和各组分随着质量浓度的提高,增加了邻苯三酚的氧化速率,从而提供了更多的超氧阴离子,但S1、S2、S3组分下降速率缓慢,因此清除能力均高于商品果胶。当质量浓度为3.0 g/L时,S3组分清除率可达到58.7%,是商品果胶超氧阴离子自由基清除能力的10 倍,这一研究结果与郝杰等[30]的研究结果一致。综上所述,水热法降解果胶多糖显著提高了其对超氧阴离子自由基的清除能力。
3 结 论
采用水热法对果胶多糖进行限制性水解,通过单因素试验和正交试验,确定水热法降解果胶多糖的最佳工艺条件为:水热处理温度140 ℃、水热处理时间30 min、pH 6;在此条件下,果胶多糖降解产物得率最高为46.2%。
通过乙醇分级沉淀可实现果胶多糖降解产物的有效分离,分别获得重均分子质量为13.4、7.5 kDa和5.7 kDa的3 个果胶多糖降解产物组分。在此基础上,通过高效液相离子交换色谱法分析可实现不同分子质量果胶多糖降解产物的定量分析。
抗氧化活性研究表明,果胶多糖降解产物对DPPH自由基和超氧阴离子自由基的清除能力显著高于商品果胶。其中,S1组分对DPPH自由基的清除能力最强,清除率可达到49.8%,是商品果胶多糖清除率的4 倍;在质量浓度0.5~3 g/L范围内,与商品果胶和S1、S2组分相比,S3组分对超氧阴离子自由基的清除能力最强。由此可见,水热降解有效提高了果胶多糖对DPPH自由基和超氧阴离子自由基的清除能力。
