慎选卤代烃消去反应实验代表物
2019-07-02刘怀乐
刘怀乐

摘要: 理论上,溴乙烷与强碱(NaOH或KOH)的乙醇溶液共热,溴乙烷会发生消去反应生成乙烯。有数据表明,1-溴丙烷的沸点比溴乙烷的沸点高;1-溴丙烷比溴乙烷更容易发生消去反应。现行人教版高中《有机化学基础》教材中,把1-溴丙烷改换成溴乙烷,以及由它所提供的实验方案,经实验证明,该方案在教学上不具有可操作性。
关键词: 溴乙烷; 1-溴丙烷; 乙烯; 消去反应; 酸性KMnO4溶液
文章编号: 1005-6629(2019)5-0093-04 中图分类号: G633.8 文献标识码: B
近10多年来,教学同仁关于溴乙烷发生消去反应的实验探索,曾经发出过很多的议论。新近的一位探索者说[1]:“溴乙烷消去反应实验是中学化学教学中的一个重要实验,但又是一个很难做成功的实验。”笔者很有同感,也是这个实验的长期探索者。下面是笔者对这个实验的若干次实验探究和评说,希望对大家会有些裨益。
1 一个没有理由可以回避的教学演示实验
现行人教版高中《有机化学基础》教材(选修5)第41页有:
如果将溴乙烷与强碱(NaOH或KOH)的乙醇溶液共热,溴乙烷会从分子中脱去HBr,生成乙烯。
CH2HCH2Br+NaOH乙醇CH2CH2↑+NaBr+H2O
教材还设计如下的实验探究(见图1): 有人设计了如教材图2-18所示的实验方案,用酸性高锰酸钾溶液是否褪色来检验生成的气体是乙烯,并思考以下两个问题。
(1) 为什么气体通入酸性KMnO4溶液前,要加一个盛水的试管?起什么作用?
(2) 除酸性KMnO4溶液外还可以用什么方法检验乙烯?此时还有必要将气体通入水中吗?
教材有如此具体的教学要求,图1所示的“气体”显然是乙烯,至于这种气体的制法如何,那是教师课堂教学时没有理由回避的教学演示实验。记得2016年重庆市高中化学教师示范教学竞赛展示课时,曾有10多位教师以溴乙烷发生消去反应为题进行比赛活动。参赛的结果表明,几乎所有参赛教师都没能把握好这个竞赛课的实验问题,不能自圆其说。
2 C2H5Br发生消去反应的理性分析
2.1 反应的溶剂因素
众所周知,卤代烷的取代反应与消去反应是一对互相竞争的反应。一般卤代烃在消去和取代的竞争中,强碱性的乙醇溶液,有利于消去反应的进行,而强碱性的水溶液,则有利于取代反应的进行。为使烯烃产量增加,常常用降低溶剂的极性(如用乙醇)的办法,以增加卤代烷在溶液中的溶解性(所有卤代烷都不溶于水)。这就是卤代烷发生消去反应时为什么要在强碱性的乙醇溶液中进行的原因。
2.2 影响消去反应的结构因素和温度因素
除了溶剂因素以外,影响卤代烷消去反应的因素还有温度、烷基的结构以及碱的强度[2]。 CH3CH2CH2Br与CH3CH2Br虽然同属一级卤代烷(伯卤代烷),根据扎伊采夫规则[3]: 含氢原子较少的那个相邻碳原子,比较容易失去它的氢原子。这就是从结构上讲CH3CH2CH2Br比CH3CH2Br更容易发生消去反应的原因。再加上温度因素,最终导致1-溴丙烷比溴乙烷更容易发生消去反应。
2.3 卤代烷的个体差异
尽管卤代烷在强碱的醇溶液中容易发生消去反应,但是个体因素差异很大。沸点较低的卤代烷不容易在热的碱性醇溶液中完成消去反应。如:
CH3CH2Cl 12.3℃
CH3CH2Br 38.4℃
CH3CH2CH2Cl 46.6℃
CH3CH2CH2Br 71.0℃
所以,卤代烷发生消去反应在试剂的选择上,选用沸点较高的CH3CH2CH2Br比CH3CH2Br要好。在热的强碱性乙醇溶液中,一方面C2H5Br加热时很难溶入,即使溶入了也会在未发生消去反应之前早已挥发逃逸殆尽了;另一方面,一般说来反应温度是由溶剂的沸点决定的,在回流条件下,温度是上不去的,只能停留在沸点38.4℃,使消去反应难以进行。因为结构相似的卤代烃,高温有利于消去,低温有利于取代。1-溴丙烷沸点较高(71.0℃),反应温度也相应提高,因此更容易发生消去反应。
3 酸性KMnO4溶液和Br2的CCl4溶液作为检验乙烯的试剂,值得审视
笔者设计了如下几个简单实验,其现象颇耐人寻味,值得一做。
(1) 在酸性或碱性KMnO4溶液中,分别滴入几滴酒精、溴乙烷,在不断振荡的条件下,可以观察到有缓慢褪色的现象;如果稍微加热,褪色现象会来得更快,更明显。只不过前者褪成无色,后者由紫色变成浅绿色(K2MnO4)[4]。
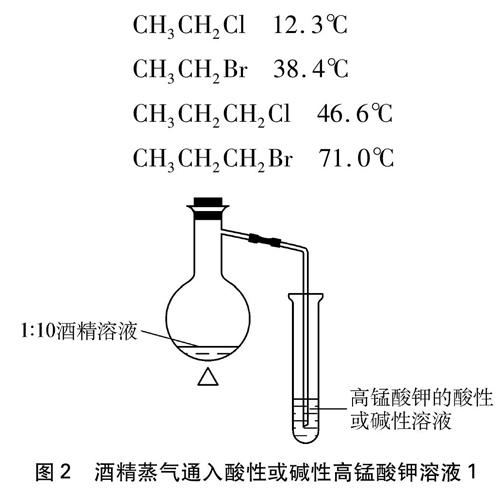
(2) 把1滴管酒精(约1mL)注入10mL水中,配成体积比约为1∶10的酒精溶液,振荡混匀,将这种稀的酒精溶液缓缓温热(见图2),当瓶内蒸气导入酸性KMnO4或碱性KMnO4溶液,也会看到有跟实验(1)所呈现的褪色和变色(紫→绿)现象。
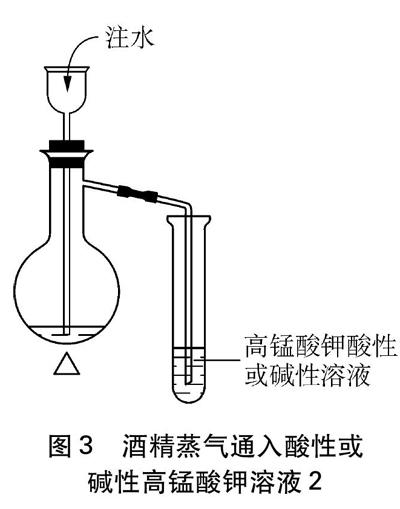
(3) 把用酒精浸淌过的烧瓶,按如图3所示装置,通过漏斗缓慢把水注入烧瓶,烧瓶中被排出的空气(含有酒精蒸气),也会使KMnO4的酸性溶液和KMnO4堿性溶液呈现与实验(1)相同的褪色和变色现象。
碱性高锰酸钾溶液2
(4) 具支试管里注入5mL水,再加入1滴管(约1mL)溴乙烷并放进50~60℃水浴烧杯中,一会可见导气管导出的溴乙烷聚集在试管底(油珠状),同时也会使酸性KMnO4溶液褪色(见图4)。
KMnO4溶液褪色
(5) 两个试管里,分别注入相同体积的浅黄色的Br2的CCl4溶液,用一个直角导管伸入其中一个试管的液面下,缓慢吹几口空气,观察Br2的CCl4溶液的颜色有什么变化(与另一个试管比较)。可见空气气流也会带走Br2的CCl4溶液中的Br2,呈现褪色的现象(见图5)。
4 值得思考和审视的几个问题
(1) 過去高中化学教材,只讲卤代烃的取代反应,没讲消去反应。自从高中化学使用(甲种本)以后的近40年间,增加了消去反应的内容。不过自2000年后的最近10多年中,卤代烷的消去反应,将1-溴丙烷改成了溴乙烷。教师的教学演示实验自然也改成了溴乙烷。问题是,教材何以要把容易发生消去反应的1-溴丙烷改换成不容易发生消去反应的溴乙烷呢?何以要把沸点较高的1-溴丙烷(沸点71.0℃),改换成沸点很低的溴乙烷(38.4℃)呢?
(2) 我们从许多科学家,大师、专家学者身上学习他们的科学思想和科学方法,即实事求是、科学严谨的思维和态度,平时体现在我们教学和实验中的东西还真不少,例如: 乙醇与浓H2SO4共热生成的气体中,使酸性KMnO4溶液褪色的不仅有C2H4,还有乙醇蒸气和SO2气体。把上述5个简单实验放在一起联想,本次溴乙烷的消去反应以及乙烯的检验的实验,用酸性高锰酸钾和溴水作为检验乙烯的试剂是否也值得审视呢?
其实,检验乙烯是不必用酸性高锰酸钾溶液的,因为氧化性太强,会有一定干扰。参照某些经典实验教材,检验乙烯的试剂是1%的高锰酸钾水溶液(即中性高锰酸钾稀溶液)或2%溴的CCl4溶液(即过去一般所说的溴水)。
(3) 教科书——教材是教师教学时必须遵循的“规矩”和“章法”,它们在法律上的合法性和在学术上的权威性,几乎是毋庸置疑的。正是鉴于此,我们不少教师把教材神化了,真理化了。认为书上所讲所做的实验都是绝对真实的,甚至把它固化奉为真理。有时真的是教材错了,也还以为是自己错了。以溴乙烷的消去反应实验为例,过去教材以1-溴丙烷为例讲消去反应,就很少有人去想那溴乙烷是否也会发生消去反应;当教材把1-溴丙烷改为溴乙烷时,就去猜想1-溴丙烷发生消去反应会有什么不恰当的问题(不然教材为什么要改呢)。当发现溴乙烷难以实现消去反应时,也不回头去想想这是不是教材在选材上有什么问题,即便全国数以万计的化学教师在照本宣科、不求甚解;即便有少数实验探究者在探究,甚至在不同的场合参与竞赛、演示、发表文章,最终几乎都以失败而告终。从某种角度讲这是教材编著者在选材上的一时疏漏所导致的结果,这难道不是我们教师以及教材编著者值得反思的吗?
(4) 无论是1-溴丙烷还是溴乙烷的消去反应,真正参与实验、实验后再思考、思考后发出质疑的人太少,究其原因,恐怕是实践者的科学精神有所欠缺。作为教师,既是知识的传播者,也应该是知识的生产者,更是当然的研究者。做研究工作有两点值得注意: 一是前人或今人都没有注意到的,但又确实值得研究的问题;二是前人或今人没有弄明白甚至没有去研究的问题。前者为发现问题,后者为解决问题。当然,对溴乙烷在热的强碱性乙醇溶液中,不是一点都没有发生消去反应,而是不宜把它取材作为演示实验,不然就会把卤代烃发生消去反应大大地泛化。当我们认清了溴乙烷如此的个性特征: 沸点仅有38.4℃时,于是一切都明白了。从这个角度讲,我们的实验探索精神,还是欠缺的。
(5) 至此,我们明白了学科教材内容的最大特点,不在乎它的高、尖、新,更多地在于它的继承性和教材内容选择上的合理性。对于卤代烷消去反应典型代表物教学实验的选择,我们教材的编著者们,似乎缺少点实际的参与和了解,竟放弃了曾经使用多年的1-溴丙烷,代之以不切实际的溴乙烷(沸点仅38.4℃),进而还在“科学探究”中进行不切实际的实验设计、检验乙烯、提出思考与交流。试想这能不出问题吗?最近10多年来,成千上万的实际参与者(教师),在溴乙烷与NaOH(KOH)的乙醇溶液共热发生消去反应的“实验创新”上屡试不爽,几乎次次都以失败告终,到头来多数实验者还认为这是自己的错。这种负面影响我们有理由归究于教材内容选择上的疏漏所致,这应当是值得吸取的历史教训。
参考文献:
[1]蒯文艺、 蒯世定. 溴乙烷消去反应的创新实验[J]. 中学化学教学参考, 2018, (6): 49.
[2]邢其毅. 有机化学基础[M]. 北京: 高等教育出版社, 1965: 86.
[3]苏企洵编. 有机化学[M]. 北京: 人民教育出版社, 1960: 67.
[4]北京师范大学无机化学教研室主编. 无机化学(下册)[M]. 北京: 高等教育出版社, 1997: 867.
