盐析法制备寒富苹果渣果胶及其抗氧化性研究
2019-06-25张欣萌吕春茂孟宪军
张欣萌,吕春茂,孟宪军,李 斌,张 琦
(沈阳农业大学食品学院,辽宁沈阳 110866)
我国苹果主产区的辽宁省因寒富苹果等具有自主知识产权的抗寒大苹果的选育成功及大面积推广,其苹果产量增长迅速,因此苹果加工业带来了大量果渣。日常管理中果渣只有少部分被添加到饲料中利用,大部分被当作加工废料遗弃,而这些废料中却含有丰富的可溶性糖、矿物质、维生素、果胶、纤维素等营养物质,合理利用苹果渣会减少资源的浪费,同时还可减少废弃物对环境的污染。
果胶是一种亲水性植物胶,分别以原果胶、果胶、果胶酸三种形态广泛存在于高等植物的根、茎、叶、果等部位的细胞壁中[1]。果胶的主要成分为半乳糖醛酸,是一种非常重要的食品添加剂,可作为胶凝剂、增稠剂、稳定剂和乳化剂等应用于食品加工业中[2]。苹果中的果胶还具有降血脂、抗癌等多种生理活性[3]。苹果渣中果胶含量约为15%~18%,利用苹果渣获取果胶是其商业化应用的关键[4],一方面可以解决苹果渣腐败变质所引起的环境污染问题,另一方面也可解决我国果胶资源紧缺的现状。
目前果胶沉淀的常用方法是醇沉法,此方法在果胶工业化生产中是应用最广泛,也是最早实现规模化生产的方法[5],但此法沉淀果胶时需要大量的酒精,生产成本较高。而盐析法是近年来被广泛应用于果胶工业化生产的方法,且果胶提取率较醇沉法明显提高。但目前盐析法后续的脱盐环节还存在金属离子残留问题,影响了产品质量。本课题系统研究了寒富苹果果渣制备果胶的盐析工艺和脱盐工艺,并就其抗氧化性进行了分析,为寒富苹果渣及其他果蔬加工废弃物的资源化利用提供了理论依据和借鉴。
1 材料与方法
1.1 材料与仪器
寒富苹果渣 沈阳市深井子金德胜果园;硫酸铝 成都西亚试剂有限公司;氯化铜、氯化铁、氯化镁、硫酸铵 上海吉生物科技发展有限公司;浓氨水 成都普菲德生物技术有限公司;无水乙醇、盐酸、亚硫酸 天津市富宇精细化工有限公司;DPPH、三羟甲基氨基甲烷(Tris) 山东鲁抗立科药业有限公司;FeSO4溶液、水杨酸、双氧水、磷酸缓冲液 江苏锐阳生物科技有限公司;邻苯三酚、VC河北百味生物科技有限公司;以上试剂均为分析纯。
PHS-25型数显酸度计 上海精密科学仪器有限公司;HH-6型数显恒温水浴振荡器 国华电器有限公司;TDL-40B型台式离心机 上海安亭科学仪器厂;TU-1810型紫外可见分光光度计 北京普析通用仪器有限公司;DHG-9070A型电热恒温鼓风干燥箱 上海精宏实验设备有限公司。
1.2 实验方法
1.2.1 酸法制备果胶提取液 选取盐酸与亚硫酸配比为3∶1 (v/v)的混合酸提取液,在酸解时间为1.9 h、反应温度90 ℃、pH为2.0、料液比为1∶17 (g/mL)的条件下进行寒富苹果渣中果胶的提取[6]。再经过温度为25 ℃,果胶粗提液流速为250 mL/h的大孔树脂脱色,制备果胶提取液。
1.2.2 盐析法沉淀果胶工艺优化
1.2.2.1 用盐的选择 选择硫酸铝、氯化铜、氯化铁、氯化镁和氯化铝5种能与果胶产生沉淀的盐,制成对应的饱和溶液各取3 mL,向每种饱和溶液中加入100 mL的果胶提取液,用浓氨水调pH至5.0,在60 ℃下保温沉淀45 min。沉淀物再经过脱盐、70 ℃的烘箱干燥至恒重等处理制得果胶,以果胶得率为主要指标,确定适用于沉淀果胶的盐。
1.2.2.2 单因素实验 采用1.2.1中果胶提取液,考察沉淀温度、保温时间、pH以及料液比(沉淀果胶用盐:果胶提取液)四个因素对盐析法沉淀制备果胶的影响。制备条件为:固定保温沉淀时间80 min,pH4.0,料液比1∶20 g/mL,考察不同温度(40、50、60、70、80、90 ℃)对果胶得率的影响;固定沉淀温度70 ℃,pH4.0,料液比1∶20 g/mL,分别考察不同保温时间(20、40、60、80、100、120 min)对果胶得率的影响;固定沉淀温度为70 ℃,时间80 min,料液比为1∶20 g/mL,观察pH(2.0、3.0、4.0、5.0、6.0、7.0)的变化对果胶得率的影响;固定沉淀温度为70 ℃,保温时间80 min,pH为4.0,考察不同料液比(1∶8、1∶12、1∶16、1∶20、1∶24、1∶28 g/mL)对果胶得率的影响。
1.2.2.3 响应面优化试验 试验采用Minitab 16软件设计响应面试验方案[7],以Box-Behnken设计建立数学模型,选取沉淀温度(X1)、保温时间(X2)、pH(X3)和料液比(X4)为自变量,以果胶得率(Y)为响应值,设计四因素三水平共计27 个试验,中心点重复3次,分析结果数据。试验设计因素及水平见表1。

表1 响应面因素和水平Table 1 Factors and levels in response surface design
1.2.2.4 果胶得率的计算

1.2.3 果胶脱盐工艺优化
1.2.3.1 脱盐液中酸含量 准备六份150 mL脱盐液(乙醇+盐酸+水),其中乙醇的含量固定为60%,盐酸的含量分别为1%、2%、3%、4%、5%、6%,其余全部为水。取3 g果胶盐粉末放入脱盐液中50 ℃下保温搅拌30 min后4000 r/min离心7 min,静置取下层沉淀放入干燥洁净的表面皿中,于70 ℃在鼓风干燥箱中干燥至恒重,测量各组果胶重量。
1.2.3.2 脱盐液的用量 分别准备100、150、200、250、300和350 mL的脱盐液(乙醇60%+盐酸3%+水37%),向其中各加入3 g果胶盐粉末,50 ℃下保温搅拌30 min,4000 r/min下离心7 min,静置取沉淀物在70 ℃的鼓风干燥箱中干燥至恒重,测量各组果胶重量。
1.2.3.3 脱盐的时间 准备五份150 mL的脱盐液(乙醇60%+盐酸3%+水37%),各加入3 g果胶盐粉末,50 ℃下分别保温搅拌20、30、40、50和60 min,4000 r/min离心7 min后静置取下层沉淀物放入干燥洁净的表面皿中,于70 ℃在鼓风干燥箱中干燥至恒重,测量、记录果胶重量。
1.2.3.4 脱盐温度 准备五份150 mL的脱盐液(乙醇60%+盐酸3%+水37%)分别加入3 g果胶盐粉末,在20、30、40、50和60 ℃下保温搅拌30 min,以4000 r/min离心7 min,静置取下层沉淀物放入干燥洁净的表面皿中,在70 ℃的鼓风干燥箱中干燥至恒重,称量各组果胶重量并记录。
1.2.4 抗氧化性实验
1.2.4.1 DPPH·清除率的测定 按照1.2.3最佳工艺制备脱盐果胶粉,配成不同浓度(0.5、0.7、0.9、1.2、1.5、2.0、2.5 mg/mL)的待测果胶样品各2 mL,加入等量0.2 mmol/L的DPPH-乙醇溶液,摇匀之后避光常温下放置0.5 h。DPPH·溶于乙醇后形成的紫色溶液最大吸收波长为517 nm[8],利用紫外分光光度计测定517 nm下吸光度A样品。再以相同浓度的果胶样品2 mL,加入2 mL乙醇溶液作为对照组,测定其吸光度A对照。向2 mL蒸馏水加入2 mL 0.2 mmol/L的DPPH-乙醇溶液作为空白组,测定吸光度A空白。共测定3次,取每组平均值计算清除率。以VC为阳性对照,结果越大,说明样品的抗氧化性越强[9],计算公式如式(1)。
式(1)
1.2.4.2 ·OH自由基清除率的测定 利用Fenton反应体系[10]来测定苹果渣果胶对于·OH自由基的清除作用。准备果胶样品(0.5、0.7、0.9、1.2、1.5、2.0、2.5 mg/mL)各1 mL,取2 mL 1.8 mmol/L的FeSO4溶液和1.5 mL 1.8 mmol/L的水杨酸-乙醇溶液,再加入0.1 mL含量为0.3%的双氧水,充分混合摇匀。在37 ℃的下水浴保温0.5 h,利用分光光度计在510 nm处[11]测得吸光度A样品,以蒸馏水代替果胶样品作为对照A对照。以VC为阳性为对照计算自由基的清除率,公式如式(2)。
式(2)


式(3)
1.2.4.4 卵黄脂蛋白脂质过氧化抑制率的测定 制备卵黄悬液:取鸡蛋中的卵黄部分,再取与卵黄等体积的0.1 mol/L pH7.4的磷酸缓冲液充分混合配成悬液。用磷酸缓冲液将悬液稀释25 倍,放入冰箱冷藏室备用。
取配制好的1 mL悬液放入具塞试管中,分别加入0.5 mL果胶样品(0.5、0.7、0.9、1.2、1.5、2.0、2.5 mg/mL)、1 mL 25 mmol/L的硫酸亚铁和1 mL磷酸缓冲液,混合均匀,放入水浴振荡器(37 ℃)振荡15 min。完毕后再向试管中分别加入1 mL 20%的三氯乙酸混合均匀,4500 r/min离心15 min。取上清液3 mL,分别加入1 mL 0.8%的硫代巴比妥酸,盖好管塞,放入沸水中加热10 min。待加热完成后取出试管,冷却至室温,采用分光光度计在532 nm处测定吸光度A样品,用蒸馏水代替果胶样品作为对照A对照,以样品的抗氧化活性判断果胶对卵黄脂蛋白氧化的抑制程度,以VC做阳性对照[13]。卵黄脂蛋白脂质过氧化抑制率见式(4)。
式(4)
1.3 数据处理
实验中所有数据测定全部重复三次,结果以平均数±标准偏差表示。数据处理[14]采用SPSS 18.0分析软件对实验数据进行差异显著性分析,p<0.05为差异显著,p<0.01为差异极显著。响应面优化试验中利用Minitab 16软件对数据进行Box-Behnken组合设计,建立数学模型进行结果分析。
2 结果与分析
2.1 盐析法沉淀果胶工艺优化结果
2.1.1 果胶提取液中果胶含量 根据1.2.1中果胶提取工艺,粗体液经过大孔树脂纯化后,在寒富苹果渣中果胶得率为14.96%。制成的果胶提取液供后续盐析法沉淀果胶的工艺优化使用。
2.1.2 不同盐种类对沉淀果胶效果的影响 如图1,硫酸铝沉淀的果胶得率为11.68%,氯化铜的果胶得率为11.54%,氯化铁对应的果胶得率为9.89%,氯化铝对应的果胶得率为7.96%,氯化镁对应的果胶得率最低仅为5.69%。硫酸铝和氯化铜的果胶得率差别不大,但经硫酸铝沉淀的果胶颜色最浅,而氯化铜所沉淀的果胶颜色偏深,对果胶的品质产生影响[15],且铜离子为重金属离子,若后续脱盐不彻底会导致果胶产品中的重金属超标,因此,选择硫酸铝为最佳用盐。

图1 不同用盐对于果胶得率的影响
2.1.3 盐析法沉淀果胶单因素试验的结果分析
2.1.3.1 沉淀温度对果胶沉淀效果的影响 如图2,随着温度的升高果胶得率也呈现上升趋势,当温度为40 ℃时,果胶得率仅为6.23%,温度上升到70 ℃时果胶得率显著增加至13.48%(p<0.05)。然而随着温度继续上高,果胶的得率开始略有下降。由于盐析沉淀果胶过程会伴有解聚现象发生,当温度过高,解聚现象增强[16],导致果胶得率开始下降;而温度过低时则使果胶沉淀缓慢,反应体系变得粘稠,同样导致产率偏低,因此选择70 ℃为最优的沉淀温度。

图2 温度对果胶得率的影响
2.1.3.2 保温时间对果胶沉淀效果的影响 如图3所示,果胶得率随着保温时间的延长逐渐上升,当时间过短,不利于果胶与金属盐离子充分形成果胶盐沉降下来,导致果胶得率偏低。保温时间为20 min时果胶得率为8.16%,在60 min处达到峰值,果胶得率显著增加到13.58%(p<0.05),而后随着时间继续增加得率趋于平稳且无明显变化。因此选择60 min作为最佳保温时间。

图3 保温时间对果胶得率的影响
2.1.3.3 不同pH对于果胶沉淀效果的影响 如图4,pH小于5.0时,随着pH的增大,果胶得率逐渐升高。当pH为5.0时果胶盐充分沉淀,果胶得率达到最大14.02%(p<0.05),大于5.0时,随着pH继续增大果胶得率略有下降。因此选择pH为5.0作为最佳实验条件进行后续实验。

图4 pH对果胶得率的影响
2.1.3.4 不同料液比对果胶沉淀效果的影响 不同料液比对果胶沉淀效果的影响如图5所示。果胶得率随着料液比的增大先增大后逐渐降低,当溶剂较少时,果胶得率偏低,可能是溶剂量少,物料粘度大,导致果胶从溶液中的析出量少[17],从而果胶得率低。当料液比在1∶16 (g/mL)处果胶得率达到峰值为13.67%(p<0.05),因此选择料液比1∶16 (g/mL)作为果胶沉淀的最佳比例。

图5 料液比对果胶得率的影响
2.1.4 响应面优化试验结果分析
2.1.4.1 建立响应面模型与显著性分析 本试验采用Box-Behnken组合设计,利用Minitab 16软件对果胶的提取进行定量研究并建立数学模型,研究提高盐析法沉淀果胶的得率方法,试验设计及结果如表2所示。

表2 Box-Behnken组合试验设计及试验结果Table 2 Experimental design and results of extraction by Box-Behnken
通过对表2进行统计分析得出表3回归方差分析结果,并且建立二次回归方程如下:

表3 响应面回归模型的方差分析(ANOVA)Table 3 ANOVA analysis for response surface design
2.1.4.2 响应面及等高线图分析 根据表3可知,沉淀温度与pH、保温时间与料液比相互作用对果胶得率影响显著,为了方便考察模型中交互项对于果胶得率的影响,在其他条件保持不变的情况下,分析两个因素相互作用对果胶得率的影响,利用Minitab 16软件分析,得到响应面图及等高线图如图6所示。
如图6,由3D响应面图及等高线图可以直观地反映沉淀温度、保温时间、料液比、pH与响应值果胶得率的关系。影响因素的增大,导致果胶得率的变化也随之增大,但当果胶得率到达顶点后,又伴随着影响因素的增大而开始下降[18]。最终结果与方差分析一致,在交互项中沉淀温度与pH相互作用对果胶得率的影响显著(p<0.05),料液比与保温时间两两作用对果胶得率的影响显著。

图6 盐析的响应面及其等高线
2.1.4.3 盐析法沉淀果胶工艺参数的优化验证 根据响应面试验并通过软件优化得到盐析法沉淀果胶的最佳工艺参数为:沉淀温度73.93 ℃,保温时间68.68 min,pH5.01,料液比1∶16.56 g/mL,在此最佳条件下苹果渣果胶得率的理论值为15.63%。考虑到实际操作,将最佳工艺修正为:沉淀温度74 ℃,保温时间为69 min,pH为5.0,料液比为1∶17 g/mL。在此盐析工艺下进行验证,果胶得率可达15.59%±0.51%,与理论值15.63%相近,表明该模型对盐析法沉淀果胶的方案可行。
2.2 脱盐条件结果分析
果胶脱盐部分的结果好坏直接影响果胶的品质及其用途,硫酸铝滴入果胶中形成的氢氧化铝与果胶相遇后,两种胶体发生聚沉继而使果胶沉淀出来,此过程可逆。之后再通过酸将铝离子溶解出来,从而达到脱盐的目的[19]。
2.2.1 脱盐液中盐酸的用量 当脱盐液中酸量过少时,无法把全部的铝离子都置换出来,铝离子的残留导致果胶成品中铝离子的超标,影响果胶品质;当酸量过多则会引起果胶一定程度上的降解,并导致果胶成品的颜色过深,影响果胶品质。
如图7所示,含酸量为1%时所得的果胶质量为1.25 g,虽然得胶量大,但由于酸量的不足导致铝离子残留,所得的果胶量并不是真实的含量;当含酸量增大的时候果胶质量开始趋于平稳,含酸量为3%时所得果胶质量为0.86 g(p<0.05),含酸量为4%时所得果胶质量为0.85 g,含酸量继续增大果胶质量下降不足0.2 g,故选择酸的添加量为3%,因此脱盐液的组成为60%乙醇+3%盐酸+37%水。

图7 盐酸用量对脱盐效果的影响
2.2.2 脱盐液的用量 在对果胶脱盐的试验中,脱盐液的用量对脱盐效果的影响也是至关重要的。如图8,脱盐液为100 mL时,所得果胶质量为1.12 g,随着脱盐液用量的增大,果胶得量开始下降后趋于平稳。这是由于初期脱盐液量不足导致果胶盐中的金属离子无法充分溶出,果胶脱盐不彻底从而果胶品质下降,所得果胶量也不能真实反应果胶的实际质量。当脱盐液增加到150 mL时,所得果胶质量为0.89 g(p<0.05),之后继续增加脱盐液用量果胶得量几乎保持不变,当脱盐液量过多虽然可以保证脱盐效果很好,但是造成浪费增加生产成本,所以通过试验找到一个合适的用量是必要的。故每3 g果胶盐选择脱盐液用量为150 mL为最佳用量。

图8 脱盐液用量对脱盐效果的影响
2.2.3 脱盐时间 脱盐时间的长短对果胶脱盐是否彻底,有着很重要的影响。如图9所示,脱盐时间为20 min时,所得果胶质量为1.02 g,随着反应时间延长,果胶脱盐越充分,但果胶质量开始下降,这是由于当脱盐时间不充足,反应无法充分完成,但反应时间过长则会导致部分果胶开始发生降解[20],当脱盐时间为40 min时所得果胶质量为0.88 g(p<0.05),脱盐时间为50 min时所得果胶为0.87 g,时间继续增大为60 min时果胶质量都有一定程度的下降,造成浪费资源。因此选择40 min为最合适的脱盐时间。

图9 脱盐时间量对脱盐效果的影响
2.2.4 脱盐温度 脱盐过程中合适的反应温度对于提高反应的完成速度和效果有着重要影响,温度过低,会使反应耗时过长,温度过高又会使果胶降解影响果胶品质。如图10,温度为20 ℃时,所得果胶质量为0.92 g,温度继续升高后,果胶质量发生明显变化。当温度到达40 ℃时,所得果胶的质量为0.85 g(p<0.05),而后产量开始平稳或略有减少。因此选择脱盐温度为40 ℃最佳。
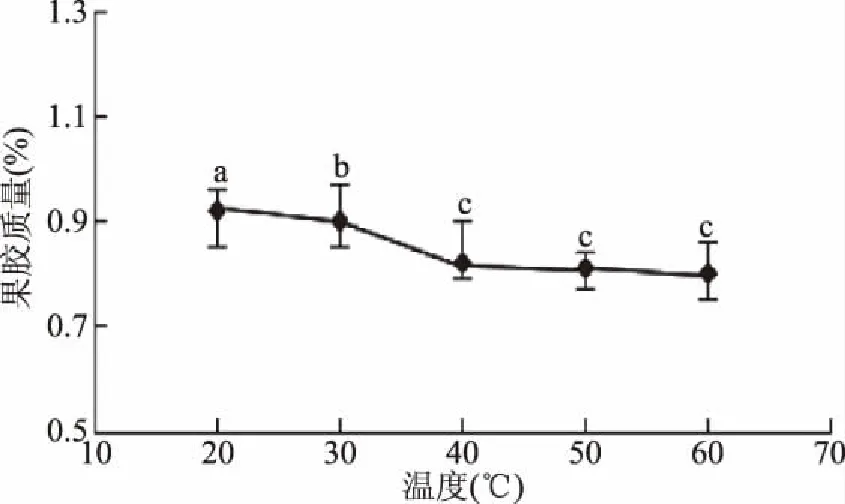
图10 脱盐温度对脱盐效果的影响
2.2.5 最佳脱盐工艺验证 根据以上四组试验确定果胶脱盐的最佳工艺参数为:脱盐液中盐酸含量为3%(60%乙醇+3%盐酸+37%水),脱盐液用量为每3 g果胶盐用150 mL,脱盐时间为40 min,脱盐温度为40 ℃。在此条件下验证结果为果胶所得质量(0.89±0.10) g。
2.3 苹果渣果胶抗氧化性结果分析
2.3.1 DPPH·清除效果 如图11,此浓度下的VC对DPPH·清除率保持在90%以上。由于果胶样品是随着果胶浓度的增大,溶液产生褪色反应,对DPPH自由基的清除效果逐渐增强[21]。当果胶浓度为2 mg/mL时,清除率达到最大为73.34%(p<0.05)。

图11 果胶样品和VC的DPPH·的清除能力
2.3.2 ·OH自由基清除效果分析 如图12,果胶样品对于羟基自由基具有一定的清除效果,当果胶浓度为0.5 mg/mL时,清除率仅为2.45%,浓度增大到1.5 mg/mL时,清除率增加至24.98%(p<0.05)。VC对其的清除效果则是随着浓度升高而大大增强,当浓度到达1.2 mg/mL,清除率基本稳定在90%以上。可以明显看出苹果渣提取的果胶清除·OH自由基能力低于VC。
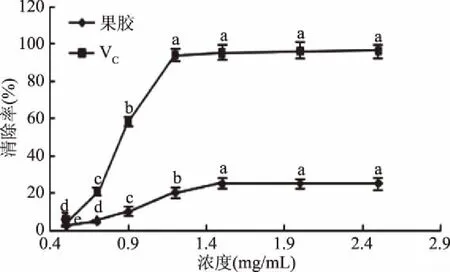
图12 果胶样品和VC的·OH的清除能力
2.3.3 清除超氧阴离子自由基效果分析 由图13可知,随着样品和VC浓度的增加对于超氧阴离子的清除效果逐渐增强,当VC的浓度达到1.2 mg/mL时,其对超氧阴离子自由基的清除率稳定在90%以上。当果胶样品浓度为0.5 mg/mL时其对于超氧阴离子的清除率仅为5.19%,增加果胶样品的浓度至2 mg/mL时,清除率最大为32.66%(p<0.05)。
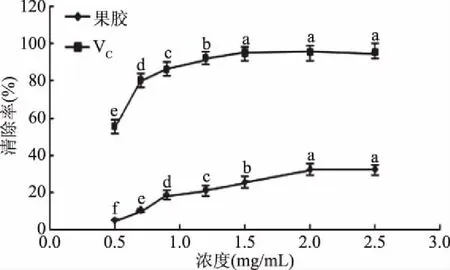
图13 果胶样品和VC对于超氧阴离子自由基的清除效果 free radical removal capability of pectin and VC
2.3.4 卵黄脂蛋白脂质过氧化抑制效果的分析 如图14,随着样品的供试浓度逐渐增大,过氧化抑制效果也逐渐增强,VC对于脂质过氧化的抑制效果基本保持在80%以上,果胶样品则是浓度达到1.2 mg/mL时,抑制率最高为61.42%(p<0.05)。

图14 果胶样品和VC对于卵黄脂蛋白过氧化的抑制效果
3 结论
在盐析法提取果胶过程中的适宜用盐、盐析沉淀果胶的工艺条件和脱盐条件试验中,通过对几种盐的比较,利用果胶得率确定盐析法的最佳工艺。研究结果表明,在同样的条件下用硫酸铝制取的果胶无论是得率还是品质都有着明显的优势;在盐析法沉淀果胶的工艺优化中,确定最佳工艺参数为盐析温度74 ℃,时间为69 min,pH为5.0,料液比1∶17 (g/mL)。此工艺下果胶得率达到15.59%。在脱盐试验中主要考察了脱盐液中酸的含量、脱盐液用量、脱盐时间以及脱盐温度对果胶得率的影响,最终确定了脱盐的最佳工艺为脱盐液中盐酸含量为3%(60%乙醇+3%盐酸+37%水),脱盐液用量为每克果胶盐50 mL,脱盐时间为40 min,脱盐温度为40 ℃。通过果胶对DPPH·、·OH、超氧阴离子的清除效果以及对卵黄脂蛋白脂质过氧化的抑制效果考察苹果渣果胶的抗氧化能力。以VC作为对比参考,发现苹果渣果胶对于DPPH·自由基的清除效果和对卵黄脂蛋白脂质过氧化的抑制效果优于另外两种体系,证明了苹果渣果胶具有一定的清除自由基和抑制脂质过氧化的能力,可作为一种天然的抗氧化剂进行开发。
