杭州市PM2.5中PAHs和PAEs气固分布特征及其安全风险研究
2019-06-11
(浙江工业大学 环境学院,浙江 杭州 310014)
随着城市工业经济的迅猛发展和汽车保有量的不断增加,挥发性有机化合物(VOCs)的排放量逐渐增大。VOCs一旦进入大气,会在颗粒相和气相之间进行分配,进而影响其氧化、光解反应与干湿沉降速率[1-3]。多环芳烃(PAHs)是一种常见的VOCs污染物,在环境中分布十分广泛,其毒性仅次于二噁英和多氯联苯,具有致癌、致畸和致突变的“三致”特性[4-5],其来源主要为生物质、化石燃料的不完全燃烧和一些工业活动[6]。Park等[7]研究表明:城市空气中分布于气相中的PAHs质量浓度高于颗粒物中的,且易与其他污染物反应生成毒性更强的衍生物。邻苯二甲酸酯(PAEs)是一种常用的增塑剂,已被广泛地应用于塑料制品中[8]。现有研究表明[9-14]:低分子量的PAEs,如邻苯二甲酸乙酯(DEP),对眼睛和呼吸系统具有刺激作用,而高分子量的PAEs,如邻苯二甲酸丁基苄酯(BBP)和邻苯二甲酸双(2-乙基己基)酯(DEHP),则会损伤肝脏、肾脏和生殖系统,甚至可能致癌。因此,研究PAHs和PAEs在大气环境中的气固分布特征,有助于预测其迁移、转化和归趋行为[3,15],对人类健康防护具有重要的意义。
杭州市是浙江省经济发展中心,随之而来的环境污染也日益严重,目前有关PAEs的研究[16-19]主要针对其在大气中浓度水平、检测方法及来源解析,对大气中PAEs的气固分布情况的研究较缺乏,无法全面评估杭州市大气PAEs的环境效应。而对于PAHs的研究[1,4,20-22]主要集中在颗粒物中的浓度水平及TSP与气相的气固分布,对PM2.5与气相的气固分布以及不同季节气固分布情况研究较少。因此,笔者同时采集PM2.5及气体样品,对杭州市主城区大气环境中PAHs和PAEs的气固分布情况进行了系统研究,以期全面反映PAHs和PAEs的气-固分布特征,为空气污染防治提供理论依据。
1 实验材料与方法
1.1 样品的采集
选取经纬度为120°09′44.63"E,30°17′35.28"N的采样点,如图1所示。该采样点位于杭州市老城区,附近主要为居民区、街区和商业区,属居民、商业混合区,可以探究生活污染物对大气的影响。采样高度约为15 m,采样时间为2016年12月—2017年5月。本研究采用崂应2030型中流量智能大气颗粒物采样器采集PM2.5和气相样品。PM2.5和气相样品分别利用玻璃纤维滤膜和聚氨酯泡沫(PUF)进行采集,采样流量均为100 L/min。每个样品连续采集48 h,气固采集时间同步。雨雪天气不进行采样。笔者采集了3 组平行样,共获得108 个有效样品,其中包括54 个气相样品和54 个固相样品。
图1 样品采样点示意图Fig.1 Location of sampling site
采样前,将玻璃纤维滤膜在马弗炉中高温烘烤4 h后再超声清洗3 次,在60 ℃烘箱中烘干后冷藏保存;PUF则索氏提取24 h,于烘箱中烘干后置于密封袋冷藏保存。使用赛多利斯CPA225D型精密电子天平称量采样前后的玻璃纤维滤膜,所有玻璃纤维滤膜称量2 次并且保证差值小于0.03 mg,取平均值。
1.2 样品预处理
在玻璃纤维滤膜样品中加入质量浓度均为0.2 mg/L的回收率指示物(包括萘-D8、二氢苊-D10、菲-D10、-D12、苝-D12)1 mL后置于索氏提取瓶中,加入80 mL的提取剂(V(二氯甲烷)∶V(丙酮)=4∶1),在60 ℃条件下索氏提取18 h。提取液经R201型旋转蒸发仪浓缩至约5 mL左右,随后转至硅胶层析柱进行净化洗脱。层析柱填充物由下至上分别为5 cm氧化铝、5 cm硅胶、1 cm无水硫酸钠,填充物使用前均活化5 h左右。用50 mL洗脱液(V(二氯甲烷)∶V(正己烷)=3∶7)淋洗层析柱,所得的洗脱液经旋蒸后浓缩至1 mL左右,转至进样瓶中,氮吹至1 mL以下,然后加入200 μL质量浓度为10 μg/L的内标物六甲基苯,定容至1 mL,冷藏保存,待测。PUF的预处理过程同上,提取溶剂体积为300 mL,比例不变,提取时间为24 h,层析柱填充物高度比例由下至上调整为11∶11∶1,其余条件不变。
1.3 GC/MS分析条件
采用气相色谱质谱联用仪(安捷伦,型号:7890A/5975C)对16 种PAHs和6 种PAEs进行测定。
1) PAHs 载气为氦气(纯度为99.99%),载气流量为1.0 mL/min;进样口温度为300 ℃;不分流进样,进样量为1 μL;程序升温:初温50 ℃,保持2 min后以10 ℃/min升至180 ℃,再以6 ℃/min升至230 ℃,最后以3 ℃/min升至280 ℃,保持8 min至待测组分全部流出;电离源为电子轰击源(EI),电子能量为70 eV,离子源温度为230 ℃;扫描方式为选择离子扫描。
2) PAEs 其余条件不变,程序升温:初始温100 ℃,保持0.5 min后以30 ℃/min升至300 ℃,保持2.0 min至待测组分全部流出。
1.4 质量控制与质量保证
为了减少对PAEs测定的干扰,所有塑料制品严禁使用。为保证数据的可靠性,采用方法空白和样品空白检测预处理过程中样品损失率是否符合质量保证要求,结果均在限定范围内。每个样品平行测定3 次,相对偏差小于5%。每测定30 个样品校正一次标准曲线。在加标回收率中,除萘(43%)略低以外,其余15 种PAHs及6 种PAEs回收率均在60%~120%,与现有研究中的回收率相近[9,21,23-24]。本研究相对标准偏差小于10%,均符合质量保证要求。
2 结果与讨论
2.1 PAHs在不同相中质量浓度水平及分布特征
通过GC/MS分析得,冬季采样点气相中总PAHs的月平均质量浓度为53.07 ng/m3,PM2.5中总PAHs的月平均质量浓度为18.14 ng/m3;春季采样点气相中总PAHs的月平均质量浓度为5.95 ng/m3,PM2.5中总PAHs的月平均质量浓度为3.71 ng/m3。本地区春季大气环境中总PAHs质量浓度低于北京地区[1]春季大气环境中的总PAHs质量浓度(颗粒相质量浓度72.99 ng/m3,气相质量浓度145.73 ng/m3),冬季大气环境中总PAHs质量浓度高于沿海地区如小麦岛、獐子岛[4]冬季大气环境中总PAHs质量浓度(颗粒相质量浓度8.87 ng/m3,气相质量浓度19.64 ng/m3),说明本地区冬季PAHs污染较严重,春季有所缓解。分析结果表明:大气环境中总PAHs的相分布特征为气相占优型。这可能是由于大气环境中PAHs中以低环、易挥发的单体为主,导致整体PAHs以气相分布为主。此外,GC/MS分析结果表明:大气环境中总PAHs的季节变化规律为冬季大于春季(12,1,2 月为冬季,3,4,5 月为春季)。由于杭州地区没有集中供暖,冬春季的排放源差别不大,冬季PM2.5的质量浓度为107.52 μg/m3,春季PM2.5的质量浓度为73.85 μg/m3,冬季PM2.5质量浓度大于春季,但两个季节PM2.5质量浓度差距不大,PM2.5的稀释作用较小。所以该季节变化规律主要是因为冬季气温低,易产生逆温现象,大气环境中PAHs不易扩散;而春季对流活动相对较强,利于大气环境中PAHs的扩散,且湿度大,湿沉降对PAHs清除作用更为明显。
图2展现了16 种PAHs单体在气固相中的分布比例。结果表明:在大气环境中,分子量较小的低环(2,3环)PAHs主要分布于气相,分子量较大的高环(5,6环)PAHs主要聚集在PM2.5颗粒相中。该分布特征与其他研究报道中[1,4,6]PAHs气固浓度分布特征一致,与PAHs单体的蒸气压有关:低环数PAHs的蒸气压高,易挥发,常以气态形式存在,而高环数PAHs的蒸气压低,易与颗粒物相结合[4,6]。
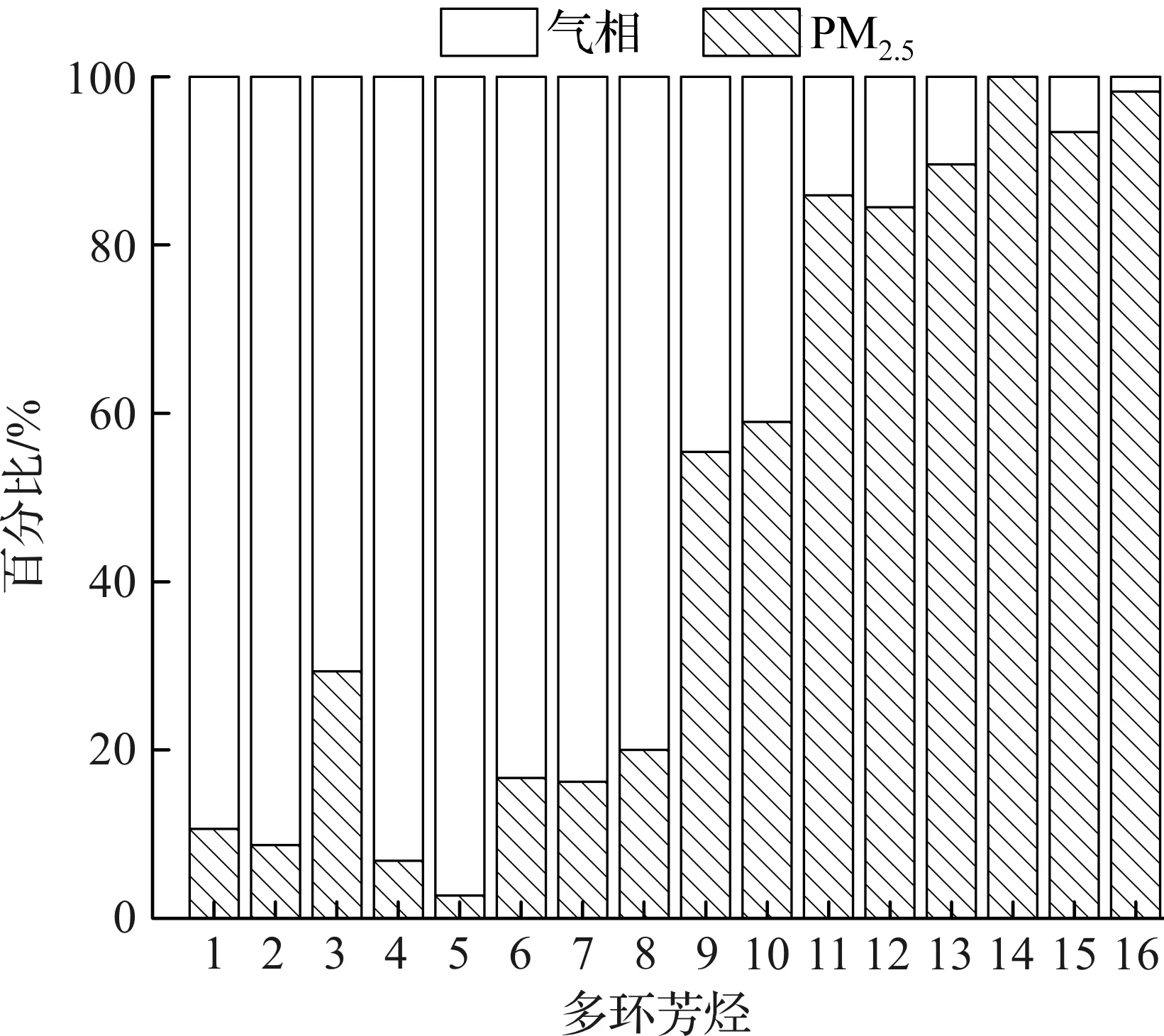
1—NAP;2—ACE;3—ACY;4—FLO;5—PHE;6—ANT;7—FLA;8—PYR;9—BaA;10—CHR;11—BbF;12—BkF;13—BaP;14—IcdP;15—DahA;16—BghiP图2 PM2.5和气相中PAHs的分布比例Fig.2 Distribution ratios of PAHs in PM2.5 and gas phase
2.2 PAEs在不同相中质量浓度水平及分布特征
通过GC/MS分析得,冬季采样点气相中总PAEs的月平均质量浓度为20.16 ng/m3,PM2.5中总PAEs的月平均质量浓度为21.91 ng/m3,春季采样点气相中总PAEs的平均质量浓度为5.81 ng/m3,PM2.5中总PAEs的月平均质量浓度为6.83 ng/m3。本地区冬春季PM2.5中总PAEs的平均质量浓度略低于天津市[16]冬春季PM2.5中总PAEs的平均质量浓度(34.75 ng/m3)。分析结果表明:大气环境中总PAEs的相分布特征为固相占优型,这可能是由于大气环境中PAEs以大分子量、易吸附在颗粒物中的单体为主,导致整体PAEs以固相分布为主。此外,GC/MS分析结果表明:大气环境中总PAEs的季节变化规律为冬季大于春季。由于冬春两季PAEs的排放源差别不大,且PM2.5的稀释作用较小,因此该季节变化规律可能由于冬季的扩散条件差,污染物不易扩散,而春季光照辐射增强,对有机物有一定的分解作用,而且风力较大,有机物易扩散。
图3展现了6 种PAEs单体在气固相中的分布比例。结果表明:在大气环境中,低分子量的邻苯二甲酸甲酯(DMP)、DEP、邻苯二甲酸二正丁酯(DBP)易存在于气相中,而高分子量的BBP、DEHP、邻苯二甲酸正辛酯(DNOP)易吸附于颗粒相中。有研究表明[13]:低分子量的PAEs易挥发,如C1至C4具有较短的二烷基链(分子量<252,例如DMP和DEP),是气相中最丰富的同系物,而高分子量的PAEs不易挥发,如C6至C8(分子量>252)具有较长的二烷基链,与空气中颗粒的结合能力更大(例如DEHP为22.7%,25%为DOP)。这种PAEs的相分布规律具有强烈的分子量依赖性[13]。
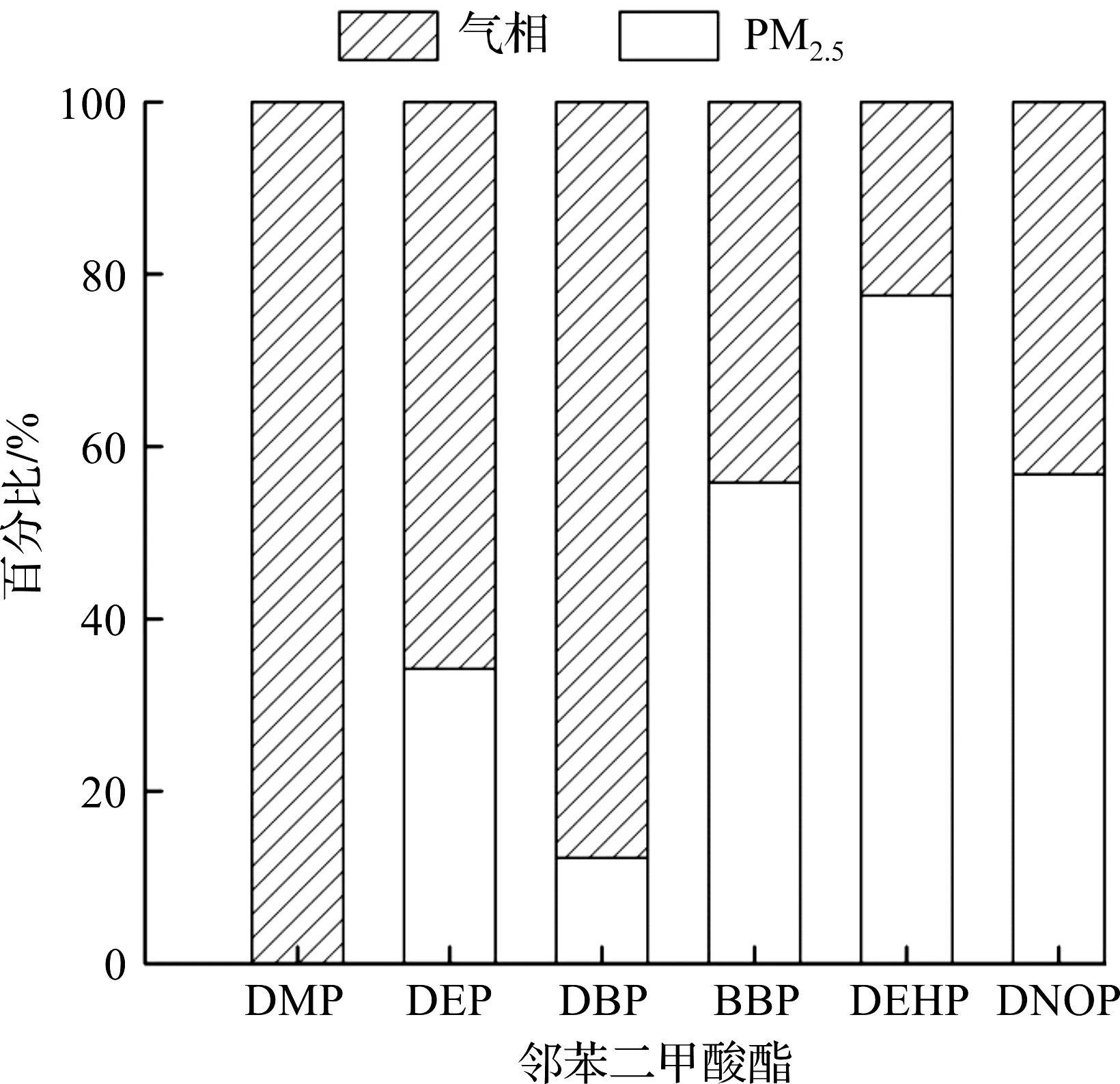
图3 PM2.5和气相中PAEs的分布比例Fig.3 Distribution ratios of PAEs in PM2.5 and gas phase
2.3 PM2.5中PAHs和PAEs分配系数规律
大气环境中有机物的相分布规律一般用分配系数(Kp)进行表征[3,24-25],计算方法为
Kp=(Cp/CPM2.5)/Cg
(1)
式中:Cp和Cg分别为有机物在固相和气相中的质量浓度,ng/m3;CPM2.5为PM2.5的质量浓度,μg/m3;Kp为分配系数,m3/μg。Kp越大,有机物越容易与颗粒物结合[1,4]。本研究中,气相样品的平均采样效率为84.2%,则大气环境中PAHs和PAEs的Kp值计算公式可修正为
Kp=0.842(Cp/CPM2.5)/Cg
(2)
如表1所示,对15 种PAHs单体(除IcdP外)的分配系数(Kp)进行计算,结果表明随着环数增大,PAHs的Kp值增大,其越容易与颗粒物结合。这一结论正好解释了前文中PAHs单体的气固分布特征:低环的PAHs更易分布在气相中,而高环的PAHs更易分布在固相中。
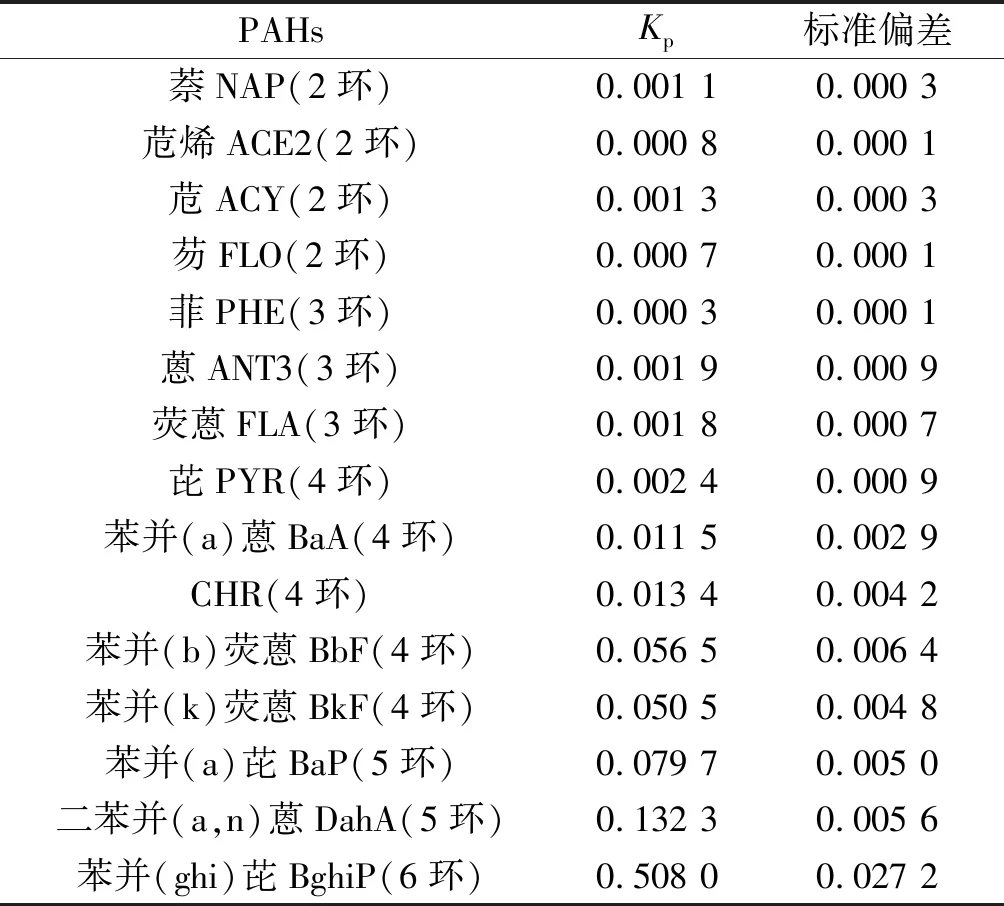
表1 15 种PAHs单体的Kp值Table 1 Kp values of 15 PAHs monomers
表2给出了6 种PAEs的Kp值。结果表明:随着分子量的增大,PAEs的Kp值增大,其越容易与颗粒物结合,即低分子量低Kp的DMP,DEP,DBP易存在于气相中,而高分子量高Kp的BBP,DEHP,DNOP易吸附于颗粒相中。
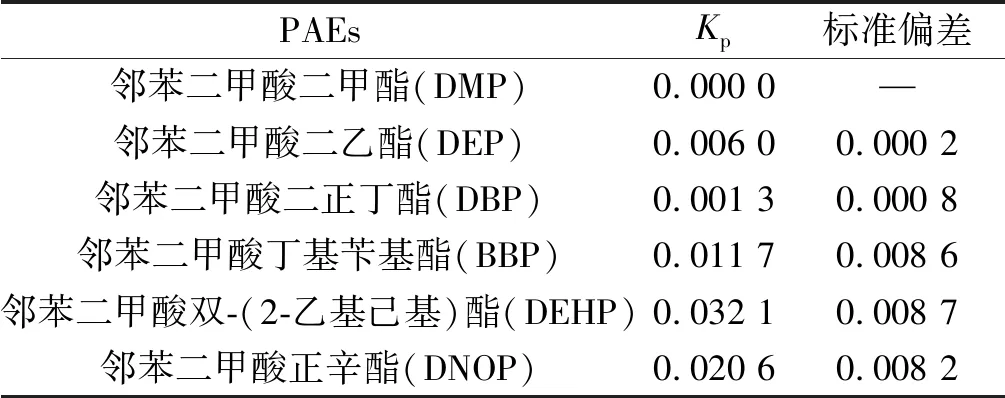
表2 6 种PAEs单体的Kp值Table 2 Kp values of 6 PAEs monomers
2.4 PM2.5中PAHs和PAEs气固分布随季节变化趋势
图4,5给出了冬、春两季中PAHs和PAEs的气固分布比例,用以评价不同季节对有机物在气固相中比例变化的影响,更好地评价有机物的分布行为。气相和固相分布比例的计算公式为
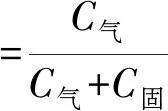
(3)


图4 不同季节中PAHs的气固分布比例Fig.4 Gas-solid distribution ratios of PAHs in different seasons

图5 不同季节中PAEs的气固分布比例Fig.5 Gas-solid distribution ratios of PAEs in different seasons
2.5 PAHs和PAEs的安全风险研究
苯并[a]芘(BaP)被证实是PAHs中致癌性最强的物质,因此对其健康风险的研究也进行得最为深入。致癌风险研究中常以BaP为标准参考物,一般假定其毒性当量因子(TEF)为1[29]。根据各PAHs单体质量浓度,计算得PAHs的BaP总致癌等效浓度,即TEQBaP。计算公式[30]为
TEQBaP=C×TEFBaP
(4)
式中:C为PAHs的质量浓度,ng/m3;TEQBaP是基于BaP的毒性当量,ng/m3;TEFBaP为各PAH单体相对于BaP的毒性当量因子。
表3为16 种PAHs单体的毒性当量浓度。其中,PM2.5中总PAHs的毒性当量TEQBaP为10.887 5 ng/m3,气相中总PAHs的毒性当量为29.8201 ng/m3,表明气相中总PAHs的毒性当量远大于PM2.5,因此研究PAHs在大气环境中的气固分布特征,对人类健康防护具有重要的意义。PAHs单体毒性分析结果表明:PM2.5中高环PAHs的毒性远大于低环,气相中低环PAHs的毒性大于高环,这是因为PAHs的毒性当量与PAHs的浓度有关,PM2.5中主要吸附了高环PAHs,而气相中主要聚集了低环PAHs。
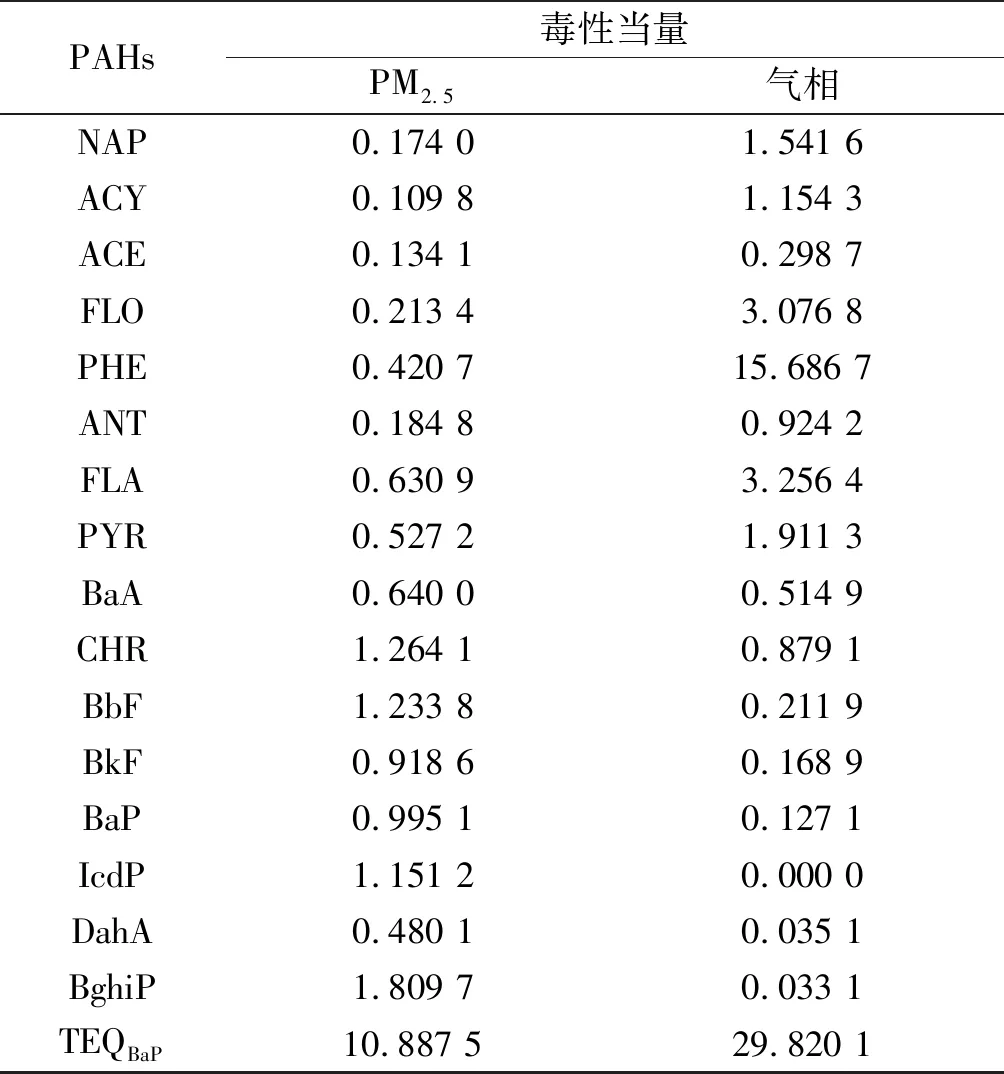
表3 多环芳烃致癌毒性当量Table 3 The TEQBaP for PAHs ng/m3
美国EPA研究表明:DEHP对人体健康有较大影响,低浓度下也有较强的致癌性[31]。因此,本研究主要估算PAEs中DEHP的致癌风险。DEHP的致癌风险(R)估算模型[32]为
R=q×E
(5)
式中:q表示剂量—反应关系确定的致癌斜率因子,对于DEHP,其值[32-33]为0.014 kg·d/mg;E表示每天DEHP暴露量,mg/(kg·d)。根据文献[32]得暴露量E的公式为
(6)
式中:Ci为气相和颗粒相DEHP总质量浓度,mg/m3;IR为呼吸速率,m3/h;CF为人体暴露因子,0.9;ED为暴露时间,h/d;BW为暴露者体重,kg。其中成人和儿童的平均呼吸速率、体重以及暴露时间来自文献[34-35]。
DEHP的致癌风险如表4所示,可知成年人的致癌风险为3×10-8,儿童的致癌风险为5×10-8~6×10-8,儿童的致癌风险高于成年人,需引起重视,但两者均未超过USEPA所规定的最低致癌风险值(1.0×10-6)[31,33],因此不具有致癌风险。
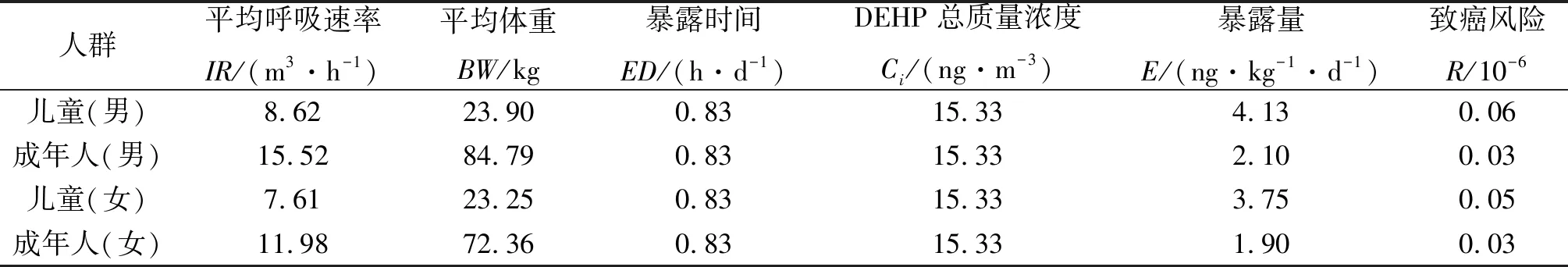
表4 DEHP的致癌风险Table 4 Carcinogenic risk of DEHP
3 结 论
笔者研究了杭州市主城区大气环境中PAHs和PAEs的气固分布特征。由于大气环境中PAHs中以低环、易挥发的单体为主,导致整体PAHs以气相分布为主,其呈现气相占优型相分布规律;由于大气环境中PAEs以大分子量、易吸附在颗粒物中的单体为主,导致整体PAEs以固相分布为主,其呈现固相占优型相分布规律。根据GC/MS分析结果,计算两类化合物的气-固分配系数(Kp),结果表明单体PAHs或PAEs的分子量越大,Kp值越大,越容易与颗粒物结合,致使低环PAHs和分子量较低的PAEs易分布于气相,而高环PAHs和分子量较高的PAEs易分布于颗粒相。此外,该地区的大气PAHs和PAEs浓度呈季节变化规律:冬季大于春季,且冬季中两者的气相比例更大。由PAHs和PAEs的安全风险研究可知,PAHs存在一定的致癌风险,需引起重视,PAEs则未超过最低致癌风险值。
