正交设计优化磷酸川芎嗪-冰片脂质体的制备工艺*
2019-06-06刘剑敏唐静宜
刘剑敏,唐静宜,程 路,陈 凡
(湖北省武汉市第一医院药学部,湖北 武汉 430022)
天然活性成分川芎嗪(TMP)为常用脑血管疾病治疗药物[1-2]。目前,临床常用川芎嗪普通制剂有片剂、胶囊剂和注射剂[3-4]。其口服制剂半衰期短(0.5~2 h)、生物利用度低(10%~30%)[5],静脉注射4~6 h可达血药浓度要求,但给药用药不方便。与静脉给药相比,经鼻给药能迅速将药物经嗅球直接转运至大脑和脊髓,达到相同的生物利用度[6]。ILLUM[7]报道,鼻喷雾剂给药能有效提高TMP在脑内的转运,这种非侵入性的高效方式对脑缺血损伤的疗效显著。脂质体作为经鼻给药的载体具有天然优势,首先具有较强的生物黏附性,药物可缓慢释放,具有脑部靶向性[8-9],另外还具有生物利用度高、刺激性小、不良反应少等优点[10]。冰片常作为川芎的药对组合用于治疗心脑血管疾病,配伍冰片对脑缺血损伤的保护明显优于单用[11-12],具有明显的脑靶向优势,也为缺血性脑损伤防治提供了可能。本研究中探讨了磷酸川芎嗪(TMPP)与冰片(B)配伍脂质体的制备方法,为该剂型药物抗脑缺血损伤的应用提供参考。现报道如下。
1 仪器与试药
1.1 仪器
LC-20AT型高效液相色谱仪(岛津贸易<上海>有限公司);RE-5299型旋转蒸发仪(上海振荣科学仪器有限公司);XSP-1C型粒径测定仪(上海精密仪器厂);W201D型数控恒温水浴锅(上海申顺科技有限公司);葡聚糖凝胶-G50(北京化学试剂公司)。
1.2 试药
磷酸川芎嗪对照品(中国药品生物制品检定所,批号为100845-201702,纯度为99.2%);冰片(四川青神康华制药有限公司,批号为170314);Triton-X100(进口分装,中国碧云天公司,批号为ST795);磷酸川芎嗪原料(北京燕京制药厂,批号为20170123,纯度>99%);大豆磷脂(山海太伟药业有限公司,批号为20170307),胆固醇(北京化学试剂公司,批号为20170402);甲醇为色谱纯,其他试剂均为分析纯。
2 方法与结果
2.1 TMPP-B脂质体的制备
取一定比例的大豆磷脂和胆固醇,置圆底烧瓶,精密称定,加入十八胺,以乙醇溶解,水浴减压蒸发除去溶剂,得分布均匀的薄膜,加入一定浓度的硫酸铵溶液水化,超声得空白脂质体混悬液[13]。将空白脂质体经葡聚糖凝胶G-50微型柱(10 cm×1 cm)以pH=7.4磷酸盐缓冲液(PBS)进行洗脱,收集洗脱后的空白脂质体,加入固定比例的TMPP-B药液,于水浴中孵化,即得TMPP-B脂质体。
2.2 包封率测定
2.2.1 色谱条件
色谱柱:Agilent Zobox C18柱(150 mm×4.6 mm,5μm);流动相:甲醇-水(50∶50,V/V);检测波长:295 nm;流速:1 mL/min;柱温:25℃;进样量:20μL。磷酸川芎嗪保留时间为7.5 min,色谱图见图1,空白脂质体在此保留时间未出峰。
2.2.2 溶液制备
对照品溶液:称取TMPP适量,精密称定,加入甲醇-水(50∶50)溶解,制备成质量浓度为100 mg/L的贮备液,备用。
供试品溶液:取TMPP-B脂质体适量,置离心管中,以15 000 r/min的转速离心30 min。分别取离心后的上清液和未离心脂质体溶液各适量,后者加Triton-X100溶解,即得。
2.2.3 方法学考察

图1 高效液相色谱图
标准曲线制备:用50%甲醇将对照品贮备液稀释成5.0,10.0,25.0,50.0,100.0 mg/L的系列标准溶液,按拟订色谱条件分别进样20μL。以峰面积(A)对质量浓度(C,mg/L)进行线性回归,得回归方程A=0.562 1C-0.481 8,r=0.999 3(n=5)。结 果 表 明,TMPP质量浓度在5.0~100.0 mg/L范围内与峰面积线性关系良好。
精密度试验:取质量浓度为20.0 mg/L TMPP对照品溶液,按拟订色谱条件进样6次,计算TMPP含量。结果的RSD为0.34%(n=6),表明仪器精密度良好。
重复性试验:配制TMPP对照品溶液6份,分别按拟订色谱条件进行检测,计算6份溶液中TMPP峰面积与称样质量的比值。结果的RSD为0.58%(n=6),表明方法重复性良好。
稳定性试验:分别精密吸取TMPP-B脂质体0.5mL,以Triton-X100溶解并定容至50 mL,得供试品溶液。分别于0,1,2,3,5,8 h时依法进样测定。结果的RSD为1.26%(n=6),表明供试品溶液在8 h内稳定。
加样回收试验:取20.0 mg/L对照品溶液1,2,3 mL,加入空白脂质体,以Triton-X100溶解并定容至20 mL,按拟订色谱条件进样测定。结果TMPP的平均回收率为101.38%,RSD为1.09%(n=3)。
2.2.4 样品含量测定
取2.2.2项下供试品溶液和对照品溶液适量,按2.2.1项下条件测定TMPP含量,得到WT和WF,计算包封率(E,%)=(WT-WF)/WT×100%。
2.3 制备工艺优化
根据前期单因素考察预试验结果,以磷脂-胆固醇质量比(因素A)、TMPP-(磷脂+胆固醇)质量比(因素B)、水化时间(因素C)及(NH4)2SO4浓度(因素D)为考察因素,进行正交设计。采用乙醇注入式(NH4)2SO4梯度法制备TMPP-B脂质体,以包封率为考察指标,分别对试验结果进行直观分析和方差分析。结果见表1和表2。
由表1可知,这4项因素对TMPP-B包封率的影响程度为A>D>B>C,且最佳工艺条件为A1B2C1D2,即磷脂-胆固醇(2∶1),(磷脂+胆固醇)-TMPP(15∶1),水化时间为30 min,(NH4)2SO4质量浓度为0.2μmol/L。由表2可知,因素A,B,D影响显著。以最优工艺制备3批TMPP-B脂质体,计算得包封率为(73.14±0.71)%,该工艺稳定可行。
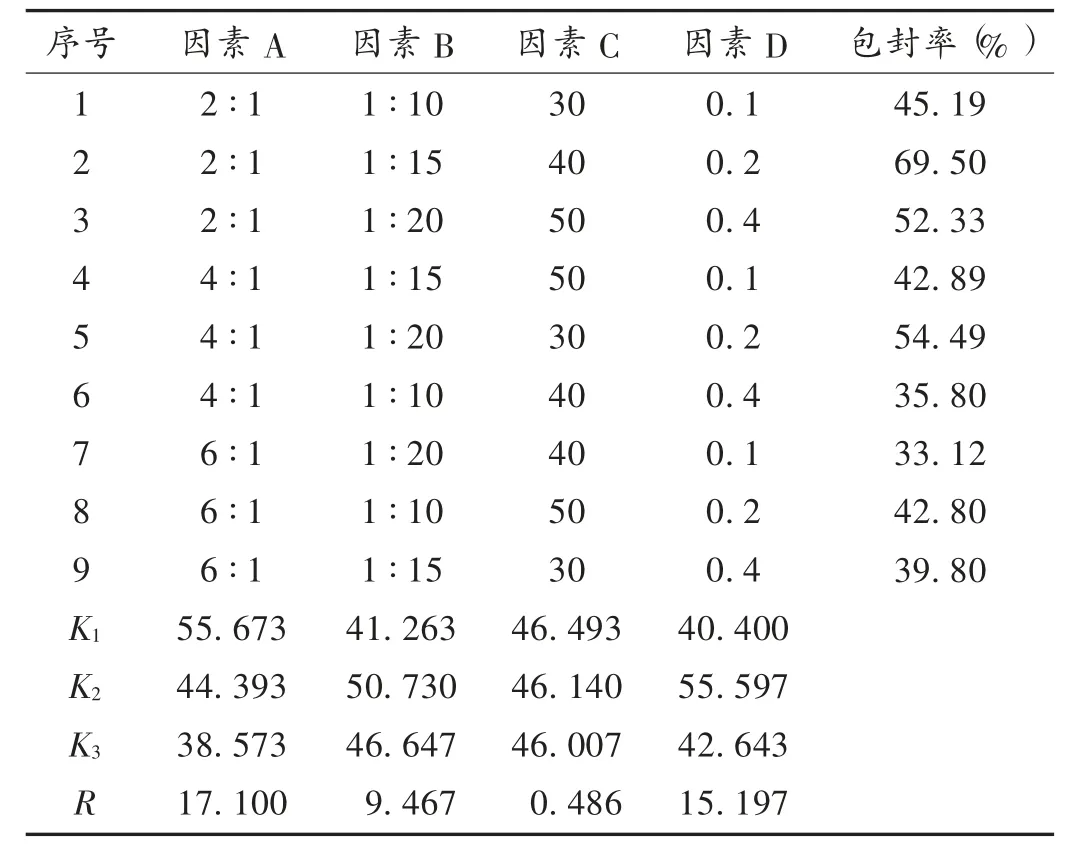
表1 TMPP-B脂质体制备L9(34)正交设计及直观分析
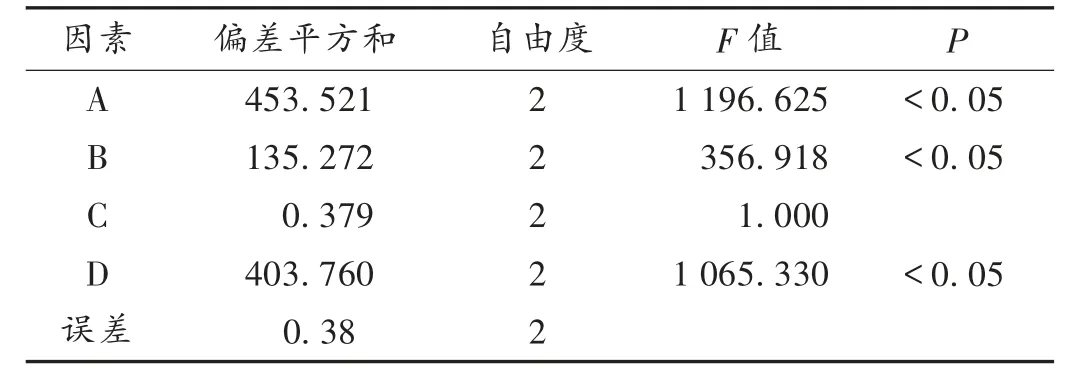
表2 方差分析结果
2.4 其他评价指标
TMPP-B脂质体粒径,以XSP-1C型粒径测定仪进行粒径分布测定,粒径分布在113~145 nm范围内,平均粒径为(136.10±6.30)nm,分布均匀;Zeta电位为(-35.70±3.60)mV。取最优工艺制备3批TMPP-B脂质体,置4℃冰箱,放置4周,未见分层、变色、沉淀和破乳等改变,表明该工艺质量稳定。
3 讨论
3.1 脂质体制备方法
常规的制备方法有被动载药法中的薄膜分散、注入法等,主动载药法中的pH梯度法、(NH4)2SO4梯度法等[9]。新型制备方法较多,如超临界反相蒸发法、冷冻干燥法、温度敏感脂质体、配体靶向修饰脂质体等[9]。常规制备方法虽存在脂质体包封率较低、粒径不均一、有机溶剂残留等缺点,但由于对所需设备要求低、生产周期较短、具体方法简单易行、所得产品性质稳定性良好等众多优势而应用广泛。
TMPP水溶性良好,故选用改进的乙醇注入式(NH4)2SO4梯度法,制备条件温和,避免了高温对磷脂的氧化,且有机溶剂残留少,所得TMPP-B脂质体包封率达(73.14±0.71)%,且载药量适宜,稳定性良好。在包封率测定方法的选择上,预试验中对比分析了凝胶过滤法和离心法2种测定方法,结果发现以15 000 r/min离心30 min分离游离TMPP和脂质体,所得结果与凝胶过滤法无明显差异,故本研究中选择操作更方便快速的离心法进行。
3.2 物料比例
TMPP-B脂质体制备时,预试验考察了影响最终产品质量的诸多因素,发现磷脂-胆固醇质量比、TMPP-(磷脂+胆固醇)质量比、(NH4)2SO4浓度及水化时间为主要影响因素。磷脂与胆固醇合适比例对稳定脂质体结构和提高包封率起至关重要的作用,磷脂浓度增加,药物包封率随之提高。但磷脂用量过大会造成水化不完全,且易凝聚,不利于产品稳定性。胆固醇比例过大会使脂质体易破裂,造成药物的渗漏;而过少又会增加脂质体的膜流动性。磷脂与胆固醇的比例控制在2~7比较好[14]。
3.3 研究价值
正交设计、直观分析和方差分析结果显示,以包封率为考察指标,考察四因素不同水平对TMPP包封率的影响,结果表明,该制备工艺的脂质体包封率高,分布均匀,形态好,质量稳定,该方法简单、合理。
冰片可促进川芎嗪在脑部的分布[11-12],两者联用治疗脑血管疾病更快速。随着新剂型的开发,药物生物利用度的提高,穿透血脑屏障实现脑靶向成为可能,为后期的脑缺血损失治疗研究提供参考。
