基于近红外光响应性的盐酸阿霉素纳米脂质体的制备工艺优化Δ
2019-05-31祝侠丽王莎莎李玲华巴妍妍刘黎明贾永艳
祝侠丽,王莎莎,李玲华,巴妍妍,刘黎明,贾永艳
(河南中医药大学药学院,郑州 450046)
恶性肿瘤已成为威胁人类健康的一大杀手,也是现代医药学研究领域面临的巨大挑战。盐酸阿霉素(Doxorubicin hydrochloride,DOX)作为一种广谱抗肿瘤药物,因其普通剂型具有明显的系统毒性而被临床限制使用[1]。纳米脂质体可通过高通透性和滞留效应(Enhanced permeability and retention effect,EPR)将化疗药物靶向输送到肿瘤组织,可提高药物的疗效,并降低毒性,同时具有明显的缓释作用和较高的生物相容性[2]。尽管聚乙二醇(PEG)化的DOX脂质体已应用于临床,但仍存在药物被动释放速度过慢等问题[3]。近年来,基于纳米材料的肿瘤光热治疗(Photothermal therapy,PTT)技术作为一种新型的治疗方法,因其特异性强、创伤小、并发症少等优势,逐渐受到学者的关注[2]。纳米硫化铜因具有成本低、光热稳定性好、细胞毒性低以及粒径、形貌可控等特点[4],在PTT领域具有较大的应用前景。为此,本研究将纳米硫化铜和DOX共同包裹制备了具有近红外光响应性的DOX纳米脂质体,并通过星点设计-响应面法优化DOX纳米脂质体的制备工艺,旨在为PTT的研究提供参考。
1 材料
1.1 仪器
BSA224S-CW型电子天平(赛多利斯科学仪器有限公司);KQ-100型数控超声波清洗器(昆山市超声仪器有限公司);N-1100-OSB-2100型旋转蒸发仪(上海爱郎仪器有限公司);92-llN型超声波细胞粉碎机(宁波新芝生物科技股份有限公司);T6-1650E型新世纪紫外-可见分光光度(UV)计(北京普析通用仪器有限责任公司);Nano-ZS90型电位及粒度分析仪(英国马尔文仪器有限公司);MW-GX-808/3000 mW型激光器(中国科学院长春激光所)。
1.2 药品与试剂
DOX原料药(大连美伦生物技术有限公司,批号:25316-40-9,纯度:≥99%);豆磷脂(天津市光复精细化工研究所,批号:20160403);胆固醇(郑州奇华顿化工产品有限公司,批号:20150527);纳米硫化铜(河南中医药大学药学院自制,批号:20180317);磷酸盐缓冲溶液(PBS,pH 7.4,批号:20171204)、聚维酮(批号:20161009)均由北京博奥拓达科技有限公司提供;三氯甲烷、甲醇等均为分析纯,水为超纯水。
2 方法与结果
2.1 DOX纳米脂质体的制备
采用薄膜分散法[5-6]。精密称取豆磷脂、胆固醇各适量,置于同一茄形瓶中,加三氯甲烷适量溶解,摇匀,后将茄形瓶于40℃下旋转减压蒸发以除去有机溶剂,至形成均匀的薄膜,后加入含有DOX和聚维酮、纳米硫化铜的PBS溶液,超声(功率:500 W,频率:40 kHz)处理20 min,后再超声(功率:250 W,频率:25 kHz)处理,每次3 s,间歇3 s,共循环20次,即得含有纳米硫化铜的DOX纳米脂质体。另取薄膜,加入含有聚维酮、纳米硫化铜的PBS溶液,按上述操作“超声处理20 min起至超声处理”,即得空白脂质体。
2.2 DOX纳米脂质体的含量测定
2.2.1 检测波长的确定 采用UV法测定含量[7]。精密称取DOX原料药5.05 mg,置于5 mL量瓶中,加甲醇溶解并定容,制成质量浓度为1.01 mg/mL的DOX贮备液;取上述DOX贮备液适量,加甲醇稀释,制成质量浓度为8.08µg/mL的DOX供试品溶液。另取“2.1”项下空白脂质体适量,加甲醇破乳,加甲醇稀释100倍,即得空白脂质体供试品溶液。以甲醇为空白对照,取上述DOX供试品溶液、空白脂质体供试品溶液于200~400 nm波长范围内进行全波长扫描,详见图1。由图1可知,DOX供试品溶液的最大吸收波长为232 nm,而空白脂质体供试品溶液在232 nm波长处无吸收,表明空白辅料对测定无干扰,故选择检测波长为232 nm。
2.2.2 线性关系考察 精密量取“2.2.1”项下DOX贮备液,加PBS溶液稀释,制成质量浓度分别为1.01、4.04、8.08、12.12、16.16 µg/mL的系列线性关系工作溶液,取上述系列线性关系工作溶液适量,分别于232 nm波长处测定吸光度。以质量浓度(x,µg/mL)为横坐标、吸光度(y)为纵坐标进行线性回归,得DOX的回归方程为y=0.056 7x+0.014 9(r=0.999 7),结果表明,DOX检测质量浓度线性范围为1.01~16.16µg/mL。经方法学验证,精密度、稳定性、重复性均符合2015年版《中国药典》(四部)要求[8]。
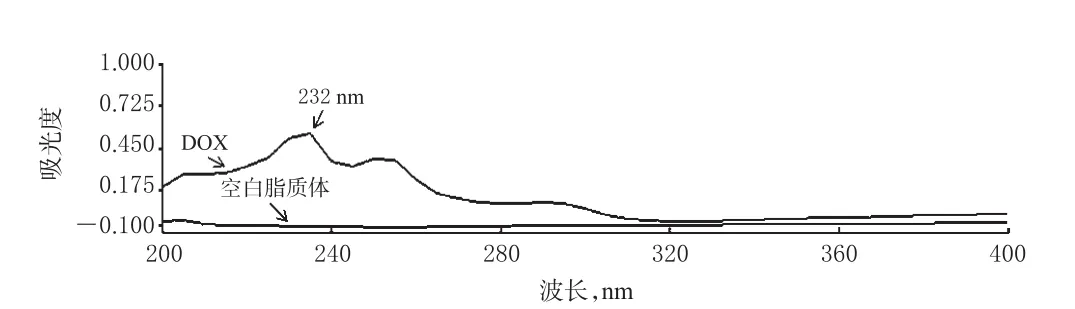
图1 紫外吸收光谱图Fig 1 UV absorption spectrum
2.3 包封率、载药量、粒径的测定
采用超滤离心法测定包封率和载药量[9-10]。精密量取“2.1”项下DOX纳米脂质体0.2 mL,加甲醇破乳并定容至5 mL,于232 nm波长处测定吸光度,记为A总。精密量取“2.1”项下DOX纳米脂质体1 mL,置于超滤管(30 kDa)中,以5 000 r/min离心20 min,滤过,取续滤液0.2 mL,加水定容至5 mL,于232 nm波长处测定吸光度,记为A游。将A总、A游按“2.2.2”项下回归方程计算DOX质量浓度,并按如下公式计算包封率和载药量。包封率(%)=(W总-W游)/W总×100%,载药量(%)=(W总-W游)/M总×100%(式中,W总表示总的药物质量,W游表示游离药物的质量,M总表示DOX纳米脂质体的总质量)。另取“2.1”项下DOX纳米脂质体适量,加超纯水稀释10倍,采用粒度分析仪测定粒径。
2.4 DOX纳米脂质体处方工艺优化
2.4.1 星点试验设计与结果 参考预试验结果及相关文献[11-13],选择以豆磷脂与药物质量比(X1,mg/mg)、豆磷脂与胆固醇质量比(X2,mg/mg)、超声时间(X3,min)为因素,以粒径(Y1,nm)、包封率(Y2,%)、载药量(Y3,%)为指标,采用3因素3水平试验方案。因素与水平见表1,试验方案与结果见表2。
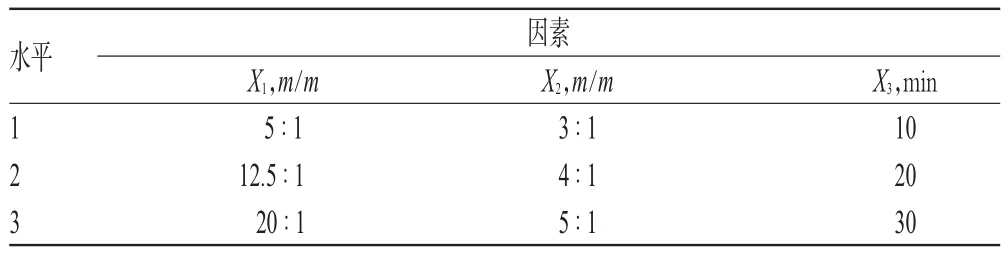
表1 因素与水平Tab 1 Factors and levels
2.4.2 模型拟合 采用SPSS 17.0软件对表2数据进行分析,得P=0.411(P>0.05),提示包封率在各组之间的差别相对较小(P>0.05)。因此,以粒径和载药量为指标,采用Design-expert 8.0.6软件进行多元二次多项回归拟合,得粒径和载药量对X1、X2、X3的数学回归模型。以粒径为指标时,Y1=215.30-123.90X1+13.82X2+13.13X3-33.07X1X2-25.38X1X3+1.23X2X3+77.49X12+5.09X22+2.94X32(r=0.985 4);以载药量为指标时,Y3=5.56-4.40X1+0.21X2-0.046X3+0.075X1X3-0.017X2X3+2.38X12-0.056X22-0.021X32(r=0.999 9)。r均大于0.9,提示模型设计的拟合效果及预测性均较好。对该模型进行方差分析,结果见表3。
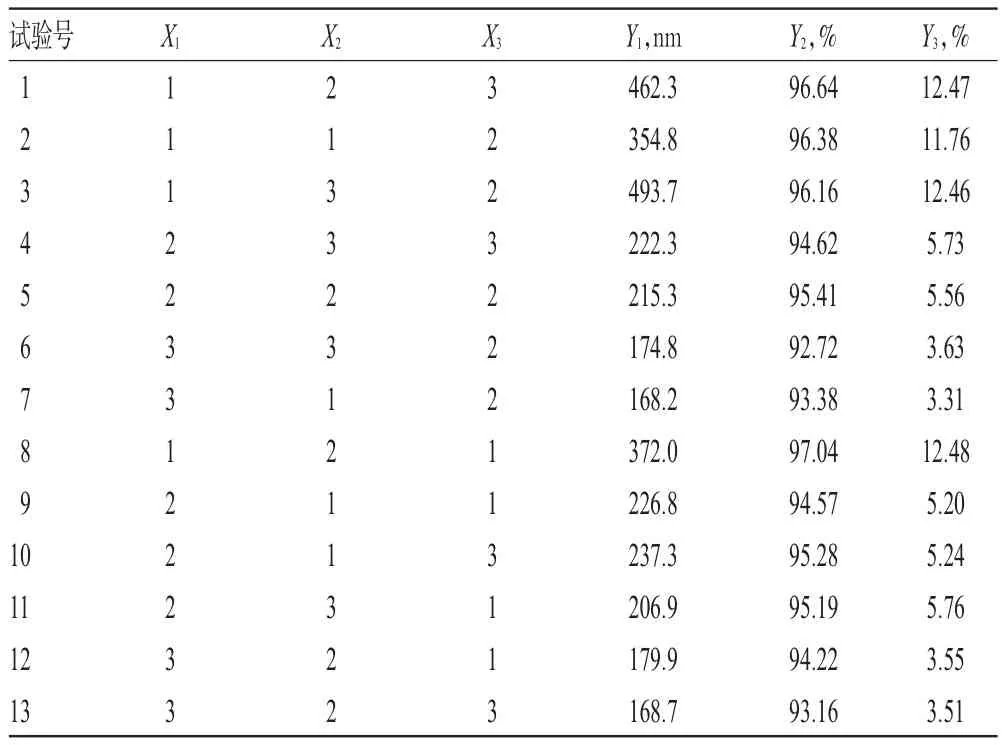
表2 试验方案与结果Tab 2 Experiment plan and results
2.4.3 各因素交互作用分析 采用Design-expert 8.0.6软件以豆磷脂与药物质量比(X1,mg/mg)、豆磷脂与胆固醇质量比(X2,mg/mg)、超声时间(X3,min)为因素,以粒径(Y1,nm)和载药量(Y3,%)为指标,绘制响应面图,详见图2。
由图2A可知,因素X1与X2交互作用显著,随着X1增大,粒径也随之增大;由图2B可知,因素X2与X3交互作用显著,随着X2的增大,粒径呈现先减小后增大的趋势;由图2C可知,因素X1与X2交互作用显著,随着X2的增大,载药量逐渐减小;由图2D可知,因素X1与X3交互作用显著,随着X1的增大,载药量也逐渐减小。
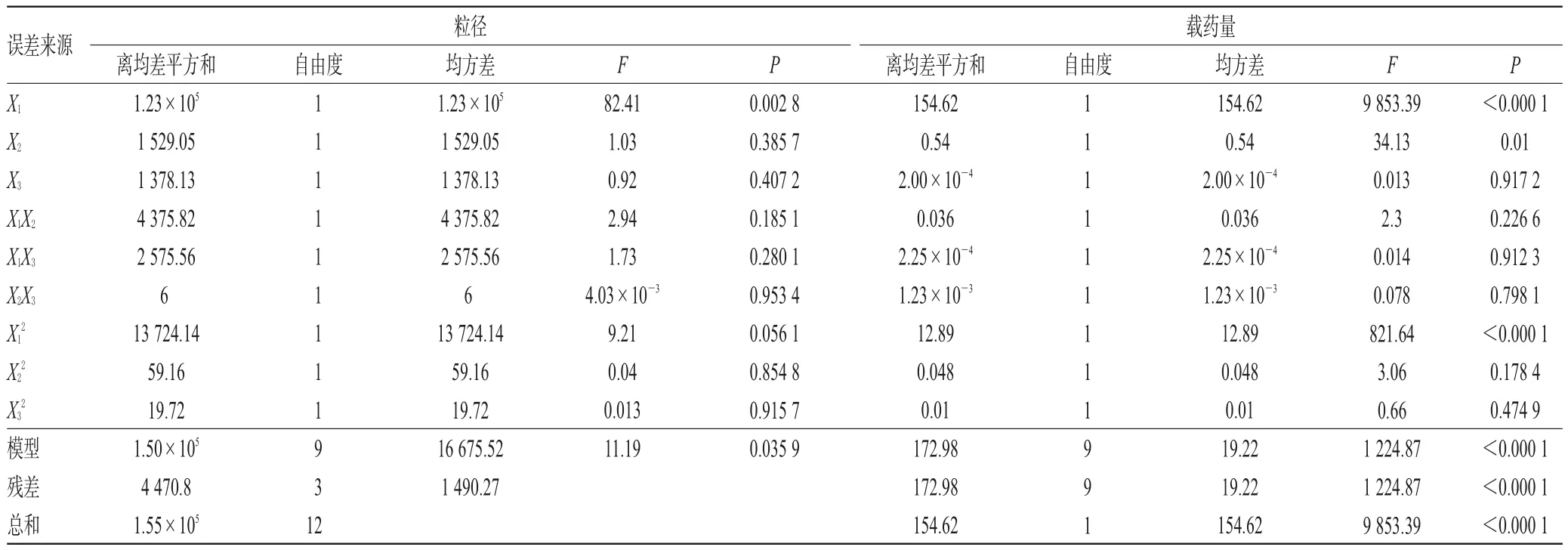
表3 方差分析结果Tab 3 Results of variance analysis
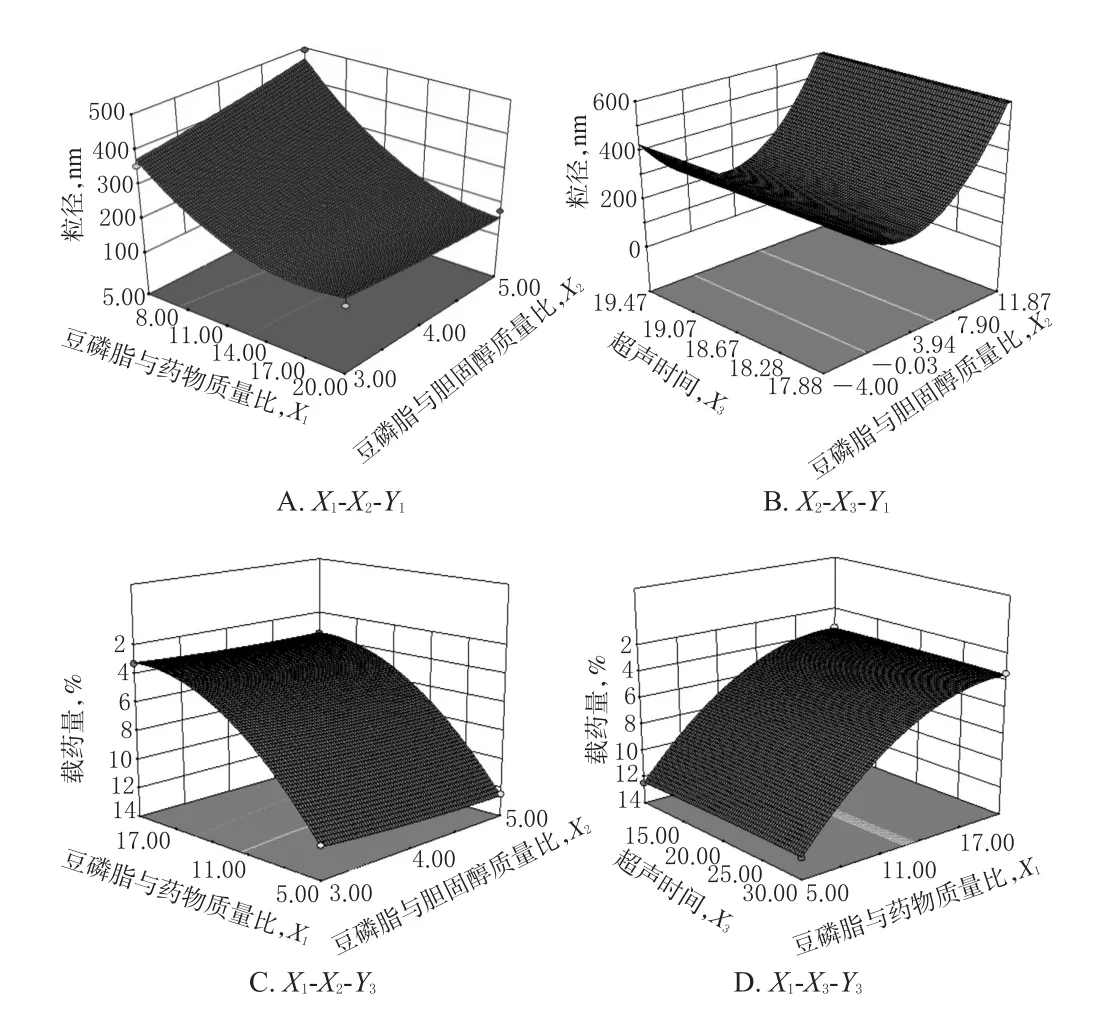
图2 各因素对粒径和载药量影响的响应面图Fig 2 Response surface plots of each factor to particle size and drug-loading amount
2.4.4 最优制备工艺的确定 基于Design-expert 8.0.6软件对所建模型进行参数最优分析,得最优制备工艺为豆磷脂与药物质量比13.30∶1(mg/mg)、豆磷脂与胆固醇质量比4.09∶1(mg/mg)、超声时间10 min,得到预测粒径为196.3 nm,载药量为10.68%。
2.4.5 验证试验 按上述最优制备工艺进行验证,平行制备3批DOX纳米脂质体,详见表4、图3。由表4、图3可知,实测值与预测值一致性良好,提示优化所得制备工艺简单、可行,其粒径符合正态分布。

表4 最优制备工艺验证结果Tab 4 Results of optimal preparation technology validation
2.5 DOX纳米脂质体的光热转换试验
参考相关文献进行DOX纳米脂质体的光热转换试验[14]。取“2.1”项下DOX纳米脂质体,加水稀释,制成纳米硫化铜质量浓度为0.1、0.2、0.5 mg/mL的纳米混悬液。分别取上述纳米混悬液3 mL,置于石英比色池中,采用激光器(2.5 w/cm2)照射(激发波长:808 nm),每30 s记录1次温度随时间的变化值,以水为对照组,以时间为横坐标、温度为纵坐标,采用OriginPro 8.5.1软件绘制光热转换曲线,详见图4。
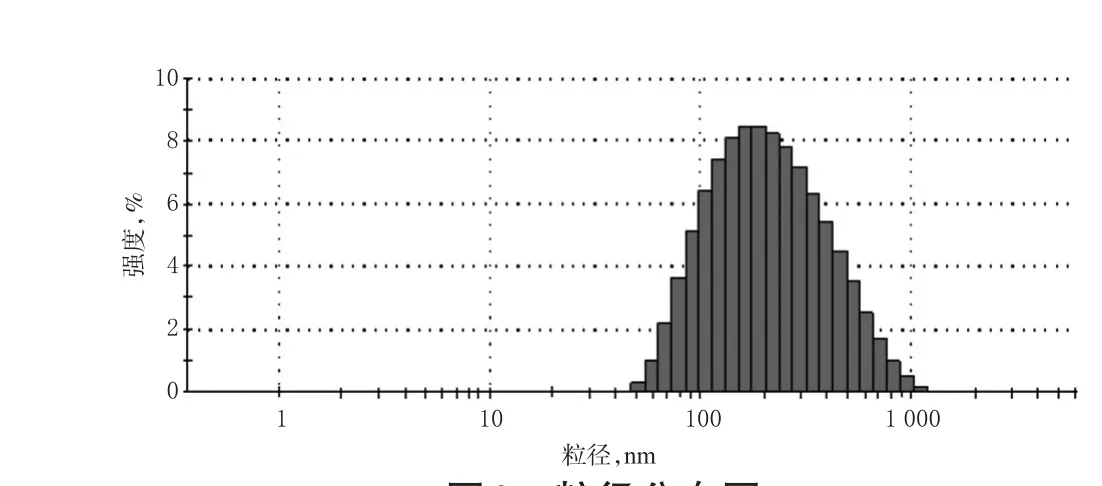
图3 粒径分布图Fig 3 Distribution of particle size
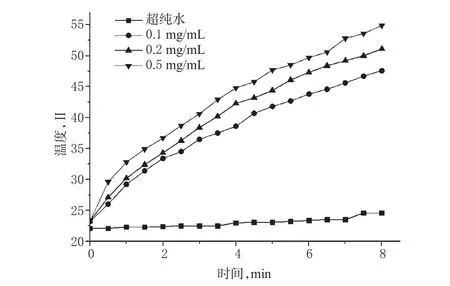
图4 光热转换曲线图Fig 4 Light heat transformation curve plot
由图4可知,含有纳米硫化铜不同质量浓度的DOX纳米脂质体在808 nm激光照射下,温度可随照射时间的延长明显上升,浓度越高温度上升越快。当照射时间为8 min时,纳米硫化铜质量浓度为0.1、0.2、0.5 mg/mL时的温度分别为47.6、51.1、54.9℃,此时超纯水温度基本不变,维持在24.6℃。提示,DOX纳米脂质体具有浓度和时间依赖性的光热转换效应,可结合近红外激光照射进行PTT治疗。
3 讨论
本课题以亲水性纳米硫化铜为光热转换剂,采用薄膜分散法制备了DOX纳米脂质体,试验中通过旋转减压蒸发,可有效避免纳米脂质体中有机溶剂的残留;此外磷脂易吸潮,在保存过程中应注意避潮,可将其放入真空袋中以保持干燥性。DOX是一种需要避光保存的药物[15],研究过程中需注意避光操作,且制得的DOX纳米脂质体也应避光保存。
本研究采用星点设计-响应面法优化了DOX纳米脂质体的制备工艺,优化后的最佳工艺为豆磷脂与药物质量比13.30∶1(mg/mg)、豆磷脂与胆固醇质量比4.09∶1(mg/mg)、超声时间10 min。按此优化工艺所得DOX纳米脂质体的粒径为(200.5±25.1)nm、载药量为(11.02±0.20)%,该工艺简单、可行。光热转换试验结果显示,DOX纳米脂质体具有浓度和时间依赖性的光热转换效应,这可为近红外光响应性肿瘤靶向递药载体的进一步研究提供参考。
综上所述,本研究所建含量测定方法简便、准确度较好,优化所得制备工艺简单、可行。
