人Autotaxin基因3个蛋白亚型的生物信息学比较分析*
2019-05-25潘薇薇谢海军
曹 睿 潘薇薇 赵 邑 谢海军
(山西省生物研究院有限公司 山西太原 030000)
0 引言
Autotaxin(ATX)首次在人的黑色素瘤细胞系A2058 中被发现[1],是一种自分泌活性因子,是血液中重要的酶,具有磷酸二酯酶活性,能催化溶血磷酰胆碱LPC 生成溶血磷脂酸(LPA),进一步激活脂类相关的G 蛋白偶联受体(LAPR),被归为磷酸二酯酶家族(ENPP1-ENPP7)[2]。Autotaxin 在许多肿瘤中均有异常表达情况,例如在黑色素瘤、甲状腺癌、乳腺癌、非小细胞肺癌、 肝癌、胰腺癌中均有异常增 高[3-8],由此 可见Autotaxin 在肿 瘤 的 发生和 发 展过程中有重要作用,被认为是肿瘤治疗中一个可能的靶点。
Autotaxin 基因位于人类8 号染色体长臂2 区4 带1 亚带2 次亚带 (8q24.12), 编码29 个外显子, 目前主流观点认为该基因选择性剪切产生3个蛋白亚型:ATX-α、ATX-β、ATX-γ, 也有科学家近期鉴定出其他的亚型:ATX-δ、ATX-ε[9]。 虽然这些亚型在结构上十分相似, 但具体的生理功能却有很大差异。 ATX-β,畸形癌亚型,即血浆中的lysoPLD,最初是从畸形癌细胞系克隆的,是最短、 也是最主要的ATX 亚型;ATX-α, 黑素瘤亚型;ATX-γ,脑特异的亚型,主要在少突胶质细胞中表达[10]。本文重点比较ATX-α、ATX-β、ATX-γ这3 个蛋白亚型在序列、二级结构、结构域、理化性质、跨膜区域等方面的异同,为进一步挖掘其生物学意义提供理论基础和研究思路。
1 材料与方法
1.1 序列来源 人Autotaxin 蛋白3 个亚型的fasta 数据来自NCBI 蛋白数据库,ATX-α、ATXβ、ATX-γ全长分别为915aa、863aa、888aa,GI 号分别为91823274、91823602、195947389。
1.2 方法
1)蛋白亚型的序列比对及二级结构对比采用ESPript 3.0[11]。 ESPript 软件能根据序列比对信息和蛋白质二级结构信息,将比对结果图形化。软件需要的序列比对结果为.aln 格式数据, 二级结构信息为.pdb 格式的数据。 其中.aln 格式的序列比对结果可通过Alignment By Muscle、ClustalX 等多种比对软件得出,参考序列的PDB 文件可通过PDB 网 站(http://www.rcsb.org/pdb/home/home.do)进行下载, 也可通过对目标蛋白进行3D 结构的预测获得。
2)结构域预测采用simple modular architecture research tool(SMART)[12]。 SMART 是蛋白结构预测和功能分析的工具集合。 可预测蛋白的一些二级结构,例如跨膜区(transmembrane segments)、复合螺旋区(coiled coil regions)、信号肽(signal peptides)、蛋白结构域(PFAM domains)等。 运行软件可直接用各个数据库蛋白的ID, 例如Uniprot/Ensembl ID/accession number(ACC)或直接使用蛋白质序列,本文使用的是蛋白序列。
3)理化性质分析采用ProtParam tool[13]。 Prot-Param 是一个可根据蛋白的Swiss-Prot/TrEMBL AC 编号、ID 号或序列进行理化性质分析的软件(本文使用的是蛋白序列), 可分析的理化性质包括相对分子量、理论PI 值、原子组成、半衰期、不稳定系数等。
4)亲疏水性分析采用ProtScale[13]。ProtScale 可根据蛋白的UniProtKB/Swiss-Prot 或UniProtKB/TrEMBL 的AC 编号、ID 号或序列进行疏水性区域的预测,本文使用蛋白序列直接进行预测。
5)跨膜结构预测采用TMHMM[14]。TMHMM 综合了跨膜区疏水性、电荷偏倚、螺旋长度和膜蛋白拓扑学限制等性质, 采用隐马氏模型(Hidden Markov Models),对跨膜区及膜内外区进行整体的预测。 TMHMM 是目前最好的进行跨膜区预测的软件, 尤其在区分可溶性蛋白和膜蛋白时准确性高,是判定一个蛋白是否为膜蛋白的首选软件,本文使用蛋白序列对3 个亚型的跨膜区域分别进行了预测。
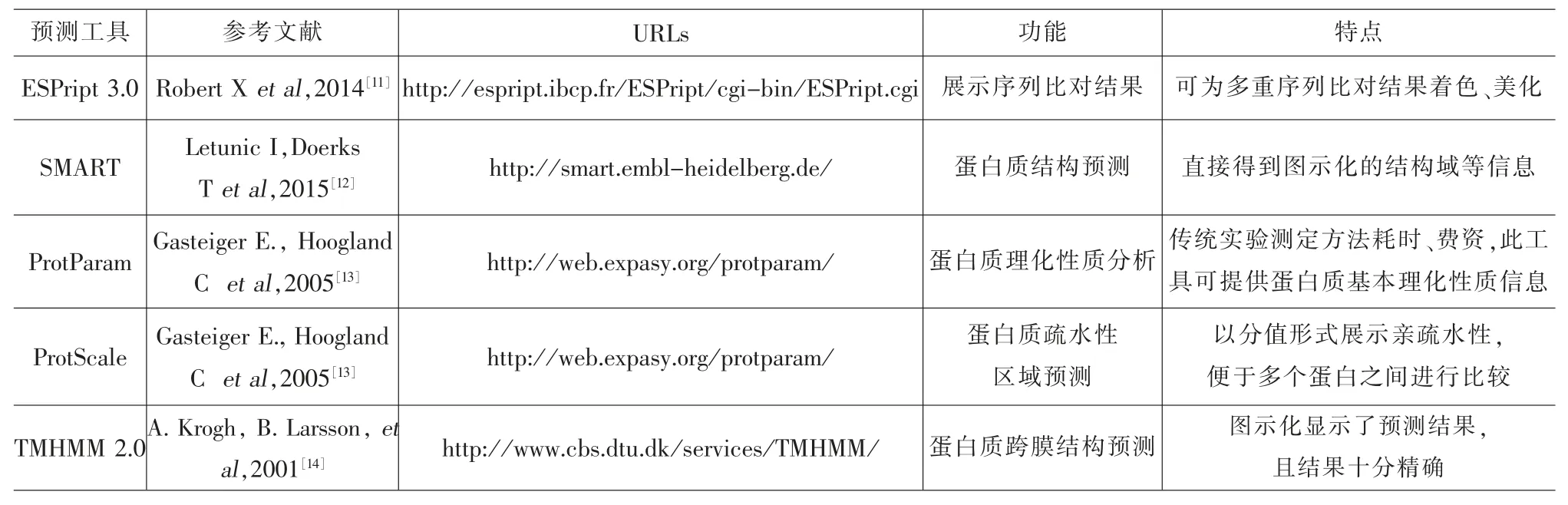
表1 预测工具软件简介
2 结果与分析
2.1 序列比对及二级结构对比结果 在进行序列比对时,本文采用ClustalX 多重序列比对软件,属于Clustal 系列工具之一,另外一个ClustalW 工具是命令行形式的界面,适合数量较多的批量序列比对,而ClustalX 是图形化界面,适用于习惯使用windows 操作系统的用户。 ATX-α、ATX-β、ATX-γ 3 个亚型的序列比对使用ClustalX,以ATX-β 的二级结构作为参考,3 个亚型序列及二级结构比对结果如图1 所示(本文附图见封四)。
从图1 显示的分析结果看,ATX-α 与ATXβ、ATX-γ 相比,从第323 个碱基开始,有一段52个碱基的插入,其二级结构为η 折叠,这段插入可能与ATX-α 定位到细胞外基质有 关[10],从后续的结构域预测及疏水性分析看, 此插入片段可能造成了ATX-α 与其他2 个亚型在结构域上及疏水性上的差异;ATX-γ 与ATX-α、ATX-β 相比,从第593 个碱基开始,有一段25 个碱基的插入,其结构为α 螺旋,其生物学作用未知,从后续的分析看, 此插入片段没有造成蛋白质结构域上的改变,但是从第590 个氨基酸开始,蛋白的疏水性与其他亚型产生了差异。
2.2 结构域预对比结果 利用SMART 及蛋白亚型序列文件, 预测出每个亚型的结构域类型及位置,比较结果如图2 所示。
从图2 比较结果看,ATX-α 与ATX-β、ATXγ 相比, 有一个300 bp 左右的Phosphodiest 结构域,而ATX-β、ATX-γ 是2 个较短的Phosphodiest结构域相连接, 造成这种差异的原因可能是因为ATX-α 在第323 处有一段52 个氨基酸的插入片段。 与此同时ATX-γ 第593 处开始的25 个氨基酸的插入片段则没有造成蛋白质结构域上的改变。 Phosphodiest 结构域的生物学作用是使得蛋白具有磷酸二酯酶活性。
3 个蛋白亚型的共同点是: 均具有1 个跨膜区域、2 个SO 结构域及1 个NUC 结构域(图3)。SO 结构域的生物学作用是使得蛋白具有类生长调节素B(Somatomedin B-like)的功能。 NUC 为非特异性内切酶作用区域。
2.3 理化性质对比结果 根据3 个亚型序列文件, 使用ProtParam 得出分子量、PI 值等理化性质结果,比较数据如表2。

表2 ATX 基因3 个蛋白亚型的理化性质分析结果
从表2 结果看,ATX-α、ATX-β 与ATX-γ 在原子组成、氨基酸数目、分子量等各种理化性质上均有差异, 尤其在具有重要生物学意义的PI 值、不稳定系数、 亲水性上均具有较大差异。 总体上ATX-α 与ATX-β 及ATX-γ 的差异较大,ATXβ、ATX-γ 相对比较相似。
3 个蛋白亚型的相同之处主要表现在: 具有相同的半衰期;均具有较高的不稳定系数,均属于不稳定的蛋白质,从数值的大小看,3 个蛋白亚型的不稳定性ATX-α>ATX-β>ATX-γ;均具有较高的脂肪系数,脂肪系数反应蛋白的热稳定性,从数值大小看,ATX-β>ATX-γ>ATX-α。
2.4 亲疏水性对比结果 根据序列信息, 使用ProtScale 软件得到每个亚型每个位点的疏水性值,根据每个位点的疏水性值绘制比较结果图4。
根据图4 中不同颜色曲线的重叠程度看,蓝色代表的ATX-α 与其他2 个亚型差别较大,而ATX-β 与ATX-γ 相似性较高, 这一点从3 个蛋白亚型的平均亲水性分值也可以得到佐证, 分别是:-0.575,-0.495,-0.541。 从差异开始的位置看,ATX-α 与其他2 个亚型的差异从第320 个氨基酸开始,ATX-β 与ATX-γ 的差异从第590 个氨基酸开始, 这一点可以从3 个蛋白亚型序列差异上得到佐证:ATX-α 从第323 个氨基酸开始,有一段52 个氨基酸的插入;ATX-γ 从第593 个氨基酸开始,有一段25 个氨基酸的插入。
2.5 跨膜结构对比结果 TMHMM 软件根据3个蛋白亚型的序列信息得出跨膜位置信息, 具体比较结果如表3。
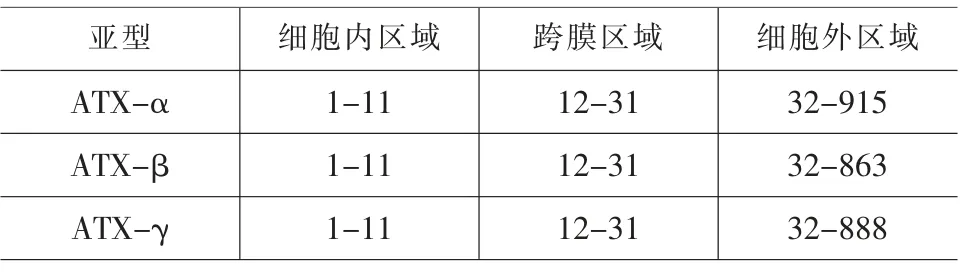
表3 ATX 基因3 个蛋白亚型的跨膜区域结果
首先,3 个亚型都有跨膜区域,表明3 个蛋白都是跨膜蛋白;其次,从跨膜区域看,3 个蛋白亚型的跨膜位置没有区别,高度一致,可以推测使得3 个蛋白亚型具有不同功能的区域主要是从3 个蛋白的第32 个氨基酸开始。
3 讨论与结论
人类大约有2~3 万个基因,但如今研究者已知的人类细胞中不同蛋白质的数量或许远超于10 万个。由相同基因编码产生的不同蛋白亚型在组织和细胞中或许发挥完全不同的生物学功能,然而这些蛋白质亚基在结构上却非常相似[15]。 通过关注细胞、组织或器官中的癌症相关的蛋白质亚型,对于开发新型药物提供了一定的思路。ATX 基因在肿瘤的发生和发展过程中有重要作用,本研究对于ATX基因3 个蛋白亚型的分析,对于深入理解该基因的生物学功能等多方面研究具有一定的帮助。
本研究从序列、二级结构、结构域、理化性质、亲疏水性、跨膜结构方面分析了ATX 基因3 个蛋白亚型的异同。 上文已经从横向各个角度详细分析了3 个亚型的异同,纵观各方面的差异,会发现这些异同是有紧密联系的。例如,在序列上的差异直接导致二级结构、结构域、理化性质、亲疏水性方面的差异。具体分析可以看到,ATX-α 从第323处开始的一个长度为52 个氨基酸的插入片段,直接造成从第320 个位置开始亲疏水性发生改变,且可能导致2 个较短的Phosphodiest 结构域连接成一个较长的结构域。 ATX-γ 从第593 处开始的一个长度为25 个氨基酸的插入片段,直接造成从第590 个位置开始亲疏水性发生改变, 但没有引起结构域的变化。 与此同时,引起一个猜测,氨基酸序列上的变化是否导致蛋白质从变化位置前3位开始发生亲疏水性改变,这一猜测有待验证。
