不同实验条件对锰矿法制备介孔纳米四氧化三锰性能的影响
2019-05-21罗绍华辛海霞牟文宁翟玉春
滕 飞,罗绍华,辛海霞,王 庆,康 雪,牟文宁,翟玉春
(1.东北大学冶金学院,沈阳 110819;2.东北大学秦皇岛分校资源与材料学院,秦皇岛 066004;3.秦皇岛市资源清洁转化与高效利用重点实验室,秦皇岛 066004)
1 引 言
过渡金属纳米氧化物可以表现出比较特殊的电学、光学和磁学性质,因此在很多方面有着比较重要的应用[1]。锰是一种过渡金属元素,Mn3O4是锰的稳定氧化物之一[2],在催化、磁性材料、防腐材料、分子吸附、电化学以及空气净化等领域存在着广泛的应用价值[3]。高纯度、高比表面积四氧化三锰在作为电子专用材料曾被国家发展计划委员会和科学技术部列为当前优先支持发展的高技术产业,是国家鼓励优先发展的高新技术产品[4]。近年来研究表明,由于Mn3O4和LiMn2O4都是尖晶石结构,用 Mn3O4合成LiMn2O4的过程中不存在剧烈的结构变化[5],更易合成性能优异的LiMn2O4[6],因此,四氧化三锰成为非常具有发展前景的锂离子电池正极材料原料之一[7]。比表面积大、粒径小,纯度高的 Mn3O4,其更能满足 LiMn2O4合成中对原料的特殊要求[5]。因此,能够研究制备出高纯度、粒径小及高比表面积的四氧化三锰产品具有重要的意义。
近年来,随着人们对四氧化三锰研究的深入,高品质四氧化三锰的制备及性质引起学术界和工业上的高度重视[8]。Mn3O4的制备方法有很多种,按所使用的锰原料的不同分为:金属锰粉(片)悬浮液氧化法、高价锰氧化物法、二价锰盐+二氧化锰法、电解法、二价锰盐氧化法、锰矿法[9-12]。金属锰法工艺成熟、产量高、污染小,但原料来源贵,生产成本高,产品比表面积较小,含有硒,这些制约了Mn3O4满足某些特定领域的需求[4,13]。高价锰氧化物法制备过程简单,但样品颗粒较大,比表面积小,且对原料要求高,不适合工业化生产[5]。二价锰盐+二氧化锰法是将MnO2微粉均匀分散在含有锰盐的水溶液中,然后在密闭的情况下滴加碱液,调节pH大于7并持续保温搅拌一定时间,最后过滤、洗涤滤饼,制得单相Mn3O4产品[14]。电解法工艺过程较复杂,所需时间较长,槽产量较低,生产成本较高,因此限制了它的实际应用[10]。二价锰盐氧化法分为干法、湿法、液相法联合热分解法,二价锰盐主要有碳酸锰、硫酸锰、氯化锰、硝酸锰、乙酸锰。干法是焙烧二价锰盐制备四氧化三锰。湿法是利用二价锰盐溶液在碱性条件下通空气或氧气将二价锰氧化生成Mn3O4。它使用的主要原料为MnSO4溶液和氨水。此法成本低廉,产品比表面积大、表面活性高,但是产品中硫含量高,很难降低[4,13]。锰矿法是二价锰盐氧化法的拓展应用,用硫酸将锰矿溶解后制得高纯硫酸锰溶液,碱化沉淀,中间产物经氧化、洗涤和烘干获得四氧化三锰产品。由于该法使用的主要原料为锰矿、硫酸和氨水,来源广泛,容易获得,市场价格稳定,锰矿法具有比锰盐法更大的经济优势,产品比表面积大,不含硒、铬,被认为是一种最有发展前途的方法,受到国内外化工行业的高度重视。目前该方法的研究和报道还很少,值得我们进一步研究[15]。
本文就是用简单易行,成本低廉的锰矿法,以软锰矿硫酸焙烧熟料溶出液、氨水为原料,通空气氧化制备出高比表面积、具有介孔结构的纳米四氧化三锰产品。
2 实 验
2.1 试剂与仪器
主要实验试剂:硫酸锰溶出液;氨水,乙醇,硫酸铵,聚乙二醇均为分析纯;实验用水为去离子水。
实验仪器:BT100-2J蠕动泵,DF-101S集热式恒温加热磁力搅拌器,CT-101充氧泵,DZF-6050真空干燥箱,SHB-3循环水式多用真空泵,SK1200H-J超声波清洗器,AL104/01电子天平,RigakuSmartLabX射线衍射仪,Zeiss Supra 55扫描电子显微镜,SSA-4300孔隙比表面仪。
2.2 实验方法
2.2.1 两步法(a、b、c、d、e、g)
将100 mL 硫酸锰溶出液与一定量NH3·H2O(1∶9)反应,控制滴加速度为2.5 mL/min, 反应温度为30 ℃,搅拌速度为300 r/min。反应结束后,抽滤,并使用去离子水淋洗滤饼三次,置于烘箱中在60 ℃干燥6 h,得到中间产物。将得到的中间产物移置于烧杯中,加入200 mL去离子水,调浆,控制温度60 ℃,搅拌速度200 r/min下通空气氧化4 h,抽滤、洗涤后,将滤饼置于烘箱中于120 ℃干燥4 h。其中样品a是将NH3·H2O加到MnSO4中;样品b是将MnSO4加到NH3·H2O中;样品c 是MnSO4加到 NH3·H2O中,氧化时加少许乙醇分散;样品d 是MnSO4加到 NH3·H2O中,氧化时加少量硫酸铵稳定溶液电位;样品e 是MnSO4加到 NH3·H2O中,沉淀结束后超声10 min,氧化时加少量硫酸铵稳定溶液电位;样品g是MnSO4加到 NH3·H2O中,沉淀时加10%表面活性剂。
2.2.2 一步法(f)
将一定量NH3·H2O(1∶9)水浴加热到60 ℃后,控制搅拌速度为200 r/min的同时以2.5 mL/min的滴加速度向氨水溶液中滴加100 mL硫酸锰溶出液,并通空气氧化4 h,结束后超声10 min,抽滤、洗涤后,将滤饼置于烘箱中于120 ℃干燥4 h。
2.3 实验原理
本实验用氨水沉淀硫酸锰溶液中的锰,以空气为氧化剂将中间产物氧化为四氧化三锰。涉及的主要化学反应如下[7]:
MnSO4+2NH3·H2O=Mn(OH)2+(NH4)2SO4
(1)
2MnSO4+2NH3·H2O=Mn2(OH)2SO4+(NH4)2SO4
(2)
6Mn(OH)2+O2=2Mn3O4+6H2O
(3)
(4)
3Mn2(OH)2SO4+O2+6NH3·H2O= Mn3O4+6H2O+3(NH4)2SO4
(5)
3 结果与讨论
3.1 不同制备条件对Mn3O4物相的影响
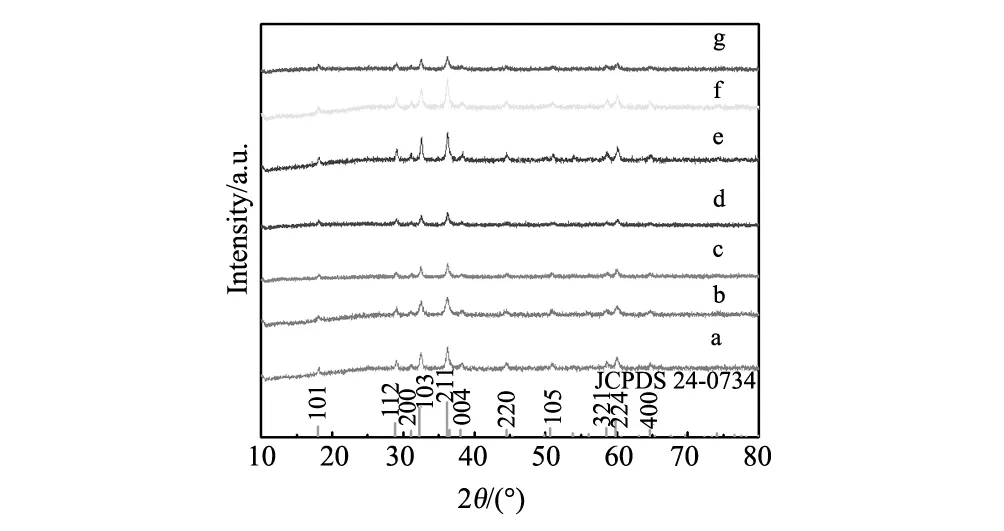
图1 不同条件下制备Mn3O4产物的XRD图Fig.1 XRD patterns of the Mn3O4obtainedunder different experimental conditions
图1为不同条件下制备Mn3O4产物的XRD图与标准图谱的对比,从图谱可知,不同条件下制备出的Mn3O4产物的衍射峰均与四氧化三锰标准卡片(JCPDS 24-0734)密切吻合,且无杂峰,说明所得产物为单一的四氧化三锰,属四方晶系尖晶石结构,其空间点群为I41/amd(141),其晶胞参数为a=b=0.5762 nm,c=0.9469 nm[16]。同时说明不同的实验条件对所得产物的物相组成没有明显影响。但图谱中衍射峰的强度及明显度e,f>a,b>c,d,g,说明不同的实验条件对所得产物的结晶度有明显影响。经过超声处理的样品结晶度更好。
3.2 不同制备条件对Mn3O4形貌的影响
图2是不同条件下制备Mn3O4颗粒的SEM图,从图中可以看出,a和f样品均为球状纳米级颗粒,粒径大小均匀,大多数颗粒尺寸为50 nm到至100 nm,b样品除球状颗粒外,出现了细棒状形貌,球状颗粒较小,大部分粒径小于50 nm,细棒状无序杂乱地排列,与球状颗粒相互交织在一起,形成树枝状结构。说明不同的滴加方式会影响产物的形貌。这可能是由于反应体系中硫酸锰和氨水的浓度不同或PH值的不同的缘故,将氨水逐滴加入硫酸锰溶液时,锰离子浓度较高,氨水浓度较低,且反应开始时由硫酸焙烧软锰矿得到的硫酸锰溶液的pH值约为2;而将硫酸锰反加到氨水中时,反应体系中锰离子浓度较低,氨水浓度较高,反应开始时1∶9氨水溶液的PH值约为12~13。相比样品b,加入少许乙醇的样品c呈现葡萄状结构,纳米棒起支撑作用,说明加入的少许乙醇起到了一定的分散作用。样品d相比c细棒状在一定程度上出现破坏,变成较短的纳米棒。样品g相比c细棒状和纳米球均出现一定程度的破损,说明添加少量添加剂和表面活性剂均会改变产物的形貌。氧化过程中加入表面活性剂聚乙二醇作为软膜版,有效降低纳米粒子的高表面能,防止纳米颗粒间的相互团聚,起到一定的分散作用[17]。样品e相比d大小均匀,表面光滑。这一点从f样品上也能体现,说明超声能增强样品结晶度,这与XRD分析结果一致。

图2 不同条件下制备Mn3O4产物的SEM图Fig.2 SEM images of the Mn3O4obtained under different experimental conditions
3.3 不同制备条件对Mn3O4比表面积及孔结构的影响
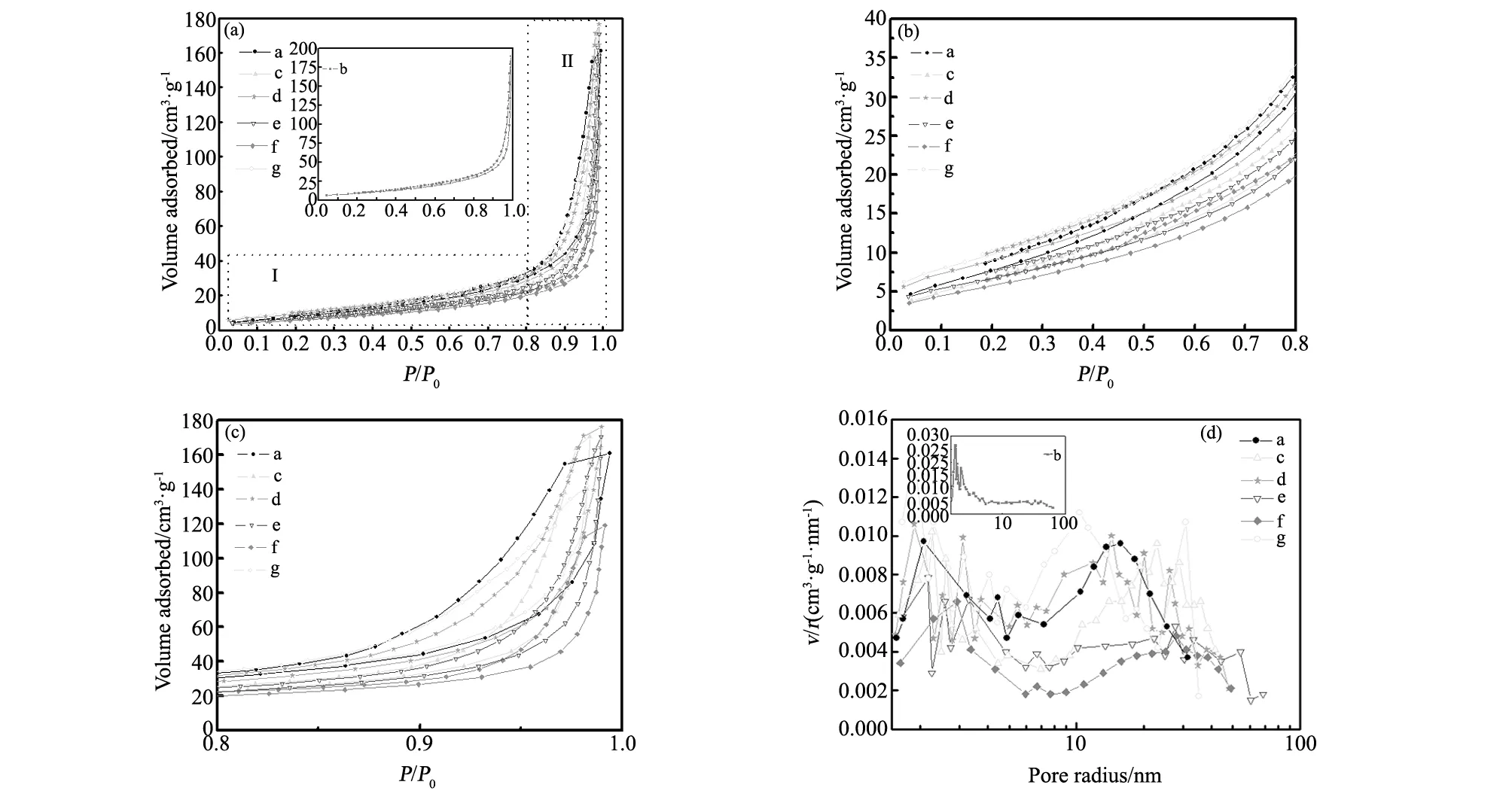
图3 不同条件下制备Mn3O4产物的N2吸附-脱附等温线及孔径分布图Fig.3 Nitrogen adsorption-desorption isotherms and pore size distributionof the Mn3O4obtained under different experimental conditions
通过Brunauer-Emmett-Teller(BET)测量进一步研究了不同条件下制备Mn3O4产物的比表面积和孔径分布。图3(a)为四氧化三锰样品的N2吸附-脱附曲线,图3(b)和图3(c)分别为图3(a)局部放大图,分别对应I区域和II区域。从图3中可以看出,氮气吸附-脱附等温线存在陡峭狭窄回滞环,为典型的H1滞后回线,说明所制备的Mn3O4产物具有介孔结构[18]。a~g样品的吸附-脱附曲线形状无明显差异,说明制备条件的改变并未改变孔结构,只改变孔的数量[19]。表1列举了根据BET方程计算得出的a~g样品的比表面积,表中数值均高于HG/T2835-1997优等品的质量标准(10~20 m2·g-1)[20]。所得样品的比表面大小顺序为b>g>d>a>c>e>f。b样品比表面积高于其他样品,为35.05 m2/g,这从图3(a)中也可以体现,这可能是b样品纳米棒与纳米球颗粒排列较紧密,互相交错,缝隙较多,颗粒较小的缘故,这与SEM结果一致。
基于BJH方法计算出的Mn3O4产物孔径分布图如图3(d)所示,表明所制备出的Mn3O4颗粒具有较宽的孔径分布,所制备样品的孔径分布相似,绝大部分孔径低于50 nm,且孔径集中在2~3 nm和10~30 nm之间,其中样品b孔径更小,主要分布在5 nm以下,这明显是介孔材料的特点,这与比表面积值和SEM结果具有一致性。结果表明,不同的实验条件可以调节Mn3O4产物的孔体积和比表面积[19]。

表1 不同条件下制备Mn3O4产物的比表面积Table 1 Specific surface area of the Mn3O4obtained under different experimental conditions
4 结 论
以软锰矿硫酸焙烧熟料溶出液为原料、采用碱化沉淀-空气氧化法得到四方尖晶石结构、单一物相、高比表面积、具有介孔结构的纳米级四氧化三锰。不同的实验条件对所得产物的物相组成没有明显影响,但经过超声处理的样品结晶度更好;不同的实验条件对Mn3O4的形貌有较大影响,但所得产物均为纳米级四氧化三锰;不同的实验条件可以改变Mn3O4产物的孔体积或比表面积,但并未改变孔结构。未加任何添加剂,MnSO4反加到 NH3·H2O中的沉淀-氧化两步法时所得四氧化三锰产物由球状颗粒和细棒状组成,球状颗粒的粒径最小,大部分小于50 nm,比表面积最大,为35.05 m2/g。
