静脉注射环磷酰胺对新西兰兔胚胎和胎仔的发育毒性研究
2019-05-16龚英菲曾现欢赵维俊左俊涛朱钟凯王湛博
龚英菲 曾现欢 赵维俊 左俊涛 朱钟凯 王湛博 刘 伟 王 昀 杨 勇
(中国药科大学新药安全评价研究中心,南京 211198)
生殖毒性试验的目的是通过动物试验反映受试物对哺乳动物生殖功能和发育过程的影响。胚胎-胎仔发育毒性试验(即Ⅱ段生殖毒性试验) 是评价新药生殖毒性的首选方法之一。妊娠动物自胚胎着床至硬腭闭合给药,观察受试物对妊娠动物母体、胚胎和胎仔发育的影响,包括胚胎胎仔的死亡、生长改变和结构变化等,为母体孕期接触新药可能对胎儿造成的影响提供临床前的试验依据[1]。环磷酰胺(Cyclophosphamide)是一种氮芥类烷化剂,对多种肿瘤具有明显的抑制作用,对增殖细胞群的各期均有杀伤作用,具有较强的致畸、致癌和致突变作用。研究表明环磷酰胺可造成精子缺乏、精子畸形、停经等生殖系统毒性,妊娠初期给予可致畸胎。但目前生殖毒性研究主要集中于大鼠和小鼠[2-6],用于兔生殖毒性研究很少。根据国家食品药品监督管理局2006 年发布的《药物生殖毒性研究技术指导原则》,兔是胚胎-胎仔发育毒性研究中优先选用的非啮齿类动物,但II 段生殖毒性试验中关于兔阳性药物的致畸背景资料较少[7]。因此,选用阳性对照物并确定相关的致畸作用对新开展此项试验具有实际指导意义[8]。
1 材料与方法
1.1 药品和试剂
环磷酰胺(批号P01637) 购自阿达玛斯贝塔(上海)化学试剂有限公司,白色结晶或结晶性粉末,临用前用生理盐水配制;茜素红(批号20110315) 购自天津市化学试剂研究所,褐色固体粉末;硫化铵(批号13071020653) 购自南京化学试剂有限公司,白色固体结晶;氢氧化钾(批号20131230) 购自上海凌峰化学试剂有限公司,白色固体粉末;丙三醇(批号20140118) 购自江苏强盛功能化学股份有限公司,无色澄清溶液;乙醇(批号20140821) 购自国药集团化学试剂有限公司,无色澄清溶液。
1.2 动物
新西兰兔购自青岛康大生物科技有限公司,普通级,动物生产许可证SCXK (鲁) 2012-0005,饲养于中国药科大学新药安全评价研究中心,普通级动物房,实验动物使用许可证SCXK (苏) 2013-0013,温度21~25 ℃,相对湿度44%~68%,光照12 h; 单只饲养于不锈钢笼内。饲料为北京科澳协力饲料有限公司生产的兔生长繁殖饲料,饮用水为CENTRA-R200净化系统净化处理的实验动物饮用水,笼具和托盘每日清洁更换。
1.3 仪器
体式显微镜,型号(SZX7),Olympus;正置生物显微镜,型号(BX43),Olympus; 电子天平,型号(QUINTIX224-1CN,QUINTIX1102-1CN, PRACTUM2102- 1CN);赛多利斯;游标卡尺,型号(BZ),成都成量工具集团有限公司。
1.4 方法
1.4.1动物分组与给药方案:购买4~5月龄的孕兔40只,交配成功日计为 GD0,并按照体质量均衡原则随机分为对照组和环磷酰胺组。最终纳入统计对照组(0.9%氯化钠注射液,i.v)16只,环磷酰胺组(30 mg/kg,i.v.)17只。
1.4.2观察和检测:试验期间进行一般临床症状观察,体质量和摄食量的测定。GD28对孕兔进行过量CO2安乐死,剖宫称取怀孕子宫总质量、子宫、胎盘、卵巢及脑质量。记录黄体数、死胎数、活胎数、吸收胎数、着床腺数,并计算子宫、卵巢脏体、脏脑系数。取出胎仔,存活胎仔自腹腔注射戊巴比妥钠溶液实施安乐死后记录胎仔性别、胎仔质量、顶臀长、尾长及外观。全部胎仔进行内脏和骨骼检查,其中除心脏、脑、肾脏用4%甲醛溶液固定后检查,其余内脏当即检查,骨骼标本用95%的乙醇固定和茜素红染色后检查。胎仔外观畸形检查包括头部、四肢、躯干、尾部和肛门。胎仔内脏畸形检查包括有无腭裂、脑水肿、肾积水,眼球是否正常,心、肝、脾、肺、肾和子宫等脏器大小和位置是否异常等。胎仔骨骼畸形检查包括骨化程度、有无胸骨节缺失、骨化不全、胸骨节错位、多肋、少肋、肋骨分叉、肋融合、波状肋等。
1.5 统计方法
采用SPSS 20.0软件进行统计分析。计量资料用均值±标准差(x±s)来表示,先进行方差齐性检验,如果采用P>0.05再进行t检验,如果P<0.05进行秩和检验;有吸收胎的孕兔百分率、有死胎的孕兔百分率、妊娠率、窝别外观(内脏、骨骼)畸形率和窝别内脏(骨骼)变异率等采用百分率表示,采用Fisher确切概率法进行分析。P<0.05确认为有统计学意义。
2 结果
2.1 对一般临床症状观察、体质量和摄食量的影响
一般临床症状观察未见明显异常。GD14~16孕兔的体质量增长环磷酰胺组较对照组明显降低(P<0.05),给药后环磷酰胺组的摄食量较对照组出现一过性的降低(GD11P<0.05)。
2.2 对孕兔生殖功能及胚胎形成的影响
与对照组相比,孕兔终末体质量(GD28)、怀孕子宫质量、胎盘质量、子宫质量、卵巢质量及其脏体和脏脑系数均未见明显差异。
环磷酰胺组较对照组着床后丢失率提高近一倍。黄体数、死胎数、着床腺数、活胎数、吸收胎数、总丢失率无明显异常。详见下表1:

表1 环磷酰胺对孕兔生殖功能及胚胎形成的影响Table 1 The effect of Cyclophosphamide on rabitreproduxtion and embryo-fetal development
2.3 对胎仔外观的影响
与对照组相比,胎仔总质量,均质量分别降低9.62%和16.47%;胎仔身长、尾长分别减少8.00%和17.55%(P<0.05);腭裂畸形率(32.95%)明显高于对照组,与对照组比差异有统计学意义(P<0.05),且窝别的腭裂畸形率为73.33%,与对照组比有统计学差异(P<0.05)。详见下表2:
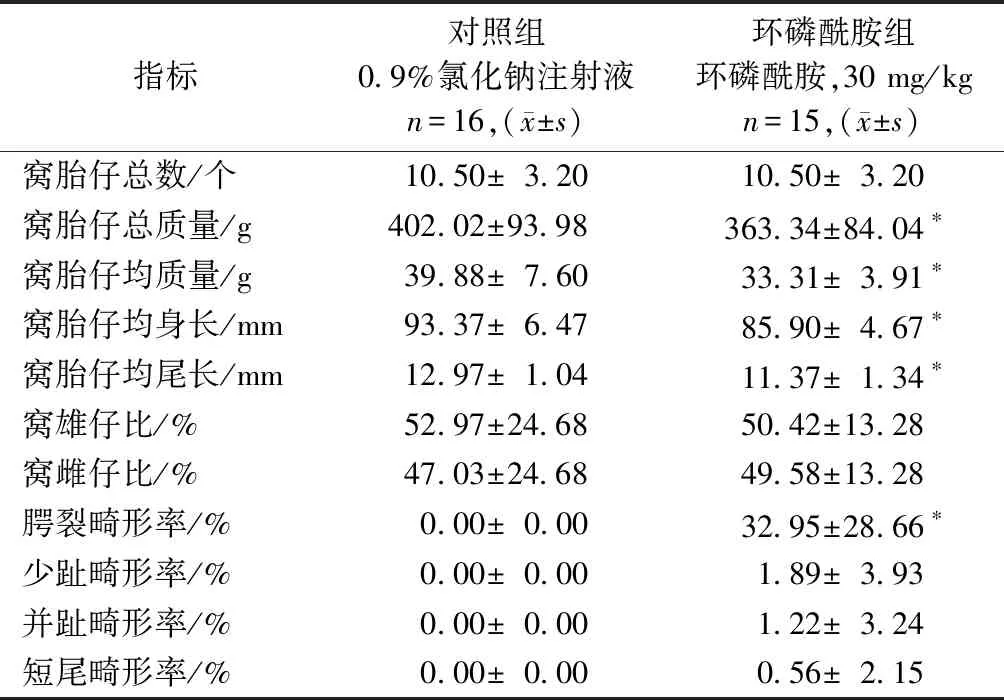
表2 环磷酰胺对胎仔外观的影响Table 2 The effect of Cyclophosphamide onappearance of fetal rabits
注:*表示与对照组比P<0.05
Note:*Compared with the control groupP<0.05
2.4 对胎仔内脏的影响
环磷酰胺组:胎仔的窝别内脏变异率为80.00%,与对照组相比,差异具有统计学意义(P<0.05),主要变异类型为左心室偏大;胎仔的窝别内脏畸形率为73.33%,与对照组相比,差异具有统计学意义(P<0.05),主要畸变类型为肾皮质髓质分界不清。详见下表3:

表3 环磷酰胺对胎仔内脏检查指标的影响Table 3 The effect of Cyclophosphamide on fetal organs
注:*表示与对照组比P<0.05
Note:*Compared with the control groupP<0.05
2.5 对胎仔骨骼的影响
环磷酰胺组:除胸椎、肋骨骨化数与对照组相比有显著性差异(P<0.05)外,枕骨骨化程度、其他骨化数及胎仔窝别骨骼变异率差异均无统计学意义。胎仔骨骼畸变率为86.67%,与对照组相比,差异具有统计学意义(P<0.05)。详见下表4:

表4 环磷酰胺对胎仔骨骼检查指标的影响Table 4 The effect of Cyclophosphamide on fetal skeleton
注:*表示与对照组比P<0.05
Note:*Compared with the control groupP<0.05
3 讨论
本研究中,以环磷酰胺作为阳性药物,采用静脉注射途径、给药剂量30 mg/kg、给药时间GD11,观察环磷酰胺对新西兰兔胎仔畸形的影响以确定此方法可行程度。
环磷酰胺作为广谱的抗癌药物,药物的不良反应也较突出,特别是在生殖方面。环磷酰胺能透过血胎屏障和血乳屏障,所以临床上妊娠妇女禁用,哺乳期妇女用药时必须停止哺乳。
不同给药途径的相对吸收率不同,一般依次为静脉注射>经口给药>皮下注射[9]。有报道给兔GD6~20连续灌胃给予环磷酰胺18 mg/kg畸形比例适当,胎仔生长发育也受到明显的影响[10]。皮下注射环磷酰胺畸形比例较高,胎仔的体格和生长发育会受到明显影响,吸收胎数量较多,导致可供进行检查的胎仔数量略少[8],但本研究前期预实验中,新西兰兔GD6~20进行连续经口灌胃给予环磷酰胺18 mg/kg·d-1会导致孕兔出现流产,亦会导致检查的胎仔数量减少。所以正式试验的过程中选择静脉注射,耳缘静脉注射给药操作较为简单且对动物造成的应激性较小,静脉注射吸收率高从而使用环磷酰胺较少。
本研究中发现给药后环磷酰胺组较对照组体质量和摄食量有一定的降低,说明本试验采用的30 mg/kg环磷酰胺在试验过程中对孕兔产生了一定的毒副作用,为一过性的。如果剂量加大或者是给药频次增加,可能会导致毒性太大,对胎仔产生不可逆的影响,致使胎仔出现死亡或者流产,会导致样本缺失,无法分析。从胎仔的外观上来看,环磷酰胺组和对照组窝胎仔总数没有明显差异,但环磷酰胺组胎仔的均质量、身长、尾长均低于对照组,四肢的畸变率明显高于对照组。对胎仔内脏进行检查,环磷酰胺组的变异率和畸形率明显高于对照组。对胎仔的骨骼进行检查,环磷酰胺组骨骼的畸变种类和数目都明显高于对照组。有报道雌性大鼠GD7~11 静脉注射环磷酰胺5 mg/kg·d-1,GD20剖取胎仔,发现对中轴骨骼畸形的诱导具有阶段和部位特异性。本研究采取的GD11亦处于中轴骨骼发生畸形的敏感期[11]。本研究中环磷酰胺GD11 给药组骨骼畸形的比例为86.67%,基本全部集中于中轴骨骼。环磷酰胺作用机理体内被肝脏或肿瘤内存在的过量磷酰胺酶或磷酸酶水解变成活化的磷酰胺氮芥与DNA发生交叉联结,抑制DNA的合成,特别是G2期(DNA合成后期),干扰RNA的功能,从而导致胎仔发育迟缓,外观、内脏、骨骼的畸变。环磷酰胺还会使T细胞和B细胞的绝对数目减少,从而影响免疫系统的发育[12]。综上所述可知我们采用30 mg/kg环磷酰胺在GD11给予孕兔,对胎仔产生的畸变种类较为合适。选用环磷酰胺作为生殖毒性试验的阳性对照是合适的。
在本实验条件下。30 mg/kg环磷酰胺对孕兔生殖功能及胚胎形成无明显影响,但可显著影响胎仔发育,可引起胎仔外观畸形、内脏变异、内脏畸变和骨骼畸变。本次实验方法可靠。
