多模态导航辅助可视化硬通道手术治疗高血压脑出血
2019-05-15姚瀚勋沈书颖黄永旺唐乐剑彭志柱王文波
姚瀚勋 沈书颖 黄永旺 唐乐剑 彭志柱 王文波
脑出血是指原发于脑实质内的、非外伤性出血,其大多数是由于高血压伴发的脑小动脉病变在血压骤升时破裂所致,称为高血压脑出血[1]。为了尽可能降低手术造成的脑组织损伤,目前越来越多的医学中心开始应用神经内镜来进行血肿清除手术,而不是通过传统的开颅手术清除血肿。可视化硬通道技术采用透明鞘管穿刺结合神经内镜直视下操作的方法治疗高血压脑出血,然而术中在内镜二维视野下不能测量残留血肿,也很难确定内镜在血肿腔内的具体位置。为了提高了手术的精确程度,笔者在高血压脑出血的治疗中分别应用了手术导航系统和术中超声技术,在临床使用的过程中总结两种导航定位方法的优缺点,并由此提出了“多模态导航辅助技术”。现报道如下。
资料与方法
一、纳入与排除标准
选择桂林医学院附属医院神经外科自2013年6月至2017年3月收治的75例高血压脑出血患者为研究对象。纳入标准:(1)选择脑内自发性的高血压性出血,幕上出血量在30~60 mL之间,脑疝前期,预计不需要行去骨瓣减压的患者;(2)手术前的GCS评分≥8分;(3)发病48 h以内接受手术治疗;(4)年龄<72 岁[2]。排除标准:(1)出血量>60 mL,术前已有瞳孔散大等脑疝征象,预计要行去骨瓣减压术的患者;(2)由颅内动脉瘤、动静脉畸形等破裂导致的继发性脑出血;(3)伴有心、肺、肝、肾等其他重要器官功能障碍的患者。
二、临床资料
(1)多模态导航组:患者26例,其中男性17例,女性9例,行术前CT+术中超声导航辅助内镜下经可视化硬通道微创血肿清除术。(2)CT导航组:患者29例,其中男性18例,女性11例,行单纯术前CT导航辅助内镜下经可视化硬通道微创血肿清除术。(3)术中超声组:患者20例,其中男性14例,女性6例,行单纯术中超声引导内镜下经可视化硬通道微创血肿清除术。3组患者的性别、年龄、血肿侧别、术前血肿量及GCS评分差异无统计学意义(P>0.05),均具有可比性(表1)。
三、手术方法
多模态导航组:术前行头颅CT及CTA检查并将头颅CT影像导入神经导航系统,采用STORZ神经内镜系统及内镜专用手术器械。患者全身麻醉后仰卧位,根据术前头颅CT选择血肿腔长轴最长的层面,沿血肿腔长轴的延长线与额部的交点作为手术入路的定位点。在定位点处作长度约4 cm直切口,颅骨钻孔后扩大骨孔至直径约2 cm,“十”字形切开硬脑膜。在手术导航系统引导下用透明鞘管进行穿刺,确认管芯顶端到达血肿腔后三分之一处后将管芯拔出,透明鞘管留置于血肿腔内,便于确认鞘管周围的血肿和出血点以及判断血肿清除程度[3]。沿鞘管置入超声探头,利用超声回波探测管壁周围血肿所在的位置,术中根据需要随时重复应用超声导航修正和验证手术路径[4,5]。经透明鞘管置入神经内镜,术中内镜沿血肿腔的长轴清除血肿,逐渐撤出透明鞘管的过程中周围血肿继续移入中央被清除,在术中超声引导下逐步向外退出鞘管的同时清除血肿,如果血肿腔里出现活动性出血,则使用与内镜配套的双极电凝镊电凝止血。确认血肿充分清除并且已无活动性出血后用手术止血纱贴敷血肿残腔,然后用生理盐水注满血肿腔。关颅时紧密缝合硬脑膜,回复小骨瓣并固定,依次缝合皮下及皮层。

表1 3组患者一般情况比较(Mean±SD)
CT导航组:术前行头颅CT及CTA检查并将头颅CT影像导入神经导航系统。术中在手术导航系统引导下进行穿刺,经透明鞘管置入神经内镜。全程在术前CT影像导航定位下清除血肿,不使用超声探头,其余操作步骤与多模态导航组相同。
术中超声组:钻2个骨孔:用于置入内镜的骨孔与上述2组一样位于额部,用于放置超声波探头的骨孔则位于颞部,骨孔的具体位置可以根据血肿腔的位置做适当调整。在2个骨孔处的皮肤上做直切口。用于超声探测的颞部骨孔在颅骨钻孔后硬脑膜不切开,因为超声波能够穿过硬脑膜而且保留硬脑膜可以保护大脑表面不受损伤。首先通过额部内镜骨孔应用超声确定血肿位置决定透明鞘管插入的方向,然后通过颞部骨孔置入另一枚探头进行探测,在超声引导下将透明鞘管从额部骨孔插入到血肿的中心。血肿清除后,用生理盐水注满血肿腔,此时可以在水环境中应用超声再次探测血肿腔,以确保血肿清除的程度[6]。
四、评价指标及其计算方法
比较3组患者的手术时间、术中出血量和血肿清除率。术前行头颅CT扫描,通过CT软件(Neusoft PACS/RIS影像诊断子系统Version 3.1,沈阳东软集团股份有限公司)在计算机上逐层勾画血肿轮廓后软件自动测出每个血肿层面的手术前血肿面积,血肿体积=所有层面血肿面积之和×层厚。术后24 h再次行头颅CT扫描,同样用上述软件勾画血肿轮廓后计算出手术后残余血肿体积。血肿清除率=(手术前体积-手术后体积)/手术前体积×100%。对生存患者进行术后3个月的短期随访观察,观察3组患者的预后,按照美国国立卫生院神经功能缺损评分(National Institute of Health stroke scale,NIHSS)分为5级,Ⅰ~Ⅲ级定义为预后良好,Ⅳ~Ⅴ级及死亡定义为预后不良[7]。
五、统计学分析
应用SPSS18.0软件对数据进行处理。计量资料以均数±标准差(Mean±SD)表示,采用单因素方差分析,组间两两比较,若方差齐性,选择LSD-t检验法;若方差不齐,则选择Tamhane’s T2检验。计数资料以率(%)表示,采用 Pearson χ2检验。以 P<0.05 为差异有统计学意义。
结 果
一、3组手术时间、术中出血量及血肿清除率比较多模态导航组的手术时间为(2.12±0.33)h,CT导航组为(1.93±0.15)h,术中超声组为(2.01±0.37)h,差异无统计学意义(P>0.05)。多模态导航组的术中出血量为(164.95±13.33)mL,CT 导航组为(169.07±24.87)mL,术中超声组为(159.65±28.44)mL,差异无统计学意义(P>0.05)。多模态导航组的血肿清除率显著高于CT导航组和术中超声组,差异具有统计学意义(P<0.05),CT导航组与术中超声组之间差异无统计学意义(P>0.05)。具体内容表2。
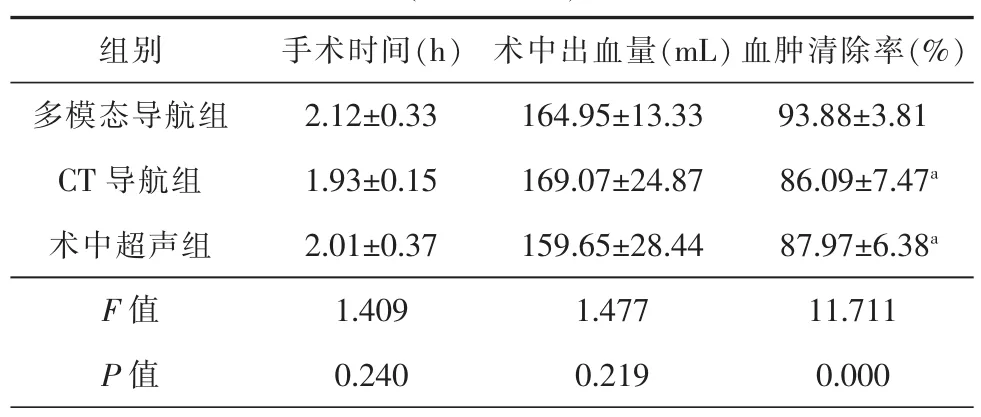
表2 3组患者手术时间、术中出血量、血肿清除率比较(Mean±SD)
二、患者短期预后评分结果
本组患者全部存活,术后3个月首次复查时进行NIHSS评分后发现:多模态导航组预后良好患者为22例,CT导航组预后良好患者为21例,术中超声组预后良好患者为14例,差异无统计学意义(P>0.05,表 3)。
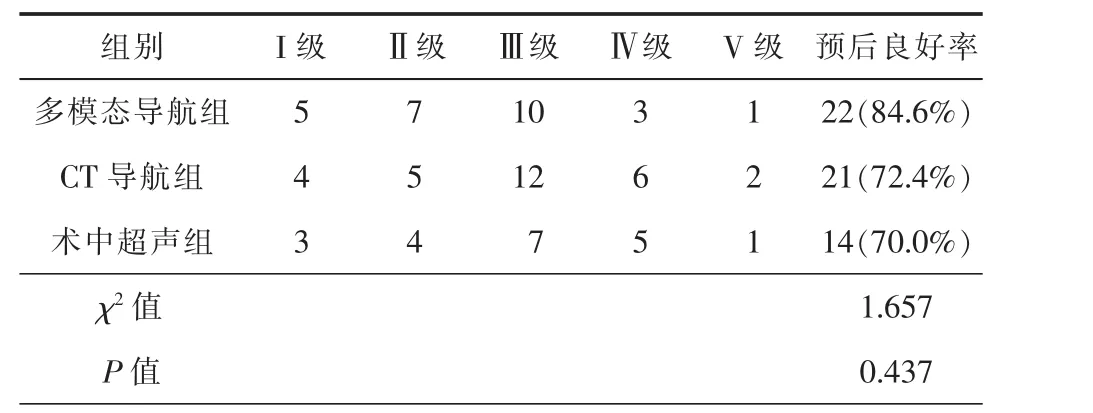
表3 3组患者术后3个月NIHSS评分比较
讨 论
一、内镜下经可视化硬通道清除颅内血肿的优势
高血压脑出血是神经外科常见疾病,起病急、进展快、死亡率及致残率高,其首选治疗方法是外科手术清除血肿[8]。随着神经内镜技术的不断进步,在内镜下清除颅内血肿已成为一种重要的治疗方法[9,10]。内镜能提供良好的深部视野,更好地暴露和观察脑实质内深部结构。而使用透明鞘管的优点是可以清楚地看到管壁侧方的血肿和出血点,结合30°镜可获得血肿腔侧面的良好照明与暴露,大大减少了观察死角,便于在直视下通过各个角度进行手术操作,从而避免遗漏血块并达到确切止血的目的[11]。笔者所使用的是塑料质地的透明鞘管,并在管芯的尾端加装了手术导航系统配套的手术器械适配器,可以在导航实时引导下穿刺血肿,而且管芯穿刺后无需抽吸以确认血肿腔,避免了额外的损伤,使得术后再出血的发生率大大降低[10,12]。
二、导航辅助定位的必要性及传统手术导航技术的缺点
由于额部切口经血肿腔长轴入路距离血肿腔较远,穿刺的位置和方向的把握就显得尤为重要,一旦穿刺方向稍有不准,在鞘管抵达的目标区域就会产生较大的偏差,而手术导航技术的出现成功地解决了这一问题[13]。目前,CT和MRI导航技术已经被广泛应用在脑、脊髓肿瘤等手术中。然而,无论是CT还是MRI导航,其成像定位都是基于术前静态信息,是根据患者术前的影像来定位手术中的实际病变部位,术中随着脑脊液的释放和血肿的清除,必然会产生脑组织移位,这是发生影像飘移最根本的原因。因此,依据术前影像资料的传统导航技术无法跟踪监测术中脑组织的移位和血肿体积的减少,也就无法准确地指导手术。于是,术中CT和术中MRI技术应运而生,有效地解决了导航手术中影像飘移这一问题[14]。但是,所需的特殊设备要占用两个手术室的空间,并需要术者中断手术操作才能证实有无残余血肿,尤其是MRI检查时间过长导致手术时间大幅增加,而且相关设备价格昂贵。
三、术中超声引导技术的优点和不足
术中超声是一种微创的二维成像诊断技术,通过多个平面术中超声扫描后,可以重建出三维超声脑组织局部虚拟影像进行导航[15]。颅骨会干扰超声波的投射,所以需要在颞部再钻一个骨孔。与基于术前CT/MRI影像的传统导航技术不同,术中超声获得的是实时的图像,可以避免影像飘移,增加血肿清除的效率。但是术中超声探测影像是虚拟的,不能精确测量血肿边缘到大脑皮层表面的距离,也就不能确定血肿的实际边界,从而在穿刺血肿时无法提供精确的定位。此外,还存在以下问题:(1)超声探头探测到的是二维声谱图,而手术医生想要看到的是三维仿真图像,两者之间的转换存在一定的困难;(2)内镜鞘管内的空气会干扰超声波的穿透;(3)清除血肿并电凝止血后形成的不规则血肿腔壁与周围脑组织密度不同,使声波的衰减程度不同,从而产生伪影[16];(4)手术器械的干扰。总之,术中超声的主要优势在于其安放在颞部颅骨骨孔硬脑膜上的超声探头可以提供关于内镜和残余血肿位置的实时信息,不受脑组织移位的影响,花费低,其不足之处在于图像清晰度有限,无法确定功能区,术中图像判读受主观影响较大,而且该方法需在颞部做一个额外的皮肤切口和颅骨钻孔,使手术损伤和风险相对增加。
四、多模态导航辅助技术的优点
CT导航的优势主要在于是真实的影像,血肿边界显示清晰,可以精确计算血肿边缘到颅骨的距离。在穿刺血肿时,脑组织尚未发生移位,此时用CT导航定位可以确保透明鞘管穿刺到血肿腔的中心。在血肿逐渐清除的过程中,脑组织会发生移位,此时再根据术前的CT影像进行导航定位必然会产生误差,导致血肿清除不彻底,而术中超声导航仍能对内镜和透明鞘管的位置进行实时定位,这也是术中超声最重要的应用价值。在临床应用这两种技术的过程中,笔者产生了综合两者优点的想法,参考目前国际上已有的术中超声融合术前MRI的导航技术,笔者提出了 “多模态导航技术”(即术中超声结合术前CT的导航技术):在穿刺血肿腔时,基于术前影像资料进行导航定位;在清除血肿的过程中,通过超声探头扫描得到的术中超声图像对术前图像进行修正,避免遗漏残余血肿。该技术的要点:(1)在穿刺血肿时,最关键的问题是如何使鞘管尽可能穿刺到血肿腔的中轴线,此时通过CT导航定位是最佳的选择;(2)在清除血肿时,最重要的问题是如何避免术中影像飘移,实时观察脑组织的移位情况以及检查管壁周围是否还有隐藏的残余血肿,此时沿内镜鞘管置入超声探头是最佳的选择。超声探头与内镜使用同一颅骨骨孔,虽然这样无法同时观察内镜在血肿腔内的位置,但颅骨是不会移位的,因此内镜在颅内的位置依然可以通过术前影像确定,而且此时最关键的问题已经是如何尽可能地清除残余血肿。而且该方法避免了在颞部再做一个切口,在颅骨上再钻一个骨孔,手术损伤更小。
综上所述,多模态导航技术是一种可行有效的方法,提高了内镜下经可视化硬通道清除颅内血肿的效率,应用该技术治疗高血压脑出血具有微创高效的特点,值得在临床上推广。
