川明参醇提取物抗氧化性及热稳定性研究
2019-04-29肖丹桃王淑君王越梅
万 重,肖丹桃,王淑君,王越梅,张 清
(四川农业大学 食品学院,四川 雅安 625014)
川明参(ChuanminshenViolaceumSheh et Shan)属伞形科、川明参属根下植物,因极易与其他品种相混而未在历代本草中收载,从现今对川明参的报道来看,其开发利用的程度较低。有研究应用乙醇提取川明参根粉中的成分,鉴定出7种化合物,包括香豆素伞形花内酯、阿魏酸、胡萝卜苷、印度枸橘素等[1]。董红敏等[2]应用超声辅助提取川明参中的挥发油,并检测出76种成分,鉴定并确定其中42种化合物,含量较多的为镰叶芹醇、亚油酸和欧前胡素等。此外,还应用95%乙醇超声辅助提取其中的抗氧化活性成分,发现成分中蛋白质和多糖含量较多,且具有较强的抗氧化能力[3]。香豆素是川明参的重要成分,有研究显示超声辅助醇提法可以提高香豆素的提取率[4]。川明参还包括黄酮、甾醇、有机酸、酚类、鞣质和萜类等化学成分[5-6]。川明参干燥根中至少含有13种氨基酸,其中含量较高的有天冬氨酸、谷氨酸、缬氨酸、亮氨酸[7]。有研究认为把川明参粉加入到猪油中可以减缓油脂的氧化,提示川明参可以进行开发利用,有潜力作为食品抗氧化剂应用于食品加工领域[8]。
油脂在加热或煎炸过程中会发生氧化、水解及聚合等一系列化学反应,不仅破坏其原有的不饱和脂肪酸及维生素等营养成分,而且还产生醛、酮等有害物质。一般来说,添加抗氧化剂及经过一些物理方式的处理可以延长油脂的使用寿命。抗氧化剂根据其来源可分为天然抗氧化剂与合成抗氧化剂。天然抗氧化剂主要为植物中提取出来的活性物质,包括生育酚、鼠尾草酚、类黄酮和芝麻酚等;合成抗氧化剂通常使用的为丁基羟基茴香醚(BHA)、二丁基羟基甲苯(BHT)、没食子酸丙酯(PG)和叔丁基对苯二酚(TBHQ)等[9]。虽然天然抗氧化剂具有高效和低毒等优势,但大多数的天然抗氧化剂的热稳定性较差,容易在加热反应中挥发出去。合成抗氧化剂均能表现出较好的抗氧化性,但对人体健康的潜在威胁使其有限量要求[10]。因此,需从天然材料中寻找有效的抗氧化剂并能应用于油脂的抗氧化。本实验以川明参为原料,采用超声辅助乙醇提取技术提取川明参粉中的抗氧化活性物质,并将川明参醇提取物添加到大豆油中,探究其对油脂加热氧化的影响。
1 材料与方法
1.1 实验材料
1.1.1 原料与试剂
无添加抗氧化剂的大豆油,购于九三集团营销有限公司;川明参采自四川省金堂县,采摘时间为2018年3月下旬,新鲜川明参采摘后立即带回实验室,洗净放入-20℃冰箱,取出晾干后,用粉碎机粉碎成100~200目粉末。
乙醚、无水乙醇、2,4-二硝基苯肼、苯、三氯乙酸、甲苯、甲醇钠、氢氧化钾、三氯化铁、抗坏血酸(VC)和TBHQ均为分析纯,正己烷、甲醇为色谱纯,购于雅安万科试剂公司;1,1-二苯基-2-三硝基苯肼(DPPH)、2′-联氨-双-3-乙基苯并噻唑啉-6-磺酸(ABTS)和37种脂肪酸混合标准品(CRM47885),购于Sigma试剂公司。
1.1.2 仪器与设备
艾拓金牌节能型电炸炉,BS 214D电子天平,UV-6100紫外分光光度计,7890A-5975C气相色谱-质谱联用仪,电子温度计(德国易克赛思国际有限公司),DK-9811恒温水浴锅,AUW22D十万分之一天平(日本岛津仪器公司)。
1.2 实验方法
1.2.1 川明参醇提取物的提取
川明参醇提取物的提取参照董红敏[11]的醇提取方法,略有改进。准确称取50 g川明参干燥粉,加入500 mL 80%乙醇溶液,在49℃下超声(225 W)辅助提取38 min。过滤提取液在45℃下真空旋转蒸发呈浓缩物,再经100 mL无水乙醇分3次洗涤,滤去不溶解的多糖成分。滤液在45℃下真空旋转蒸发,直到乙醇蒸发干,得到川明参醇提取物,将其收集后保存在4℃条件下,备用。
1.2.2 DPPH自由基清除率的测定
以无水乙醇为溶剂,分别配制浓度为2×10-4mol/L的DPPH溶液,质量浓度分别为5.0、10.0、15.0、20.0、25.0 mg/mL的川明参醇提取物溶液和质量浓度分别为0.01、0.02、0.03、0.04、0.05 mg/mL VC溶液。精确吸取4 mL不同质量浓度的川明参醇提取物溶液和VC溶液,加入4 mL DPPH溶液,摇匀后在暗室下放置30 min,以无水乙醇为对照,在517 nm波长处测定上述溶液的吸光度[12]。按照下式计算DPPH自由基清除率。
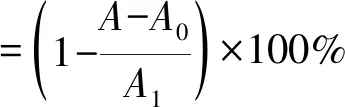
式中:A为样品与DPPH混合溶液的吸光度;A0为样品与无水乙醇混合溶液的吸光度;A1为无水乙醇与DPPH混合溶液的吸光度。
1.2.3 ABTS+自由基清除率的测定
将ABTS及过硫酸钾用少量水溶解,再用无水乙醇配制浓度为7×10-3mol/L的ABTS溶液和浓度为2.5×10-3mol/L的过硫酸钾溶液,并将二者等体积混合,在暗处放置12 h后待用。配制质量浓度分别为5.0、10.0、15.0、20.0、25.0 mg/mL的川明参醇提取物溶液和质量浓度分别为0.01、0.02、0.03、0.04、0.05 mg/mL VC溶液。精确吸取1 mL不同质量浓度川明参醇提取物溶液和VC溶液,加入5 mL ABTS和过硫酸钾的混合溶液,摇匀后在室温条件下避光反应30 min,以无水乙醇为对照,在734 nm波长处测定上述溶液的吸光度[13]。按照下式计算ABTS+自由基清除率。
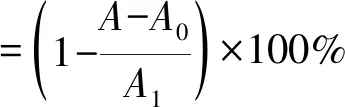
式中:A为样品与ABTS和过硫酸钾混合溶液的吸光度;A0为样品与无水乙醇混合溶液的吸光度;A1为无水乙醇与ABTS和过硫酸钾混合溶液的吸光度。
1.2.4 川明参醇提取物对铁还原能力的测定
用无水乙醇配制质量浓度分别为5.0、10.0、15.0、20.0、25.0 mg/mL的川明参醇提取物溶液和质量浓度分别为0.01、0.02、0.03、0.04、0.05 mg/mL 的VC溶液,分别取1 mL上述溶液于试管中,依次加入0.2 mol/L磷酸盐缓冲液2.5 mL、1 g/100 mL铁氰化钾2.5 mL,混匀并在50℃水浴保温20 min,再加入10 g/100 mL三氯乙酸2.5 mL,3 000 r/min离心10 min后取上清液2.5 mL于试管中,再加入去离子水2.5 mL和0.1 g/100 mL三氯化铁0.5 mL,常温反应5 min后在700 nm波长处测定吸光度[14]。
1.2.5 加热氧化实验
将0%、0.05%、0.1%、0.3%和0.5%的川明参醇提取物及0.02%的TBHQ分别添加到500 mL大豆油中,在室温下混匀并室温放置24 h。将上述各大豆油样品分别装入试管中,进行180℃油浴加热实验。分别在0、3、6、9、12、15、18 h和21 h取样,待冷却后,放入-4℃冰箱中待测。
1.2.6 酸价、羰基价与脂肪酸组成的测定
酸价的测定参照GB 5009.229—2016《食品安全国家标准 食品中酸价的测定》,羰基价的测定参照GB 5009.230—2016《食品安全国家标准 食品中羰基价的测定》。
油样甲酯化采用碱化催化法[15]。称取油样25~30 mg于20 mL具塞试管中,加入1 mL无水甲苯,再加入1 mL浓度为0.5 mol/L的甲醇钠-甲醇溶液,50℃恒温处理10 min。冷却后依次添加0.1 mL冰醋酸和1 mL去离子水,摇匀,然后用5 mL正己烷洗涤,取上层清液有机相1 mL用正己烷稀释5倍,最后用无水硫酸钠脱水、0.22 μm的有机滤膜过滤,放入-4℃冰箱保存待测。采用气相色谱-质谱联用法进行脂肪酸组成分析。
气相色谱条件:HP-88毛细管色谱柱(60 m×0.25 mm×0.2 μm);不分流进样,进样量1 μL;进样口温度250℃;氦气流速1 mL/min;柱温箱初始温度120℃保持1 min,以5℃/min升到175℃保持10 min,以5℃/min升到190℃保持5 min,以5℃/min升到200℃保持5 min。
质谱条件:离子源和四极杆温度分别为230℃和150℃;质谱扫描范围(m/z)为40~400;采用全扫描模式。
1.2.7 数据分析
所有数据进行3次重复实验,应用SPSS 22.0进行数据统计与分析,显著性差异采用Duncan以及ANOVA检验,应用Origin 8.5软件作图。
2 结果与分析
2.1 川明参醇提取物对DPPH自由基的清除能力(见图1)
由图1A可知,在质量浓度(5.0、10.0、15.0、20.0、25.0 mg/mL)范围内,川明参醇提取物对DPPH 自由基具有明显的清除能力,且清除能力随其质量浓度的增加而增强。川明参醇提取物在质量浓度为5~25 mg/mL时,其对DPPH自由基的清除率为39.39%~95.52%。由图1B可知,VC质量浓度为0.02~0.05 mg/mL时,其对DPPH自由基清除能力变化不显著。将川明参醇提取物对DPPH自由基清除能力与VC进行比较,发现质量浓度为25 mg/mL 的川明参醇提取物对DPPH自由基的清除能力高于质量浓度为0.04 mg/mL的VC。可推断川明参醇提取物中含有抗氧化活性物质,对DPPH自由基具有显著的清除能力,且在质量浓度为5~20 mg/mL时,其对DPPH自由基清除能力增加趋势较快,质量浓度为20~25 mg/mL时的增加趋势变缓。
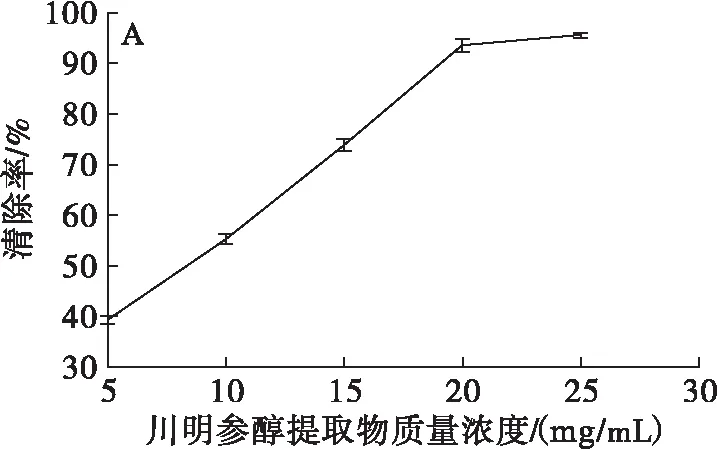
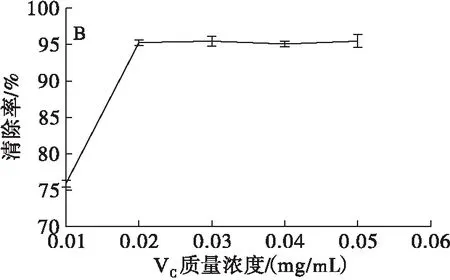
图1 川明参醇提取物、VC对DPPH自由基的清除能力
2.2 川明参醇提取物对ABTS+自由基的清除能力(见图2)
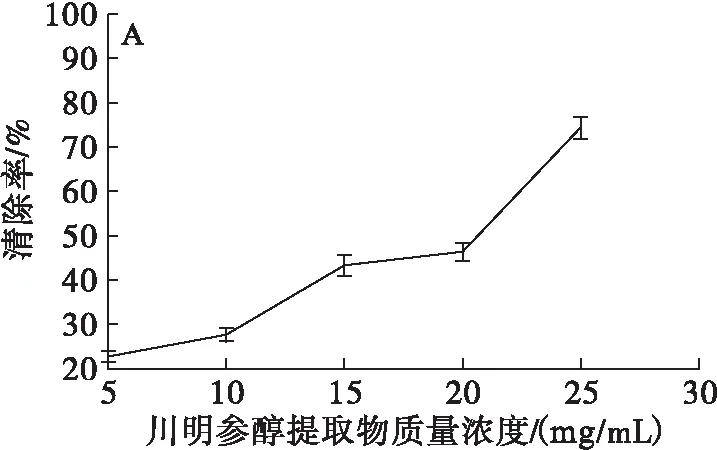
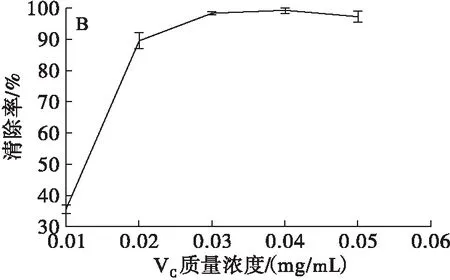
图2 川明参醇提取物、VC对ABTS+自由基的清除能力
由图2A可以看出,在质量浓度(5.0、10.0、15.0、20.0、25.0 mg/mL)范围内,川明参醇提取物对ABTS+自由基具有明显的清除能力,其清除能力随质量浓度的增加而增强。当川明参醇提取物质量浓度为25 mg/mL时,对ABTS+自由基的清除能力为74.41%。由图2B可知,VC质量浓度为0.02~0.05 mg/mL时,对ABTS+自由基的清除能力均大于89%,且增加趋势不明显。将VC与川明参醇提取物对ABTS+自由基的清除能力相比,川明参醇提取物对ABTS+自由基的清除能力相对较弱。但随着川明参醇提取物质量浓度的增加,其对ABTS+自由基的清除能力也会逐渐升高。可推断川明参醇提取物对ABTS+自由基的清除能力与其质量浓度相关,质量浓度越大,对ABTS+自由基的清除能力越强。
2.3 川明参醇提取物的铁还原能力(见图3)
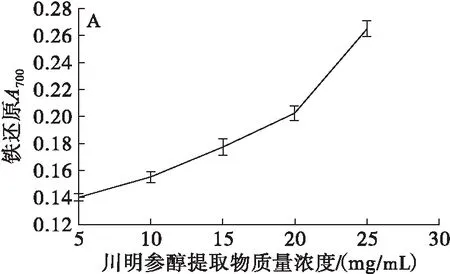
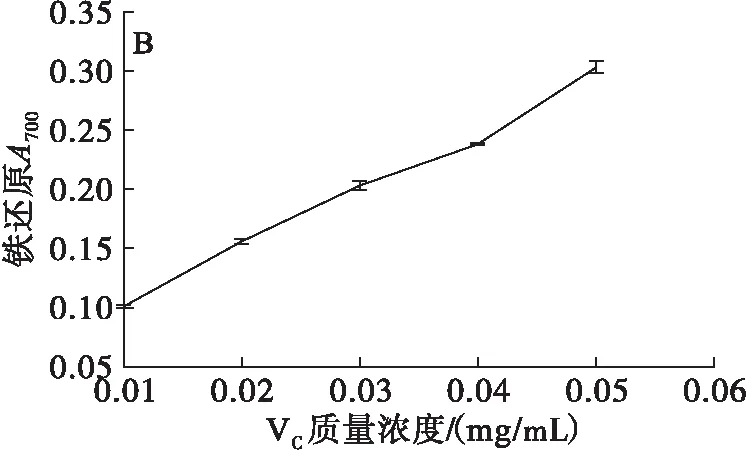
图3 川明参醇提取物、VC的铁还原能力
由图3可以看出,川明参醇提取物和VC在一定的质量浓度范围内都具有较强的铁还原能力,且随着质量浓度的增加,铁还原能力增强。VC质量浓度为0.01~0.05 mg/mL时,吸光度为0.10~0.30,川明参醇提取物质量浓度为5~25 mg/mL时,吸光度为0.14~0.26。川明参醇提取物对铁离子的还原能力随着质量浓度的增加趋势相比VC缓慢。
2.4 川明参醇提取物的热抗氧化能力
通过添加不同量的川明参醇提取物(CE)在大豆油中,以添加0.02%TBHQ和无添加抗氧化剂的大豆油(Blank)为对照,分析不同加热时间每种油样的酸价、羰基价,结果如图4~图5所示。
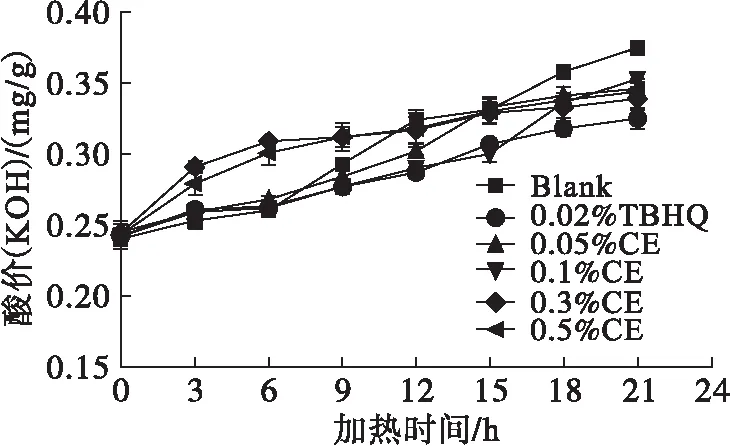
图4 不同条件下大豆油在加热过程中酸价的变化
由图4可知,随着加热时间的延长,每种大豆油的酸价逐渐增大,但增加的趋势有明显差异。其中无添加抗氧化剂的大豆油酸价的增加趋势最快,在21 h内酸价(KOH)的变化范围为0.24~0.37 mg/g;添加0.02%TBHQ的大豆油酸价增加趋势最缓慢,在21 h内酸价(KOH)的变化范围为0.24~0.33 mg/g。在21 h时添加川明参醇提取物的大豆油中,添加0.3%川明参醇提取物的大豆油酸价(KOH)最低,为0.34 mg/g。TBHQ和川明参醇提取物在大豆油加热过程中,对抑制大豆油酸价的增加都有明显的效果,然而在不同添加量的川明参醇提取物作用下,大豆油酸价表现出不同的增加趋势。
由图5可知,随着加热时间的延长,每种大豆油的羰基价逐渐增大,但增加的趋势有显著差异。其中无添加抗氧化剂的大豆油羰基价增长趋势最快,在21 h的羰基价达到52.78 meq/kg;同时间下添加0.02%TBHQ的大豆油羰基价为46.48 meq/kg,添加0.1%、0.3%和0.5%的川明参醇提取物的大豆油羰基价均小于TBHQ的。可见,添加川明参醇提取物对大豆油羰基价的增加具有明显的延缓效果。
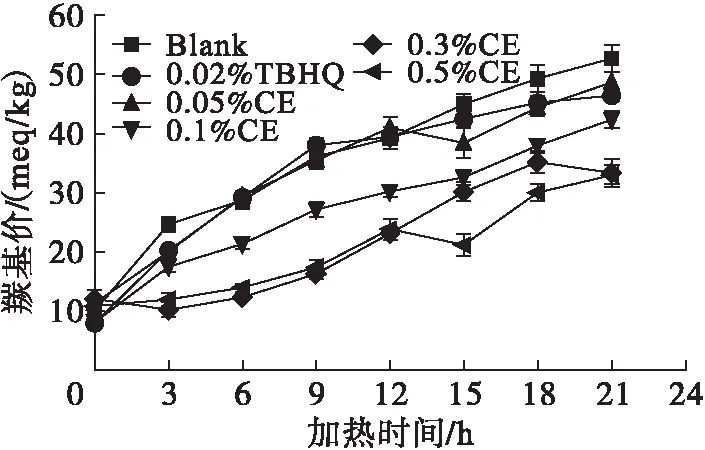
图5 不同条件下大豆油在加热过程中羰基价的变化
在180℃条件下加热21 h,无添加抗氧化剂、添加0.02% TBHQ和不同添加量的川明参醇提取物的大豆油脂肪酸组成变化情况如表1所示。
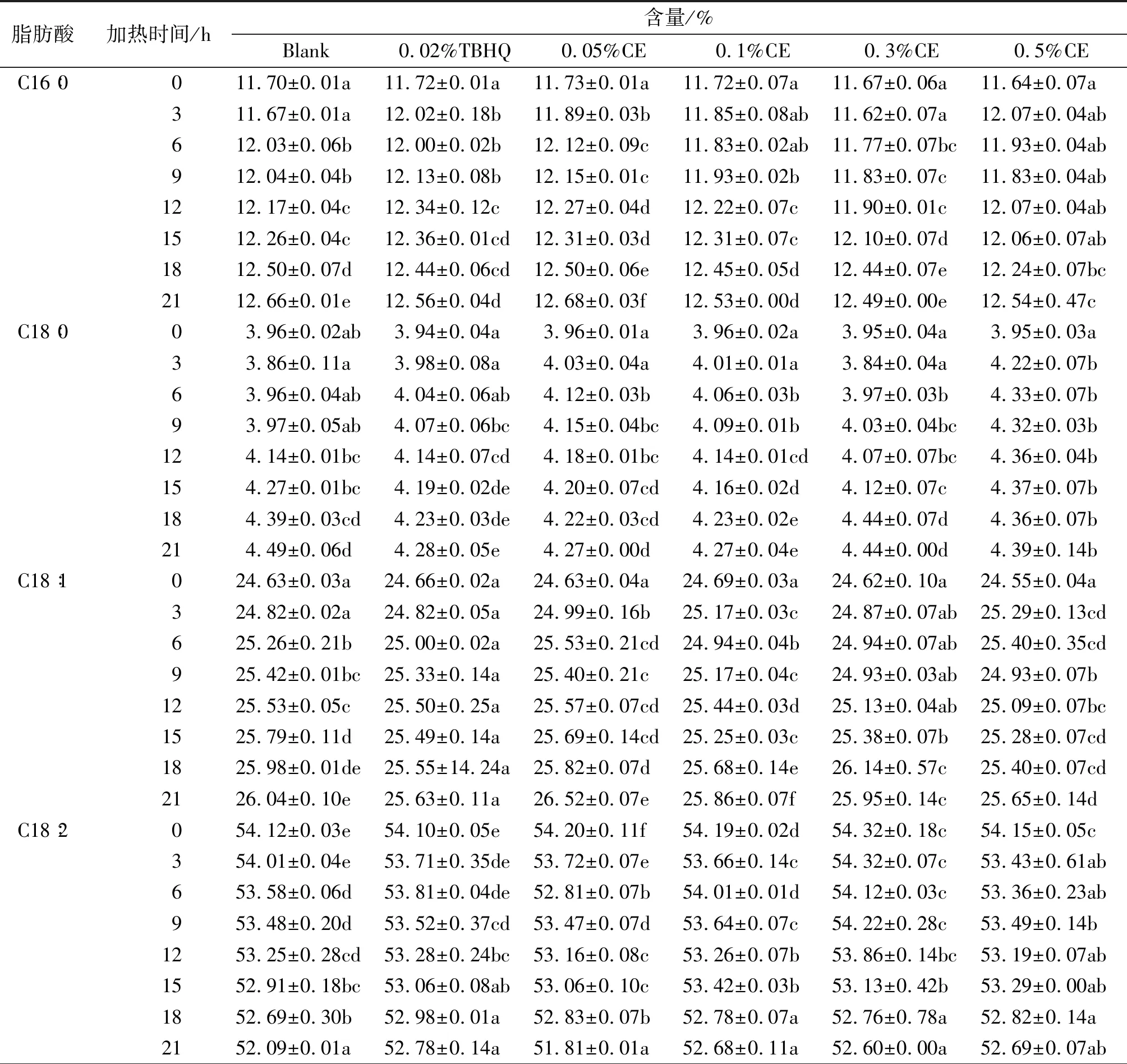
表1 不同条件下大豆油在加热过程中主要脂肪酸组成的变化情况
续表1
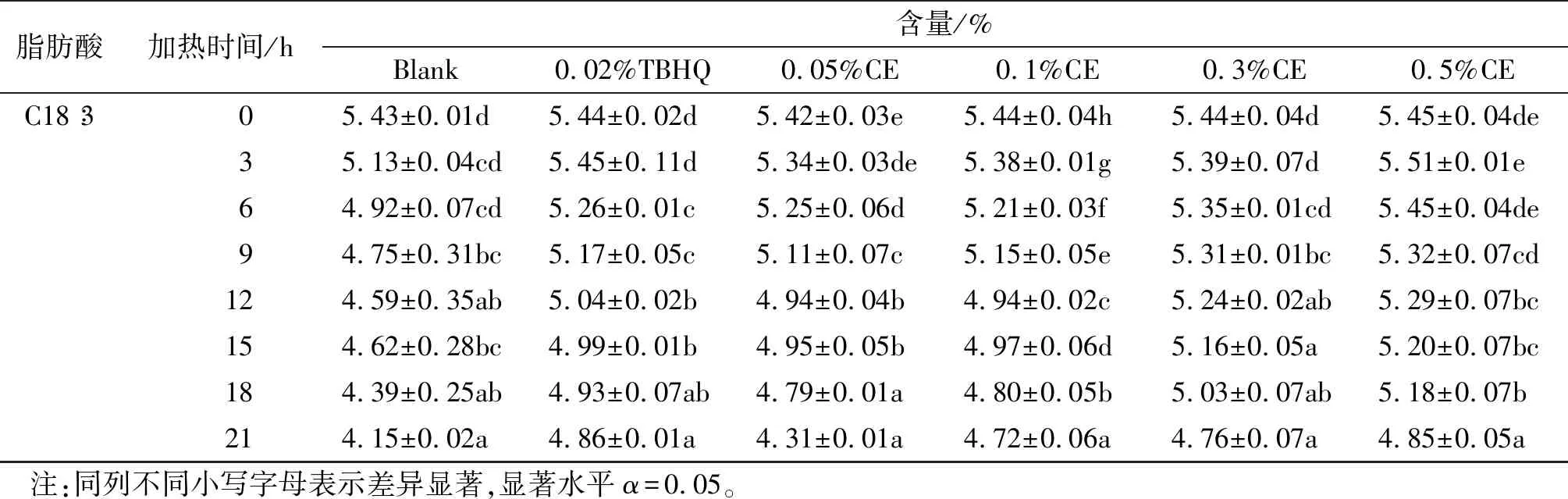
脂肪酸加热时间/h含量/%Blank0.02%TBHQ0.05%CE0.1%CE0.3%CE0.5%CEC18∶3005.43±0.01d05.44±0.02d05.42±0.03e05.44±0.04h05.44±0.04d05.45±0.04de305.13±0.04cd05.45±0.11d05.34±0.03de05.38±0.01g05.39±0.07d05.51±0.01e604.92±0.07cd05.26±0.01c05.25±0.06d05.21±0.03f05.35±0.01cd05.45±0.04de904.75±0.31bc05.17±0.05c05.11±0.07c05.15±0.05e05.31±0.01bc05.32±0.07cd1204.59±0.35ab05.04±0.02b04.94±0.04b04.94±0.02c05.24±0.02ab05.29±0.07bc1504.62±0.28bc04.99±0.01b04.95±0.05b04.97±0.06d05.16±0.05a05.20±0.07bc1804.39±0.25ab04.93±0.07ab04.79±0.01a04.80±0.05b05.03±0.07ab05.18±0.07b2104.15±0.02a04.86±0.01a04.31±0.01a04.72±0.06a04.76±0.07a04.85±0.05a 注:同列不同小写字母表示差异显著,显著水平α=0.05。
由表1可知,大豆油中不饱和脂肪酸(除C18∶1)含量随加热时间的延长而减少,饱和脂肪酸含量增加。C16∶0增加量最小的为添加0.1%川明参醇提取物的大豆油(增加量0.81个百分点),其次为添加0.3%川明参醇提取物的大豆油(增加量0.82个百分点)。C18∶2和C18∶3在加热过程中,随加热时间的延长而逐渐降低。添加0.02%TBHQ的大豆油C18∶2减少量最小,为1.31个百分点,减少量最大的为添加0.05%川明参醇提取物的大豆油,为2.38个百分点。对大豆油C18∶2的减少量延缓效果顺序为0.02%TBHQ>0.5%川明参醇提取物>0.1%川明参醇提取物>0.3%川明参醇提取物> 无添加>0.05%川明参醇提取物。C18∶3减少量最小的为添加0.02%TBHQ的大豆油,为0.57个百分点,其次为添加0.5%川明参醇提取物的大豆油,为0.61个百分点。对大豆油C18∶3的减少量延缓效果顺序为0.02%TBHQ>0.5%川明参醇提取物>0.3%川明参醇提取物>0.1%川明参醇提取物>0.05%川明参醇提取物>无添加。
由此可见,在大豆油加热过程中,添加川明参醇提取物,对大豆油饱和脂肪酸的增加及多不饱和脂肪酸的减少,均有一定的抑制作用,且不同添加量的川明参醇提取物对各种脂肪酸的组成变化有明显差异。
3 结 论
本实验采用体外抗氧化能力测试和大豆油加热氧化测试,对川明参醇提取物的抗氧化能力进行评价。由抗氧化指标分析显示,川明参醇提取物中含有抗氧化活性物质,对DPPH、ABTS+自由基清除能力和铁还原能力都具有明显效果,且随质量浓度的增加,其抗氧化能力逐渐增强。川明参醇提取物对大豆油的热氧化具有明显的抑制效果,其抑制酸价增加效果最好的是0.3%川明参醇提取物;抑制羰基价增加效果最好的是0.5%川明参醇提取物。对于C16∶0、C18∶0的增加量,不同添加量的川明参醇提取物均表现出明显的抑制效果。对于C18∶2和C18∶3的减少量,添加0.5%的川明参醇提取物对延缓其减少的效果略低于TBHQ。因此,川明参醇提取物在油脂高温加热过程中可以有效延缓油脂的氧化速率,有潜力应用于食用油的贮藏或高温加热,从而延长油脂的使用寿命。
