川芎标准汤剂制备及质量标准研究
2019-04-25冯玉甄亚钦田伟范帅帅李军山
冯玉 甄亚钦 田伟 范帅帅 李军山


摘要:目的 制备川芎饮片标准汤剂,测定川芎标准汤剂中阿魏酸的含量,并建立特征图谱以进行质量标准研究。方法 依照标准汤剂的制备要求,制备15批不同产地的川芎饮片标准汤剂。以阿魏酸作为定量检测指标,计算转移率与出膏率,并建立超高液相色谱特征图谱,用《中药色谱指纹图谱相似度评价系统(2012版)》软件进行特征图谱分析。结果 15批川芎标准汤剂的出膏率范围为5.4%~10.1%;阿魏酸含量范围为2.39~4.44 mg/g,转移率范围为9.28%~17.24%。川芎标准汤剂特征图谱共标定了10个共有峰,指认其中4个共有峰。15批川芎饮片标准汤剂相似度均大于0.90。结论 川芎饮片标准汤剂制备规范,测定方法精密度、稳定性和重复性良好,可为川芎配方颗粒的质量控制提供参考。
关键词:川芎;标准汤剂;配方颗粒;转移率;出膏率;特征图谱
中图分类号:R284.1 文献标识码:A 文章编号:1005-5304(2019)04-0068-06
川芎为伞形科植物川芎Ligusticum chuanxiong Hort.的干燥根茎,味辛,性温,归肝、胆、心包经,具有活血行气、祛风止痛功效[1],主产于四川彭州、眉山、都江堰等地[2-3]。川芎含有苯酞类、萜烯类、有机酸及其酯、生物碱、多糖等多种类型的化学成分[4-5],其中苯酞类化合物主要有藁本内酯、丁基酞内酯、丁烯基酞内酯等,萜烯类主要有6-丁基-1,4-环庚二烯、桉叶二烯、松油烯等,有机酸及其酯类主要有阿魏酸、咖啡酸、芥子酸、琥珀酸等,生物碱类主要有川芎嗪、黑麦碱、三甲胺、腺嘌呤等[4,6]。阿魏酸、川芎嗪是川芎的主要有效成分[4]。川芎具有使离体及在体心脏收缩振幅增大、减慢心率、扩张冠脉血管、增加冠脉流量、舒张外周动脉血管、改善脑循环、保护脑缺血损伤、抑制血小板聚集、抗血栓形成、解除平滑肌痉挛、增强记忆、抗氧化等药理作用[7-8]。
中药配方颗粒在服用、携带、贮藏、运输、调剂等方面较传统中药饮片有明显优势,已广泛应用于临床各科并初步显示出较好的临床疗效。作为中药新剂型,配方颗粒既可满足中医随证加减需要,又为需服中药但不方便煎煮的患者提供了一条便利途径,与中药饮片互为补充,呈现出良好的发展趋势[9]。尽管如此,中药配方颗粒与传统中药饮片煎剂疗效是否相等仍是目前关注的核心问题[10]。中药饮片标准汤剂是以中医理论为指导、临床应用为基础,参考现代提取方法,经标准化工艺制备而成的单味中药饮片水煎剂,用于标化临床用药,保障用药的准确性和剂量的一致性。中药饮片标准汤剂综合体现了饮片和制备工艺等影响疗效的关键因素[11]。中药饮片标准汤剂能够作为一种标准,标化不同的临床用药形式,提高用药的准确性和剂量的一致性[12-13]。中药配方颗粒的生产工艺参数确定、质量控制方法和指标选择、限度制定等药学研究,均须与标准汤剂进行对比,以保证其质量。本研究遵循标准汤剂制备方法,选用主产区15批川芎饮片,制备标准汤剂,以阿魏酸为指标成分,测定其含量,计算转移率和出膏率范围,并进行特征图谱研究,为川芎饮片标准汤剂质量标准的制定提供基础研究数据,同时提高川芎配方颗粒的质量控制水平。
1 仪器与试药
ACQUITY UPLC H-Class系统(PDA检测器),美国沃特世公司;Empower3色谱工作站,美国沃特世公司;LC-15C高效液相色谱仪(SPD-15C型紫外检测器、SIL-10AF自动进样器、CTO-15C柱温箱),日本岛津公司;Pilot5-8L真空冷冻干燥机,北京博医康实验仪器有限公司;TB-215D、BSA224S-CW电子分析天平,北京赛多利斯;JY10001型电子天平,上海民桥精密科学仪器有限公司;KQ-250型超声波清洗器(功率250 W,频率40 kHz),昆山市超声仪器有限公司;RE-3000型旋转蒸发器,上海亚荣生化仪器厂;BJH-W200F型陶瓷自动中药煲(电源220 V、50 Hz,功率300 W,容量3.0 L),广东天际电器股份有限公司。
阿魏酸对照品(批号110773-201313,纯度98.8%)、咖啡酸对照品(批号110885-200102)、藁本内酯对照品(批号111737-201608),中国食品药品检定研究院;绿原酸对照品(批号PY20170216),南京普怡生物科技有限公司;甲醇为色谱纯(美国Fisher),乙腈为色谱纯,水为超纯水,其他试剂均为分析纯。15批川芎饮片由神威药业集团有限公司提供,经检验均符合2015年版《中华人民共和国药典》规定,样品来源见表1。
2 方法与结果
2.1 標准汤剂的制备
取川芎饮片100 g,煎煮2次。一煎加9倍水,浸泡30 min,武火煮沸,文火保持微沸30 min;二煎加7倍水,武火煮沸,文火保持微沸20 min。趁热用200目筛网过滤,合并2次煎液,迅速冷却,55 ℃真空减压浓缩至200 mL左右,将浓缩液置于培养皿,-40 ℃冻存24 h后冷冻干燥,即得标准汤剂干粉。
2.2 阿魏酸含量测定
2.2.1 色谱条件
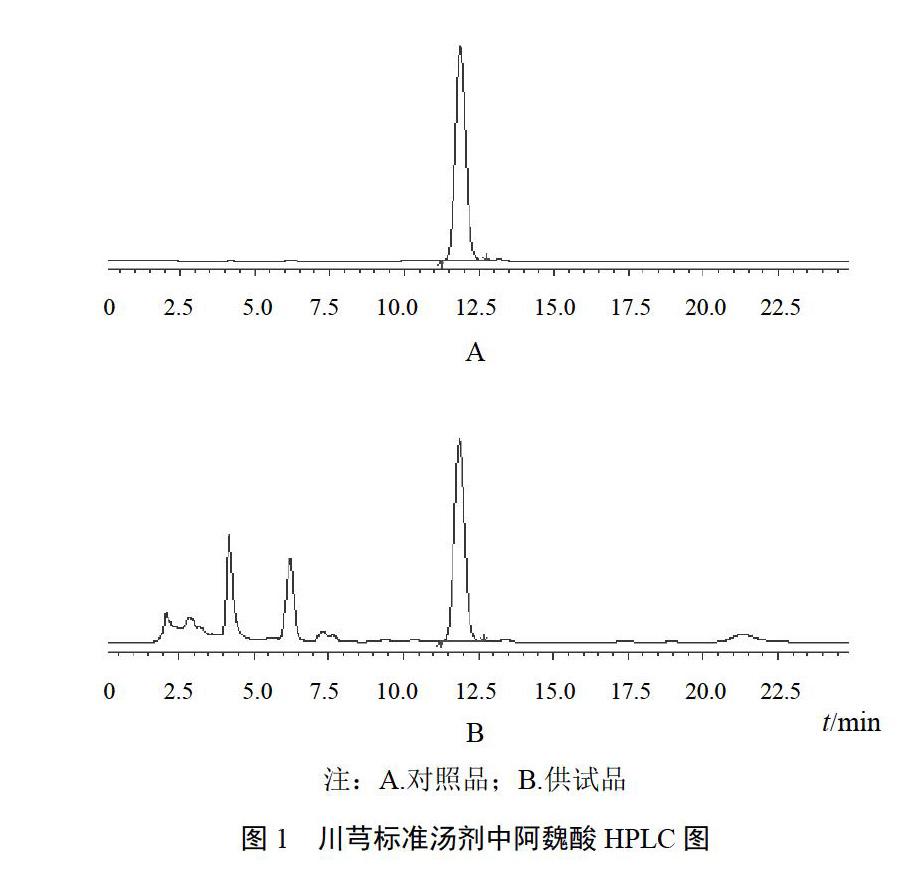
以十八烷基硅烷键合硅胶为填充剂,以甲醇-1%冰醋酸溶液(30∶70)为流动相,流速1.0 mL/min,柱温35 ℃,检测波长321 nm。色谱图见图1。
2.2.2 对照品溶液的制备
精密称取阿魏酸对照品10.05 mg(以98.8%计),置10 mL棕色容量瓶中,加70%甲醇溶解并稀释至刻度,摇匀,得阿魏酸对照品贮备液;精密吸取贮备液0.2 mL,置10 mL量瓶中,加70%甲醇稀释至刻度,摇匀,即得浓度为0.019 9 mg/mL的对照品溶液。
2.2.3 供试品溶液的制备
取川芎干粉约0.1 g,精密称定,置具塞锥形瓶中,精密加入70%甲醇25 mL,密塞,称定质量,超声处理(功率250 W,频率40 kHz)10 min,放冷,再称定质量,用70%甲醇补足减失的质量,摇匀,过滤,取续滤液,即得。
2.2.4 方法学考察
2.2.4.1 线性关系考察
精密吸取对照品溶液2、4、8、12、16、20 ?L,按“2.2.1”项下色谱条件测定,以阿魏酸进样量为横坐标,峰面积为纵坐标,绘制标准曲线,得回归方程Y=4.982 2×106X-1.274 7×104,r=0.999 9,结果表明,阿魏酸进样量在0.039 8~0.398 0 ?g范围内线性关系良好。
2.2.4.2 精密度试验
精密吸取对照品溶液10 ?L,按“2.2.1”项下色谱条件连续进样6次,结果峰面积RSD=0.19%,表明仪器精密度良好。
2.2.4.3 稳定性试验
取川芎干粉(批号1705102)约0.1 g,精密称定,按“2.2.3”项下方法制备供试品溶液,精密吸取该供试品溶液10 ?L,按“2.2.1”项下色谱条件分别于0、2、4、8、12、20、30 h进样测定,结果阿魏酸峰面积RSD=0.75%,表明供试品溶液在30 h内基本稳定。
2.2.4.4 重复性试验
取同一批川芎干粉(批号1705102)6份,每份约0.1 g,精密称定,按“2.2.3”项下方法制备供试品溶液,精密吸取供试品溶液10 ?L,按“2.2.1”项下色谱条件进样,计算得同一批川芎干粉测得的阿魏酸含量均值为3.44 mg/g,RSD=0.60%,表明本方法的重复性良好。
2.2.4.5 加样回收率试验
取已知含量的同一批川芎干粉(批号1705102)9份,每份约0.05 g,精密称定,精密加入相当于样品含有量80%、100%、120%的阿魏酸对照品,每个水平平行3份,按“2.2.3”项下方法制备供试品溶液,按“2.2.1”项下色谱条件测定,每份平行测定2次,计算得阿魏酸的平均回收率为103.13%,RSD=1.12%,表明本方法准确度良好。
2.2.5 样品测定
按2015年版《中华人民共和国药典》(四部)通则0800项下水分测定法第二法测定15批川芎標准汤剂干粉的水分。取每批干粉各约2 g,平铺于干燥至恒重的扁形称量瓶中,精密称定,开启瓶盖,在105 ℃干燥5 h,将瓶盖盖好,转移至干燥器中,放冷30 min,精密称定,再在上述温度干燥1 h,放冷,称定质量,至连续2次称量的差异不超过5 mg为止,根据减失的质量计算水分含量(%)。根据干粉质量计算出膏率,并按上述确定的含量测定条件对15批川芎标准汤剂进行测定,计算阿魏酸转移率。结果见表2。以均值上下浮动30%规定出膏率和转移率,则出膏率为5.4%~10.1%,阿魏酸转移率为9.28%~17.24%。
2.3 特征图谱
2.3.1 色谱条件
采用Waters ACQUITY UPLC BEH C18色谱柱(2.1 mm×100 mm,1.7 ?m);流动相A为乙腈,B为0.1%磷酸,梯度洗脱(见表3);流速:0.3 mL/min;检测波长:276 nm;柱温:35 ℃;进样量:2 ?L。在此色谱条件下,各色谱峰与相邻峰的分离度良好,峰形对称。供试品和混合对照品色谱图见图2。
2.3.2 混合对照品溶液的制备
取绿原酸、咖啡酸、阿魏酸、藁本内酯对照品适量,加70%甲醇配制成每1 mL含绿原酸0.041 mg、咖啡酸0.012 mg、阿魏酸0.019 mg、藁本内酯0.038 mg的混合对照品溶液。
2.3.3 供试品溶液的制备
取川芎干粉约0.1 g,精密称定,置具塞锥形瓶中,精密加入70%甲醇25 mL,密塞,称定质量,超声处理(功率250 W,频率40 kHz)10 min,放冷,再称定质量,用70%甲醇补足减失的质量,摇匀,过滤,取续滤液,即得。
2.3.4 方法学考察
2.3.4.1 精密度试验
取同一批川芎干粉(批号1705102)约0.1 g,精密称定,按“2.3.3”项下方法制备供试品溶液,精密吸取供试品溶液2 ?L,连续进样6次,按“2.3.1”项下色谱条件进行测定,计算各共有峰的相对保留时间和相对峰面积的RSD,结果显示两者的RSD均小于3%,表明仪器精密度良好。
2.3.4.2 稳定性试验
取同一批川芎干粉(批号1705102)约0.1 g,精密称定,按“2.3.3”项下方法制备供试品溶液,精密吸取供试品溶液2 ?L,分别在0、1、2、4、6、8、10 h进样,按“2.3.1”项下色谱条件进行测定,计算各共有峰的相对保留时间和相对峰面积的RSD,结果表明两者的RSD均小于3%,表明供试品溶液在10 h内稳定性良好。
2.3.4.3 重复性考察
取同一批川芎干粉(批号1705102)6份,每份约0.1 g,精密称定,按“2.3.3”项下方法制备供试品溶液,精密吸取供试品溶液2 ?L,按“2.3.1”项下色谱条件进样测定,计算各共有峰的相对保留时间和相对峰面积的RSD,结果表明两者的RSD均小于3%,表明该方法重复性良好。
2.3.5 主成分分析与聚类分析
以10个共有峰峰面积为变量,采用SPSS22.0统计软件,对15批川芎标准汤剂指纹图谱进行主成分与聚类分析,计算成分特征值、贡献率及累计贡献率,前4个主成分的累计贡献率为87.972%,可以反映15批川芎标准汤剂的质量。计算15批川芎标准汤剂的主成分得分,得到15批样品主成分得分三维图及聚类分析结果,见表4、图3、图4。分析结果表明,主成分分析与聚类分析结果一致,编号为10的样品与其他样品较离散,其他样品较为集中,表明15批川芎标准汤剂质量稳定性良好。
2.3.6 特征图谱的建立及相似度评价
按“2.3.3”项下方法制备供试品溶液,按“2.3.1”项下色谱条件,测定15批川芎标准汤剂特征图谱,结果见图5。运用国家药典委员会《中药色谱指纹图谱相似度评价系统(2012版)》软件,采用中位数法计算15批川芎标准汤剂相似度,结果见表5。川芎标准汤剂特征图谱中确定了10个共有峰,根据色谱峰匹配结果进行相似度分析,各批次川芎标准汤剂与共有模式对照指纹图谱相似度分别为0.998、0.996、0.997、0.994、0.986、0.996、0.991、0.984、0.966、0.947、0.999、0.998、0.996、0.993、0.997,均大于0.90,符合指纹图谱相似度要求。选取阿魏酸色谱峰(5号峰)作为参照峰,计算得各共有峰的相对保留时间RSD均小于0.58%,各峰相对峰面积RSD介于18.01%~37.81%。结合主成分分析与聚类分析结果,表明15批川芎标准煎液质量稳定性良好。
3 讨论
根据《中药配方颗粒质量控制与标准制定技术要求(送审稿)》中第四部分标准汤剂要求:标准汤剂的制备包括煎煮、固液分离、浓缩和干燥等步骤,应固定方法、设备、工艺参数和操作规程。本研究对川芎标准汤剂的制备工艺进行了吸水率、加水量、煎煮时间、筛网目数、水煎液静置时间的单因素考察,以标准汤剂的出膏率和阿魏酸含量为衡量指标,最终确定标准汤剂的制备工艺为“2.1”项下方法。本研究还对川芎标准汤剂干粉不同的提取方法(超声提取及回流提取)进行了试验比较,并对不同浓度的提取溶剂(50%甲醇、70%甲醇、纯甲醇)及不同提取时间(10、20、30 min)进行了试验筛选,结果确定为用70%甲醇超声提取10 min。
中药化学成分复杂,基原品种、产地来源、生长环境、采收季节、加工炮制工艺等诸多因素进一步增加了中药质量控制与评价研究的难度,仅凭传统的外观鉴别、显微鉴别及少数有效成分分析鉴定中药存在一定的不准确性[14]。近年来,超高效液相色谱指纹图谱技术在中药质量评价中显示出独特的优势。中药及其制剂以其整体发挥作用,中药指纹图谱能全面反映中药内在化学成分的种类与数量。目前中药的有效成分尚未完全明確,采用中药指纹图谱方式能有效表征中药质量[15]。本试验采用DAD检测器进行全波长监测,结果显示,在波长276 nm处基线较平稳,检出峰各峰比例适中,能基本反映川芎饮标准汤剂中多成分的整体面貌,故选择以276 nm作为检测波长,同时对流动相梯度条件进行了考察,确定了流动相梯度洗脱条件。15批川芎标准汤剂的特征图谱共标定了10个共有峰,指认出其中4个共有峰。15批川芎标准汤剂的特征图谱相似度均大于0.90,并结合主成分分析与聚类分析,表明15批川芎标准汤剂的质量稳定性良好。
中药配方颗粒最核心的问题是建立质量标准,运用现代科学方法对配方颗粒中指标性成分进行鉴别和含量测定。本试验对川芎标准汤剂进行了出膏率、转移率、阿魏酸含量测定及特征图谱研究,并进行了方法学考察,其精密度、稳定性、重复性的RSD均小于3%,表明此方法准确、可行、重复性良好,可用于川芎饮片及配方颗粒的质量控制。
参考文献:
[1] 国家药典委员会.中华人民共和国药典:一部[M].北京:中国医药科技出版社,2015:40-41.
[2] 金玉清,洪远林,李建蕊,等.川芎的化学成分及药理作用研究进展[J].中药与临床,2013,4(3):44-48.
[3] 王丽芝,谭世强,孙思杰,等.不同产地川芎种质与藁本、辽藁本的ITS2序列分析[J].河北农业大学学报,2017,40(1):25-31.
[4] 金玉青,洪远林,李建蕊,等.川芎的化学成分及药理作用研究进展[J].中药与临床,2013,4(3):44-48.
[5] 侯家玉,方泰惠.中药药理学[M].北京:中国中医药出版社,2007:153.
[6] 舒冰,周重建,马迎辉,等.中药川芎中有效成分的药理作用研究进展[J].中国药理学通报,2006,22(9):1403-1407.
[7] 张晓琳,徐金娣,朱玲英,等.中药川芎研究新进展[J].中药材,2012, 35(10):1706-1711.
[8] 黄勤挽,黄媛莉,韩丽,等.川芎配方颗粒的药理等效性试验[J].华西药学杂志,2007,22(2):157-159.
[9] 孟凡辰,郭兆安.中药配方颗粒与传统中药汤剂的对比[J].中国医药科学,2015,5(3):89-90.
[10] 马海涛,吴国水.中药配方颗粒临床应用概况、困境与对策[J].中医药管理杂志,2017,25(13):12-13.
[11] 陈士林,刘安,李琦,等.中药饮片标准汤剂研究策略[J].中国中药杂志,2016,41(8):1367-1375.
[12] 刘冲,刘荫贞,乐智勇,等.桂枝饮片标准汤剂质量标准研究[J].中草药,2017,48(8):1577-1583.
[13] 林伟雄,乐智勇,车海燕,等.甘草饮片标准汤剂的研究[J].中国中药杂志,2017,42(5):830-835.
[14] 刘东方,赵丽娜,李银峰,等.中药指纹图谱技术的研究进展及应用[J].中草药,2016,47(22):4085-4094.
[15] 程谊.中药指纹图谱在质量评价中的作用概述[J].中国中医药信息杂志,2008,15(6):107-108.
(收稿日期:2018-06-27)
(修回日期:2018-07-16;编辑:陈静)
