高浓度乳液稳定性评价方法及其应用
2019-04-23雷群张玉荣罗健辉韩荣成耿向飞吕晓东刘岩王远
雷群,张玉荣,罗健辉,3,韩荣成,耿向飞,3,吕晓东,刘岩,王远,*
1中国石油天然气股份有限公司勘探开发研究院,北京 100083
2北京大学化学与分子工程学院,北京分子科学国家实验室,分子动态与稳态结构国家重点实验室,北京 100871
3中国石油天然气集团公司纳米化学重点实验室,北京 100083
1 引言
乳液是一种液体以微小液滴的方式分散于另一种不相溶的液体中形成的分散体系,其中液滴为内相,连续相为外相1。乳液广泛应用于油田开采、食品、医药、化工等诸多领域,其稳定性是乳液的重要性质之一2,3。目前评价乳液稳定性常用的方法为“瓶试法”,即通过测量乳液中析出水的体积与制备乳液时所用水的体积比随时间的变化来评价乳液的稳定性4-6。该方法因操作简单而被广泛采用7,但它不能反映乳液微观结构的变化,在很多情况下难以区分导致乳液不稳定的因素。乳液中分散相液滴的粒径及其分布是影响乳液性质的重要因素,其随时间及环境的变化可用于评价乳液的稳定性。
迄今,人们已发展了一些测量乳液分散相液滴粒径方法,例如,动态光散射法(Dynamic Light Scattering,DLS)8-13、聚焦光反射测量方法(Focused Beam Reflectance Measurement,FBRM)14-18和光学显微镜法19,20。然而这些方法难以满足油田开采等领域对高浓度乳液中分散相液滴真实粒径及其分布进行快速、准确分析的要求。DLS并不能直接测量乳液分散相液滴粒径,而是通过其它物理量的转换获得等效尺寸的信息,当样品分散相浓度较高时还需要对样品进行稀释,其对高浓度乳液的测量结果与真实情况有较大差别。FBRM 利用激光焦点在分散相液滴上扫过的弦长计算液滴的粒径,该方法仅适用于测量粒径较大的分散相,其测量结果受样品浓度等因素干扰严重21,22。光学显微镜法可以给出直观的乳液分散相液滴形貌特征,但该方法通常要求所测样品中分散相呈单层分布,否则在形成二维图像时将导致不同分散相液滴的图像重合,因此该方法也难以用于测量分散相浓度较高的样品22。
激光扫描共聚焦显微成像技术(Confocal Laser Scanning Microscope,CLSM)采用逐点照明和空间针孔调制去除来自非焦点处的散射光,大大提高了图像的对比度和空间分辨率,已被广泛用于活细胞的动态检测、生物样品光学切片和三维结构重构等方面的研究23-28。将CLSM应用于乳液分散相液滴粒径分析时,会遇到两个棘手的问题:首先,难以保证所获得的某张图像的焦平面对应的是液滴的最大截面;其次,在做光学切片分析时,样品因布朗运动可能发生随机的移动。因而采用传统的共聚焦成像分析方法测量乳液分散相液滴粒径及其分布不仅耗时长、效率低,而且还存在较大误差。
为解决上述问题,本文提出一种准确、高效的乳液分散相液滴粒径成像分析方法,可用于测量高浓度乳液液滴粒径或评价乳液的抗凝聚稳定性。我们采用该方法研究了表面活性剂、原油模拟物和水形成的分散体系的稳定性。
2 实验部分
2.1 实验试剂和仪器
正癸烷、十六烷基三甲基溴化铵(CTAB)、萘和十氢萘(国药集团化学试剂有限公司),聚乙二醇辛基苯基醚(OP-10,江苏海安石油化工厂),四苯基卟啉(TPP,上海笛柏化学品技术有限公司)和氯化钠(北京化工厂)试剂均为分析纯。实验用水采用18 MΩ·cm超纯水。
采用上海嫩谷电机设备有限公司生产的NSR-I数显高速乳化均质机制备乳液;采用转盘式共聚焦荧光显微镜(Observer,Z1,ZEISS)拍摄乳液分散相液滴的光学切片图像。
2.2 原油模拟物-水乳液的制备
原油模拟物制备:将3.0 g萘和3.0 mL十氢萘溶解于94.0 mL正癸烷中,再将10.1 mg荧光剂四苯基卟啉(TPP)溶于上述溶液中制得原油模拟物备用。
将6.0 mL上述原油模拟物加入到4.0 mL含乳化剂OP-10的水溶液中(OP-10在水溶液中的质量百分比浓度为0.5%),在6000 r·min-1转速下搅拌2 min,得到乳液I。
将8.0 mL原油模拟物加入到2.0 mL含乳化剂OP-10的水溶液中(OP-10在水溶液中的质量百分比浓度为0.5%),按上述条件搅拌,得到乳液II。
将6.0 mL原油模拟物加入到4.0 mL含乳化剂OP-10的氯化钠水溶液中(OP-10在水溶液中的质量百分比浓度为0.5%,氯化钠水溶液的质量百分比浓度为20.0%),按上述条件搅拌,得到乳液III。
将6.0 mL原油模拟物加入到4.0 mL含乳化剂CTAB的水溶液中(CTAB在水溶液中的质量百分比浓度为0.5%),按上述条件搅拌,得到乳液IV。
将6.0 mL原油模拟物加入到4.0 mL含乳化剂CTAB的氯化钠水溶液中(CTAB在水溶液中的质量百分比浓度为0.5%,氯化钠水溶液的质量百分比浓度为20.0%),按上述条件搅拌,得到乳液V。
2.3 乳液成像分析方法
将待测乳液置于共聚焦皿中,使用转盘式共聚焦荧光显微镜(Observer,Z1,ZEISS)对待测样品进行连续步进式光学切片荧光成像分析。荧光显微成像条件:物镜,Plan-Apochromat 63×/1.40 Oil M27;观察方式,荧光成像;激发波长,405 nm;检测波长,(629 ± 31) nm;相邻两张光学切片的纵向间距(焦平面间距)δz为 0.5 µm。
3 结果与讨论
3.1 高浓度乳液分散相液滴粒径测量方法
如前所述,采用传统的共聚焦成像分析方法测量乳液分散相液滴粒径,存在耗时长且测量结果不准确等问题。为解决上述问题,我们发展了一种准确、高效的乳液分散相液滴粒径的成像分析方法,即用荧光染料标记乳液,采用激光扫描共聚焦显微镜对所标记乳液以连续步进的方式进行光学切片荧光成像分析,获取三张焦平面间距确定的乳液光学切片。测量上述三张光学切片图像中液滴的表观直径,当三张光学切片图像中某液滴表观直径从第一张至第三张为连续递增或递减时,按公式(1)和(2)分别计算出同一液滴粒径的计算值。
公式(1)和(2)依据图1所示的几何关系得出,其中,D1、D2、D3分别为从第一张、第二张和第三张光学切片图像中测得的同一液滴的表观直径;DC1-2、DC2-3分别为利用第一张与第二张光学切片图像和利用第二张与第三张光学切片图像计算的液滴直径;δz为相邻两张光学切片焦平面之间的间距(图1)。
设2|DC1-2-DC2-3|/(DC1-2+DC2-3) =X,X值越小,表明粒子在测量中移动的程度越小,计算值(DC1-2+DC2-3)/2越接近粒子的真实粒径。本文作者的实验结果表明,当X小于15%时,所获得的计算值与从数十张光学切片图像中寻找最大截面的方法获得的实验结果相差不大(差值~10%)。因此,本文中将X< 15%所对应的平均粒径值取为所测液滴的有效粒径。
另一方面,当三张光学切片图像中某液滴的表观直径满足D1=D2≥D3或D1≤D2=D3时,则取相等的表观直径为所测液滴的有效粒径。
根据所测得液滴(200个以上)的有效粒径可获得乳液液滴的平均粒径及粒径分布。该测定方法结合了乳液荧光染料染色、双光学切片成像分析和移动误差消除等策略,可用于准确、高效地测定高浓度原油模拟物-水乳液液滴粒径。
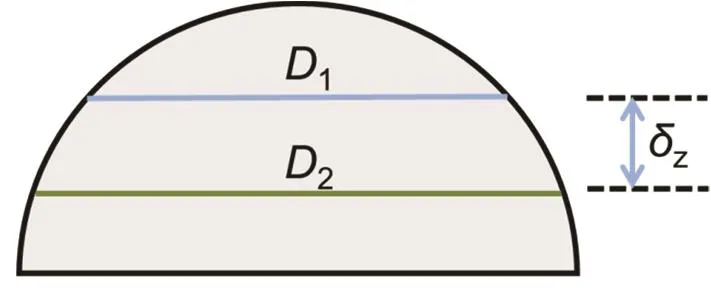
图1 液滴直径测量与计算方法示意图Fig. 1 Schematic diagram of the droplet diameter measurement and calculation method.
3.2 乳液液滴有效粒径测量方法验证
如实验部分所述,我们以OP-10作为乳化剂,将原油模拟物(质量百分比:正癸烷92.3%、萘4.1%和十氢萘 3.6%、TPP 0.1‰)分散于水中,制得油相体积浓度为60.0%的乳液I。采用转盘式共聚焦荧光显微镜(Observer,Z1,ZEISS)对该乳液进行步进式成像分析,连续拍摄了30张光学切片,每张曝光时间90 ms,焦平面间距0.5 μm。选择其中任意相邻的三张光学切片图像(图2A,焦平面位置Z为6-8,选择图像的原则为所测量液滴的图像清晰),按照前述(3.1)乳液分散相液滴有效粒径计算方法获得了乳液I荧光图像中1至3号液滴的有效粒径,结果列于表1 (Dc)。表1中Dmax为从30张光学切片中找出的1至3号液滴的最大截面直径,各液滴最大截面直径对应的光学切片图像如图2B所示。
对比图2A和2B可知,焦平面位置对液滴的表观直径有显著影响。因此,共聚焦显微镜照片上某液滴的表观粒径与其真实粒径之间可能存在很大差别。以图2中的1号液滴为例,在不同的光学切片(如Z= 6和Z= 16)图像中的表观直径有较大差别(16.9和22.2 μm)。因此,若取单张光学切片图像中各液滴的表观直径作为乳液液滴的粒径,会存在较大误差。本文提出根据三张光学切片图像中给出的乳液液滴表观直径及其纵向间距,计算得出液滴的真实粒径。由该方法得到的1至 3号液滴的有效粒径分别为 22.5、22.0和 8.1 μm。上述粒径值与从30张光学切片图像中寻找的相应液滴的最大截面直径(22.2、20.9和 8.1 μm)非常接近,表明本文发展的乳液液滴粒径测量法具有较好的准确性。另外,本文报道的方法仅需拍摄乳液的 3张光学切片,即可实现对高浓度乳液液滴粒径的准确测量,相较于从数十张光学切片中寻找最大截面的测量方法具有更高的效率,且可以减小乳液液滴随机运动导致的误差。

图2 不同焦平面位置处乳液I的荧光显微图像Fig. 2 Fluorescence images of the emulsion I at different focal plane positions.
3.3 高浓度原油模拟物-水乳液稳定性表征
如实验部分所述,我们以乳化剂 OP-10、所配制原油模拟物、水制得了油相体积浓度为60.0%的乳液I和油相体积浓度为80.0%的乳液II。首先以传统的“瓶试法”来考察乳液的稳定性。乳液I和乳液II放置5 h后,油相体积浓度为60.0%的乳液I出现了分层现象,而油相体积浓度为80.0%的乳液II却未出现分层现象。
我们采用本文所述成像方法及成像条件,分别对新制的乳液I和乳液II进行荧光成像分析,然后再对放置5 h后再经缓慢摇匀的乳液I和乳液II进行荧光成像分析,两次所拍摄的荧光成像图如图3所示。
按照本文所述乳液分散相液滴有效粒径测量方法,测得乳液I和乳液II的粒径分布如图4所示。由图4可见,实际测得乳液I和乳液II液滴的平均粒径及其分布很接近且在观测时间内未发生明显变化。这表明乳液 I和乳液 II在放置5 h后,其液滴之间并没有发生凝聚现象,即乳液 I和乳液II均具有较好的抗凝聚稳定性。因此,“瓶试法”之所以反映出乳液II的稳定性高于乳液I,是由于当油水比为60.0%时,在新制备的乳液中,分散相液滴均匀地分散在水相中,随着放置时间的延长,乳液液滴在浮力作用下上浮,呈较为紧密的堆积状态,而多余的水(含有少量乳液液滴)则留在了下层,使乳液 I出现了分层现象。而当油水比为 80.0%时,分散相形成更多紧密堆积的乳液液滴,填满这些乳液液滴之间空隙所需的水量增加,而制备这种乳液时所加的水全部填充到乳液液滴之间的空隙中了,因此乳液II未出现分层现象。
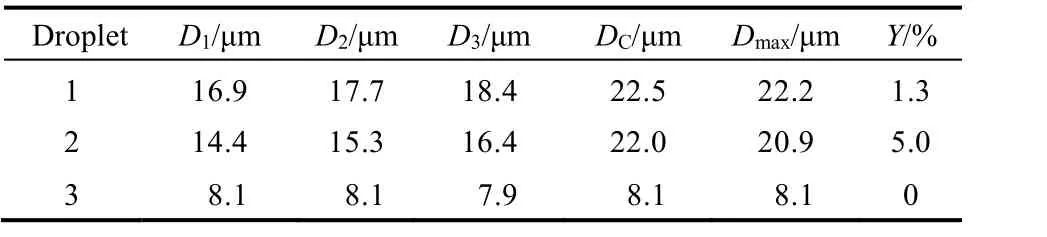
表1 乳液分散相液滴粒径分析结果Table 1 The sizes of droplets in different emulsion samples.
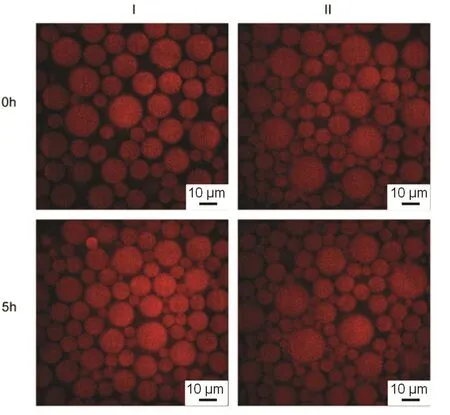
图3 新制备及放置5 h后乳液I和乳液II的荧光显微图像Fig. 3 Fluorescence images of emulsions I and II 0 and 5 h after the preparation.

图4 乳液I和乳液II分散相液滴粒径分布图Fig. 4 Size distributions of dispersed-phase droplets in emulsion I and emulsion II.
上述实验结果表明,用传统的“瓶试法”评价乳液的稳定性具有一定的局限性,乳液的动力学不稳定、乳液液滴絮凝或融合都可能造成乳液分层,传统的“瓶试法”并不能很好地反映乳液分层的原因。此外,对于高浓度的乳液,即使其液滴紧密地堆积在一起,由于分散介质体积小,乳液也可能不出现分层现象。而本文提出的评价方法弥补了“瓶试法”的不足,可以更准确地评价乳液液滴的抗凝聚稳定性。
3.4 不同乳化剂形成乳液的耐盐稳定性
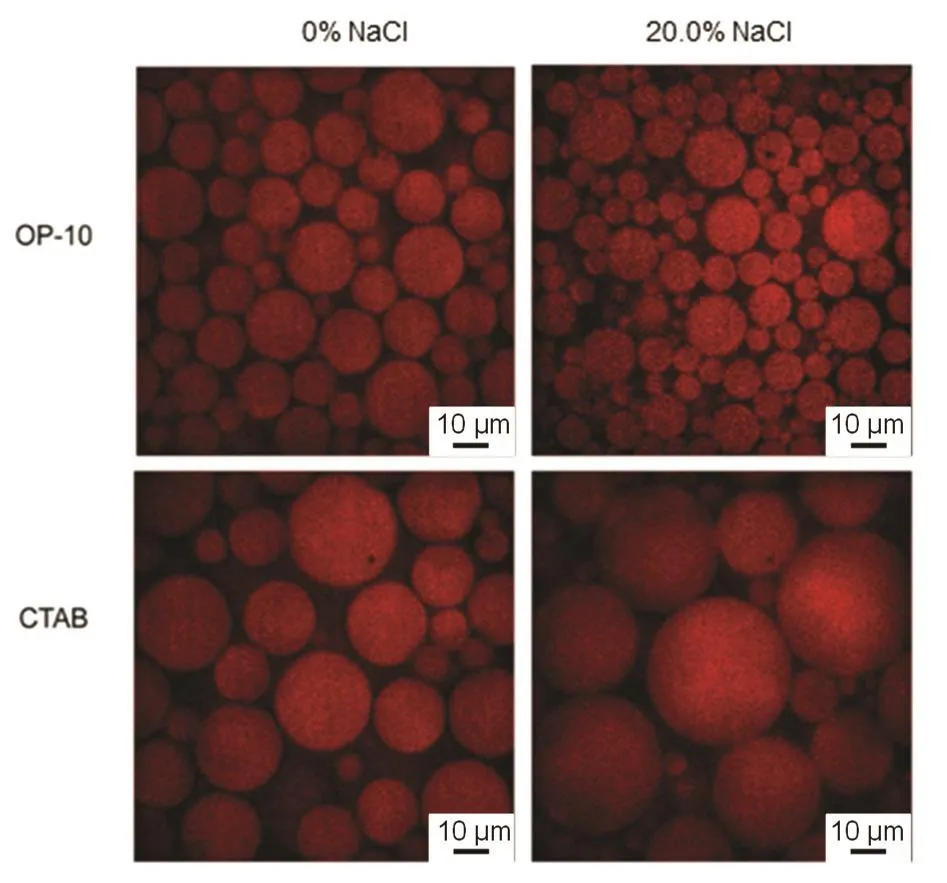
图5 采用乳化剂OP-10和CTAB及不同质量浓度的氯化钠溶液制得乳液的荧光图像Fig. 5 Fluorescence images of emulsions prepared with OP-10, CTAB and aqueous solutions with different contents of sodium chloride.
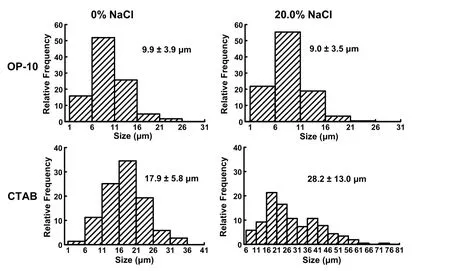
图6 采用乳化剂OP-10和CTAB及不同质量浓度的氯化钠溶液制得乳液液滴粒径分布图Fig. 6 Size distributions of emulsions prepared with OP-10, CTAB and aqueous solutions with different contents of sodium chloride.
我们以乳化剂OP-10、原油模拟物、水制得了油相体积浓度为60.0%的乳液I;由乳化剂OP-10、原油模拟物、20.0%氯化钠水溶液制得油相体积浓度为 60.0%的乳液 III。采用上述成像方法及成像条件对乳液I和乳液III进行了荧光成像分析。其荧光图像如图 5所示。按照本文提出的乳液分散相液滴有效粒径测量方法,测得乳液I和乳液III分散相液滴粒径及分布如图6所示。由图6可见,乳液I和乳液III分散相液滴的平均粒径及粒径分布变化不大,这表明 OP-10乳化剂形成的乳液具有较好的耐盐稳定性。OP-10属于非离子型表面活性剂,乳液液滴之间的空间位阻等作用是阻止其液滴之间发生絮凝(flocculation)或融合(coalescence)的主要因素。因此,OP-10乳化剂形成的乳液受强电解质的影响较小,表现出很好的耐盐稳定性。
如实验部分所述,我们以乳化剂CTAB,原油模拟物,水制得了油相体积浓度为 60.0%的乳液IV;由乳化剂CTAB,原油模拟物,20.0%氯化钠水溶液制得油相体积浓度为60.0%的乳液V。采用上述成像方法及成像条件对乳液IV和乳液V进行了荧光成像分析,其荧光图像如图 5所示。按照上述乳液分散相液滴有效粒径测量方法,测得乳液IV和乳液V分散相液滴粒径尺寸及分布如图6所示。由图6可见,与乳液IV相比,乳液V分散相液滴的粒径大且分布宽,表明CTAB乳化剂形成的乳液耐盐稳定性不高。CTAB是阳离子表面活性剂,在 20.0%氯化钠水溶液环境中,强电解质的存在会使CTAB乳化剂形成的乳液液滴表面上的双电层受到压缩,降低了相邻液滴间的斥力,液滴之间更易靠近,进而发生液滴融合,使液滴粒径变大。
4 结论
本文报道了一种测定乳液分散相液滴粒径的成像分析方法,该方法结合了乳液荧光标记、双光学切片成像分析和移动误差消除等策略,可以对浓度高、颜色深的乳液分散相液滴粒径及其分布进行准确、高效的测定。
采用本文提出的方法研究了乳液I和II的抗凝聚稳定性,结果表明,虽然乳液I和II经放置后分层情况完全不同,但它们液滴的抗凝聚稳定性相似。我们考察了乳化剂OP-10和CTAB形成乳液的耐盐稳定性,结果表明当氯化钠水溶液浓度为20.0%时,乳化剂OP-10形成的乳液耐盐稳定性明显优于CTAB形成的乳液的耐盐稳定性。本文提出的方法克服了“瓶试法”的不足,为深入研究高浓度乳液微观结构的衍化提供了一种有效的方法。
