SOX方案联合阿帕替尼一线治疗晚期胃癌的临床研究
2019-04-22韩忠诚马丽丽崔智文冯燕艳王芳
韩忠诚 马丽丽崔智文冯燕艳 王芳
作者单位:830000 乌鲁木齐 1新疆维吾尔自治区人民医院肿瘤科;835000 伊犁 2伊犁州新华医院肿瘤科;830000 乌鲁木齐 3新疆维吾尔自治区人民医院皮肤科
晚期胃癌大多已丧失手术治疗机会,5年生存率较低,预后差。基于铂类药物联合氟尿嘧啶类抗代谢化疗药物是常用的化疗方案,但疗效欠佳[1]。靶向治疗成为近年的研究热点,血管内皮生长因子研究的深入和血管生成抑制剂的研发,为此类患者治疗提供了新的思路。阿帕替尼是我国自主研发的血管内皮生长因子受体2(vascular endothelial growth factor receptor,VEGFR-2)拮抗剂,单独应用于胃癌患者的疗效已得到证实[2],但与替吉奥和奥沙利铂联合应用的疗效及安全性尚不明确[3]。本研究探讨阿帕替尼联合替吉奥、奥沙利铂一线治疗晚期胃癌的临床疗效,并随访生存情况,以期为此类患者的治疗提供新思路。
1 资料与方法
1.1 一般资料
选择2015年2月至2016年10月于新疆维吾尔自治区人民医院就诊的晚期胃癌患者。纳入标准:⑴符合《胃癌规范化诊疗指南(试行》[4]晚期胃癌的诊断标准;⑵病例资料完整,年龄18~65岁;⑶既往均未行手术治疗和放疗;⑷明确分期、病理学分型和转移部位;⑸无化疗禁忌证,ECOG评分0~2分;⑹至少有一个CT或MRI可测量的客观靶病灶;⑺预计生存时间超过3个月。排除标准:⑴既往接受替吉奥、奥沙利铂或阿帕替尼治疗;⑵合并严重心脑血管疾病或其他系统严重疾患;⑶合并其他原发肿瘤疾病;⑷对本研究所用药物过敏或有明显过敏倾向;⑸治疗和随访依从性较差。本研究经医院伦理委员会批准(编号:2015007),患者或其家属知情同意。
1.2 治疗方法
根据患者纳入研究的序号,采用随机数表法分为对照组和试验组,每组44例。给予对症支持治疗的基础上,对照组采用替吉奥联合奥沙利铂方案(SOX方案):替吉奥胶囊(山东新时代药业有限公司,国药准字 H20080802,替加氟 20 mg、吉美嘧啶 5.8 mg、奥替拉西钾19.6 mg)口服,体表面积大于1.50 m2者,60 mg/次;小于 1.25 m2者,40mg/次;介于 1.25~1.50 m2者,50 mg/次;2 次/d,连续 14 d;疗程第 1天给予奥沙利铂注射液(深圳海王药业有限公司,国药准字H20031048)130 mg/m2+葡萄糖溶液(质量浓度为5%)250~500 mL,输注 2 h,21 d为 1周期。试验组在对照组的基础上给予甲磺酸阿帕替尼片(江苏恒瑞医药股份有限公司,国药准字H20140105,0.425 g×14片),于餐后30 min口服,每次850 mg,1次/d,21 d为1个周期,预计完成2个周期治疗。
1.3 观察指标
主要评价指标为无疾病进展生存期(progressionfree survival,PFS)和总生存期(overall survival,OS),OS定义为患者纳入研究随机化分组至因任何原因死亡的时间;PFS定义为患者纳入研究随机化分组至肿瘤进展(任何方面)或死亡(因任何原因)的时间。
次要评价指标为近期疗效和不良反应。客观疗效评价按实体瘤疗效评价标准(RECIST 1.1)[6],分为完全缓解(CR):所有靶病灶全部消失;部分缓解(PR):靶病灶最长径之和与基线状态比较,至少减少30%,或者出现一个或多个新病灶;疾病进展(PD):靶病灶最长径之和与治疗开始后所记录的最小靶病灶最长径之和比较,至少增加20%;疾病稳定(SD):靶病灶减小程度未达PR,增加程度未达PD,介于两者之间。总有效率(RR)=(CR+PR)/总例数×100%,疾病控制率(DCR)=(CR+PR+SD)/总例数×100%。
依照美国卫生及公共服务部国立卫生研究院国家癌症研究所的常见毒性分级标准(CTCAE)4.03版对患者出现的治疗相关不良反应进行统计和分析,重点观察Ⅲ级以上血液学和非血液学不良反应发生率。
1.4 随访
每月进行电话随访,治疗后第1个月,之后每2个月门诊复查,每个化疗周期结束后行腹部超声、血清肿瘤标志物检查,如腹部超声和血清肿瘤标志物检查提示出现新发可疑病灶,行腹部增强CT扫描进一步明确。治疗结束前结合门诊复查随访,治疗结束后每2个月采用电话、微信等形式随访,每6个月行腹部超声和血清肿瘤标志物检查。随访截止时间为2017年10月31日。
1.5 样本量估算和试验监管
根据主要评价指标PFS采用PASS 15.0进行样本量估算,既往研究表明晚期胃癌患者放化疗后中位PFS为6个月[5],本研究将中位PFS提高至12个月,临床界值δ=20%,使用双侧检验α=0.05,β=0.20,把握度设为80%,需入组患者32例每组,假设脱落率为15%,共需患者74例。
试验监管:本研究遵照《赫尔辛基宣言》和国家食品药品监督管理局《药物临床试验质量管理规范(2003版)》以及新疆维吾尔自治区人民医院临床试验管理规范指导原则,在本院组织的安全检查委员会监督下进行试验设计、数据收集、分析和解读。
1.6 统计学处理
采用SPSS 23.0软件进行数据处理。服从正态分布的计量资料以均数±标准差(±s)表示,组间比较采用独立样本t检验,不服从正态分布的计量资料以中位数(四分位数间距)表示;计数资料采用例数(构成比)的形式表示,组间比较采用χ2检验;采用Kaplan-Meier计算生存率,组间比较行Log-rank检验。以P<0.05为差异有统计学意义。
2 结果
2.1 基线资料比较
2015年2月至2016年10月共纳入晚期胃癌患者88例。全部患者均接受试验干预,无退出病例,两组患者各失访2例。两组患者的各项基线资料比较差异均无统计学意义(P>0.05),见表1。

表1 两组患者的基线资料比较Tab.1 Comparison of baseline data between two groups
2.2 近期疗效比较
两组患者均完成治疗计划,可评价疗效。试验组获CR 2例,PR 16例,SD 20例,PD 6例;对照组获CR 0例,PR 9例,SD 22例,PD 13例。试验组RR高于对照组,差异有统计学意义(40.91%vs20.45%,χ2=4.238,P=0.037);DCR 亦高于对照组,但差异无统计学意义(86.36%vs70.45%,χ2=3.289,P=0.070)。
2.3 生存分析
试验组中位OS为12(8~12)个月,对照组为9.5(5~12)个月,差异有统计学意义(χ2=4.254,P=0.039),见图1。试验组中位PFS为9(7~11)个月,对照组为6(4~9)个月,两组比较差异有统计学意义(χ2=8.815,P=0.003),见图 2。

图1 两组患者的总生存期曲线Fig.1 Overall survival curves of two groups
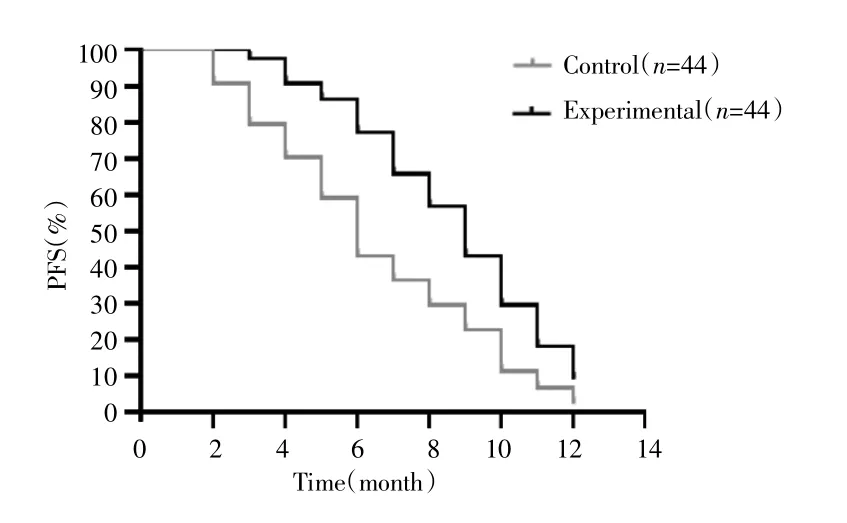
图2 两组患者的无疾病进展生存曲线Fig.2 Progression-free survival of curves of two groups
2.4 不良反应
两组患者均可评价不良反应,试验组3例、对照组1例患者因无法耐受不良反应暂停用药,经对症治疗后继续化疗,无治疗相关死亡。主要不良反应为血液学毒性、胃肠道反应、高血压、蛋白尿、手足综合征、疲劳等。试验组高血压和手足综合征总发生率高于对照组,差异有统计学意义(P<0.05);试验组Ⅲ级以上不良反应总发生率与对照组比较,差异无统计学意义(43.18%vs25.00%,χ2=3.237,P=0.072),但试验组Ⅲ级以上蛋白尿、高血压和手足综合征更常见,见表2。
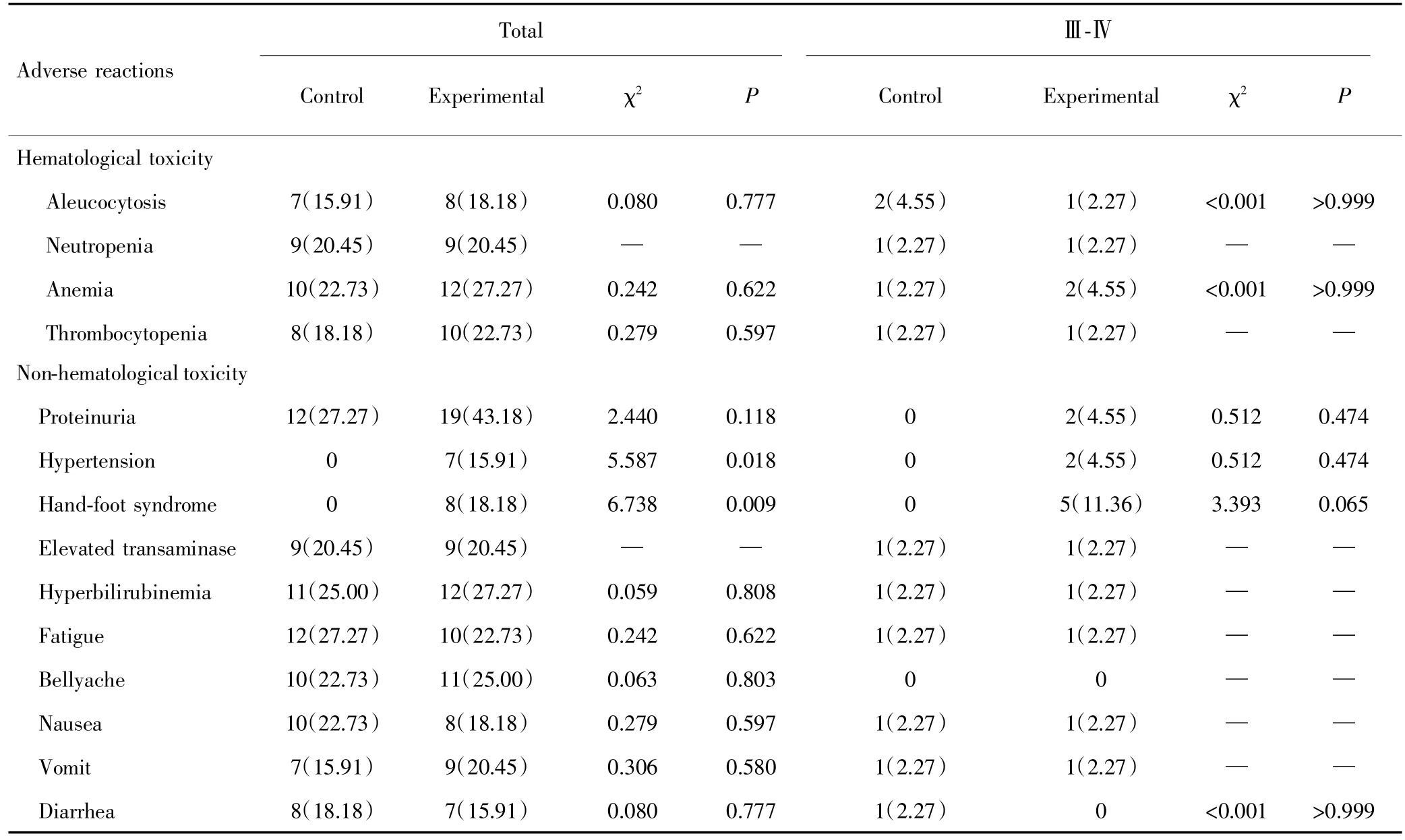
表2 两组患者不良反应比较[n(%)]Tab.2 Comparison of adverse reactions between two groups[n(%)]
3 讨论
胃癌是全球癌症相关死亡第三大病因,而近一半的新发病例发生在中国[7]。化疗是胃癌患者重要的治疗方法,血管生成抑制剂在肺癌、乳腺癌和肾癌等恶性肿瘤治疗中可取得良好疗效[8-10],但对于晚期胃癌此类药物的作用尚存争议。5-FU是最早应用的氟尿嘧啶类化疗药物[11],多种酶类参与了肿瘤细胞对5-FU的水解,其中二氢嘧啶脱氢酶(DPD)是5-FU水解起始酶和限速酶[12]。替吉奥是由替加氟、吉美嘧啶和奥替拉西钾组成的复方制剂。吉美嘧啶作为DPD抑制剂,通过抑制DPD活性,可降低5-FU被水解而失效的风险,能使5-FU长久发挥抗肿瘤作用。奥替拉西钾对分布于消化道的乳清酸磷酸核糖基转移酶有选择性拮抗作用,可选择性抑制5-FU失活,增强抗肿瘤作用,降低消化道毒性[13-14]。奥沙利铂是新一代铂类抗肿瘤代谢药物,与DNA结合的速率高,耐药性低。欧美大型研究以及基于东方人群的研究均显示,替吉奥联合奥沙利铂在晚期胃癌患者的治疗中的疗效较明确[15-16]。虽然替吉奥联合奥沙利铂化疗方案能控制病情进展,延长患者总生存时间,但中位生存时间仍难以突破12个月[17],仍亟需寻找更好的治疗方案改善患者预后。
血管内皮生长因子(VEGF)和VEGFR-2介导的信号传导和血管生成在胃癌的发病机制中起重要作用[18]。阿帕替尼是我国自主研发的抗血管生成靶向药物,是VEGFR-2的酪氨酸激酶抑制剂,在胃腺癌动物模型中表现出了明显的抑制肿瘤生长和血管形成作用[19]。杨欣怡等[20]回顾性分析38例采用不同方案行二线治疗晚期胃癌患者的临床疗效,发现采用阿帕替尼联合替吉奥方案治疗的患者DCR和PFS明显高于单一用药患者。LI等[21]一项纳入267例经二线及以上化疗后复发的晚期胃癌患者的多中心、随机双盲试验也显示,相对于应用安慰剂治疗的患者,采用阿帕替尼治疗的患者中位OS和PFS明显改善。此外,经荟萃分析研究阿帕替尼作为胃癌二线和三线治疗的疗效亦得以认可[22]。本研究采用替吉奥和奥沙利铂联合阿帕替尼一线治疗晚期胃癌,发现替吉奥联合奥沙利铂治疗的患者DCR高达70.45%,与联合阿帕替尼治疗患者的DCR(86.36%)无明显差异,说明采用常规化疗药物一线治疗晚期胃癌患者已可较好地控制疾病,然而虽然对照组患者取得较好的DCR,但RR却较试验组明显降低,反映了晚期胃癌患者化疗后病情进展迅速的特点。提高患者的生存预期是恶性肿瘤治疗的根本目的[23]。本研究结果显示试验组中位OS和中位PFS均显著高于对照组,提示联合阿帕替尼后有效延长了患者的生存期,原因可能与联合阿帕替尼后新生血管生成明显受抑制,减少了原发灶和转移灶的新生血供,延缓远处转移发生、减缓病灶扩散速度等有关[24-25]。此外,阿帕替尼还可通过影响胃癌患者VEGFR-2的循环浓度,减弱肿瘤侵袭性,降低患者的病情进展风险,从而提高化疗疗效[26]。
阿帕替尼于2014年被国家食品药品监督管理总局批准上市,前期临床研究表明阿帕替尼的严重不良反应较低,患者可耐受[27]。中国临床肿瘤学会抗肿瘤药物安全管理专家委员会学者发布的《阿帕替尼治疗胃癌的临床应用专家共识》中指出蛋白尿、高血压和手足综合征为阿帕替尼常见的不良反应[28]。本研究中两组患者的血液学与非血液学毒性不良反应比较,试验组高血压和手足综合征总发生率高于对照组,且Ⅲ级以上蛋白尿、高血压和手足综合征更为常见,与上述专家共识结论一致,但组间差异并不明显,且两组患者不良反应经对症治疗后均可缓解,未影响后续化疗,无治疗相关死亡,说明替吉奥和奥沙利铂联合阿帕替尼治疗并未增加非预期的不良反应,患者均可耐受,安全性良好。
本研究显示,替吉奥、奥沙利铂联合阿帕替尼作为晚期胃癌患者的一线治疗方案具有较好的临床疗效,患者生存可获益,不良反应可耐受,但本研究为单中心、小样本短期研究,尚需大样本、多中心的随机双盲研究进一步验证其疗效。
