艾康片制备工艺药效学筛选研究
2019-04-20姚荣妹毛鑫包蕾高英杰王彦礼崔晓兰
姚荣妹,毛鑫,包蕾,高英杰,王彦礼,崔晓兰
(中国中医科学院中药研究所,北京 100700)
艾康片是由川芎、茯苓、灵芝、金银花、野菊花、苦参、甘草等13味药组成的中药复方,我们前期对其进行了大量的中药组方筛选和药理药效研究,发现艾康片可以增强机体免疫功能,在抗肿瘤(肺)方面表现出很好的药效作用。提取工艺是中药复方制备的关键环节,直接影响临床疗效,为进一步筛选艾康片最佳的工艺提取方法,我们根据其临床适应症设计了相应的药效学实验,为其进一步工艺路线的确定和工艺参数的选择提供参考。本实验利用裸小鼠建立移植性肺癌动物模型[1-3],结合体内抗肿瘤的药效学评价方法,观察艾康片3种提取工艺在抑制肺部肿瘤生长方面的效果。
1 实验材料
1.1 动物及细胞株
BALB/CA-nu品系的裸小鼠,体质量(19±1)g,雌雄各半,SPF级,购自北京维通利华实验动物技术有限公司,许可证号:SCXK(京)2012-0001。A549人小细胞肺癌传代细胞,购自中国医学科学院基础医学研究所细胞资源中心。
1.2 药品及试剂
艾康片提取物,中国中医科学院中药研究所中药制剂研究中心提供,批号:20160912-1、20160912-2、20160912-3,规格:200 mL/瓶;复方环磷酰胺片,购自通化茂祥制药有限公司,批号:160702。PBS磷酸缓冲液(美国Gibco,批号1789842);DMEM高糖培养基(美国Gibco,批号8116489);胎牛血清(美国Gibco,批号1390781);双抗(美国Hyclone,批号J130061);0.25%胰酶(美国Gibco,批号1616025)。
1.3 仪器
CO2培养箱(美国Thermo Scientific,Thermo-371);洁净工作台(美国AIRTECH,SW-CJ-2FD);离心机(德国Eppendorf,5810R);倒置显微镜(日本OLYMPUS,CKX41);高温蒸汽灭菌器(ALP,CLG-32L);自动细胞计数仪(上海睿钰生物科技有限公司,countstar-IC1000);电子天平(上海梅特勒-托利多仪器有限公司,AL204);数显卡尺(上海恒胜工具有限公司,METR-ISO)。
2 实验方法
2.1 剂量设计
艾康片成人临床推荐剂量为7.6 g生药/60(kg·d),换算成裸小鼠等效用量为1.4 g/(kg·d)。实验中采用2.8、1.4、0.7 g/(kg·d)3个剂量组(分别相当于人临床用量的2倍、等倍、1/2倍)。该药3种提取工艺含药量均为2 g生药/mL,故3种提取物高、中、低剂量为1.4 mL/(kg·d)、0.7 mL/(kg·d)、0.35 mL/(kg·d)。复方环磷酰胺片成人临床推荐剂量175 mg/60(kg·d),实验中小鼠用量按人用量的11倍计算,小鼠的给药剂量为32 mg/(kg·d)。
2.2 人肺腺癌细胞株(A549)的培养
细胞株培养条件为10%胎牛血清的DMEM培养液, 37℃ 5% CO2恒温培养箱内,细胞培养至80%~90%融合率,0.25%胰蛋白酶消化,离心后传代,待细胞培养至一定数量,用PBS稀释成肿瘤细胞悬液接种于实验动物体内。
2.3 细胞体外活性检测及肿瘤细胞悬浮液的制备
在无菌条件下取生长良好的A549肿瘤细胞,用0.25%胰蛋白酶消化、离心后,用PBS混悬细胞,采用台盼蓝染色法,使用全自动细胞计数仪检测细胞活性并计数。用PBS稀释成2×107个细胞/mL浓度的肿瘤细胞悬浮液。
2.4 制备人肺癌移植瘤模型
在无菌条件下,将裸鼠用75%乙醇皮肤消毒后,在裸鼠右腋皮下接种人肺腺癌A549细胞悬液,0.2 mL/只,接种后定期观察小鼠的精神、饮食及排便等情况。接种1周左右,可见接种部位皮下长出小米粒大小的硬结,为移植瘤模型建成。
2.5 分组及给药
待肿瘤生长至100 mm3左右,挑选瘤块、体质量均匀的裸小鼠,随机分为11组,分别为模型对照组、环磷酰胺阳性对照组、艾康1号高、中、低3个剂量组、艾康2号高、中、低3个剂量组、艾康3号高、中、低3个剂量组,每组7只,分组当天开始灌胃给药,每日1次,连续21 d,给药容积为0.2 mL/10 g。
2.6 观察指标及计算方法
平均瘤重、肿瘤生长抑制率、肿瘤体积、相对肿瘤体积、相对肿瘤增殖率。
肿瘤体积(tumor volume,TV):TV=1/2×a×b2或π/6×a×b×c,其中a、b、c分别表示长宽高。
相对肿瘤体积(relative tumor volume,RTV):RTV=Vt/V0,其中V0为给药前测量所得肿瘤体积,Vt为每一次测量时的肿瘤体积。
相对肿瘤增殖率T/C(%):T/C%=TRTV/CRTV×100%,(TRTV为治疗组RTV;CRTV为阴性对照组RTV)。
2.7 统计方法
3 结果
3.1 对人肺腺癌细胞株(A549)裸小鼠模型肿瘤体积生长情况的影响
艾康片3种工艺样品在给药2 d后起肿瘤体积与模型对照组比较均有所下降,给药组裸鼠肿瘤体积的生长曲线均位于模型对照组下方。2号、3号样品在给药8~20 d后肿瘤体积与模型对照组比较明显下降(P<0.01,P<0.05),1号样品在给药12~20 d后肿瘤体积与模型对照组比较明显下降(P<0.01,P<0.05),其中3号药品中剂量组肿瘤体积在给药4~20 d后5个检测时间点与模型对照组比较均有差异(P<0.01),从数值上看差异也最为显著。(见表1、图1)。

图1 艾康片治疗后肿瘤体积生长曲线
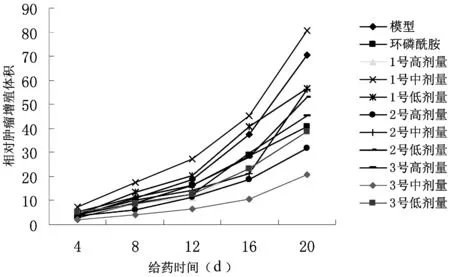
图2 艾康片对人肺腺癌细胞株(A549)裸小鼠相对肿瘤增殖体积的影响
3.2 对人肺腺癌细胞株(A549)裸小鼠相对肿瘤增殖体积(RTV)及相对肿瘤增殖率的影响
艾康3号中剂量组的相对肿瘤增殖体积在给药期间与模型对照组比较有差异(P<0.05),其余各用药组与模型组无差异。与模型对照组比较,艾康1号高剂量组、艾康2号高剂量组、艾康3号中剂量组的相对肿瘤增殖率在28%~70%之间,艾康1号中剂量组和艾康1号低剂量组相对肿瘤增殖率在给药前16 d均高于模型组,其余用药组的相对肿瘤增殖率在50%~90%之间。见图2、图3。
3.3 对人肺腺癌细胞株(A549)裸小鼠相对肿瘤重量的影响
艾康片各剂量组瘤块重量与模型对照组比较均有差异(P<0.01),艾康3号中剂量组肿瘤块重量最小,见表2。
表1 艾康片对人肺腺癌细胞株(A549)裸小鼠模型肿瘤体积生长情况的影响
续表1 艾康片对人肺腺癌细胞株(A549)裸小鼠模型肿瘤体积生长情况的影响
注:与模型对照组比较,*P<0.05,**P<0.01
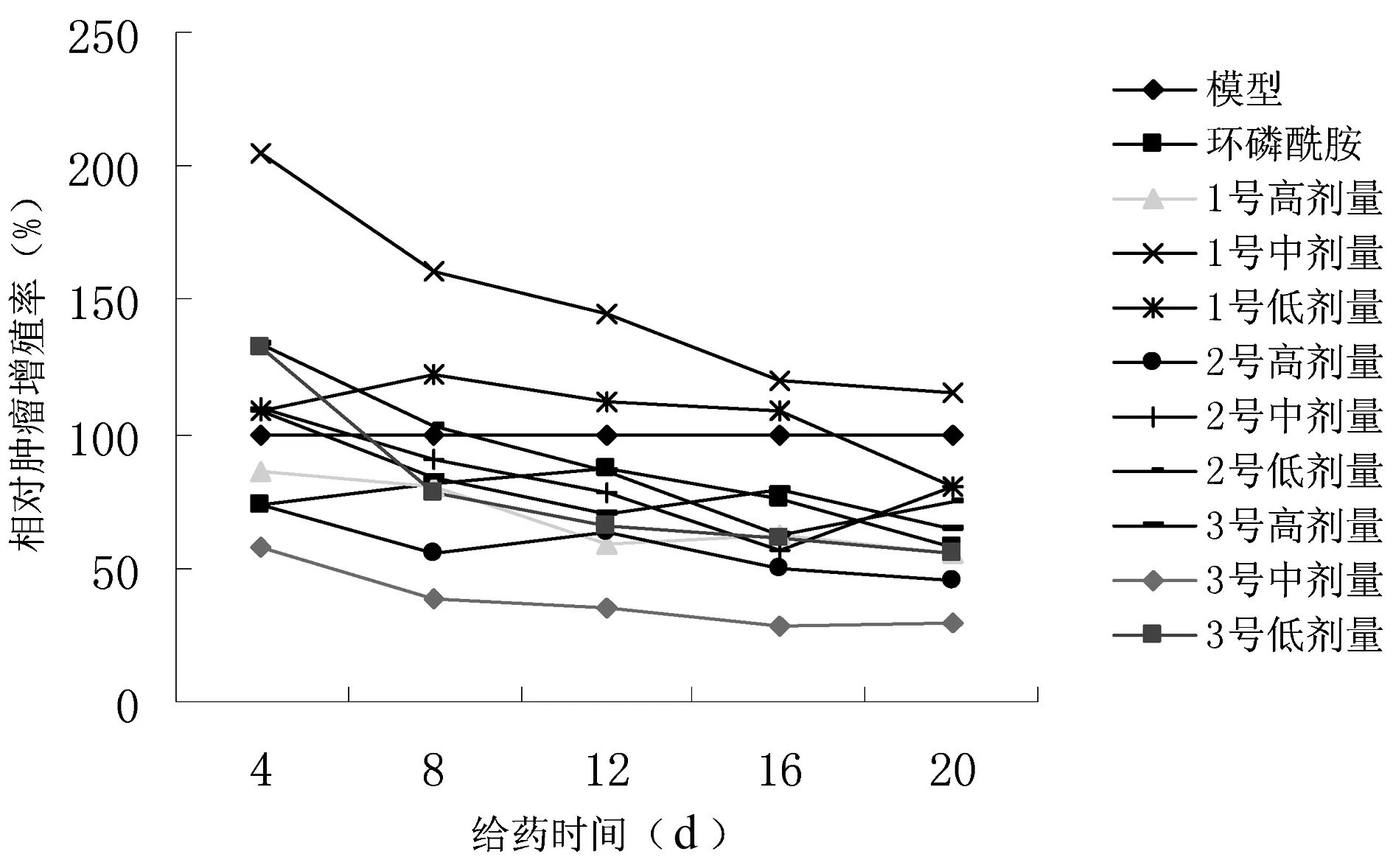
图3 艾康片对人肺腺癌细胞株(A549)裸小鼠相对肿瘤增殖率的影响
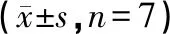
表2 艾康片对人肺腺癌细胞株(A549)裸小鼠模型肿瘤重量的影响
注:与模型对照组比较,**P<0.01
4 讨论
肺癌已成为世界上发病率和死亡率最高的恶性肿瘤之一,且发病率还在持续增加[4-6]。世界卫生组织国际癌症研究署2015年发布的GLOBOCAN癌症报告显示,预测到2025年,中国每年新增肺癌病例将超过100万,将成为全球肺癌患者最多的国家。因此,抗肺癌药物的研究开发在我国显得尤为迫切,也是为当前的科研热点之一。中国是天然药物资源大国,从积累了数千年临床经验的中草药宝库中发掘有效的抗肿瘤新药是我国医药界的重要研究方向。艾康片从经典古方化裁而来,方中川芎之类活血通脉,茯苓之类补肺脾,灵芝补气安神,金银花、野菊花之类清热解毒,甘草调和以上药物的烈性兼备止痛功效,诸药合用共奏活血化瘀、补气宁心、清热解毒、滋补强身之功,具有抑制肿瘤生长,改善机体不适症状,增强机体免疫功能的作用。
将人类肺癌细胞系移植到免疫缺陷动物皮下是对恶性肿瘤进行体内实验研究的首选方法[7]。裸鼠移植性肺癌动物模型是把肺癌组织块或肺癌细胞系接种于实验动物体内形成的荷瘤动物模型,主要包括异位移植、原位移植和转基因动物模型三类。目前常用的肺癌细胞系包括人肺腺癌A549、SPC-A-1、Calu-3、LTEP-a-2、人肺扁平上皮癌QG-56、人高转移肺癌95-D、人肺癌大细胞系NCI-H460以及人肺癌小细胞系NCI-H446等[8]。本研究在裸小鼠右腋皮下接种人肺腺癌A549细胞悬液制备肺癌移植瘤模型,观察艾康片3种提取物的抑瘤作用。实验结果显示,3种提取样品均有降低裸鼠肿瘤体积、相对肿瘤增殖体积、肿瘤增殖率、肿瘤重量的作用,其中3号样品中剂量组肿瘤体积明显减小,是仅有的在相对肿瘤增殖体积方面与模型对照组比较有差异的用药组,其相对肿瘤增殖率在给药8 d后在40%以下,且瘤块重量最小。上述药效学研究数据提示,3号样品制剂在抑制肿瘤方面有效、剂型合理,且未表现出明显毒副作用,该样品的提取工艺有推广应用价值。
