离子液体在虾壳甲壳素提取中的应用研究进展
2019-04-16何晓燕严来喜
李 艳 高 静,2,3 何晓燕 严来喜
(1.广东海洋大学食品科技学院,广东 湛江 524088;2.水产品深加工广东省普通高校重点实验室,广东 湛江 524088;3.广东省水产品加工与安全重点实验室,广东 湛江 524088)
甲壳素又名几丁质,是地球上蕴藏量最丰富的有机物之一。如图1所示,甲壳素是由β-1,4-2-乙酰氨基-2-脱氧-D-葡萄糖通过β-1,4糖苷键连接起来的线性高分子多糖[1],脱乙酰度达到50%以上的甲壳素又被称为壳聚糖[2]。甲壳素及壳聚糖因具有优异的生物相容性、生物降解性和热化学稳定性被广泛应用于食品、医药、农业、纺织等领域[3]。地球上每年甲壳素的生物合成量约为100亿t,是年产量仅次于纤维素的可再生天然资源[4-5]。海产品加工副产物虾、蟹壳是甲壳素的主要原料,占生物合成甲壳素总量的80%[6]。从水产品加工下脚料中提取回收甲壳素不仅可以缓解资源浪费,而且使副产物得到高值化利用[7]。
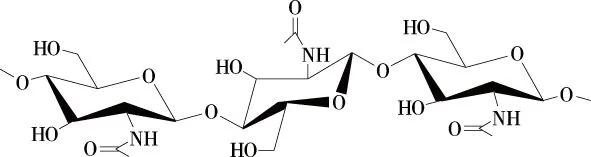
图1 甲壳素的化学结构
虾壳主要含有甲壳素15%~25%、碳酸钙25%~50%、蛋白质35%~50%[6]。长期以来,工业提取甲壳素采用强酸脱碳酸钙和碱脱蛋白质。此方法对酸、碱需求量大,还造成严重的环境污染。而且,碱处理会导致甲壳素部分脱乙酰和聚合物水解,使甲壳素分子量降低[8-9]。近年来,微生物发酵法和酶法提取甲壳素因反应条件温和、环境友好和耗能少等优点而备受关注,但提取时间长、效率低和脱蛋白不充分等缺陷限制了其工业化应用[10]。
离子液体是由有机阳离子和有机或无机阴离子组成的低温熔融盐,又称室温熔盐,具有可设计性强和热稳定性高的特点[11-13]。对纤维素、甲壳素等多糖有很强的溶解能力[14-16]。近年来,利用离子液体从虾壳中提取回收甲壳素的研究得到了广泛关注[17-19]。文章主要从甲壳素和虾壳在离子液体中的溶解特性、甲壳素提取物成分分析以及结构表征3个方面综述以离子液体为溶剂从虾壳中提取回收甲壳素的研究进展,旨在为对虾加工下脚料的高值化利用提供理论依据。
1 甲壳素在离子液体中的溶解性
1.1 离子液体的阴离子对甲壳素溶解度的影响
离子液体(ILs)具有“可设计性”,不同阴、阳离子组合的离子液体对物质的溶解能力不同[20-21],表1列举了甲壳素在多种离子液体中的溶解度。离子液体的氢键接受能力(β值)受其阴离子支配,具有较强氢键接受能力的阴离子(如Ac-、Br-、Cl-)容易与甲壳素氨基上的H原子形成稳定的氢键,从而促进甲壳素的溶解[29]。Qin等[23]发现在100 ℃、19 h条件下甲壳素在[Emim]Ac中的溶解度可达15.2%,而在[Emim]Cl中的溶解度仅为4.2%。类似的,甲壳素在[Amim]Cl和[Amim]Ac中的溶解度分别为0.5%[24]和5.0%[25]。一般情况下,离子液体的阴离子对甲壳素溶解能力顺序为:Ac->Cl-。
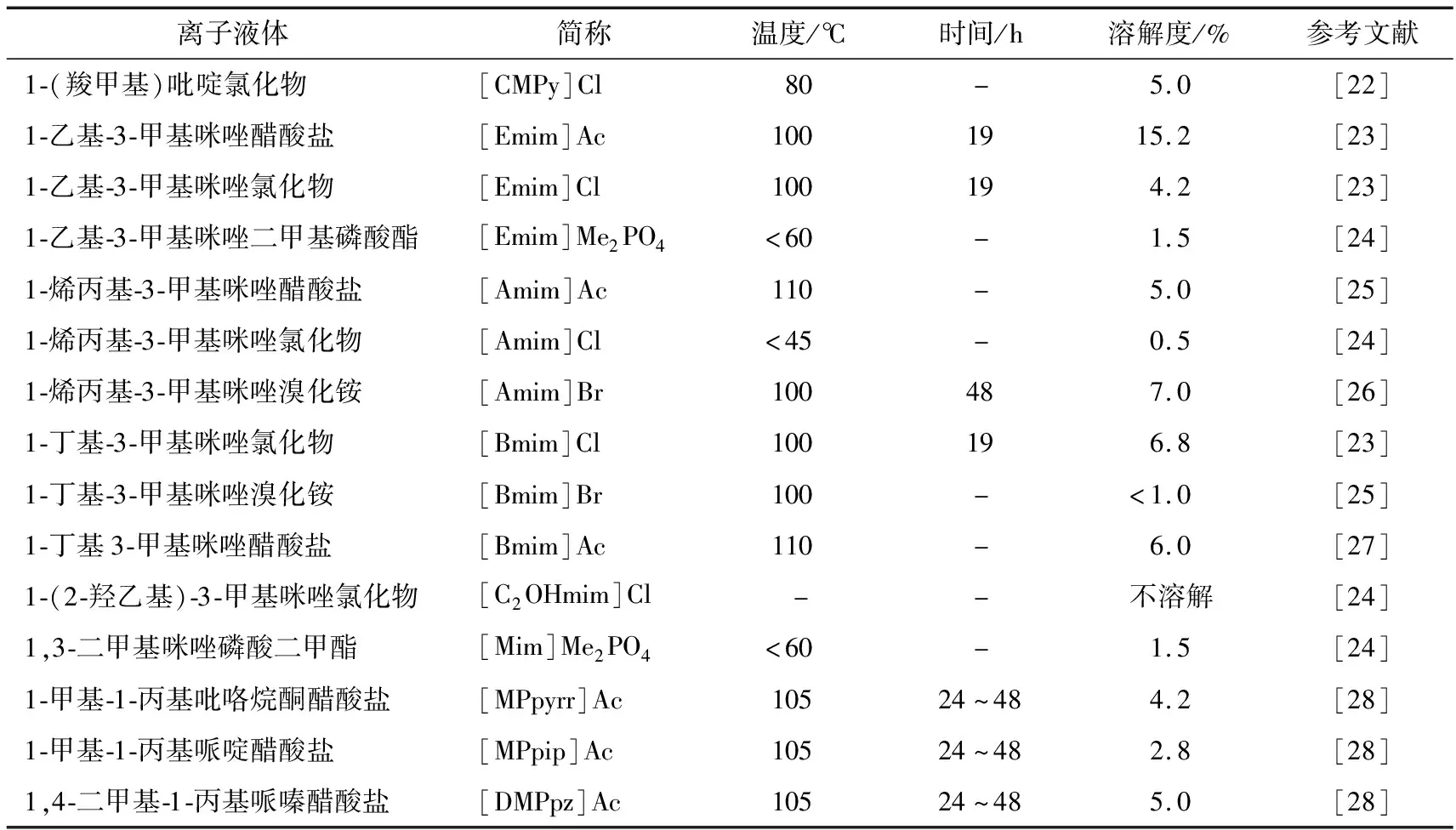
表1 甲壳素在不同离子液体中的溶解度†
† “-”表示文献中未指出。
1.2 离子液体的阳离子对甲壳素溶解度的影响
咪唑类离子液体溶解甲壳素的能力较吡咯烷、哌啶和哌嗪类离子液体强,因为咪唑基离子液体结构中包含1个 5元环,比6元环组成的离子液体显示出更高供给质子的能力和更强的酸性[29]。此外,由于阳离子疏水性和黏度均随烷基链长度的增加而增大,不利于分子的溶解[30]。不仅如此,受阳离子烷基链官能团的影响,甲壳素在Cl-基离子液体中的溶解度关系为[Emim]+>[Amim]+>[C2OHmim]+[23-24]。因此,体积小、极性强的阳离子[Emim]+能够与甲壳素中—OH的氧原子和—NH 的氮原子产生较强的氢键作用。
如图2所示,离子液体溶解甲壳素的机理为:阴离子与甲壳素的乙酰胺基和羟基形成氢键,削弱了甲壳素分子内和分子间氢键作用,导致甲壳素分子链的扭曲和剥落。同时,离子液体的阳离子穿透甲壳素分子链之间的空隙,防止剥离后结晶相的恢复。最后,甲壳素链以完全分离的分子形式分散在离子液体中[31]。
2 离子液体提取虾壳中甲壳素的工艺
[Emim]Ac等离子液体对甲壳素的良好溶解性,为提取虾壳中甲壳素的良好溶剂。一般情况下,以离子液体为溶剂提取虾壳中甲壳素的工艺流程如图3所示。离子液体与虾壳粉按照一定比例混合后,在适当加热温度和搅拌时间处理下能够溶解矿物质、蛋白质和甲壳素,向混合体系加入反溶剂(水等[28,32])后,甲壳素可沉淀出来,而矿物质和蛋白质则溶解在离子液体废水溶液中被有效脱除。表2总结了不同提取溶剂、提取温度和时间、固液比等条件下甲壳素的得率和纯度。
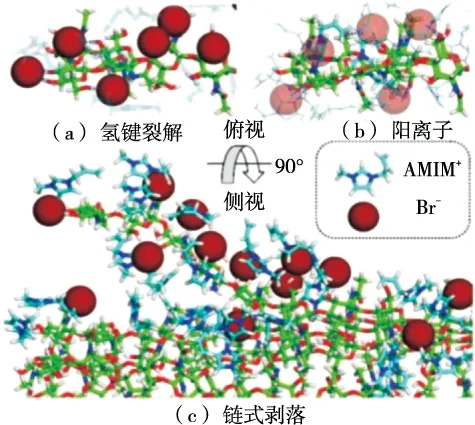
图2 离子液体溶解甲壳素的结构模型
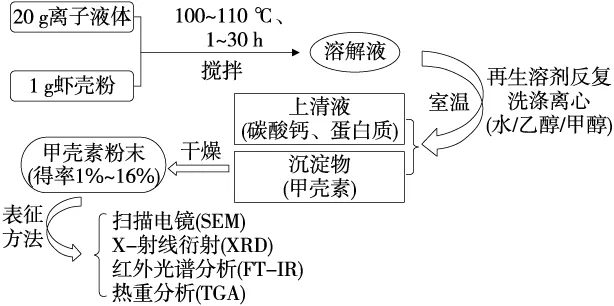
图3 离子液体提取虾壳中甲壳素的工艺流程图
2.1 离子液体种类的影响
对甲壳素有较好溶解能力的离子液体也显示出良好的甲壳素提取效果,如利用[Emim]Ac从虾壳中提取甲壳素得率为16.2%[36];而[Amim]Cl对甲壳素的溶解度较低(0.5%)[25],相对应地得到的甲壳素仅为1.57%[37]。利用成本较低的铵基类离子液体溶解虾壳可以获得与咪唑类离子液体相当的甲壳素产量和纯度。例如,[NH3OH]Ac获得的甲壳素纯度>80%[30]。吕兴梅等[32]利用一种季铵盐类离子液体一步脱除虾蟹壳中的碳酸钙和蛋白质等杂质,获得甲壳素的纯度>85%。由表2可知,含Ac-的离子液体对甲壳素的提取率比Cl-和P-都高,另外咪唑类离子液体[Emim]Ac比铵基类离子液体[DIPEA]Ac、[DMBA]Ac具有更高的甲壳素提取率。

表2 不同溶解条件下甲壳素得率和纯度的比较†
† [Emim]DMP指1-乙基-3-甲基咪唑磷酸三甲酯;“-”表示参考文献中未指出或未测定。
2.2 提取温度和时间的影响
离子液体的黏度大小主要由氢键能和范德华力大小决定[41],温度对离子液体的黏度影响很大,大多数离子液体的黏度随温度的升高而急剧下降,从而影响分子的传质速度和溶解性[42]。Setoguchi等[43]以[Amim]Br为溶剂从蟹壳中提取甲壳素,发现得率随温度的升高而增大,随反应时间的延长而逐渐增加。周雅文等[37]指出虾壳在离子液体[Amim]Cl中的溶解度随温度的升高先增大后下降,且随反应时间的延长呈现先增加后减少的趋势。过高的温度和过长的时间会导致虾壳中有机成分的降解,离子液体黏度增加,从而不利于甲壳素的提取。由表2 可知,甲壳素的提取通常需要在较高的温度条件下(100~110 ℃),与铵基类离子液体相比,咪唑类离子液体提取甲壳素需要的时间较短(约为1 h)。
2.3 提取体系固液比的影响
传统酸碱法显示虾壳的脱矿程度受固液比影响,在1∶3~1∶12(g/mL)固液比范围内,随固液比的增大虾壳脱矿率增加[34]。固液比通过影响溶质与溶剂间的相互渗透作用而影响虾壳在离子液体中的溶解。高静等[35]发现1∶5~1∶25(g/mL)固液比范围内,虾壳在[Emim]Ac中的溶解度随固液比的增大而逐渐增加。一般情况下甲壳素的提取体系选择固液比在1∶20~1∶25(g/mL)的提取效果最佳。
3 甲壳素提取物的化学组成分析
甲壳动物的外骨骼是由一个3层的角质层构成的,内层由甲壳素与蛋白质包裹组成,甲壳素与矿物质一起组成中间层,而外层则由碳酸钙与蛋白质组成[44]。其中甲壳素—蛋白纤维是由大约10~20个被蛋白质包裹的甲壳素反平行链组成[45]。离子液体及含离子液体的多元体系具有溶解蛋白质、甲壳素和灰分的能力[40,46],所以甲壳素提取物中可能含有蛋白质、碳酸钙等杂质。通常使用灰分测定法、凯氏定氮法、氨基酸分析法及元素分析法对甲壳素提取物的化学组成进行分析鉴定[35,47-48]。
3.1 碳酸钙的脱除率
虾壳中矿物质的含量是影响甲壳素溶解能力的重要因素[49],虾壳中的矿物质主要是碳酸钙,传统酸法处理可有效去除虾壳中的矿物质成分,脱矿率高达90%以上[50-51],如Younes等[50]报道的0.5 mol/L盐酸对虾壳的矿物质脱除率达100%。离子液体主要通过阴、阳离子与碳酸钙的相互作用而实现虾壳的脱矿过程。在反应温度100 ℃、时间1 h时,虾壳经过[Emim]Ac处理后矿物质脱除率最高仅为42.84%[35]。而110 ℃温度条件下,虾壳在[DIPEA]P中反应时间超过18 h后脱钙率可达100%[38]。离子液体对虾壳的脱矿效果的不同可能与离子液体种类、作用温度和作用时间等多种因素有关。
3.2 蛋白质的脱除率
虾壳溶解过程中,离子液体的阴、阳离子与蛋白质的氨基酸形成强的氢键作用,从而使甲壳素—蛋白纤维的氢键断裂[52]。传统脱蛋白常用碱法和酶法,脱除率可达90%以上[53-54]。当反应温度120 ℃,时间8 h时,[Emim]Ac对虾壳中蛋白质脱除率为67.13%[35]。相较而言,铵基类离子液体([DIPEA]Ac、[DIPEA]P、[DMBA]Ac)处理30 h后提取的甲壳素中不含Ca元素,N元素<1.1%,具有良好的脱除矿物质和蛋白质的能力[38]。这可能与提取的时间有关,虽然甲壳素能够在短时间内溶解于[Emim]Ac等离子液体,但是当虾壳在离子液体中溶解时间越长,越利于蛋白质和矿物质的脱除,提取的甲壳素纯度越高。
4 再生后甲壳素提取物的结构表征
通常采用扫描电镜(SEM)、X-射线衍射(XRD)、红外光谱分析(FT-IR)和热重分析(TGA)等技术对再生后甲壳素提取物的表观形貌、结晶度、分子结构和热性能进行测定与鉴定[38,55-57]。
4.1 表观形貌分析
市售甲壳素表面为一种粗糙而致密的层状结构,而传统酸碱法提取的甲壳素呈现多孔和纤维的表观形貌[55]。根据报道[35,38],利用离子液体从虾壳中获得的甲壳素提取物表面呈现鱼鳞状、多孔,而且出现黏附的丝状纤维。而甲壳素直接在离子液体中溶解,再生甲壳素的表面不仅孔隙率增加,而且甲壳素样品颗粒结构也有所变化,如经[Emim]Cl和[Bmim]Cl再生的甲壳素样品的平均粒径减小[27,56]。这些形貌的改变主要源于矿物质和蛋白质的脱除。
4.2 分子结构表征
α-甲壳素在1 660,1 627 cm-1FTIR光谱处有明显的两个吸收带,而β-甲壳素只在1 656 cm-1处有一条吸收带[57]。周雅文等[37]发现虾壳溶解再生物的红外吸收在1 650,1 555 cm-1的酰胺振动带有明显的吸收波长。另外,Tolesa等[38]通过对比了市售甲壳素与离子液体提取的甲壳素的红外吸收图谱,发现甲壳素提取物在1 660,1 560,1 312 cm-1处均有明显的吸收波长。说明了利用离子液体提取的甲壳素含有酰胺基(—NHCOCH3),具有与α-甲壳素类似的分子结构。
4.3 结晶结构分析
Li等[58]指出经离子液体预处理后,甲壳素的结晶度降低了25%。图4为[Emim]Ac溶解处理前后虾壳的XRD比较图,与未处理虾壳对比,经过离子液体处理后的再生甲壳素结晶度最低可降至58.7%[35]。还有研究[38]指出,与市售甲壳素相比[DIPEA]Ac、[DIPEA]P和[DMBA]Ac提取虾壳中的甲壳素结晶度分别降低55%,46%,45%。根据结构图的峰高和峰宽可直接判断看出物质的结晶度变化,与虾壳原料相比,离子液体提取的甲壳素的结晶度下降,因为离子液体去除了虾壳中的矿物质[35,38]。
4.4 热稳定性分析
甲壳素的质量损失通常分为两步,第一步是甲壳素结构中的水分蒸发,第二步是多糖环的脱水、甲壳素的乙酰化和脱乙酰基的聚合[59-60]。Setoguchi等[43]研究结果表明利用离子液体提取的蟹壳中的甲壳素与市售甲壳素的TGA曲线几乎一致。类似地,如图5所示,Tolesa等[38]发现甲壳素的TGA曲线与市售甲壳素的TGA曲线基本吻合,说明二者具有相似的热稳定性,有利于提取的甲壳素在抗热材料中的应用。对比图4和图5发现,离子液体提取的甲壳素结晶度的降低导致了甲壳素第二步质量损失的起始温度下降,说明利用离子液体提取甲壳素会对其热稳定性有一定的影响。
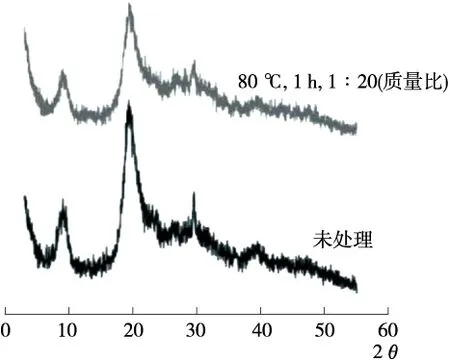
图4 [Emim]Ac溶解处理前后虾壳XRD图

图5 再生甲壳素的TGA图
5 展望
离子液体溶解虾壳提取甲壳素的能力与传统酸碱法相当,可作为传统酸碱试剂的良好替代品。近年来,利用离子液体提取虾壳中甲壳素的研究不再局限于咪唑类离子液体,其他一些离子液体也逐渐被发掘。但是,离子液体黏度大的特点,严重阻碍了其与虾壳之间的传质作用,降低了甲壳素的提取率。离子液体的低毒特性和昂贵的价格,也极大地限制了其使用。因此,在提高甲壳素提取率和纯度的同时,可寻找一些其他试剂替代部分离子液体以降低其黏度和生产成本。另外,天然无毒离子液体的合成和加强离子液体循环利用是未来的研究需要进一步关注的问题。
