用钛铁矿制备Fe3O4/TiO2复合物及其光催化降解性能考察
2019-04-04
(绍兴文理学院 化学化工学院,绍兴 312000)
1 引言
近年来,随着工业的快速发展,环境污染和能源短缺已成为当今世界面临的两大难题,与之带来的工业废水排放量越来越大。以印染工业废水为例,其具有成分复杂、色度高、可生化性差等特点,一直以来,如何有效解决印染工业污水对环境的危害成了水处理中的难题。
罗丹明B(Rh B)作为一种典型的三苯甲烷类染料曾被广泛应用于印染等行业,目前对于含有罗丹明B等染料的废水,较为常用的方法为物理化学法、化学法、生物法,其中生物法中的光催化降解方法,是解决上述难题的有效方法之一,并已成为近年来人们研究的热点[1]。
二氧化钛(TiO2)因其具有化学性质稳定、无毒、成本低等优点,已被广泛应用在光催化领域,但TiO2在光催化过程中难以有效分离回收再利用,因此有效分离回收纳米TiO2并提高催化剂的稳定性亦称为研究的关键[2]。而我国钛资源及其丰富,尤其是钛铁矿作为主要的含钛矿物之一,不仅具有丰富的钛源,还含有大量的铁,以钛铁矿中的钛和铁为原料,制备Fe3O4/TiO2复合物,不仅可以利用铁掺杂来提高催化剂的催化活性,还能利用复合物磁性,实现催化剂的分离回收,实现重复利用。目前常用液相沉积法、超声波合成法分别制备了TiO2/Fe3O4/SiO2、FexOy-TiO2磁性复合材料[3-5],但此类方法成本较高,不利于在工业生产中推广应用。
本实验以钛铁矿为原料,利用简单易操作的溶液法合成Fe3O4/TiO2光催化复合物,以罗丹明B模拟废水为目标物,研究产物对罗丹明B的光催化性能和循环稳定性。
2 实验部分
2.1 试剂
试验原料钛铁矿由巩义市东方净化材料有限公司生产;硫酸、氢氧化钠、氨水、乙二醇、无水乙醇、罗丹明B均为分析纯,购于国药集团化学试剂有限公司;水为去离子水。
2.2 实验步骤
2.2.1 Fe3O4/TiO2复合物的制备
取20g钛铁矿粉,加入37mL浓硫酸,170℃加热搅拌,反应3h后,稀释至800mL,浸取1h后,抽滤,滤渣用蒸馏水洗涤数次,浸取液待用。取一定量浸取液,滴加6mol/L NaOH溶液,调pH值至11出现褐色沉淀,加入一定量水合肼和蒸馏水,60℃下搅拌反应2h后过滤,制得磁性的Fe3O4磁流体,取一定量的浸出液于装有大量热水的三颈烧瓶中,加热搅拌一段时间后,加入一定量的尿素,调pH值为3,通氮气,100℃恒温水浴加热,加入5mL Fe3O4磁流体,搅拌2~3h,磁性分离得到产物,分别用去离子水和无水乙醇洗涤3次,烘干后得到Fe3O4/TiO2复合物。
2.2.2 产物表征
产物的物相分析在X-射线衍射仪(型号:Empyrean,荷兰帕纳科公司,Cu-Kα靶,λ=1.5406埃)上进行,衍射范围为100~900,扫描速度50/min;傅立叶红外光谱仪(型号:NEXUS)对产物中的特征官能团进行表征,紫外-可见光谱采用日本岛津UV-2550紫外-可见光谱仪测定。
2.2.3 光催化性能表征
称取1.25mg罗丹明B固体,配成浓度为1×10-5mol/L罗丹明B溶液;取5mL的罗丹明B溶液加入到石英试管中;称取5mg的光催化剂加入石英管中;黑暗中搅拌30min,达到吸-脱附平衡,在紫外可见光源下,照射反应60min;每个一定时间取样5mL,离心分离,测其吸光度,绘制任意时刻吸光度A与时间t曲线,比较其降解效率。
3 结果与讨论
3.1 结构分析
为了确定Fe3O4/TiO2光催化复合物粒子的晶型,对所制备的样品进行XRD分析。图1是产物的X射线衍射图,图中1为锐钛矿TiO2,在2θ=25.210、37.970、47.950、55.020、62.590出现的衍射峰分别对应锐钛矿型TiO2的(101)、(004)、(200)、(211)、(204)特征峰;图中2为2θ=30.300、35.670、43.300、53.780、57.310、62.840出现的衍射峰,分别与Fe3O4的(220)、(311)、(400)、(222)、(511)、(440)的特征峰相吻合[6],且无其他杂峰,说明生成的Fe3O4纯度较高,没有其他铁氧化物存在。

图1 TiO2、Fe3O4及Fe3O4/TiO2复合物的XRD图
3.2 光谱性质
为进一步证明该产物为Fe3O4/TiO2复合物,分别对样品进行红外光谱分析。图2为Fe3O4/TiO2复合物的红外光谱(FT-IR)图。 由图可知,578.9cm-1是Fe3O4中铁氧键(Fe-O)的特征吸收峰,为Fe-O键的振动振动峰;1394.31cm-1是TiO2中钛氧键(Ti-O)的特征吸收峰;1636.56cm-1与3423.16cm-1的吸收峰均属于羟基的伸缩振动峰,可以归属Fe3O4粒子表面的羟基伸缩振动峰,说明在该样品中既含有Fe3O4又含有TiO2。
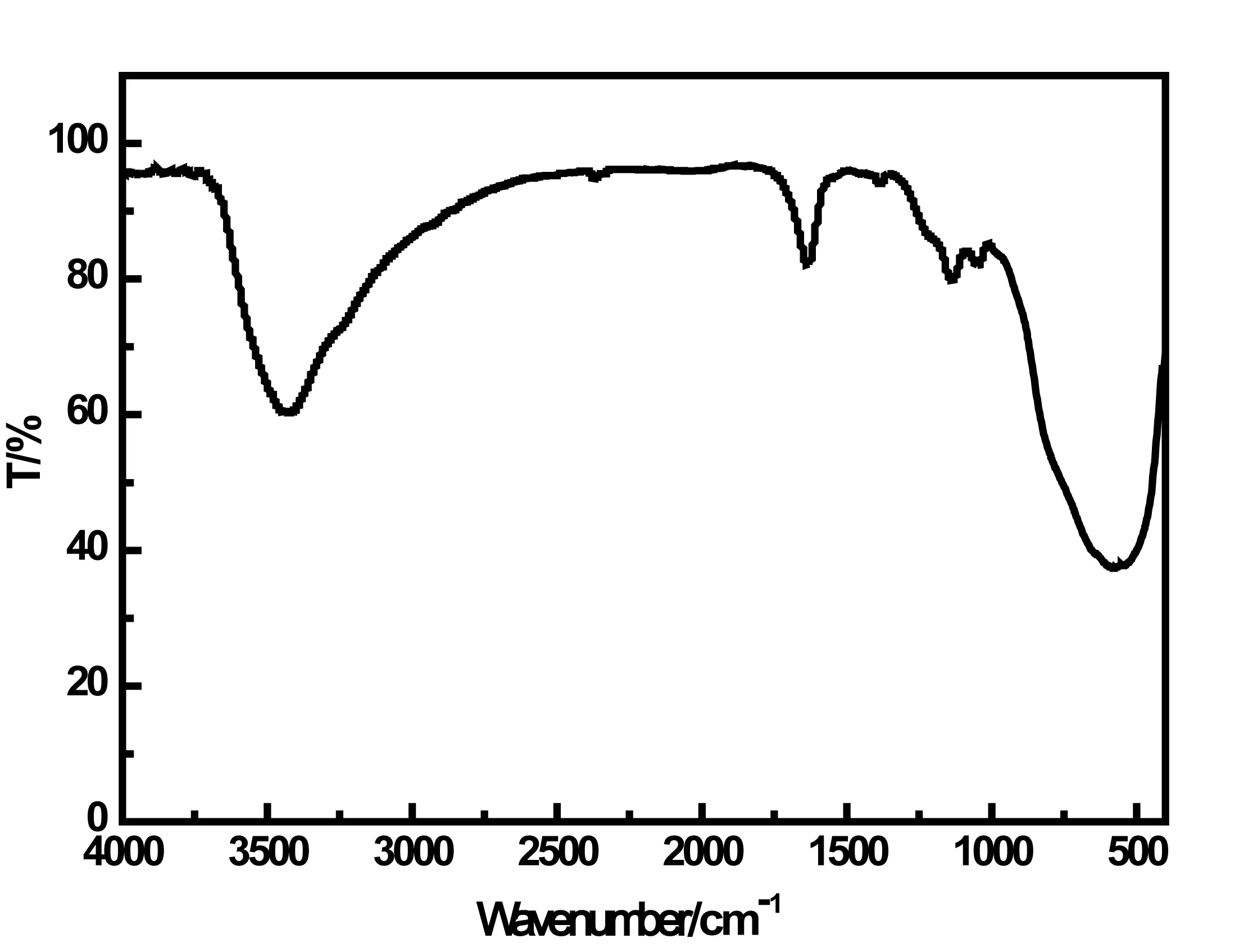
图2 Fe3O4/TiO2复合物的FT-IR图
图3是Fe3O4/TiO2复合物的红紫外可见光谱(UV-vis)图。
由于半导体材料的光诱导电子及空穴迁移与自身的电子结构有关[7]。这是影响光催化或性的关键因素。锐钛矿型TiO2对光吸收范围在320-400nm,超过400nm的可见光吸收较少,这是由于O原子的2p轨道电子受激发跃迁至Ti原子的3d轨道所致[8,9]。如图3所示Fe3O4/TiO2复合物光吸收范围比TiO2要宽,在400~800nm可见光范围内有吸收,Fe原子和O原子的相互作用可能使光电子跟空穴发生分离,产生晶格点缺陷,使TiO2价带位置上移,禁带宽度变小,因此吸收光谱带发生红移,光响应范围变大,表明Fe3O4/TiO2复合物对有机污染物的光催化降解效果更好。
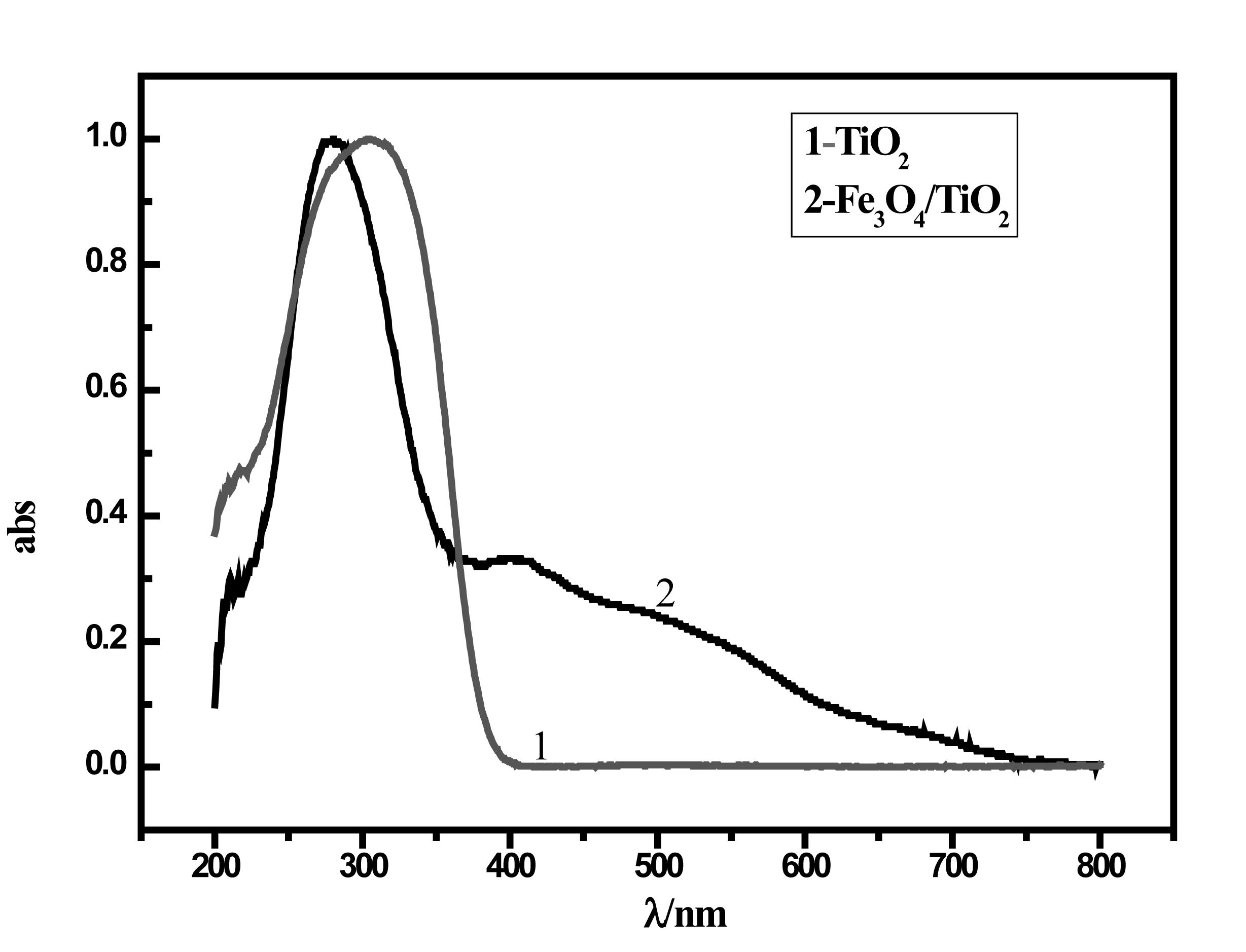
图3 TiO2和Fe3O4/TiO2复合物的UV-vis图
3.3 光催化性能
分别以TiO2单体、Fe3O4/TiO2复合物光催化降解罗丹明B溶液,任意时刻吸光度随时间曲线图如图4、5所示。图4为TiO2复合物光催化降解罗丹明B的紫外可见吸收光谱吸光度随时间的变化情况。由图4中的曲线6可知,罗丹明B的最大吸收峰在波长为550nm附近;用单体TiO2作催化剂,降解罗丹明B效果较明显,但与图5相比较,在相同的光照时间下,Fe3O4/TiO2复合物作为光催化剂的降解效果最佳,相同条件下,降解率达到95%以上,并且实验中发现Fe3O4/TiO2光催化剂在催化降解罗丹明B时最大吸收峰发生蓝移,这可能使由于包裹在TiO2表面的磁性Fe3O4不容易团聚,分散度较好,能够提供更多的活性中心跟反应位点,从而提高了光催化活性。
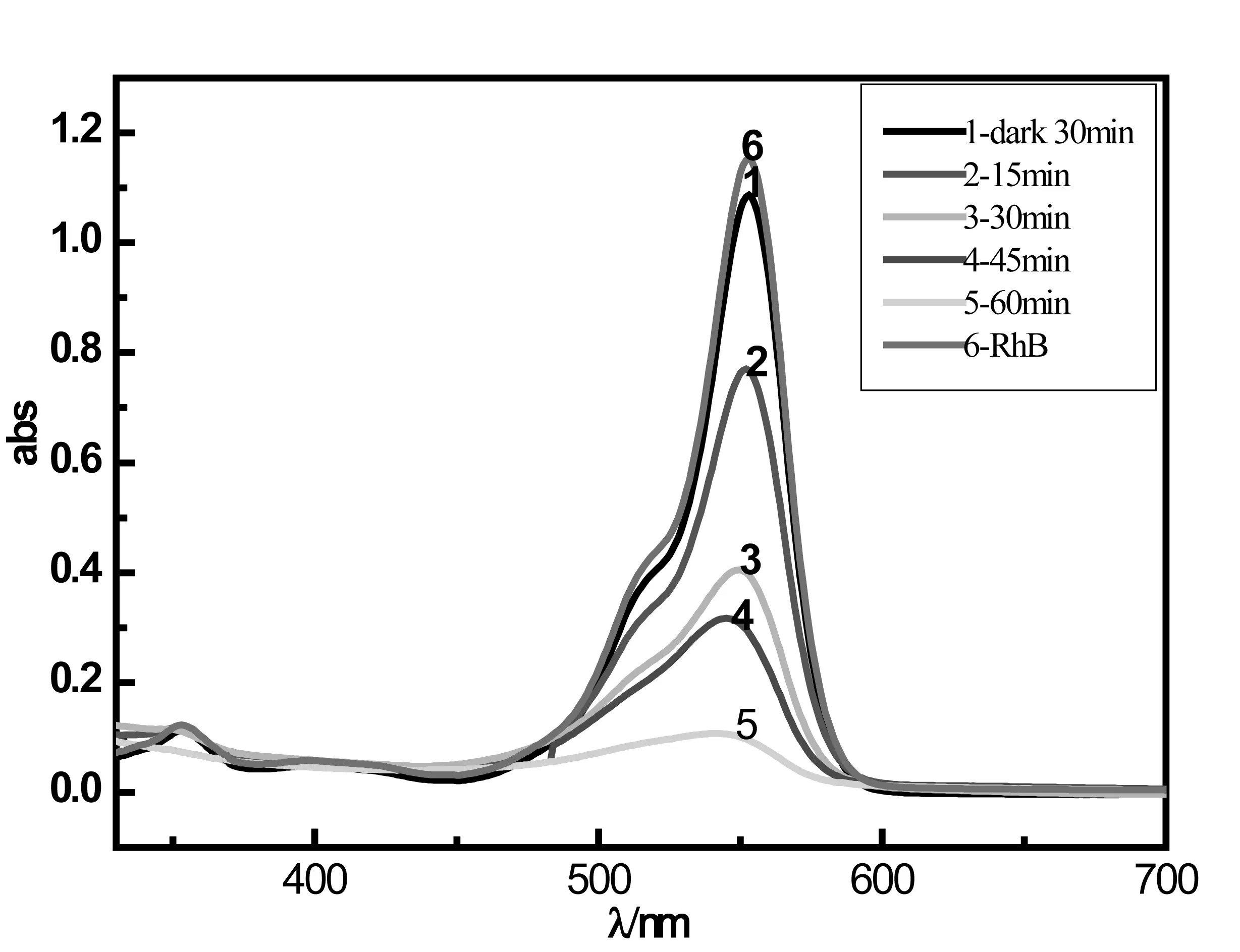
图4 TiO2单体降解罗丹明B的紫外-可见吸收图谱
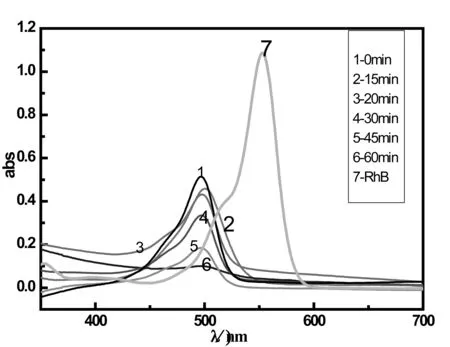
图5 Fe3O4/TiO2降解罗丹明B的紫外-可见吸收图谱
3.4 Fe3O4/TiO2光催化剂的回收和重复使用
光催化反应后,利用磁铁对溶液中的Fe3O4/TiO2复合物进行分离回收,并用水跟乙醇洗涤数次、干燥,备用。催化剂的重复使用次数是衡量催化剂性能的一个重要指标。将Fe3O4/TiO2复合物催化剂重复5次用于催化降解罗丹明B,实验结果如图6所示。催化剂在循环利用过程中对罗丹明B的降解率有所下降,但下降幅度较小,可能是在后处理过程中催化剂有损失所致,但仍可以认为Fe3O4/TiO2复合催化剂是一种较为理想的循环催化剂。

图6 Fe3O4/TiO2复合物对罗丹明B光催化降解循环稳定性
4 结论
以廉价钛铁矿为原料,采用溶液法制备了一种结构稳定、可回收、具有优良光催化性能的Fe3O4/TiO2复合催化剂,XRD、FT-IR、UV-vis等表征结果显示该产物中既有面心立方结构Fe3O4又有锐钛矿型TiO2,Fe3O4/TiO2复合光催化剂对罗丹明B有较好的光催化降解作用,并具有较优的循环稳定性,利用外磁场可以实现催化剂的分离回收,具有很好的工业应用前景。
