喹诺酮金属配合物的研究进展
2019-03-28胡健
胡 健
(南京洵安文化传媒有限公司,江苏 南京 210009)
喹诺酮类也被称作吡酮酸类或吡啶酮酸类,是一大类人工合成的具有抗菌活性的化合物,具有效果好,口服吸收好,生物利用度高等特点[1-2]。按研发时间的先后顺序及抗菌谱及适应症的不同,喹诺酮类分为一到四代,各代都是以前代或同代其它化合物为基础,对母核及侧链进行不同程度的修饰,在抗菌谱和适应症方面逐渐扩大。此类药物近三十年来发展极为迅速,不但品种层出不穷,新一代产品的治疗效果已不逊于同期常用的头孢类抗生素,由于头孢类抗生素开发成本持续提高,因而开发抗菌活性更强、抗菌谱更广、不易产生耐药、对常见耐药菌有效、半衰期更长、不良反应更少的喹诺酮类抗生素成为相关研发机构关注的热点。
配位聚合物由于其结构特点往往具有独特的功能,在医疗等领域有着广泛而重要的应用。某些可形成配合物的药物的价值有待进一步开发,喹诺酮类化合物的结构中存在多个配位点,可与某些金属离子反应生成金属配合物,为此喹诺酮类药用价值的深入挖掘提供了重要思路。
1 喹诺酮类药物的发展过程
美国 Sterling-Winthrop研究所Lesher等人于1962年发现首个喹诺酮类药物萘啶酸(图1)[3]:

图1 萘啶酸的结构式
但是仅对大多数革兰氏阴性菌有作用,药代动力学特性较差,安全性不理想,现已完全淘汰。萘啶酸自身狭窄的抗菌谱限制了临床应用范围,为了扩大抗菌谱和改善药代动力学特性,科研人员在萘啶酸母核结构基础上做了几项修饰,其中两项被认为是主要的修饰:在7号位置引入哌嗪环或另外的N-杂环及在6号(个别化合物同时在8号)位置引入氟原子(图2)。

图2 4-喹诺酮的一般结构
由此导致了20世纪80年代发现了新的4-喹诺酮类化合物——氟喹诺酮类,使得此类药物步入了快速发展的轨道。早期发明的诺氟沙星、氧氟沙星等目前依然广泛应用于临床。步入90年代以后,喹诺酮类抗生素在前期产品药代动力学及抗菌活性得到全面优化的基础上扩大了抗菌谱,已经可以普遍应用于革兰氏阳性菌、衣原体、支原体及细胞内致病菌感染。90年代中后期陆续上市的莫西沙星等喹诺酮类结构中引入的8位甲氧基加强了抗厌氧菌活性,而7位上的引入比早期产品吡哌酸结构中哌嗪环更复杂的含一氮或二氮单/双环结构则使得此类化合物具有了较强的抗革兰氏阳性菌活性,并保持了原来抗革兰氏阴性菌的活性,同时毒副作用更小,安全性更高,同时药物动力学也有很大改善,普遍具有大大低于50%的蛋白质结合率,较长的半衰期和更高的血清、组织浓度。基于抗菌谱和药代动力学特点的不同,喹诺酮类药物可以分为四代[4-8]。

表1 根据喹诺酮类药物抗菌谱和药代动力学特性的分代/分类列表
喹诺酮类以细菌DNA为靶,妨碍DNA回旋酶正常发挥功能,抑制细菌DNA的复制和转录,进一步造成细菌DNA的不可逆损害,从而导致细菌迅速死亡,由此实现抗菌效果[9-10]。
喹诺酮类抑制DNA回旋酶(DNA拓扑异构酶II)和DNA拓扑异构酶IV,DNA回旋酶由编码为GyrA和GyrB的两个亚基组成,其作用是将负超螺旋引入DNA,从而催化子代染色体的分离。 DNA拓扑异构酶IV由四个亚基:两个ParC和两个ParE亚基组成,它负责DNA的解链,从而允许两段DNA分离到两个子细胞内[11-12]。喹诺酮与酶-DNA复合物相互作用,形成药物- 酶-DNA复合物,阻止复制和转录过程[13-14]。
对革兰氏阴性菌和阳性菌都有效的喹诺酮类中早期发现的化合物对革兰氏阴性细菌DNA回旋酶的活性大于对拓扑异构酶IV的活性,对革兰氏阳性细菌的拓扑异构酶IV有更强活性。后期发现的喹诺酮类对两种酶具有几乎同等的强抑制作用[15-17]。
2 喹诺酮类药物金属配合物的研究进展
喹诺酮类经过半个多世纪的发展已经在临床药物应用中占据重要地位,早期喹诺酮药物被替代及淘汰,此类药物同样也面临耐药菌不断出现以及后续研发成本持续攀升等问题,随着生物无机化学领域的发展,氟喹诺酮出现并垄断喹诺酮类药品市场以后,氟喹诺酮类金属配合物的研究也陆续展开。
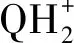

图3 2价金属阳离子与喹诺酮类以1∶2形成配合物的一般结构
进入21世纪以来,研究者对喹诺酮类金属配合物进行了广泛的研究,配体涵盖了已经发现的一到四代喹诺酮类化合物,金属离子则由最初的Mg2+、Al3+、Ca2+、Fe2+、Fe3+、Zn2+、Cu2+、Mn2+、Co2+、Ni2+、VO2+等原子量较小的离子逐步扩展至Ba2+、Bi3+、Ce3+、Y3+、Pd2+、La3+、Pt2+、Ru3+、Au3+、Eu3+等原子量较大的离子[22],其中稀土金属配合物是目前研究的一个重要领域。

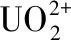

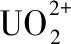
3 展望
金属离子-喹诺酮配合物是近年来发展迅速的一个研究领域,作为目前抗感染化疗领域最前沿和最容易产生新成果的领域,日益受到医药界的重视。一方面临床上应该规范此类药物的使用,尽量避免产生耐药菌株,另一方面母核修饰及金属配合物开发方面是两个重要的研究方向。喹诺酮类药物通过与某些金属离子的络合获得溶解度增强的配合物来改善其药物特性,许多金属离子-喹诺酮类配合物表现出不同的生物学特性:抗菌活性(有时与母体喹诺酮类药物相当或更好),抗癌活性,个别喹诺酮金属配合物也具有一定的抗真菌和抗寄生虫活性以及抗氧化性,更多的用途正在持续被发现。
喹诺酮金属配合物的研究广泛采用了分光光度法、荧光分光光度法和原子吸收光谱法的最新成果,同时与喹诺酮类可以形成稳定配合物的金属离子可以利用喹诺酮作为络合剂来测定。
喹诺酮类金属配合物及其应用领域的进展与具有更大生物活性的新型喹诺酮类的开发是同步的。结合近年来喹诺酮类金属配合物的研究成果,寻找具有明确分子结构及晶型并在临床上有更强效用及更广应用范围的新型喹诺酮金属配合物是未来重要的研究方向。
