补体C1q/肿瘤坏死因子相关蛋白6在结肠癌中的表达
2019-03-27勾静娴姜相君曲海霞崔艳欣
勾静娴, 姜相君, 曲海霞, 崔艳欣
青岛市市立医院消化内二科 山东 青岛 266071
补体C1q/肿瘤坏死因子相关蛋白6(complement C1q/tumor necrosis factor-related protein 6,CTRP6)发现于2010年,是近年来发现的与脂联素同源的CTRP家族成员之一,是一种含有240个氨基酸的糖蛋白,分子量为29 kDa,其结构与其他CTRP家族成员(除CTRP4外)的结构基本相同,均由4个不同结构域组成,包括氨基端的信号肽、短的可变结构域、胶原样可重复的结构域和羧基末端类似补体C1q的球状结构域[1]。CTRP6在哺乳动物中表达广泛,如脂肪组织、心脏、胎盘、大脑、滑膜组织等均有表达[1-3],并在不同组织中发挥不同的代谢作用。相关研究[1, 4-6]表明,CTRP6参与脂肪代谢及糖代谢,使其可能成为肥胖和糖尿病等代谢综合征的一个新的治疗靶点。CTRP6还显著增加巨噬细胞中抗炎因子白细胞介素-10(interleukin-10,IL-10)的表达[2]。另外,CTRP6能够改善心肌梗死后心脏功能和改善心室重构[7]。近年来,CTRP6被发现与自身免疫性疾病相关,包括1型糖尿病、白癜风、Graves病、类风湿性关节炎[3, 8-12]。
结肠癌好发部位为乙状结肠与直肠交界处,目前仍是我国甚至世界发病率及死亡率最高的恶性肿瘤之一,发病率排所有恶性肿瘤第4位,死亡率为第5位,近20多年来,世界上多数国家的发病率呈上升趋势,我国也十分明显。以40~50岁年龄组发病率最高,发病率男性高于女性[13]。治疗的关键在于早发现、早诊断,以利于手术根治,其预后也取决于早期诊断与手术能否根治及有无复发。
本研究通过检测结肠癌患者癌组织中CTRP6的表达情况及其与肿瘤大小、病理分型、浸润深度、淋巴结转移、脉管内瘤栓、神经侵犯等相关性,分析CTRP6在结肠癌的发生、发展中可能的作用,为进一步研究其在诊断、治疗方面的作用设想提供理论基础。
1 资料与方法
1.1研究对象随机选取2016年1月至2016年12月在青岛市市立医院普外科手术且经病理确诊为结肠癌的病例共121例腊块标本进行研究。所有患者在术前未经任何针对癌症的治疗。由2名病理科医师作出病理诊断,诊断结果包括:病灶大小、大体分型、浸润深度、组织学分级、脉管内瘤栓、神经侵犯、淋巴结转移情况。分级诊断标准参照《阿克曼外科病理学》[14]。121例标本中男78例,女43例,年龄39~89岁,中位年龄66.2岁;组织学分级低分化31例,中分化89例,高分化1例;肿瘤直径≥5 cm者54例,3 cm≤肿瘤直径<5 cm 51例,<3 cm 16例。肿瘤浸润深度:黏膜下层3例、肌层15例、浆膜层103例;转移情况:淋巴结转移:阳性51例,阴性70例;脉管内瘤栓:阳性49例,阴性72例;神经侵犯:阳性34例,阴性87例。本研究获得了医院伦理委员会审核并批准,入选本研究的结肠癌患者或家属均签署知情同意书,同意使用其组织标本用于本项科学研究。
1.2主要仪器设备及试剂主要试剂及来源:兔抗人CTRP-6多克隆抗体(bs-14104R)(北京博奥森公司产品);PV 9000免疫组化试剂盒(PV-9000)(中杉金桥公司产品);DAB显色试剂盒(DAB-1031)(福州迈新公司产品);EDTA抗原修复缓冲液 (MVS-0080) (福州迈新公司产品)。
主要仪器及来源: 组织芯片仪(Beecher Instruments,美国);低温冰箱(海尔公司,青岛)3.1~1 000 μl加样器(雷勃分析仪器有限公司,上海);AS325轮转式切片机(SHANDON公司,英国);可控式恒温干燥箱(湖北省黄石市医疗器械厂);电热恒温水浴箱(北京医疗设备厂);AEG-120电子天平(SHIMADZU公司,日本);半自动组织包埋机(SHANDON公司,英国);全自动真空脱水机(SHANDON公司,英国);BX-50电光源多头显微镜(OLYMPUS公司,日本);BX-50全自动显微照相系统(OLYMPUS公司,日本)。
1.3方法
1.3.1 免疫组化操作步骤:(1)脱蜡和水化;(2)抗原修复,EDTA缓冲液修复90 s;(3)阻断内源性过氧化物酶;(4)根据组织大小,滴加50 μl一抗,37 ℃孵育;PBS缓冲液冲洗;(5)滴加反应增强液100 μl,室温孵育;然后PBS缓冲液进行冲洗;(6)滴加兔抗人CTRP-6多克隆抗体(bs-14104R),室温孵育;PBS缓冲液再次冲洗;(7)DAB显色,室温孵育,显微镜下观察颜色的发展情况,自行掌握染色时间;(8)复染;(9)脱水、透明、封片。
1.3.2 结果判定:在200倍和400倍高倍镜视野下对比观察同一切片的癌细胞胞浆和正常非癌细胞胞浆的着色情况,在光学显微镜下观察细胞胞浆内黄色颗粒状信号,按染色程度(0分:阴性着色,1分:淡黄色,2分:浅褐色,3分:深褐色)判分,2~3分判定为阳性结果,0~1分判定为阴性结果。分别记录癌细胞和正常非癌细胞的着色情况。
1.4统计学处理采用SPSS 19.0软件进行统计学分析,计数资料采用χ2检验,相关性分析采用非参数Spearman秩相关检验,P<0.05为差异有统计学意义。
2 结果
2.1癌组织及癌旁组织中CTRP6的表达121例结肠癌患者中,108例患者癌细胞胞浆中的CTRP6表达阳性,13例患者癌细胞胞浆中的CTRP6表达阴性,所有结肠癌患者的正常非癌细胞中的CTRP6表达均为阴性,典型图片如图1~4所示。提示在结肠癌癌细胞中CTRP6显著高表达(P<0.05),在正常非癌细胞中几乎不表达。
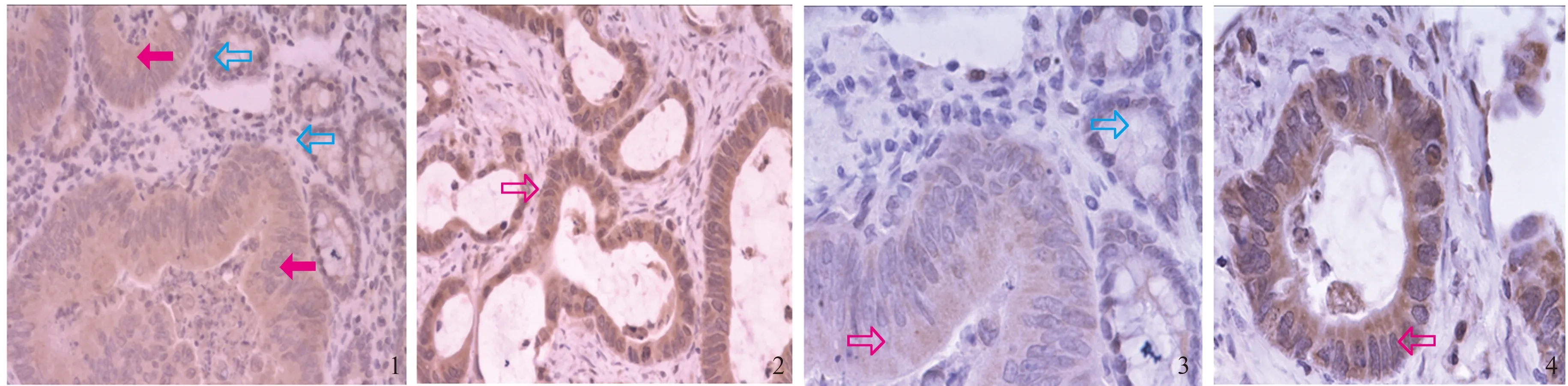
图1~2 癌细胞胞浆内见褐色颗粒状阳性信号(红色箭头);正常非癌细胞胞浆内不着色或着色弱(蓝色箭头)(200×);图3~4 癌细胞胞浆内见褐色颗粒状阳性信号(红色箭头);正常非癌细胞胞浆内不着色或着色弱(蓝色箭头)(400×)Fig 1-2 Brownish-granular positive signal was seen in the cytoplasm of cancer cells (red arrow); normal non-cancer cells were not stained or weakly stained within the cytoplasm (blue arrow) (200×); Fig 3-4 Brownish-granular positive signal was seen in the cytoplasm of cancer cells (red arrow); normal non-cancer cells were not stained or weakly stained within the cytoplasm (blue arrow) (400×)
2.2CTRP6的表达情况与患者临床病理特征之间的相关性CTRP6在结肠癌的表达与患者性别、平均年龄、肿瘤大小、分化程度、浸润深度、脉管内瘤栓、神经侵犯、淋巴结转移均无相关性(P均>0.05,见表1)。

表1 CTRP6的表达情况与结肠癌患者病理特征的关系Tab 1 Relationship between CTRP6 expression and pathological features of colon cancer patients
3 讨论
结肠癌是重要的消化道恶性肿瘤之一,其病死率高,给患者及其家庭带来了极大的经济负担及心理压力。究其原因,为其早期诊断及治疗的手段不足。结肠癌的危险因素复杂多样,但其发生、发展机制并不十分明确,仍是目前需要攻克的难题。
炎性因素被认为与结肠癌的发展有关,多个研究[15-16]表明,多种炎症介质参与调控结肠癌的发展、转移等,如IL-6、肿瘤坏死因子-α(tumor necrosis factor-α, TNF-α)、IL-10。在一项丹麦人群的研究[15]中发现,IL-10和膳食纤维之间在结肠癌发生中的相互作用,高膳食纤维摄入量似乎可以降低具有结肠癌的遗传易感性个体患结肠癌的风险。过表达CTRP6能降低致炎因子IL-1β、IL-6和TNF-α的表达,增加抗炎因子IL-10的表达[7],CTRP6通过激活细胞外信号调节蛋白激酶1/2(ERK1/2)通路而诱导IL-10在巨噬细胞的表达[2]。另有研究[5]表明,gCTRP6在肌肉组织中激活AMP依赖的蛋白激酶(adenosine 5’monophosphate-activated protein kinase, AMPK)通路呈剂量依赖性和时间依赖性,AMPK信号通路能强有力地调节巨噬细胞对炎症的反应,增加抗炎因子IL-10的表达[17],但CTRP6是否能调节促炎性反应信号通路目前未知,仍需要进一步研究。另一项在卵巢癌的研究[18]中发现,卵巢癌患者相较于正常健康志愿者,血清中CTRP6水平明显降低,并且在培养基中的细胞液的CTRP6检测得到了相同的结果。在进行肿瘤细胞的增殖性和侵袭性检测中发现,CTRP6的水平下降会导致肿瘤细胞的侵袭力加强,当重新加以CTRP6处理时,肿瘤细胞的增殖力受到抑制。研究还发现,检测出IL-8的分泌水平与CTRP6相反,且呈剂量依赖性。推测CTRP6可能通过抑制IL-8和血管内皮生长因子(vascular endothelial growth factor, VEGF)通路参与抑制卵巢癌细胞的增殖和转移[18]。CTRP6能否通过调节炎症因子这一通路来参与结肠癌的发展调控则需要进一步证实。
在肝癌的研究中,在未发生癌变的肝组织中并未检测到CTRP6,但能在21/30的肝细胞癌组织标本中检测出。这表明,CTRP6并非均匀分布,而是局限分布于肝癌细胞[19]。这个结果与我们研究CTRP6在结肠癌的表达分布类似:108例结肠癌患者癌细胞胞浆中的CTRP6表达阳性,13例患者癌细胞胞浆中的CTRP6表达阴性,所有121例结肠癌患者的正常非癌细胞中的CTRP6表达均为阴性,显示出CTRP6在结肠癌组织的高表达。且CTRP6在结肠癌的表达与患者性别、年龄、肿瘤大小、分化程度、浸润深度等均无相关性。根据此分布特征,CTRP6能否作为早期筛查结肠癌的一种标志物,目前仍需临床试验研究[20]证实,其灵敏度和特异度有待于进一步研究。目前,已经有利用重组载体转染大肠杆菌的方法,诱导表达并提纯,制备出了具有生物学活性的Trx-hCTRP6蛋白。这为探究CTRP6的生物学作用,并将其运用到疾病的诊治上,打下了基础。
CTRP6在结肠癌组织中高表达,其表达与患者性别、年龄、肿瘤大小、分化程度、浸润深度等均无相关性。
