成年人不同阶段肠道菌群及其代谢差异的研究
2019-03-27陈军奎皮雄娥费迪波朱立颖
陈军奎,刘 伟,王 欣,皮雄娥,费迪波,朱立颖
1.浙江师范大学化学与生命科学学院,浙江 金华 321004; 2.浙江省农业科学院植物保护与微生物研究所/农产品质量安全国家重点实验室培育基地
肠道微生物在人体健康中的作用已经有大量的研究报道。但肠道菌群结构和组成在个体之间存在明显的差异性和连续性,且这种特性又与年龄具有同步性。人出生后微生物就开始定植[1],在婴儿时期肠道微生态系统逐渐建立,在成年时期达到一个稳定状态,老年时期肠道菌群逐渐退化,致病菌增多[2]。通过宏基因组测序可以检测到超过1 000种肠道微生物,主要分为四大门类:厚壁菌门、细菌、放线菌和变形菌门。微生物的定植最早发生在胎儿时期,有越来越多的证据表明在胎盘、羊水和胎粪就有微生物的存在[3-5]。随着年龄的增长,肠道菌群也在不断发生改变,当宿主的年龄在2~5岁时,肠道菌群会达到稳定且平衡的状态。每个个体的肠道菌群组成都是具有高度动态性和特异性,且随着时间的推移会持续变化。与青年组相比,年龄相关的肠道菌群变化在老年组中个体差异更为明显[4]。尽管不同个体间肠道菌群组成差异明显,且受营养、生活方式、日照变化、性别、生理机能和种族等诸多因素的影响,但在生命的不同时期它都具有特定的组合方式和功能特征,例如在成年人的肠道内,拟杆菌门和厚壁菌门是肠道菌群中最常见且最重要的组成部分[6],而在婴儿肠道内以来自母乳的双歧杆菌、乳酸菌、葡萄球菌和肠球菌等为主[7]。肠道菌群的这些特征在一定程度上被认为是宿主一种强有力的生理反应,并对宿主的发育和体内平衡具有重要影响。鉴于肠道菌群在不同宿主的特异性和动态性与人生长周期的一致,现在已有学者认为肠道菌群具有预测一些代谢和疾病的能力,比如结直肠癌、餐后血糖升高、减重后体质量反弹的概率甚至是神经退行性疾病等。
人们早就认识到,肠道微生物可以帮助宿主抵御病原体,完善健康的肠道结构和免疫系统,并帮助消化难以消化的膳食纤维,因此完整的肠道菌群是维持健康的重要因素。影响肠道微生物的因素很多,饮食就是其中最重要的一项。食物中难以消化的物质为肠道微生物提供代谢基质,由于不同的微生物利用特定的基质,所以复杂饮食可以提供促进或抑制微生物生长的因子。益生元是指食物中宿主不能消化的成分在肠道中被肠道菌群选择性代谢并对宿主产生有益影响的物质。益生元可以促进肠道潜在有益菌的生长,主要是双歧杆菌和乳酸菌。肠道微生物的老化进程可能会被益生元弱化,所以越来越多的研究在探索特定饮食成分对益生菌和菌群多样性的影响,例如玉米为主的谷物食品可以提高志愿者粪便样品中双歧杆菌的丰度,豆类制品可以使厚壁菌的丰度减少,蔬菜可以提高肠道中拟杆菌/普雷沃氏菌的比例等。菊粉(INU)是从菊苣根中提取出来的,不过它也存在于小麦、洋葱、香蕉、洋姜和韭菜等其他食物中;INU还广泛应用在制药业中。INU是由2~6个果糖通过β(2-1)糖苷键练成的骨架,末端通过α(1-2)糖苷键连接一个葡萄糖。这些β(2-1)骨架不能被唾液或胰酶水解,因此INU被认为具有益生元的效果。
本文中,我们比较了20~40岁人群和40~60岁人群的肠道菌群组成,并以淀粉(STA)和INU作为主要碳源来研究两组人群的降解率、产气量、短链脂肪酸(SCFA)产量及菌群的变化情况,现将结果报道如下。
1 资料与方法
1.1一般资料本研究选择了年龄为20~40岁和40~60岁各15名健康志愿者,20~40岁组男7名,女8名,平均年龄26.6岁,40~60岁组男8名,女7名,平均年龄50.8岁。
1.2研究方法
1.2.1 粪便样品收集:所有的志愿者都是在近3个月内饮食正常,并且未服用抗生素和其他药物,且未接受过益生菌治疗。收集志愿者晨起粪便,用厌氧磷酸缓冲液(PBS)配制成质量浓度为100 g/L的粪便悬液,混匀后用0.125 mm的无菌金属筛过滤除去大的食物残渣。
1.2.2 体外发酵:本研究采用以前报道过的批量发酵系统进行[7]。基础培养基(YCFA)含有下列物质:胰蛋白胨10 g/L;酵母提取物2.5 g/L;L-半胱氨酸1 g/L;血红素2 ml/L;NaCl 0.9 g/L;CaCl2·6H2O 0.09 g/L;KH2PO40.45 g/L;K2HPO40.45 g/L;MgSO4·7H2O 0.09 g/L;维生素I 200 μl/L;刃天青(1 g/L)1 ml。维生素I溶液包括:生物素0.05 g/L,钴胺素0.05 g/L,对氨基苯甲酸0.15 g/L,叶酸0.25 g/L,吡哆胺0.75 g/L。为了研究肠道菌群的代谢情况,我们在培养基中加入质量浓度为8 g/L的INU作为唯一碳源,同时以STA培养基作为对照。培养基配置好后pH调节到6.5,然后厌氧条件下在10 ml的西林瓶中分装5 ml培养基,密封后高压灭菌。
将500 μl处理好的新鲜粪便接种液接种到培养基中,然后放置到37 ℃的恒温培养箱中培养48 h,并分别在24 h和48 h的时间点取样,然后以9 000 r/min离心3 min,取沉淀用来提DNA,上清用来做代谢分析。
1.2.3 薄层层细(TLC):TLC可以直观地观察到碳的降解率和利用率。0.2 μl的样品点在硅胶板上,然后将硅胶板底部浸泡在展开剂中,随后将硅胶板浸没在染色剂中染色,然后120 ℃干热1 min显色[8]。待颜色显示出来后立即扫描拍照。通过Quantity One(Bio-Rad,美国)扫描分析TLC图谱,并对每个样品中的碳源残留量进行定量计算。
1.2.4 DNA提取:将粪便原液和48 h的样品用来提取细菌DNA,按照QIAamp DNA Stool Mini Kit试剂盒说明书的提取方法。提取完成后用Nano Drop ND-2000测其浓度。然后-80 ℃保存。
1.2.5 SCFA分析:用气相检测样品中SCFA的浓度。样品中的乙酸、丙酸、丁酸、异丁酸、戊酸、异戊酸的浓度通过GC检测,柱子采用DB-FFAP的型号,用氢气火焰电离检测器,以巴豆酸作为内标物。
1.2.6 16S rRNA 基因序列测序:细菌16S rRNA基因扩增的引物为341F(5′-CCTAYGGGRBGCASCAG-3′)和 806R(5′-GGACTACNNGGGTATCTAAT-3′)。二代测序由利贞生物医药科技公司检测,从质量浓度为20 g/L的琼脂糖凝胶中提取扩增产物,用Axyprepdna凝胶提取试剂盒进行纯化。根据标准,在Illuminamiseq平台上,将纯化的扩增产物合并成等摩尔序列和配对序列(2×250)。原始读取存储在NCBI序列读取存档(SRA)数据库中。
1.3统计学分析采用SPSS 24.0统计软件中的非参数检验计算各组间SCFA的产量、产气量、降解率和Chao1指数、Shannon 指数和Simpson指数的差异。
2 结果
2.1志愿者原始粪便菌群差异比较两组的16S rRNA测序结果,前15种高丰度菌中,只有拟杆菌丰度在40~60岁组中较高,其他菌无显著差异(见图1A)。40~60岁组的拟杆菌相较于20~40岁组有差异,而20~40岁中的差异菌群主要是一些丰度极低的菌群,所以两组之间的菌群结构比较相似(见图1B)。两组的Shannon和Simpson指数方面无显著差异。两组间的SCFA含量也无显著差异(P>0.05,见图1C)。
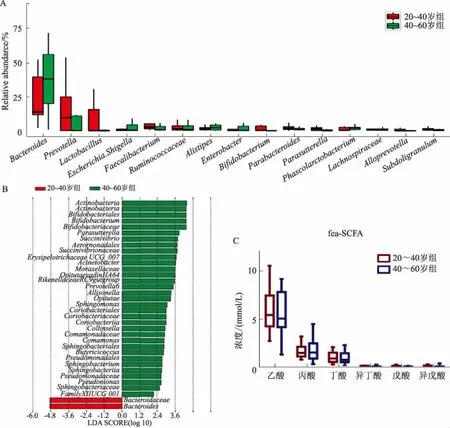
图1 原始粪便菌群差异 A: 高丰度菌群箱线图;B:Lefse分析;C:SCFA含量Fig 1 The difference of original fecal flora A: Boxplot of high fecal abundance; B: Lefse analysis; C: content of SCFA
2.2两组人群对STA和INU的降解率为了比较两组人群对STA和INU的降解率,我们对两种培养基的发酵液做了TLC检测分析。根据对每个样本的分析结果发现,无论是在24 h还是48 h,两组STA和INU的降解率差异均有显著统计学意义(P<0.01),在24 h时STA已经完全降解,而INU的降解率约70%。而20~40岁组与40~60岁组在48 h时INU的降解率差异有显著统计学意义(P<0.01),在48 h时,20~40岁组INU已经完全降解,而40~60岁组的平均降解率为90%。这些结果说明40~60岁组的肠道菌群的降解率明显不如20~40岁组。表明40~60岁人群的肠道微生物对INU的利用已经不如20~40岁人群,肠道菌群的功能已经开始出现轻微退化(见图2)。
2.324h的产气情况为了探究两组人群肠道菌群的产气差异,我们在接种24 h后测了小瓶内的气压值,以此来判断菌群产生气体的量。根据测得的每个人的气压数据可知,STA组中两组人群产气量一样,但在INU组中,40~60岁组的个体差异较大,且40~60岁组的产气量明显高于20~40岁组,这说明老年人在服用INU后肠道菌群代谢会产生更多的气体(见图3)。
2.4两组人群中SCFA的差异SCFA是使用GC 测定的。如图4所示,通过比较不同组之间SCFA含量,发现在48 h时,在INU中,40~60岁组中乙酸的含量低于20~40岁组,而丙酸和丁酸的含量均高于20~40岁组,而总的SCFA含量两组比较,差异无统计学意义(P>0.05)。而在STA中,各SCFA的含量两组比较,差异无统计学意义(P>0.05)。这些结果表明,在服用INU后,两组人群的肠道菌群对SCFA的代谢方式发生改变。

图2 两组人群对STA和INU的降解率;图3 各组间产气差异比较 Fig 2 Degradation rates of STA and INU in two groups;Fig 3 Comparison of gas production among each group
2.5STA和INU对两组人群肠道菌群的影响为了解INU和STA对肠道菌群的影响,在发酵48 h后对发酵样品进行16S rRNA测序,结果如图5所示,在以STA为碳源的培养基发酵后,20~40岁组中的Bifidobacterium、Ruminiclostridium5、Catenibacterium、Megasphaera、Comamonas、Neisseria较40~60岁组差异明显;而40~60岁组中的Adlercreutzia、Lactococcus、Faecalitalea、Turicibacter、Mitsuokella相对20~40岁组丰度较高。
在以INU为碳源的培养基发酵后,在20~40岁组中,Bifidobacterium、Lactobacillus、Christensenella、Catenibacterium、Comamonas、Actinobacillus等差异显著。在40~60岁组中,Enterococcus、Peptostreptococcus、Clostridium、Phascolarctobacterium、Rhodospirillales、Delftia、Escherichia-Shigella等差异显著。其中,有报道指出Escherichia-Shigella、Peptostreptococcus、Enterococcus等含量升高伴随着肠炎[9]、酒精性脂肪肝[10]等疾病的发生。

图4 发酵液中SCFA含量 A:SCFA总量;B:乙酸产量;C:丙酸产量;D:丁酸产量 Fig 4 Content of SCFA in fermentation broth A: total amount of SCFA; B: acetic acid yield; C: propionic acid yield; D: butyric acid yield

图5 发酵液中菌群的Lefse分析图 A:STA组;B:INU组
3 讨论
越来越多的研究结果认为,人体肠道微生态的变化与宿主免疫系统老化和与年龄有关的慢性疾病发病有关[11]。但对于“老年人”似乎无一个统一的定义,例如“65岁以上”[12]、“60岁以上”[13]或“70岁以上”[14]。ODAMAKI等[15-16]研究表明,肠道细菌结构从4岁开始一直到70岁都是处于一个平稳时期,70岁以后才发生明显的变化,主要表现在Actinobacteria的数量减少,变形杆菌数量增加。我们的研究中却发现40~60岁人群粪便样品中拟杆菌的丰度较20~40岁组显著升高。除此之外,粪便SCFA含量无明显差异。总体来说,如果仅仅通过16S rRNA测序分析粪便肠道菌群结构和SCFA的话,20~40岁组与40~60岁组肠道微生态的结构和主要代谢产物较相似。
体外发酵系统是通过建立一个适宜肠道微生态生长的环境系统,可以体外比较研究肠道微生物对膳食纤维或其他食物组分降解和发酵的速度。体外肠道模拟系统是研究非宿主相关因素对脊椎动物肠道微生物学特性影响的有效工具[17]。人体肠道微生物发酵膳食纤维后的主要代谢产物包括乙酸、丙酸和丁酸为主的SCFA、氢气、甲烷和二氧化碳[18]。参与多糖降解的肠道细菌主要有拟杆菌、双歧杆菌、罗氏菌属和瘤胃球菌属,以及一些梭菌属和肠球菌[19]。本研究中,20~40岁与40~60岁虽然在粪便肠道菌群组成上无显著差异,但在肠道菌群代谢功能方面,两组间差异显著。例如,40~60岁组的INU降解效率和降解能力不如20~40岁组,而产气量明显高于20~40岁组,这些结果表明老年人服用INU后易出现腹胀,大量的肠道气体甚至引起腹痛或肠易激综合征[20]。结肠微生物通过发酵碳水化合物和蛋白质产生SCFA,主要包括乙酸、丙酸、异丁酸、异戊酸、戊酸。发酵48 h后,20~40岁组乙酸含量明显高于40~60岁组,40~60岁组的丙酸和丁酸含量较高,但差异无统计学意义。醋酸能调节食欲[21],丁酸是肠道细胞的主要能量来源[22],丙酸可以调节糖异生过程和饱腹感信号[23]。因此,推测老年人服用INU后,菌群代谢造成的乙酸含量下降、丙酸和丁酸升高更容易引起饱腹感,而20~40岁组则未见此现象。本研究结果表明,尽管两个年龄组总体来说仍处于壮年时期,粪便肠道菌群组成并无明显差异,但平均年龄50岁人群的肠道菌群对膳食纤维INU的降解代谢能力明显不如平均年龄30岁人群。
越来越多的证据证明环境因素在确定肠道菌群结构与功能方面起到重要作用。而膳食则是改变肠道微生物组成的一个最重要因素。对近交系小鼠的研究表明,大量改变膳食营养素能在1 d内显著改变肠道微生物群落[24-25]。在本研究中,STA中两组的发酵液中菌群差异不明显,这可能是由于试验中采用的可溶性淀粉在人体中是容易被消化吸收的[26],肠道内的梭菌属、类杆菌等都是直接参与STA代谢的[27],而这些菌在两组人群内丰度较高,所以STA的利用率无较大差异。INU能在体外发酵模型中48 h内显著改变粪便微生物群落结构。对于40~60岁组,添加INU使E.coli、Delftia、Peptostreptococcus等数量增加,这些细菌大部分都属于条件致病菌。相反,添加INU使20~40岁组的益生菌,如Bifidobacterium、Leuconostoc、Acidaminococcus等含量增加。这个结果表明,虽然大量的基础科学已证明INU有益于宿主的免疫反应代谢过程和神经内分泌途径,但益生元的选择和用量需要考虑年龄的差异。
本研究结果再一次证明了肠道菌群在成年后一直保持稳定,但会随着年龄的增加而发生变化[28]。仅用16S rRNA测序粪便中的菌群结构可能无法准确区分生命过程中肠道菌群功能的变化,肠道菌群功能的衰退可能远远早于菌群结构的退化。探讨肠道菌群功能的变化,并将肠道菌群的功能和菌群的结构及年龄联系起来,可为个性化饮食和肠道疾病的治疗提供更精确更合理的指导意见。
