偶氮吡咯化合物的合成及其比色阴离子识别特性
2019-03-25张怡然尹振明
张怡然 ,李 彤 ,尹振明
(1.天津师范大学 化学学院,天津 300387;2.天津师范大学 无机-有机杂化功能材料化学教育部重点实验室,天津 300387;3.天津师范大学 天津市功能分子结构与性能重点实验室,天津 300387)
阴离子在化学、生物、医学及环境等领域有十分重要的作用,设计合成具有特定阴离子识别与传感能力的受体化合物已成为超分子化学中的一个研究热点[1-4].氢键由于具有方向性、可调性和强度适中等特点,是阴离子识别受体设计中常被考虑的非共价键作用力[5-6].吡咯是一种常见的氢键供体单元,其—NH可以与阴离子形成氢键.研究表明,杯吡咯[7-9]、二吡咯喹喔啉[10-11]、二吡咯甲烷[12-13]、2-吡咯酰胺[14-15]和吡咯希夫碱[16]都有较好的阴离子识别能力.在众多的化学检测方法中,比色检测法具有所需仪器简单、操作简便和便于观察等优点[3].构建比色阴离子识别受体的基本方法是通过共价键将阴离子识别位点与生色团连接,偶氮基团N=N是一种常见的生色团,常被应用于比色阴离子识别受体的设计[17-19].
苯基或杂环偶氮吡咯由于光电性质独特,在新材料或器件制备方面具有良好的应用前景[20-23].在2-苯基偶氮吡咯分子中,吡咯可以作为阴离子识别的位点,偶氮基团可以作为比色的信号基团,因此其本身就是一个比色阴离子识别传感器,但是迄今为止关于偶氮吡咯阴离子识别的研究还极少[24].本研究以邻氨基苯酚和吡咯为底物,设计合成2个邻羟基偶氮吡咯化合物,利用UV-Vis光谱和核磁滴定法研究它们在二甲基亚砜(DMSO)溶液中对 F-、Cl-、Br-、NO3-等几种常见阴离子的识别特性.
1 实验
1.1 仪器与试剂
仪器:AV-400型核磁共振仪,TMS为内标,DMSO-d6为溶剂,美国Bruker公司;AEIMS-50/PS 30质谱仪,美国赛默飞公司;240型元素分析仪,美国Perkin-Elmer公司;X-4数字显示显微熔点测定仪,温度计未校正,北京泰克仪器有限公司;UV-2550紫外可见分光光度计,日本Shimadzu公司.
试剂:邻氨基苯酚、吡咯、四丁基季铵盐(F-、Cl-、Br-、I-、AcO-、HSO4-、NO3-、H2PO4-),AlfaAesar(中国)化学有限公司.所有试剂均为分析纯级.
1.2 化合物(受体)1和2的合成
在50 mL圆底烧瓶内加入2.5 mmol邻氨基苯酚、5 mL水和1 mL浓盐酸,微热搅拌使固体充分溶解,待冷却至温室放入冰水浴使体系温度保持在0~5℃.另取25 mL烧杯,加入0.2 g的NaNO2和5 mL水,溶解后置于冰水浴中保持体系温度为0~5℃.将NaNO2溶液缓慢滴入圆底烧瓶中,控制滴加速度,使体系温度始终为0~5℃.滴加完成后,冰水浴搅拌30 min,所得重氮盐置于冰水中备用.
在100 mL圆底烧瓶中加入2.5 mmol(0.17 g)吡咯、25 mL乙腈和3滴冰醋酸,使体系温度保持在0℃以下.逐滴滴加预先制备好的重氮盐,滴加完成后搅拌反应2 h左右.反应液用乙酸乙酯萃取(20 mL×3),有机相用无水MgSO4干燥.蒸出有机溶剂,残余物用乙酸乙酯与石油醚的混合液(体积比为1∶5)进行硅胶柱层析分离,所得第一个带为化合物1(Rf=0.50),第二个带为化合物2(Rf=0.15).
化合物1(C10H9N3O):黄色固体0.182 g,产率39%,m.p.:88 ℃.1H NMR(400 MHz, DMSO-d6):δ 11.83(s,1H, NH), 10.02(s, 1H, OH),7.58(d, 1H, J=8.4 Hz,Ar-CH),7.28(t, 1H, J=7.2 Hz, Ar-CH), 7.18(s, 1H,pyrrole-CH), 6.98(d, 1H, J=8.4 Hz,pyrrole-CH),6.90~6.93(m, 2H, Ar-CH), 6.33(s, 1H, pyrrole-CH);13C NMR(100 MHz, DMSO-d6): δ 111.1, 113.7, 117.1,117.9, 119.6, 123.3, 131.4, 138.2, 146.0, 154.5;ESI-MS:188(M+1+).元素分析计算值(%):C,64.16; H,4.85;N,22.45.实验值(%):C,63.97;H,4.90;N,22.17.
化合物 2(C16H13N3O2):橙黄色固体 0.08 g,产率23%(以邻氨基酚的量计算),m.p.:220℃.1H NMR(400 MHz, DMSO-d6):δ 11.51(s, 1H, NH), 10.32(s,1H, OH), 10.23(s, 1H, OH), 7.71(d, 1H, J=6.8 Hz,Ar-CH), 7.60(d, 1H, J=6.8 Hz, Ar-CH),7.26(t, 1H,J=7.2Hz,pyrrole-CH), 7.19(t, 1H, J=7.2 Hz, pyrrole-CH), 6.97~7.08(m,3H,Ar-CH),6.89~6.95(m,3H,Ar-CH);13C NMR (100 MHz, DMSO-d6): δ 111.9, 116.4,117.1, 117.7, 119.5, 119.6,127.4, 128.9, 130.9,134.3, 138.7, 145.6, 154.2, 154.5; ESI-MS: 280(M+1+).元素分析计算值(%):C,68.81;H,4.69;N,15.05.实验值(%):C,69.03;H,4.63;N,14.96.
1.3 UV-Vis光谱滴定
化合物1和2先用DMSO配制成浓度为2.5×10-2mol/L的储备液,再用DMSO将其浓度稀释为2.5×10-5mol/L.量取3 mL该溶液于比色皿中,用配制好的各种阴离子溶液(以DMSO为溶剂,浓度为2.5×10-2mol/L)滴定至光谱变化平衡.识别常数通过以下方程的非线性拟合求出.
式中:CH为受体浓度;CG为加入的阴离子浓度;Ka为识别常数;A0和A分别为受体和加入阴离子后的吸光度.
利用核磁滴定法测定受体与阴离子的配位比.令二者的总浓度恒定(1×10-5mol/L),分别改变受体与阴离子的物质的量分数,以未添加阴离子的受体溶液作参比,于室温下测其紫外-可见吸收光谱.以γ为横坐标,以γ×ΔA为纵坐标作图,其中γ=[受体]/([受体]+[阴离子]),ΔA=A0-A.
2 结果与分析
2.1 化合物的合成
化合物1和2的合成路线如图1所示.
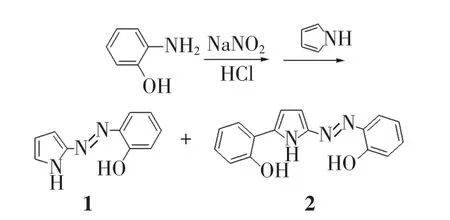
图1 化合物1和2的合成路线Fig.1 Synthesis scheme of compounds 1 and 2
首先将邻氨基苯酚进行重氮化,然后与吡咯反应,顺利合成化合物1.薄层色谱分析显示,产物中除了化合物1外,还存在另外一种产物,核磁、质谱与紫外光谱分析均表明该产物即为化合物2.化合物2的形成应该是在反应过程中重氮盐失去N2转化为苯基碳正离子或自由基,而后与偶氮吡咯化合物1发生亲电取代反应所致[25-26].
2.2 化合物1的UV-Vis光谱滴定
化合物1的DMSO溶液中滴加10倍量的F-、Cl-、Br-、I-、H2PO4-、AcO-、HSO4-或 NO3-后,UV-Vis光谱变化如图2所示.从图2可以看出,只有F-离子的加入造成了化合物1的UV-Vis光谱发生了显著变化,这说明化合物1对F-离子具有专一性识别.
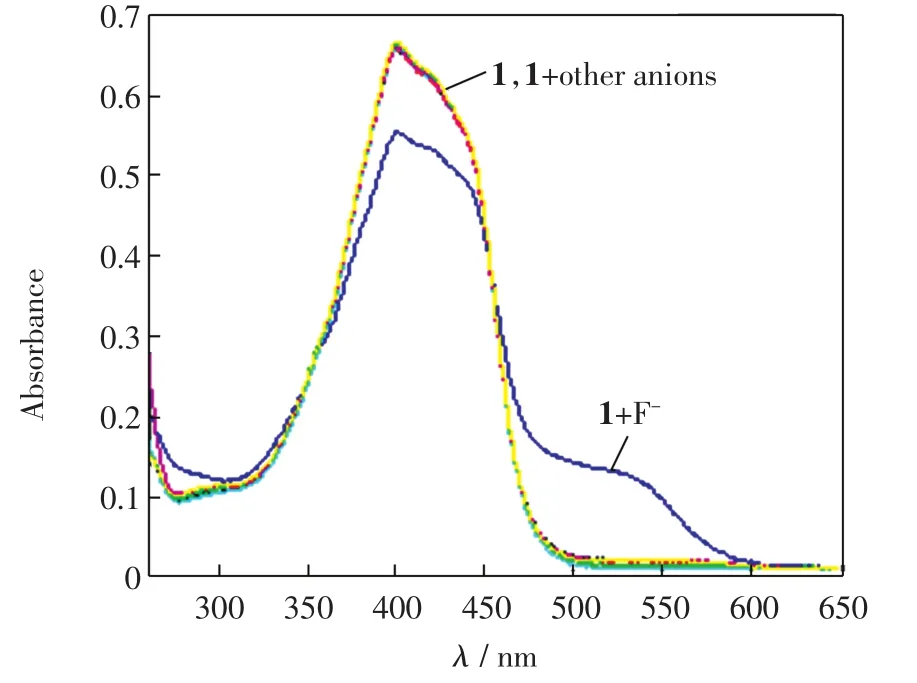
图2 化合物1的DMSO溶液中加入10倍阴离子后的UV-Vis光谱变化Fig.2 UV-Vis spectral changes of compound 1 after the addition of 10 equiv anions in DMSO
F-离子对化合物1的DMSO溶液的滴定谱图变化如图3所示.

图3 化合物1的DMSO溶液中加入F-离子后UV-Vis光谱的变化Fig.3 UV-Vis spectral changes of compound 1 after the addition of fluoride anion in DMSO
由图3可以看出,化合物1在401 nm处有最大吸收峰(归属于—N=N—基团的吸收峰).随着Fˉ离子的加入,401 nm处吸收峰的强度逐渐降低,同时在550 nm处出现新的吸收峰,并逐渐蓝移到514 nm处,此时溶液颜色也由亮黄色变为橙黄色,这表明化合物1可以作为F-离子的比色传感器.核磁滴定法证明化合物1与F-离子间形了1∶1型的配合物.非线性拟合[27]得出它的络合常数Ka=1 032 L/mol.
2.3 化合物2的UV-Vis光谱滴定
化合物2的DMSO溶液中加入10倍量的各种阴离子后,UV-Vis光谱变化如图4所示.
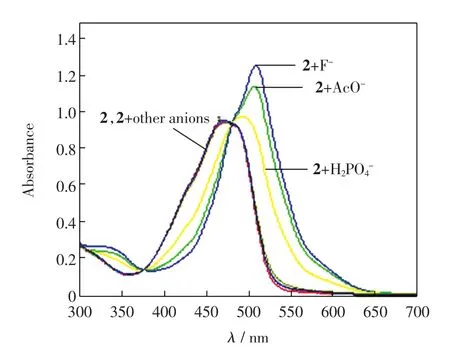
图4 化合物2的DMSO溶液中加入10倍阴离子后的UV-Vis光谱变化Fig.4 UV-Vis spectral changes of compound 2 after the addition of 10 equiv anions in DMSO
从图4可以看出,F-离子的加入造成了化合物2的UV-Vis光谱发生了显著变化,AcO-和H2PO4-也能够使化合物2的UV-Vis光谱发生变化,但吸光度值较Fˉ离子小.化合物2能够识别3种阴离子,同只能识别F-离子的化合物1相比,受体2的阴离子识别能力明显提高.化合物2的最大吸收波长位于471 nm,比化合物1的紫外吸收红移了70 nm,这可能是化合物2的共轭作用增强所致.化合物2的最大紫外吸收比2,5-双(邻羟基苯基偶氮)吡咯(在甲醇溶液中为507 nm[20])的数值减小了36 nm,这可能是由于化合物2的共轭程度小于2,5-双(邻羟基苯基偶氮)吡咯.
AcO-离子对化合物2的DMSO溶液的滴定谱图变化如图5所示.从图5可以看出,随着AcO-离子的加入,化合物2在472 nm处的吸收峰逐渐红移,最后在505 nm处出现新的吸收峰.Fˉ离子和H2PO4-离子对化合物2的滴定谱图与AcO-离子相似.随着3种阴离子的加入,化合物2的DMSO溶液颜色由橙色变为红色,如图6所示.核磁滴定法表明,化合物2与F-、AcO-和H2PO4-之间形成的均是1∶1型的配合物.非线性拟合[27]得出,化合物 2 对 F-、AcO-和 H2PO4-离子的络合常数 Ka 分别为 9.9×104、3.5×105和 7.2×103L/mol.同化合物1相比,化合物2的阴离子识别能力有了很大提升,这应该是由于化合物2中多了一个酚羟基所致.

图5 化合物2的DMSO溶液中加入AcO-离子后UV-Vis光谱的变化Fig.5 UV-Vis spectral changes of compound 2 after the addition of AcO-in DMSO

图6 化合物2的DMSO溶液在加入各种阴离子后的颜色变化Fig.6 Color changes of DMSO solutions of compound 2 after the addition of different anions
2.4 识别机理
通过核磁滴定实验研究化合物1和2对阴离子的识别机理,化合物1和2对F-离子的核磁滴定谱图如图7所示.由图7(a)可以看出,化合物1在δ为10.02和11.84处有2个信号峰,分别归属于羟基OH和吡咯NH,加入F-离子后,这2个峰信号消失.由图7(b)可以看出,化合物2在δ为10.24、10.32和11.51处有3个信号峰,分别归属于2个羟基OH和吡咯NH,随着F-离子的加入,这些信号峰逐渐向低场移动并变宽,甚至消失.核磁滴定研究表明,化合物1和2均通过羟基OH和吡咯NH与F-离子形成氢键相互作用实现阴离子识别.化合物2对AcO-和H2PO4-离子的核磁滴定谱图变化与F-离子类似.本研究据此提出了化合物1和2与F-离子作用的结构式,如图8所示.

图7 化合物1和2的DMSO-d6溶液中加入Fˉ后的1H NMR变化图Fig.7 1H NMR spectra changes of compounds 1 and 2 in DMSO-d6after the addition of Fˉ

图8 化合物1和2与Fˉ形成配合物的结构式Fig.8 Proposed structures of compounds 1 and 2 with Fˉ
3 结论
本研究通过邻氨基苯酚与吡咯的反应制备了2种偶氮吡咯化合物,采用UV-Vis光谱滴定法测试了2种化合物对阴离子 F-、Cl-、Br-、I-、AcO-、HSO4-、NO3-、H2PO4-的识别.结果表明,化合物1在DMSO溶液中对Fˉ离子有专一性的识别作用,而化合物2的识别能力大于化合物1,在DMSO溶液中对Fˉ、AcOˉ和H2PO4-离子都有较强的识别作用,尤其是对于F-.核磁滴定研究表明,2种化合物均通过氢键与阴离子相互作用,形成1∶1的配合物.化合物1和2在阴离子识别的同时均伴随着溶液颜色的变化,表明偶氮吡咯可以成为一类新型的阴离子比色传感器.本研究可为设计合成性能更优秀的阴离子识别受体提供参考.
