[Cu(N3)2(phen)]n和[CoNiL(Hcam)(H2O)]单晶配合物的合成、结构及其荧光性质
2019-03-25邓国志孙亚秋郑艳峰
邓国志 ,孙亚秋 ,信 娜 ,郑艳峰
(1.天津师范大学 化学学院,天津 300387;2.天津师范大学 无机-有机杂化功能材料化学教育部重点实验室,天津300387;3.天津师范大学 天津市功能分子结构与性能重点实验室,天津 300387)
过渡金属配合物中的多核配合物和配位聚合物由于具有出色的结构,在磁性、发光、吸附、催化等方面有巨大的应用价值[1-5].4-羟基吡啶-2,6-二甲酸是一种双官能化的氮杂环羧酸配体,不仅可以提供6个潜在的配位点,以多种配位模式与金属离子配位,还可以部分脱去质子并提供氢键的给体和受体进行超分子组装,配体本身的吡啶环又有利于形成π-π堆积作用,这就为设计合成具有新颖结构和性质的配位聚合物提供了更多的可能性[6].由于不同过渡金属离子间存在配位竞争,因此用4-羟基吡啶-2,6-二甲酸组装杂金属配合物时有一定难度.邻菲罗啉是目前最流行的二齿N,N螯合剂,是一种优良而稳定的π电子接受体,也是一种常见的分子建筑块,它上面的2个氮原子可以轻易占据金属离子的空轨道,与金属离子以反馈二键的形式结合在一起,实现与金属离子之间的配位[7-8].邻菲罗啉配合物具有极强的光化学和光物理性质,但由于邻菲罗啉配位模式的限制,无法用其合成多核或配位聚合物.1,10-邻菲罗啉具有含氮的六元杂环结构,接受π电子能力卓越,易于与各种金属离子形成稳定的有特殊光电性质[7,9-11]的配位化合物.
为了得到具有优异光学性能的配位聚合物和杂金属配合物,本研究采取混配方法,以叠氮和邻菲罗啉为共配体合成了配位聚合物[Cu(N3)2(phen)]1,以大环草酰胺单核配合物NiL和4-羟基吡啶-2,6-二羧酸离子为共配体合成异双核配合物 [CoNiL(Hcam)(H2O)]2,并对二者的结构和荧光性质进行表征。
1 实验
1.1 仪器与试剂
仪器:240元素分析仪,美国Perkin Elmer公司;IR-408红外分光光度计,日本Shimadzu公司;D型/max-2550v衍射仪,日本Rigaku公司;850荧光分光光度计,日本Hitachi公司.
试剂:邻菲罗啉、Cu(Ac)2、凯玛特(天津)化工科技有限公司;NaN3,阿拉丁试剂(上海)有限公司;4-羟基吡啶-2,6-二羧酸,北京伊诺凯科技有限公司.所有试剂均为分析纯级.按照文献[11]中的方法制备大环草酰胺单核配合物NiL.
1.2 配合物1[Cu(N3)2(phen)]的合成
利用液液扩散法设计并合成配合物1.将NaN3和邻菲罗啉加入到H型管的一侧,Cu(Ac)2则加入到另一侧,然后将水和甲醇混合溶剂(按体积比1∶1混合)缓慢加入H管中,静置数天后得到深绿色晶体,即为配合物1(C12H8CuN8).使用240元素分析仪进行元素分析.实验值(%):C,43.84;H,2.34;N,34.10.计算值(%):C,43.82;H,2.31;N,34.08.红外测试结果(v, cm-1): 3 100 v(C—H), 2 134 vas(N3-), 2 038 vs(N3-),1 517 v(C=N).
1.3 配合物 2[CoNiL(Hcam)(H2O)]的合成
将 NiL(0.05 mmol)、4-羟基吡啶-2,6-二羧酸(0.05 mmol)、Co(Ac)2·4H2O(0.1 mmol)、H2O(10 mL)和甲醇(4 mL)的混合溶液在室温下搅拌10 min,使用三乙胺将溶液pH调至6~7.将混合溶液转移到18 mL的聚四氟乙烯内衬反应器中,加热到150℃,保温72 h.将反应体系在36 h内冷却至室温,得到深棕红色晶体,即为配合物2(C26H21N5O8CoNi).元素分析实验值(%):C,48.07;H,3.24;N,10.78.计算值(%):C,48.06;H,3.23;N,10.77.红外测试结果(v,cm-1):1647vs(COO-),1 606 v(C=O), 1 584 v(C=N).
1.4 配合物的结构表征与荧光性质测试
在室温下,使用配备了石墨单色器Mo-Kα衍射线(λ=0.071 073 nm)的Bruker Smart ApexⅡCCD单晶衍射仪,采用φ/ω扫描方式,对配合物1和2进行单晶X线衍射分析.采用SADABS法进行半经验吸收修正.使用SHELXTL软件中的SHELXS程序,采用直接法解出配合物的所有结构,使用SHELXL程序进行精修.配合物1和2的晶体数据和精修参数如表1所示.CCDC参考号码:1062159-1476192.

表1 配合物1和2的晶体学数据Tab.1 Crystallographic data for complexes 1 and 2
使用Shimadzu IR-408红外分光光度计,采用KBr进行压片,在600~4 000 cm-1范围内对样品的红外光谱进行测试,使用D型/max-2550v衍射仪对样品粉体进行粉末X线衍射(XRPD)的表征测试,使用Hitachi 850荧光分光光度计对样品的荧光发射光谱进行记录.
2 结果与分析
2.1 配合物的晶体结构
配合物1的结构如图1所示.
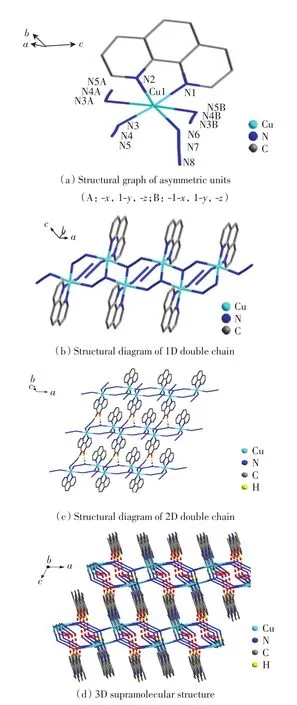
图1 配合物1的结构Fig.1 Structural diagram of complex 1
单晶X线衍射分析表明,配合物1通过叠氮与中心铜(Ⅱ)离子配位构成一维双链配位聚合物.该配合物的不对称单元结构如图1(a)所示,中心铜(Ⅱ)离子与6个氮原子配位形成六配位的畸变的八面体几何形状,6个氮原子分别来自4个叠氮离子和1个1,10-邻菲罗啉.铜(Ⅱ)离子的配位构型为拉长的八面体几何形状,其轴向位置的2个氮原子分别来自作为端基配体的N3-和1,10-邻菲罗啉,轴向键长明显比底面的4个Cu—N键要长,这是由于姜泰勒效应造成的.配合物1的主要键长和键角数据如表2所示.

表2 配合物1和2的部分键长和键角Tab.2 Selected bond length and bond angle of complexes 1 and 2
由表2可以看出,该配合物中,N与Cu之间的键长为0.197 4(3)~0.241 8(3)nm,N—Cu—N 的键角为80.76(13)°~170.42(11)°.相邻的 2 个不对称单元通过2个叠氮以μ-1,1的桥联方式构成了[Cu2(N3)2]双核单元,双核单元又通过叠氮的首尾桥联模式构成一维双链结构,如图1(b)所示.在一维框架中,叠氮离子有2种配位模式:一种是N3-配体采取μ3-1,1,3桥接模式与3个铜(Ⅱ)离子配位;另一种则是N3-作为端基配体与铜(Ⅱ)离子配位.双链通过弱的C—H…N氢键作用连接在一起构成二维网络,如图1(c)所示,dN…C为0.338 6 nm,二维网络间也是通过弱的C—H…N氢键连接在一起形成三维超分子结构,如图1(d)所示,dN…C为 0.334 2~0.337 8 nm.
配合物2是通过草酰胺桥联的杂双核配合物,其结构如图2所示.

图2 配合物2的结构Fig.2 Structural diagram of complex 2
在双核的[CoNiL(Hcam)(H2O)]结构中,钴(Ⅱ)离子与镍(Ⅱ)离子通过大环草酰胺配体桥联构成[CoNi]双核单元.镍(Ⅱ)离子分别与大环草酰胺上的4个氮原子配位构成畸变的平面四方形构型,4个氮配位原子偏离它们组成的最小二乘平面的距离N1、N2、N3和N4分别为 0.024 58、-0.022 74、-0.021 43 和 0.024 24 nm,Ni1与此平面间的距离为-0.004 65 nm.Co1分别与大环草酰胺配体的2个氧原子、4-羟基吡啶-2,6-二羧酸根离子中的2个氧原子和1个氮原子以及水分子中的1个氧原子配位,中心钴离子的配位构型为畸变的八面体几何形状.相邻的[CoNi]双核单元通过O—H…O氢键连接在一起,形成二维超分子结构,如图2(b)所示.配合物2的氢键有2种类型:一种是Hcam2-中的COO-上未配位的氧与相邻的[CoNiL(Hcam)(H2O)]中的 H2O分子形成氢键(dO…O=0.273 4~0.275 1 nm,∠OHO=168.92°~172.88°);另一种是 Hcam2-中未配位的OH与相邻的配位单元中的COO—形成氢键(dO…O=0.258 9~0.317 3 nm,∠OHO=132.30°~167.10°).
2.2 配合物的IR、XRPD和荧光性质
红外光谱结果显示,配合物1在1 517 cm-1处具有较强的吸收峰,这是由于苯环中的ν(C=N)振动现象引起的,在2 134和2 038 cm-1处的强吸收峰分别为桥联和未桥联的叠氮配体的伸缩振动.配合物2在1 647~1 603 cm-1和 1 556~1 562 cm-1区域具有较强的吸收峰,这是分别由ν(C=O)和ν(C=N)的弯曲振动所导致的.配合物2在1 680~1 720 cm-1处不存在吸收峰,说明4-羟基吡啶-2,6-二甲酸中的羧基已完全去质子化,在3 423~3 411 cm-1波段的吸收峰来自H2O和Hcam2-的羟基的特征吸收峰.配合物1晶相纯度的可靠性已经由实验的XRPD图谱所证实,得到的数据与从单晶数据模拟的结果相吻合,如图3所示.
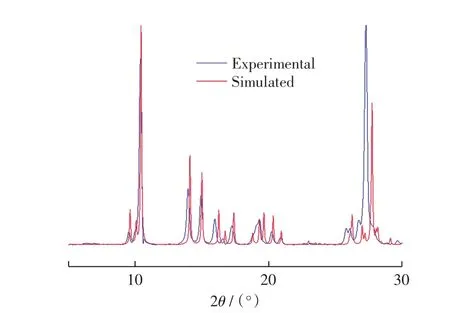
图3 配合物1的PXRD图谱Fig.3 PXRD pattern of complex 1
在室温下,激发波长为315 nm时,测定配合物1的固态荧光光谱,结果如图4所示.

图4 配合物1和邻菲罗啉的荧光光谱Fig.4 Fluorescence spectra of complex 1 and phen
由图4可以看出,邻菲罗啉的主要发射峰在364、381和402 nm处,这些发射峰是由于π*→π或π*→n电子跃迁所致.与邻菲罗啉的发射光谱相比,配合物1在364、381和402 nm处的荧光强度消失,其荧光猝灭的原因是邻菲罗啉和铜(Ⅱ)离子发生了配位.
在室温下,激发波长为279 nm时,测定配合物2、4-羟基吡啶-2,6-二羧酸和NiL的固体荧光光谱,结果如图5所示.
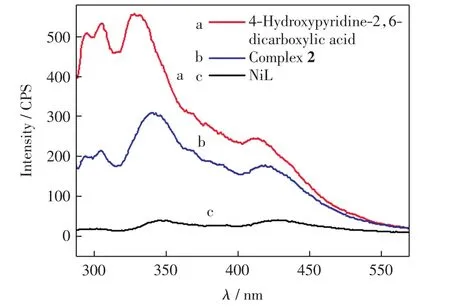
图5 配合物2、4-羟基吡啶-2,6-二羧酸和NiL的荧光光谱Fig.5 Fluorescence spectra of the complex 2,4-hydroxypyridine-2,6-dicarboxylic acid and NiL
由图5可以看出,4-羟基吡啶-2,6-二羧酸在294、305、329、413 nm处有发射峰,可能来自于π*→π或π*→n电子跃迁.与4-羟基吡啶-2,6-二羧酸发射光谱相比,配合物2的荧光强度大大降低,荧光猝灭的原因可能是由于4-羟基吡啶-2,6-二羧酸和钴(Ⅱ)离子发生了配位.
3 结论
本研究分别以叠氮与邻菲罗啉为共配体及大环草酰胺单核配合物NiL和Hcam2-为共配体,获得了一维双链配位聚合物[Cu(N3)2(phen)]n和异双核配合物[CoNiL(Hcam)(H2O)],通过 X-线单晶衍射、元素分析和光谱分析对2种配合物进行了表征.配合物1是通过叠氮桥联的一维双链结构,链与链之间又通过C—H···N分子间氢键构成三维超分子结构;杂双核配合物2通过O—H···O分子间氢键构成了二维超分子结构.通过对配合物1和2的荧光性质研究发现,与形成配合物的配体的荧光强度相比,2种配合物均发生了荧光猝灭现象,发生荧光猝灭的原因可能是由于配体与相应的金属离子之间发生了配位造成的.
