腹腔镜联合胆道镜治疗胆囊结石合并胆总管结石手术困难因素分析及临床对策
2019-03-22张敏杰樊永强董胜利
张敏杰,樊永强,董胜利
(山西医科大学第二医院,山西 太原,030001)
胆囊结石是临床最常见的胆道系统病变,腹腔镜胆囊切除术(laparoscopic cholecystectomy,LC)是其主要治疗方式。有报道称,伴有临床症状的胆囊结石患者中,胆总管结石的患病率可达10%~20%[1]。对于此类患者,LC联合腹腔镜胆总管探查术(laparoscopic common bile duct exploration,LCBDE)是常见术式,但笔者临床实践中发现,由于患者情况导致此手术的难易程度差别较大,主要体现在手术时间过长或中转开腹,甚至结石残留。本研究旨在通过回顾性分析,以明确LC联合LCBDE的困难因素,并提出相应的临床对策。
1 资料与方法
1.1 临床资料 收集2013年9月至2018年10月在我院普通外科行LC+LCBDE+T管引流术患者的临床资料。纳入标准:(1)术前经腹部彩超、CT或磁共振胰胆管造影等影像学检查明确胆囊结石合并胆总管结石,有手术指征;或术前仅诊断胆囊结石,术中见胆囊管粗大、胆总管扩张或扪及胆总管结石,有探查胆总管指征;(2)无肝内胆管结石;(3)临床资料可查,无重大缺失项。排除标准:(1)存在严重心肺疾病、肝、肾功能异常、凝血障碍等手术禁忌证;(2)术中因考虑恶性肿瘤而行快速冰冻病理检查或更改手术方式;(3)同时行其他手术。
1.2 手术方法 全麻后,患者取平卧位,常规消毒铺巾。脐下缘做1 cm弧形切口,切开皮肤及皮下组织,穿刺气腹针建立CO2气腹,压力维持在12~14 mmHg,穿刺10 mm Trocar,置入腹腔镜。探查腹腔,如存在广泛粘连等操作困难情况,及时中转开腹;如无异常,分别于剑突下、右锁骨中线肋缘下及右腋前线穿刺10 mm、5 mm及5 mm Trocar。游离胆囊管、胆囊动脉,距胆总管约0.5 cm处胆囊管用生物夹及钛夹夹闭暂不切断,胆囊动脉用生物夹夹闭后切断。游离胆总管前壁并剪开约0.8 cm,置入胆道镜探查胆总管,细小结石可用生理盐水冲出,较大结石,则用取石网篮或取石钳取出,如多次尝试仍难以取出结石,则中转开腹,避免损伤胆总管。胆道镜重复探查,直至确定胆总管无结石残留,0ddi括约肌开闭自然,取石网篮可顺利进入十二指肠。胆总管内置入T管,用可吸收线缝合,50 mL注射器抽取生理盐水注入,确认T管周围无渗漏。切断胆囊管,游离切除胆囊,自剑突下切口取出。查无活动性出血后,生理盐水冲洗术野,于网膜孔处放置引流管一根,T管及引流管分别经右锁骨中线肋缘下及右腋前线置孔引出,缝线固定。检查术野无活动性出血,清点器械敷料无误后撤除操作器械及腹腔镜,排尽腹内CO2,缝合关闭各切口。
1.3 观察指标 (1)术前观测指标:年龄、上腹手术史、术前最高体温、白细胞计数、血清总胆红素;(2)术中观测指标:胆囊大小、胆囊壁厚度、胆囊壁炎症、胆囊三角显露情况、结石嵌顿、胆总管结石形态及数量、胆总管直径。
1.4 统计学处理 应用SPSS 22.0软件进行数据分析,将各观测指标结果进行分组,统计出每个亚组患者手术难易程度分布情况,采用Pearsonχ2检验或Fisher确切概率法进行单因素分析,筛选出可能导致手术困难的危险因素,将其纳入多因素Logistic回归,采用Hosmer-Lemeshow拟合优度检验及受试者工作特征(receiver operating characteristic,ROC)曲线对回归方程进行评价。P<0.05为差异有统计学意义。
2 结 果
2.1 资料及分组 最终共116例患者纳入研究,其中男48例,女68例,11~90岁,中位年龄64岁。术者均为副高以上职称、具有丰富手术经验的医师,手术时间55~408 min,中转开腹32例,中转率27.6%。根据本院实际手术能力对其分组:(1)容易组:手术时间≤180 min,且未中转开腹,胆总管结石均被取出,共63例;(2)困难组:手术时间>180 min,或中转开腹,或残留胆总管结石,共53例。
2.2 统计学分析结果 对所纳入的临床资料进行单因素分析,结果显示,胆囊大小、胆囊壁炎症严重程度、胆囊三角解剖关系显露情况、胆总管下段是否结石嵌顿及胆总管直径均为LC联合LCBDE手术难度较大的危险因素,见表1。将以上具有统计学意义的指标及临床实践中认为可能会影响手术难易程度的因素作为自变量,手术难易度为因变量,行多因素logistic回归分析,最终发现胆囊三角显露不清、胆囊壁化脓坏疽、胆总管下段结石嵌顿及胆总管直径≥12 mm的患者行LC联合LCBDE显著困难。见表2。
2.3 回归方程的建立 建立回归方程:LC+LCBDE手术困难的概率P1=1/(1+e4.958-2.999胆囊壁炎症-2.645胆囊三角显露情况-3.136胆总管下段结石嵌顿-1.374胆总管直径);LC+LCBDE手术容易的概率P0=1-P1,e为自然对数的底数。
2.4 对回归模型进行评价 对多因素logistic回归分析所建立模型行Hosmer-Lemeshow拟合优度检验,发现χ2=0.805,P=0.938>0.05,提示模型校准度良好。以该回归模型预测值为检验变量,实际难易度为状态变量,绘制ROC曲线,结果见图1,曲线下面积为0.854,该模型区分度良好,P<0.001,有统计学意义。
3 讨 论
目前临床对于胆囊结石合并胆总管结石患者的手术方式主要有两种:(1)术前、术中或术后内镜逆行胰胆管造影(endoscopic retrograde cholangiopancreatography,ERCP)联合LC;(2)LC联合LCBDE。LC联合术中ERCP在降低ERCP术后胰腺炎发生率、再手术率等方面的优势已被证实,但因其对临床医生及手术室设施要求严格,目前难以大规模应用[2];而LC术后ERCP存在内镜下胆总管结石难以取出,需再次手术的风险,临床价值有限。笔者所在医院普遍采用术前ERCP与LC序贯进行“两步走”方案或LC联合LCBDE“一步走”方案,已有若干meta分析表明,两种手术方案疗效相当[3-4],但如何根据患者病情评估手术风险,给出个体化的建议,是临床医生需要考虑的问题。
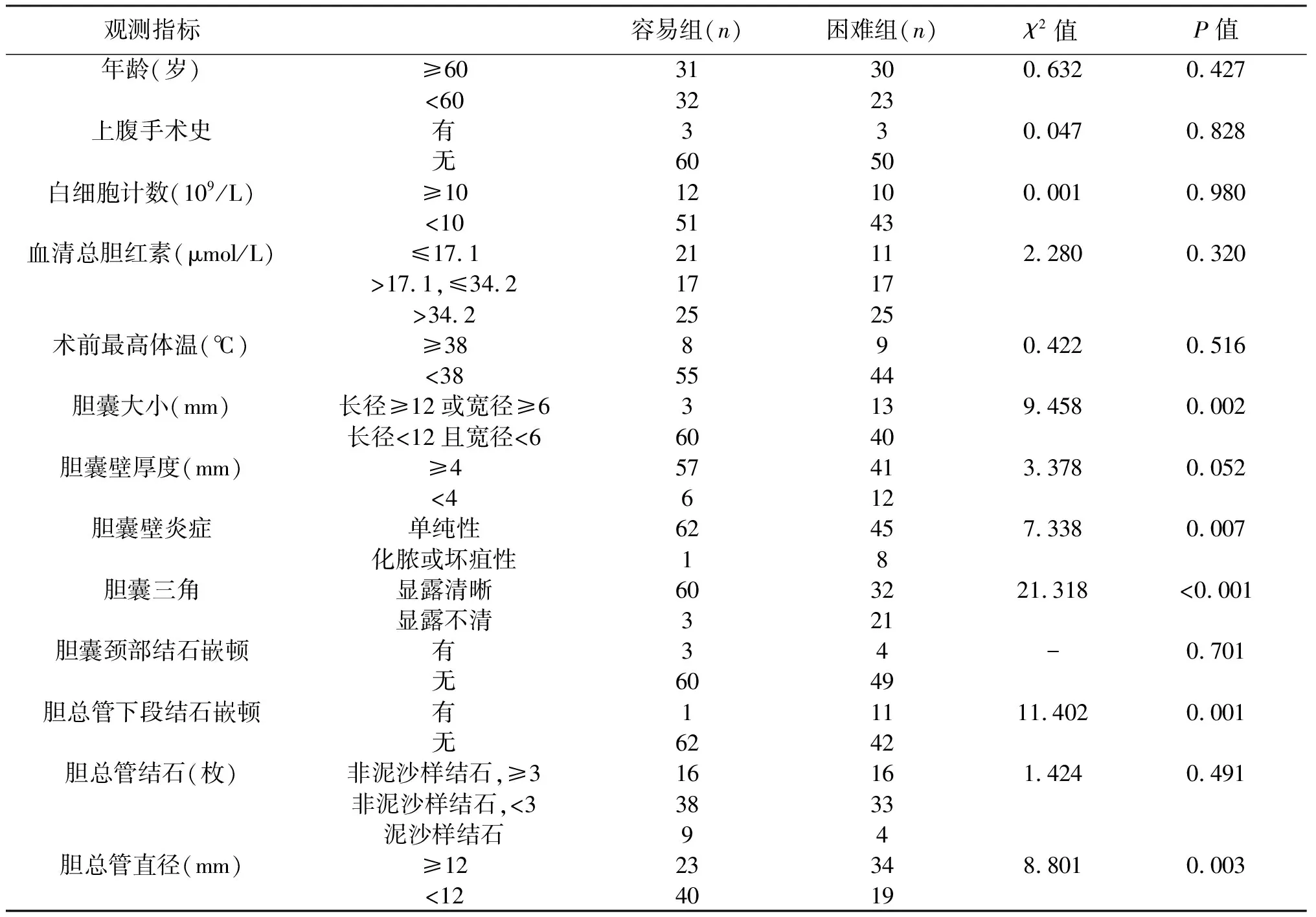
表1 LC联合LCBDE手术难易程度单因素分析
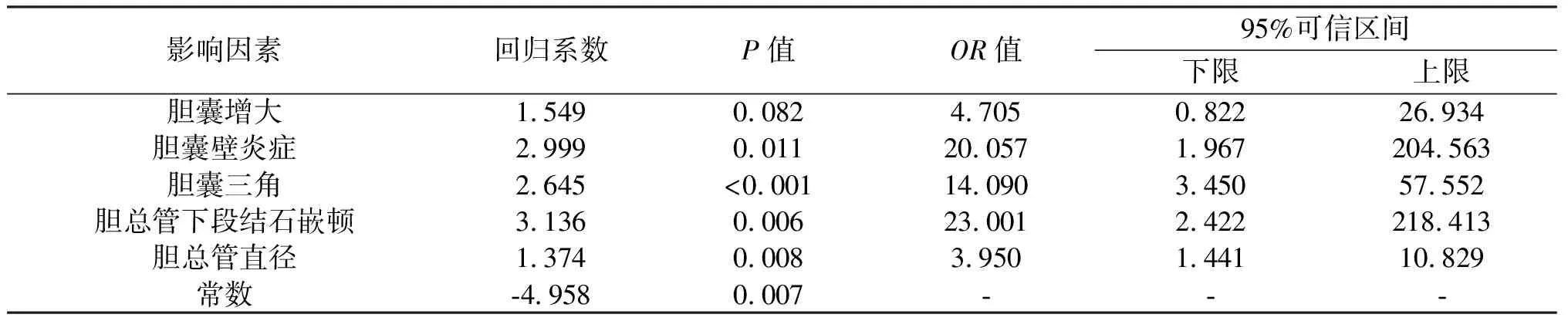
表2 LC联合LCBDE手术难易程度多因素logistic回归分析
目前关于腹腔镜手术危险因素的研究主要是针对中转开腹的风险,但笔者认为,单独强调中转开腹容易诱导术者一味追求腹腔镜手术,而忽视全麻气管插管手术时间过长导致的术中低体温、术后肺部感染及切口不愈合等风险增加[5-6],且CO2气腹可导致内脏器官缺血再灌注损伤[7],尤其老年患者,其身体重要器官储备功能下降,常合并多种基础疾病,对手术承受能力下降,手术时间过长,对预后极为不利。将手术时间与中转开腹相结合,作为评价手术难易程度的标准,并对其进行预测,具有实际意义:(1)术前可对患者进行充分告知,协助选择手术方案,有助于医患互信的建立;(2)术中根据实际情况及时预测手术难度的变化,提前做好准备,避免不必要的风险。
3.1 LC联合LCBDE手术困难因素 多因素logistic回归结果显示,胆囊三角显露不清、胆囊壁化脓或坏疽、胆总管下段结石嵌顿及胆总管直径明显增宽是LC联合LCBDE手术困难的独立危险因素。
3.1.1 胆囊三角显露不清 辨别胆囊三角解剖关系,对于腹腔镜胆道手术的安全性极为重要。笔者的经验是,术前应结合CT、MRI等影像学检查,了解胆囊管、胆总管的大致关系,有助于术中解剖游离;对于胆囊炎症反复发作者,术前应考虑到其胆囊周围粘连可能较重,更应借助影像学检查,明确胆囊与胆管解剖关系。术中采用“冷分离”技术[8],由胆囊后三角开始解剖,可在显露胆囊壶腹明确右肝管走行的同时,避免肝胆管热损伤及胆漏等并发症的发生。对于胆囊三角纤维素性粘连患者,应紧贴胆囊及胆囊管行蚕食性解剖,不要盲目求快,避免损伤胆总管,一般不难;而胆囊三角一旦形成瘢痕粘连,解剖分离难度即明显增加,常需中转开腹。

图1 二元logistic回归模型ROC曲线图
3.1.2 胆囊壁化脓或坏疽 胆囊炎急性发作如不及时处理,可进展为化脓性甚至坏疽性胆囊炎,但仅以发病时间长短区分胆囊炎病变程度并不合理[9]。临床上当急性胆囊炎患者出现高热、寒战、右上腹压痛加重、墨菲征阳性、局限性腹膜炎时,应注意胆囊化脓、坏疽、穿孔的可能,但也应注意部分老年患者痛觉、应激反应迟钝,症状及体征有时并不明显[10]。影像学检查时发现胆囊宽径≥4 cm、胆囊黏膜脱落、胆囊壁“条纹征”及胆囊壁强化减弱或消失,即提示存在胆囊坏疽可能[11-12];而应用多平面重组及最大密度投影技术对腹部增强CT图像进行重建,以胆囊动脉狭窄、闭塞征象诊断坏疽性胆囊炎的敏感度、特异度可达到85%与67%[13]。术前高度怀疑胆囊化脓、坏疽或穿孔时,即应考虑存在肠麻痹导致肠管扩张的可能,此时必须注意气腹针穿刺位置及深度,避免因误伤肠管而引起肠瘘、腹膜炎,危及患者生命。
化脓或坏疽性胆囊炎行腹腔镜手术常见的难点及对策:(1)因胆囊肿大、张力过高而难以抓持;此时应果断行胆囊穿刺减压,从而充分暴露胆囊三角,避免损伤周围组织结构。(2)胆囊周围渗出导致粘连严重:①坏疽、穿孔的胆囊与大网膜致密粘连时,缓慢游离即可;②胆囊与肝脏之间紧密粘连时,应紧贴胆囊游离,坚持“宁伤胆囊勿伤肝”的原则,一般不会引起出血,需要注意的是肝硬化患者多伴有静脉曲张,自其胆囊床上剥离胆囊时出血风险较大,此时术中应用超声刀并保留部分胆囊后壁更为安全、有效[14];胆囊三角粘连的处理方式前文已介绍,此处不再赘述。
3.1.3 胆总管下段结石嵌顿 胆总管胰腺段及十二指肠段管腔存在偏心现象,甚至憩室样改变,容易导致结石嵌顿[15],此时胆管壁常水肿,取石网篮等常规方式操作困难。本研究中此类患者中转开腹率达91.7%(11/12)。对于术前磁共振胰胆管造影明确胆总管下段结石的患者,ERCP+内镜下十二指肠乳头括约肌切开术及腹腔镜低位胆总管切开取石均是可选择的手术方式,但应综合考虑其适应证与相对禁忌证[16]。对于术中意外发现的胆总管下段结石嵌顿,可取出剑突下Trocar,腹腔镜直视下将取石钳或胆道刮匙自其切口处伸入胆总管蚕食取石,这可能是一种有效的手术方式[17],但所需时间较长,且有损伤胆道的风险。钬激光是一种新型外科手术激光,目前有学者将其应用于腹腔镜胆总管切开取石或经胆囊管取石术中[15,18-19],效果良好,但费用昂贵,且临床应避免滥用。沈云海等[15]指出,胆总管结石直径>1 cm或发生嵌顿是钬激光碎石的适应证。胆道镜取石困难时,应以患者安全性为前提,切忌盲目暴力操作,可中转开腹或留置T管,待T管窦道形成后二次取石。
3.1.4 胆总管直径≥12 mm Strömberg等[20]的前瞻性研究共纳入155例行腹腔镜经胆囊管胆总管探查术的患者,结果表明,胆总管直径6 mm以上者,结石残留率是胆总管直径6 mm及以下患者的6.9倍。笔者认为,在排除恶性肿瘤所致梗阻的前提下,胆总管直径明显增宽常预示下段结石情况复杂。本研究纳入的116例患者中,胆总管明显增宽57例(49.1%),最宽者达30 mm,术中发现其胆总管下段多枚沙砾样结石伴嵌顿;胆总管明显增宽者3枚及以上结石发生率及结石嵌顿率分别达33.3%与14.0%,高于未明显增宽者的22.0%与6.8%。当术前影像学检查发现胆总管明显增宽时,术者需做好手术困难的准备,并将风险向患者明确告知;而如术前检查未发现胆总管增宽,术中探查见情况有变时,需考虑胆囊结石掉落或胆总管结石移位的可能,可视患者具体情况选择胆总管低位切开等方式,必要时可请手术经验更为丰富的医生协助完成。
3.2 研究局限性 受实际手术量所限,本研究仅纳入116例患者,整体样本量较小,可能致使结果出现偏差,且存在上腹手术史、胆囊颈部结石嵌顿等潜在困难因素的患者较少,均有待于前瞻性或大规模回顾性分析进一步探讨。此外,手术时机与胆囊周围粘连程度关系密切[21],可能也是LC联合LCBDE手术困难的因素,但由于本院收治的患者多为基层医院转诊,无法完成发病72 h内的早期手术,因此本研究未将其纳入观测指标,颇为遗憾,此后关于此方面的研究结果令人期待。
临床医生根据以上4项独立危险因素对胆囊结石合并胆总管结石患者进行手术难度评估,选择最佳手术方案,同时自身不断钻研腹腔镜胆道手术技术,根据术中情况从容应对,方可降低手术风险,有力保障患者安全。
