顽痹清丸治疗湿热痹阻证强直性脊柱炎33例临床研究
2019-03-21李无阴
王 啸,李无阴
(1.湖南中医药大学 研究生院,湖南 长沙 410000;2.洛阳正骨医院/河南省骨科医院,河南 洛阳 471002)
强直性脊柱炎(Ankylosing Spondylitis,AS)是一种慢性自身免疫性疾病,具体病因及发病机制目前仍不明确,主要表现为中轴关节和骶髂关节慢性炎症,也可累及外周大关节和其他组织,随着病情进展,最终因脊柱强直、髋关节畸形而致残,严重影响患者的生活质量。少数研究表明病情处于早期可行腰背部椎旁肌有限剥离术能缓解症状,一定程度延缓病情进展[1]。但临床常见按照纽约或罗马标准确诊的AS病人,多是在出现强直、畸形后方才就诊治疗,大多已错过手术时机。此类病人治疗上多以非甾体抗炎药、抗风湿药物、糖皮质激素、生物制剂为主。柳氮磺吡啶(Sulfasalazine,SSZ)是磺胺类抗菌药物,被广泛用于消化道感染,临床研究显示SSZ对AS患者的腰背痛、外周关节炎、晨僵及骶髂关节炎性病变有着明显的治疗作用[2]。欧洲抗风湿联盟2006年推荐对于以外周病变为主的AS患者,建议应用SSZ配合NASIDs治疗[3]。顽痹清丸是河南省洛阳正骨医院自制复方中成药,具有清热除湿、除痹止痛的功效,在医院长期临床应用中疗效可靠[4]。本研究通过12周的临床对照观察,探究顽痹清丸联合柳氮磺吡啶治疗强直性脊柱炎的疗效及安全性,为临床治疗AS提供新的思路和方法。
1 资料与方法
1.1 一般资料
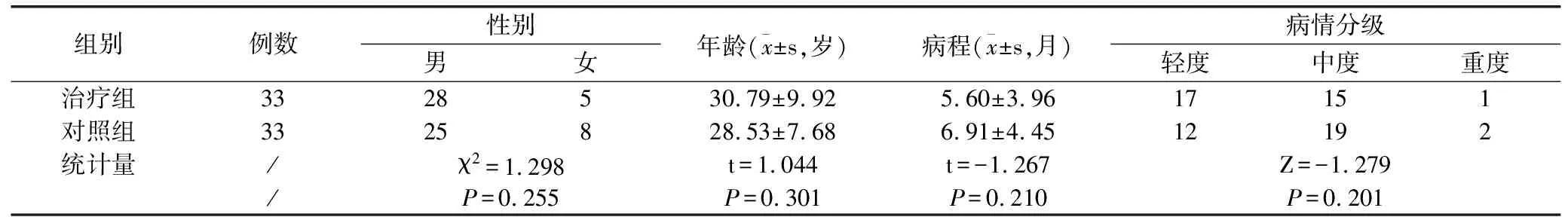
选择2017年7月—2018年1月于河南省洛阳正骨医院风湿科住院的72例AS患者,采用随机数表法将其分为对照组和治疗组,每组36例。治疗过程中两组各脱落3例,最终入组33例。两组患者及家属均签署知情同意书。两组患者的一般资料比较见表1。
[3] 曹瑞,韩月娥.椎间盘源性下腰痛的中西医临床治疗研究进展[J].中国临床研究,2015,28(11):1521-1524.
[4] 商宪敏,杨晋翔.中医内科学[M].北京:中国工人出版社,1998:499.
[5] 国家中医药管理局.中医病证诊断疗效标准[M].南京:南京大学出版社,1994:26-27.
[6] 张梅,刘珍珍,杨佳敏,等.艾灸的研究进展[J].中医药学报,2015,43(1):73-77.
[7] 吕鹏,张承舜,尹海燕,等.艾灸温热刺激的研究现状[J].成都中医药大学学报,2017,39(1):95-98.
[8] 戴海红.艾灸配合穴位按摩治疗慢性腰椎间盘突出症患者康复效果的研究[J].辽宁中医杂志,2015,42(11):2181-2183.
[9] 詹振吉,王健.艾灸对机体免疫系统的影响[J].中医学报,2016,31(3):449-452.
[10] 刘剑,黄昌林,常祺,等.0期诊断技术对军事训练所致椎间盘源性下腰痛患者血清IL-1β,6-keto-PGF1α及TNF-α水平的影响及其意义[J].现代生物医学进展,2017,17(9):1753-1757.
[11] 周纯袆,蔡慧芳,周燕,等.麦粒灸结合腰部推拿治疗老年肾虚型腰痛疗效观察[J].山西中医,2016,32(3):31-32.
(编辑:李 悦)
注:参照1984年修订的AS骶髂关节炎X线分级标准[5],其中0~Ⅱ级为轻度,Ⅲ级为中度,Ⅳ级为重度。
1.2 诊断标准
1.2.1 西医诊断标准 参照1984年纽约修订的强直性脊柱炎诊断标准[5]。
1.2.2 中医诊断标准 按照国家中医药管理局2002年制定的《中药新药临床研究指导原则》中AS诊断及湿热痹阻证辨证标准[6]。
1.3 纳入标准
符合以上诊断标准;以外周关节病变为主者;年龄18~50岁;签署患者知情同意书。
1.4 排除标准
合并严重关节畸形及其他骨与关节病变者;有其他血清阴性脊柱关节病或其他风湿免疫类疾病者;对磺胺类等实验或对照药物过敏者;有妊娠或其他研究药物使用禁忌证者;其他原因不能配合治疗者。
1.5 治疗方案
常规治疗:予以塞来昔布胶囊(辉瑞制药有限公司生产 国药准字J20120063,0.2 g×6粒)口服,每次1粒,每天2次,服用不超过4周,过程中视疼痛情况减量或停用。同时要求两组患者住院期间及出院后适当进行康复功能锻炼,包括伸展腰背、仰卧触膝、转体等,注意分寸,适可而止。
对照组患者予以柳氮磺吡啶肠溶片(上海福达制药有限公司生产,国药准字H31020840,0.25 mg×12片)口服,第1周每次2片,每天2次。第2周每次3片,每天2次。第3周及之后每次4片,每天2次,服用12周。
治疗组患者在对照组的基础上予以顽痹清丸(河南洛阳正骨医院内部制剂,由生地黄、牡丹皮、紫草、乳香、知母、薏苡仁、川牛膝、益母草、忍冬、络石藤、黄芩、土茯苓、桑枝、吴茱萸、甘草等中药制成,河南洛正制药厂生产,豫药制字 Z04030010,3 g×10包)口服,每次1袋,每天2次,服用12周。
1.6 观察指标与疗效判定标准
1.6.1 实验室指标 主要指标包括与AS活动性密切相关的血沉(ESR)、C反应蛋白(CRP)、IL-33等实验室指标,以12周为观察周期。
1.6.2 疼痛指标 采用视觉模拟评分法(visual analogue scale,VAS),以12周为观察周期,评定患者疼痛缓解情况,同时回访记录患者停用非甾体抗炎药时间。
1.6.3 证候积分评价 参照《中药新药临床研究指导原则》中证候积分评分标准制定本次研究疗效评定标准。证候积分选取腰骶疼痛、背部疼痛、脊柱活动度、晨僵、关节发热等五项,每项分轻、中、重三级,具体见表2。

表2 证候积分评定量化及分值
1.6.4 疗效评定标准 ①临床缓解:患者症状完全消失,各项化验指标恢复正常;②显效:患者症状基本消失,中医证候积分减少50%以上;③有效:患者症状有所改善,中医证候积分减少20%以上;④无效:症状无明显改善甚至加重,中医证候积分减少不足20%或增加。总有效=临床缓解+显效+有效。
1.6.5 不良反应 每月随访1次不良事件,出现不良反应事件予以对症支持治疗,无效者予以脱落。
1.7 统计学方法
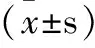
2 结果
2.1 病例脱落情况
治疗过程中因未遵医嘱服药,治疗组脱落3人,对照组脱落1人;因失访,对照组脱落2人。
2.2 两组患者治疗前后实验室指标比较
治疗前,两组患者ESR、CRP、IL-33水平比较差异无统计学意义(P>0.05),具有可比性。经过治疗,两组患者ESR、CRP、IL-33水平均显著降低,且治疗组患者各指标水平显著低于对照组,差异具有统计学意义(P<0.05)。详见表3。
2.3 两组患者治疗前后关节疼痛VAS评分比较
治疗前,两组患者VAS评分比较差异无统计学意义(P>0.05),具有可比性。经过治疗,治疗组患者VAS评分显著低于对照组,停药时间显著短于对照组,差异具有统计学意义(P<0.05)。详见表4。
表3 两组患者治疗前后实验室指标比较

表3 两组患者治疗前后实验室指标比较
组别时间ESR(mm/h)CRP(mg/L)IL-33(pg/mL)治疗组(n=33)治疗前46.22±13.2124.41±8.91217.42±70.03治疗后19.35±10.96∗▲7.97±2.79∗▲153.41±58.09∗▲对照组(n=33)治疗前46.76±15.5423.03±11.19210.79±76.28治疗后24.41±8.91∗11.09±2.87∗174.93±50.59∗
注:与同组治疗前比较:*P<0.05;与对照组治疗后比较:▲P<0.05。
表4 两组患者治疗前后VAS评分变化及停药时间比较
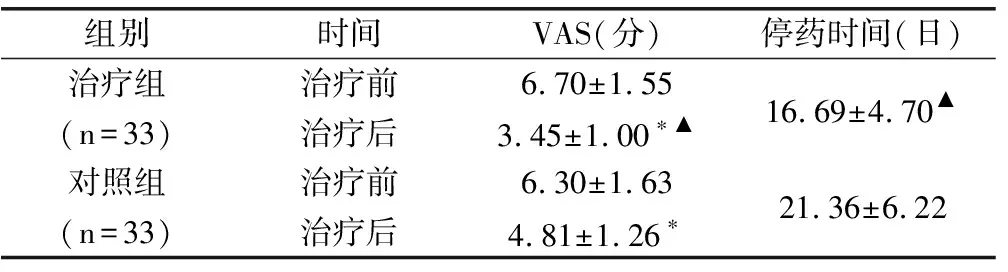
表4 两组患者治疗前后VAS评分变化及停药时间比较
组别 时间VAS(分)停药时间(日)治疗组治疗前6.70±1.5516.69±4.70▲(n=33)治疗后3.45±1.00∗▲对照组治疗前6.30±1.6321.36±6.22(n=33)治疗后4.81±1.26∗
注:与同组治疗前比较:*P<0.05;与对照组比较:▲P<0.05。
2.4 两组患者临床疗效比较
经过治疗,治疗组患者腰骶疼痛、背部疼痛、关节热痛症状积分显著低于对照组,临床总有效率显著高于对照组,差异具有统计学意义(Z=-2.321,P=0.02<0.05)。详见表5、表6。
2.5 两组患者不良反应情况比较
过程中,两组患者出现不良反应共3例,其中治疗组食欲减退1例(33.3%),对照组食欲减退1例,恶心1例,共2例(66.7%),经对症处理后不良反应消失,治疗未中断,两组患者不良反应发生率比较差异无统计学意义(χ2=0.394,P=0.555>0.05)。
表5 两组患者治疗前后中医证候积分比较

表5 两组患者治疗前后中医证候积分比较
组别时间腰骶疼痛背部疼痛晨僵活动度关节热痛总分治疗组(n=33)治疗前2.75±1.032.18±0.731.18±0.390.79±0.422.85±0.8710.39±1.52治疗后0.97±0.59∗▲1.03±0.59∗▲0.82±0.39∗0.30±0.47∗1.12±0.82∗▲4.33±1.56∗▲对照组(n =33)治疗前2.61±0.932.21±0.481.75±0.660.72±0.452.67±1.009.97±1.13治疗后1.39±0.66∗1.58±0.56∗1.09±0.46∗0.36±0.49∗1.36±0.93∗5.79±1.47∗
注:与同组治疗前比较,*P<0.05;与对照组治疗后比较,▲P<0.05。

表6 两组患者临床疗效比较 [n(%)]
3 讨论
AS作为一种自身免疫性疾病,现代医学目前尚未完全阐明其病因及发病机制。相关研究[7]表明ESR、CRP等因子与AS的病变发展过程密切相关,可作为判断病程及预后的指标。IL-33可激活多种炎症因子,与AS的发病密切相关[8]。该病治疗上以缓解症状为主,以最大程度改善生活质量、防止结构损害进展、维持关节功能及日常生活能力为目的[9]。治疗方案选择则以非甾体抗炎药、抗风湿药物、糖皮质激素、TNF拮抗剂、柳氮磺吡啶等为主。非甾体抗炎药是早期及晚期AS的对症治疗首选用药,能够迅速改善患者疼痛、晨僵及活动度,但长期服用容易导致消化道、心血管等不良反应。糖皮质激素对于某些病情较重、控制不佳的患者可以选择,同时应强调尽快减停[9];抗风湿药物多有细胞毒性,不利于患者长期服用[10]。TNF抑制剂是一种新型AS治疗药物,起效快,长期应用可维持部分缓解或低疾病活动状态[11]。但此类生物制剂价格昂贵,静脉给药使用不便且有潜在输液反应风险、感染风险等问题,对于长期使用患者的依从性提出较高要求。SSZ可以改善AS导致的腰背疼痛、外周关节炎、晨僵等症状,但起效较慢,临床需配合速效NASIDs,且无证据SSZ对中轴关节病变有可靠疗效[12],长期服用可能出现包括消化系统、血液系统、生殖系统在内的不良反应[10]。免疫系统及内分泌系统等慢性疾病是中医治疗的优势,近年来利用中医药内外合治AS已取得了较好的效果[13]。因此,寻找中西医联合用药方案,对于缓解患者症状、降低不良反应发生率、提高患者生活质量及用药依从性,进而控制AS进展、减少致残具有重要意义。
中医学中无强直性脊柱炎的概念,结合患者腰、脊、髋疼痛、活动障碍等症状、体征,本病辨病属中医学“痹病”“大偻”范畴。《素问·痹论》云:“风寒湿三气杂至,合而为痹。”清代张子和在《儒门事亲》中云:“痹病以湿热为源”,提出了湿热致痹的理论。在融会多家理论后,现代中医理论认为,患者先天不足,湿热之邪侵入机体;或风寒湿之邪久痹于内,郁而化热;或患者素体阴盛阳虚,湿热内生,痹阻经络,经输不利,营卫失和,气血阻滞,经脉痹阻不通则为病。湿热之邪痹阻关节是湿热痹阻之痹证的病因。顽痹清丸是平乐郭氏正骨经验方,针对湿热痹阻之痹证湿、热、瘀的病机特点,由生地黄、牡丹皮、紫草、乳香、知母、薏苡仁、川牛膝、益母草、忍冬、络石藤、黄芩、土茯苓、桑枝、吴茱萸、甘草等十余味中药组成。方中生地、丹皮、紫草清热凉血、活血化瘀;乳香活血行气止痛;知母滋阴清热;黄芩清热燥湿;牛膝、益母草、忍冬、络石藤活血通经止痛;吴茱萸止痛,同时取其辛温,防诸药寒凉太过;茯苓、薏苡仁增强利湿之功。诸药合用,寒热并用,使清热不伤阴,祛邪不伤正,共奏清热除湿、祛风通络、活血止痛之功效。现代药理学研究表明,上述组方中药具有良好的抗炎、抗菌、抗病毒、调节免疫力等功效[14]。
本研究表明SSZ可以降低AS活动度,缓解症状,提高患者生活质量;而SSZ联合顽痹清丸的疗效优于单纯口服SSZ,且能够缩短NASIDs类药物的使用周期。治疗组各项实验室检查指标均优于对照组,表明顽痹清丸的作用机制可能与其能减轻炎症反应,调节机体免疫及内分泌环境有关。本研究过程中,两组患者不良反应发生率无差异,这可能是由于样本量较少所致,有待进一步研究。在治疗组疗效优于对照组的同时,其NASIDs类药物的停药时间早于对照组。因此,临床可以通过联合用药,减少SSZ和NASIDs的应用剂量和疗程,增加疗效的同时减少不良反应的发生风险。在本研究进行过程中,受到诸多条件限制,本研究存在患者病情差异、治疗起始时间难统一、随访时间控制不完全一致等不足,有待进行更为规范的随机对照实验进一步验证本研究结论。联合用药对于AS预后及转归的影响亦有待进一步临床观察研究。
