炎性成肌纤维细胞瘤并发结核分枝杆菌潜伏感染一例
——文献复习及临床诊疗过程分析
2019-03-18赵彬迟晶宇王传庆侯代伦张运曾王成金锋
赵彬 迟晶宇 王传庆 侯代伦 张运曾 王成 金锋
作者单位:250013 济南,山东大学附属山东省胸科医院胸外科(赵彬、张运曾、王成、金锋),结核内科(迟晶宇),骨科(王传庆);首都医科大学附属北京胸科医院影像科(侯代伦)
炎性成肌纤维细胞瘤(inflammatory myofibroblastic tumor,IMT)是一种少见的间叶性中间性肿瘤,由异型性的成肌纤维细胞引起,常伴有淋巴细胞、浆细胞等炎症细胞浸润[1-2],诊断较为困难,当并发结核分枝杆菌潜伏感染时易误诊为活动性结核病,抗结核药物治疗效果欠佳时要及时考虑到肿瘤的可能,积极完善病理学检查明确诊断。笔者对山东大学附属山东省胸科医院收治的1例恶性IMT并发结核分枝杆菌潜伏感染患者的临床资料及诊治经过进行回顾性分析,并复习国内外相关文献,归纳IMT的临床特点,总结临床经验。
临床资料
患者,男,34岁,公务员。因“间断腰腿疼痛7个月,加重10 d”于2017年7月11日入住我院。患者既往身体健康,否认“高血压病、糖尿病、心脏病、肾病”等慢性病病史及“病毒性肝炎、结核病”等传染病病史,否认外伤、手术、输血史,否认药物、食物过敏史,否认疫区接触史,否认家族性遗传病病史,既往有少量烟酒史。
患者于2017年1月无明显诱因出现间断性腰部疼痛,夜间明显,偶有盗汗,于2017年3月在山东省东营市人民医院行腰部X线摄影检查,显示“腰椎病变”。2017年4月12日在山东省东营市胜利油田中心医院行同位素全身骨扫描,显示“左第6肋、腰4椎体代谢异常,胸3椎体代谢异常”。2017年4月19日就诊于解放军总医院,行正电子发射计算机体层摄影(positron emission computed tomography,PET)-CT检查,显示“腰4椎体骨质破坏伴左侧腰大肌内高代谢病变,骶骨右半部代谢异常,双侧锁骨区、纵隔、双肺门、腹膜后及左髂血管旁多发高代谢淋巴结”,考虑“炎性病变(结核?),左肺下叶炎症”;行椎旁病变穿刺活检,显示“腰大肌纤维及骨骼肌组织中见大量嗜酸性粒细胞及组织细胞聚集伴嗜酸性脓肿形成”,考虑“炎性病变”。后于2017年5月15日在北京积水潭医院穿刺病理会诊考虑“不除外郎罕细胞增多症、上皮样血管瘤、炎症性病变”,查布鲁杆菌病抗体阴性,给予抗感染治疗(哌拉西林/他唑巴坦4.5 g/次,2次/d;亚胺培南1 g/次,1次/12 h;均为静脉滴注)7 d无效,患者仍存在腰痛,不规律口服止痛药(布洛芬)尚可耐受。
2017年6月患者无明显诱因出现腰痛加重,伴左侧大腿牵拉痛及午后乏力,就诊于山东大学齐鲁医院,腰髓MRI显示:腰4椎体呈长T1长T2信号,腰3~5椎体左侧腰大肌旁见略短T1略长T2信号软组织肿物,椎旁病变与左侧腰大肌分界不清,最大截面积约3.8 cm×4.6 cm,上下长度约9.8 cm,骶1~3椎体左侧部亦受累,局部见骨质破坏及软组织肿物,体积约4.1 cm×5 cm×4.4 cm;增强扫描上述病变呈现明显不均匀强化;MRI诊断为“腰骶椎多发破坏并软组织占位”;再次行腰椎病变穿刺活检,病理显示:(腰椎)出血,坏死骨组织及纤维组织增生伴炎症及钙化;免疫组织化学(简称“免疫组化”)检查:周围神经雪旺细胞特异性标记蛋白(S100)、CD1a蛋白、细胞角蛋白(CK)均为阴性,考虑结核可能;查γ干扰素释放试验阳性,血红细胞沉降率63 mm/1 h(正常范围:0~15 mm/1 h)。临床诊断结核不除外。给予H-R-Z-E(H:异烟肼,0.3 g/次,1次/d;R:利福平,0.45 g/次,每晚一次;E:乙胺丁醇0.75 g/次,1次/d;Z:吡嗪酰胺0.75 g/次,2次/d;均为口服)抗结核治疗1周后,腰痛、乏力症状稍好转,后继续口服上述药物进行抗结核治疗。2017年6月底,患者卧软床后腰痛症状加重,休息3 d后稍减轻,2017年7月1日患者开车久坐后腰痛症状再次加重,休息后不能缓解。
2017年7月11日,患者来我院就诊,诉6个月体质量下降约7.5 kg。体格检查:体温36.5 ℃、脉搏84次/min、呼吸频率21次/min、血压114/64 mm Hg(1 mm Hg=0.133 kPa)、体质量73 kg。患者一般状况可,自主体位,查体合作,浅表淋巴结未触及明显肿大,呼吸系统未见阳性体征;腹部饱满,触软,无压痛、反跳痛,未触及明显肿物,肠鸣音正常,移动性浊音阴性;脊柱生理曲度正常,屈腰活动及腰部侧弯活动、腰椎旋转活动均因疼痛受限,左腿抬高轻度疼痛,其余肢体活动自如,肌力正常,关节无红肿,双下肢无水肿。胸部+腰椎CT扫描显示“左肺下叶后基底段见斑点、斑片状密度增高影,边缘模糊,密度不均(图1);其余肺野清晰,段以上支气管开口通畅;纵隔2R、3A、4R、5、6、7区见多发肿大淋巴结(图2,3)。腰椎生理曲度尚可,腰4椎体见虫噬样骨质破坏,边缘硬化,病灶周围软组织肿胀,左侧更为显著,左侧腰大肌内见液性密度影(图4~7);其余椎体未见明显异常骨质破坏区”。影像学诊断意见:(1)考虑左肺继发性肺结核;(2)纵隔多发肿大淋巴结,纵隔淋巴结结核?(3)符合腰椎结核(腰4椎体)并左侧腰大肌脓肿形成。
颈部B超显示“右侧颈部探及多个实性低回声结节,较大者位于胸锁乳突肌下段后缘,面积约0.8 cm×0.5 cm,边界清晰,门结构欠清晰;左侧颈部未探及异常肿大淋巴结”。C反应蛋白67.6 mg/L(正常范围:0~8 mg/L)。血常规:白细胞10.02×109/L [正常范围:(3.50~9.50)×109/L],中性粒细胞8.02×109/L [正常范围:(2.00~7.00)×109/L],中性粒细胞百分比0.8(正常范围:0.5~0.7),血红细胞沉降率34 mm/1 h(正常范围:0~15 mm/1 h)。肝肾功能、电解质、血糖、血脂、大小便、凝血功能、免疫功能、血管紧张素转换酶、肿瘤标志物均正常,HIV、乙型肝炎、丙型肝炎、梅毒抗体均为阴性。患者入院诊断:腰椎结核并椎旁脓肿、继发性肺结核、多发淋巴结肿大;诊断依据:患者腰部疼痛伴乏力,有慢性消耗性疾病表现。 影像学诊断:肺结核、腰椎结核并椎旁脓肿表现,PPD皮肤试验中度阳性(10 mm×11 mm),γ干扰素释放试验阳性。但患者腰椎及腰大肌病变不能完全除外肿瘤或其他细菌感染的可能,给予抗结核和抗感染治疗3周,具体用药方案:异烟肼0.3 g/次,1次/d,口服;利福平0.6 g/次,1次/d,静脉滴注;乙胺丁醇0.75 g/次,1次/d,口服;吡嗪酰胺0.75 g/次,2次/d,口服;左氧氟沙星0.6 g/次,1次/d,静脉滴注;阿米卡星0.4 g/次,1次/d,静脉滴注。患者腰腿疼痛及腹痛好转后出院。出院后继续口服抗结核药物治疗(异烟肼0.3 g/次,1次/d;利福平0.45 g/次,每晚一次;乙胺丁醇0.75 g/次,1次/d;吡嗪酰胺0.75 g/次,2次/d;左氧氟沙星0.5 g/次,1次/d)。
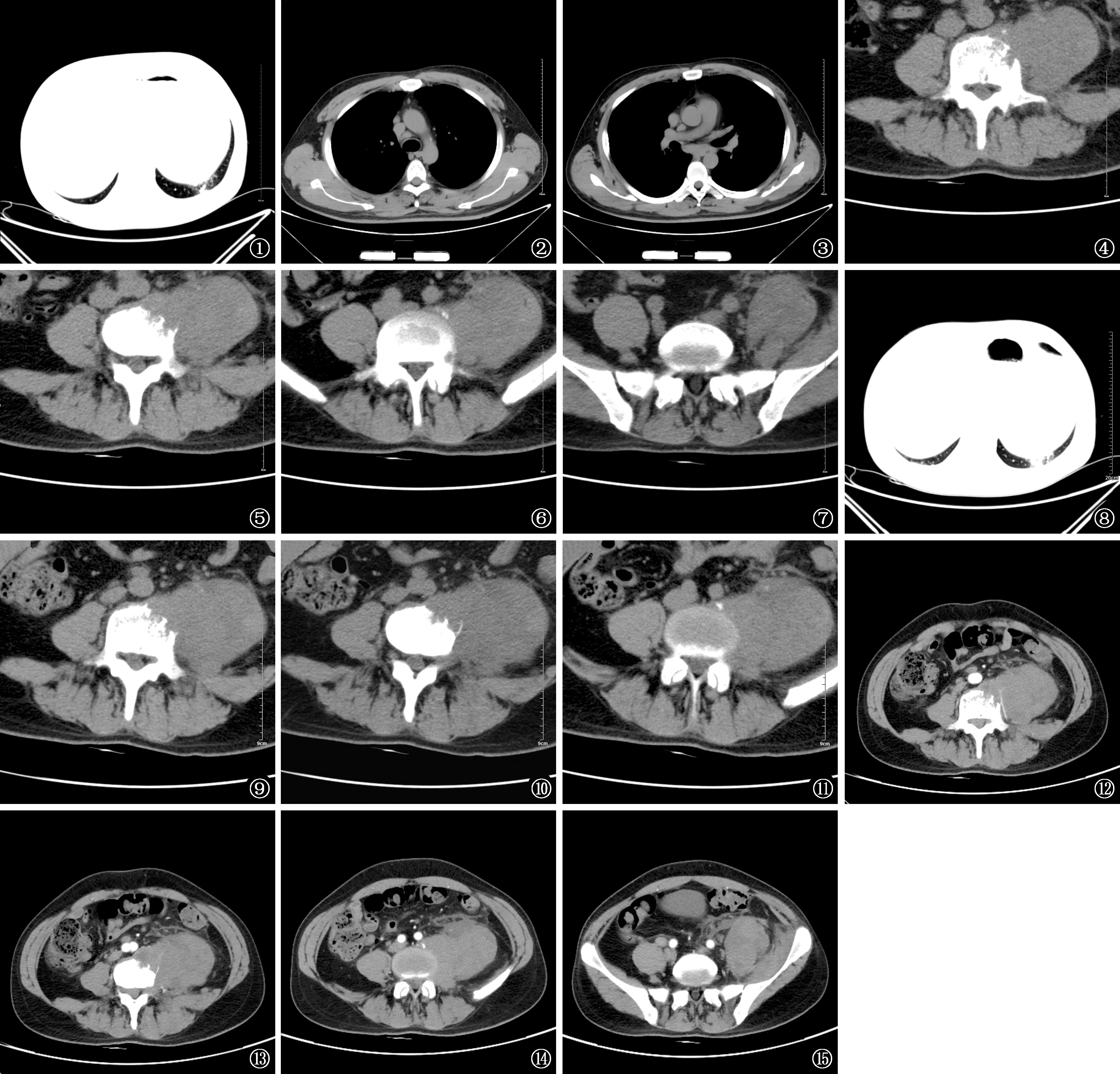
图1 2017年7月11日,患者胸部CT肺窗显示左肺下叶后基底段见斑点、斑片状密度增高影,边缘模糊,密度不均 图2,3 2017年7月11日,患者胸部CT纵隔窗显示纵隔内多发肿大淋巴结 图4~7 2017年7月11日,腰椎CT扫描显示腰4椎体见虫噬样骨质破坏,边缘硬化,病灶周围软组织肿胀,以左侧为著 图8 2017年8月23日,患者胸部CT扫描显示肺部病灶较2017年7月11日病灶增大 图9~11 2017年8月 23日,患者胸部CT扫描显示左侧腰大肌病灶较2017年7月11日病灶增大 图12~15 2017年9月28日,患者腰部CT扫描显示左侧腰大肌病灶进一步增大,存在不规则液化区
因患者口服抗结核药物治疗后腰腿疼痛再次加重,于2017年8月22日再次入我院,复查胸部+腰椎CT扫描显示右肺上叶后段、下叶基底段,左肺下叶后基底段见少量斑片状、索条状、小结节状高密度影,与邻近胸膜粘连;纵隔3A、4R、4L、7区见肿大淋巴结,密度较均匀;段以上支气管开口通畅;腰4椎体偏左前溶骨性骨质破坏,骨皮质不连续,边缘轻度硬化,周围软组织肿胀,左侧腰大肌明显肿胀,内见低密度区,并向下延伸至左侧髂腰肌;扫描野内显示腹膜后见多发大小不等的淋巴结。影像学诊断:(1)双肺感染性病变;(2)符合腰4椎体结核并左侧腰大肌、髂腰肌脓肿形成;(3)纵隔及腹膜后淋巴结肿大。CT显示肺部、腰部病灶较前有所进展(图8~11);颈部B超示右侧颈部锁骨上窝探及多个实性低回声结节,较大者面积约1.3 cm×0.7 cm,边界清晰,门结构消失;左侧颈部锁骨上窝探及多个实性低回声结节,较大者面积约1.2 cm×0.7 cm,边界清晰,门结构消失;左侧颈部出现肿大淋巴结,右侧肿大淋巴结较前增大。C反应蛋白124 mg/L。血常规:白细胞12.71×109/L,中性粒细胞10.48×109/L,中性粒细胞百分比0.824,血红细胞沉降率54 mm/1 h。血肿瘤标志物示神经元特异性烯醇化酶(NSE)26.61 μg/L(正常范围:0~25 μg/L),其余肿瘤标志物正常。血抗中性粒细胞胞浆抗体(ANCA)阴性;结核抗体阴性;血结核感染T细胞斑点试验(T-SPOT.TB):早期分泌抗原靶蛋白6(ESAT-6)33个斑点形成细胞数(SFCs)(正常范围0~6个)、培养滤液蛋白10(CFP-10)29个SFCs(正常范围0~6个)。加用莫西沙星(0.4 g/次,1次/d,静脉滴注)和糖皮质激素(地塞米松5 mg/次,1次/d,静脉推注;强的松30 mg/次,1次/d,口服)治疗,患者腰腿疼痛症状继续加重,2017年9月28日复查腰椎CT,显示腰大肌病灶进一步增大,有液化坏死灶,但液化不充分(图12~15)。
第一次病例讨论
2017年9月28日,山东大学附属山东省胸科医院对该例患者进行会诊,分析如下。
迟晶宇医师(山东大学附属山东省胸科医院结核内科主任医师):该例患者应考虑以下几种疾病:(1)结核。肺内病灶、腰椎病变从影像学角度看符合结核,且T-SPOT.TB及结核抗体均为阳性,这些表现诊断结核似乎比较合理;虽然在经过强力抗结核药物治疗后(一线、二线抗结核治疗方案)均无效,病灶增大、增多,这点也可以用类赫氏反应解释;但是,该例患者经多家医院多次穿刺病理检查均无典型结核改变,仅此一条,单纯诊断结核存在疑问。(2)除结核外的其他特殊细菌感染。感染是白细胞增高的最常见原因,该例患者外周血白细胞高且逐渐升高,中性粒细胞升高,多次病理检查结果均提示炎性改变,这些都非常符合感染的特点,患者无发热、抗感染治疗无效等均不支持一般细菌感染;特殊细菌感染中布鲁杆菌感染可出现以上影像学表现,但该例患者检查布鲁杆菌抗体阴性、外周血白细胞增高等都不支持。(3)少见的低度恶性肿瘤。非造血系统恶性肿瘤有时可出现持续性白细胞增高,以中性粒细胞增多为主,在这种情况下,患者可无急性炎症的症状且抗感染治疗无效,该例患者非常符合,之所以病理未查到癌细胞,可能是因为肿瘤为低度恶性,另外有些肿瘤虽为良性肿瘤但有恶性肿瘤生物学特征:如良性转移性平滑肌瘤病,但这种肿瘤病理无炎细胞浸润。
本例患者有以下几点需要进一步探讨:(1)结核抗体阳性、T-SPOT.TB检测阳性。我们认为应该为结核分枝杆菌潜伏感染;该例患者存在结核感染,而在不同时间段的穿刺病理表现均有炎症背景,该病是否与结核刺激诱发有关?(2)该例患者2次活检有2次病理检查描述可见嗜酸性粒细胞浸润,结合病史和查体未见过敏性因素,诊断是否考虑并发嗜酸性肉芽肿?北京积水潭医院病理考虑不除外郎罕细胞增多症;而嗜酸性肉芽肿属于郎罕细胞增多症的一种类型。(3)从临床分析推断,该例患者高度提示为低度恶性肿瘤或有恶性肿瘤生物学行为的良性肿瘤,那么原发病灶在哪儿?患者曾行PET-CT从锁骨区到左髂血管旁的淋巴结也是高代谢的淋巴结,我们认为淋巴结和其他部位应视为同一性质病变。(4)患者下一步还是要探讨如何明确诊断,建议再次行多点穿刺病理检查。
王传庆(山东大学附属山东省胸科医院骨科主任医师):从临床角度分析,诊断主要有3种可能:(1)腰椎及左侧腰大肌化脓菌感染。腰椎通常不容易出现化脓性细菌感染。在相对应部位的皮肤存在化脓感染灶,局部有穿刺、手术、小针刀或针灸等外来因素破坏了皮肤屏障,腹腔盆腔感染的蔓延,或腰椎出现外伤(如扭伤)时,才会出现椎体和(或)腰大肌的化脓性感染;通常有高热、剧痛等,病史相对较短,敏感抗生素治疗效果明显。该例患者尽管血白细胞升高达10.03×109/L,中性粒细胞达8.02×109/L,中性粒细胞百分比0.8,但不太符合单纯化脓性感染的诊断;白细胞升高可能是肿块导致的周围炎症,导致白细胞的反应性增高。(2)腰椎结核伴腰大肌冷脓肿。腰椎是脊柱结核最常见的发生部位,除表现为结核中毒症状外,腰痛也是最重要的主诉之一。影像学上主要表现为椎间隙变窄、骨质破坏、脓肿形成、脊柱畸形、脊髓受压等特点。腰椎结核最常见的类型是边缘型,常累及一个运动单元(上位椎体下缘+椎间盘+下位椎体上缘),脓肿最常形成于椎旁,将椎旁韧带抬起,在脓肿继续增大后形成腰大肌脓肿,向下流注。该例患者的影像学检查所见特征与此不符。但PPD皮肤试验硬结平均直径达10 mm×11 mm,结核抗体阳性,T-SPOT.TB检测ESAT-6为33个SFCs,CFP-10为29个SFCs,γ干扰素释放试验阳性,血红细胞沉降率58 mm/1 h,C反应蛋白107.3 mg/L,符合国家卫生健康委员会2017年颁布的《WS 196—2017 结核病分类》中结核分枝杆菌潜伏感染的诊断条件。既往的抗结核药物治疗曾经有效,多次穿刺都未能明确诊断的情况下,为保证治疗的连续性,不建议停用抗结核药物,但应积极寻求能够明确诊断的方法。(3)腰椎或腰大肌肿瘤性疾病。该例患者无其他脏器的肿瘤病史,因而椎体转移瘤基本可以排除。从影像学角度看,该例患者骨质破坏仅在腰4椎体左前方,椎旁韧带无任何抬起,未见明显死骨,病史8个月之久亦未见任何修复,无椎体结核“边破坏边修复”的特性;椎旁肿块与腰大肌相连,内有少许液化,大部分以实性为主,包膜较为完整,但呈膨胀性生长,与结核性冷脓肿形态相差甚远。因此,肿瘤的可能性不能排除。
在椎体的常见原发恶性肿瘤中,如骨肉瘤等,很少可以形成如此巨大的肿块,也较少见到骨质破坏仅局限在椎体的左前1/4范围,往往会累及全椎体或椎体附件。结合肿块巨大而腰椎破坏仅限于腰4椎体左侧的特性,来自肌肉组织肿瘤的可能性更大,且可能为低度恶性肿瘤(包括肉瘤)或交界性肿瘤(如良性疾病恶性行为)。或者也不排除在感染的基础上,疾病性质发生了改变。这类肿瘤诊断较为困难,穿刺常不能获得满意的标本,或难以穿刺到靶目标,即使手术标本充足,诊断有时也较为困难。综上,建议在维持现有抗结核药物治疗及其他治疗的前提下,积极采取手术或其他方法,获取较大块病灶组织,行病理学、细菌学、免疫学等相关检查,明确诊断,采取更为有针对性的治疗措施。
金锋(山东大学附属山东省胸科医院胸外科主任医师):患者自发病以来,历经地市级三级甲等综合医院、国家级综合医院、国家级专科医院、省级三级甲等综合医院、省级三级甲等专科医院等就诊,3次穿刺活检均未查到恶性肿瘤细胞,未能明确诊断。患者抗结核、抗炎治疗效果欠佳,患者病变需进一步鉴别于恶性肿瘤、耐药结核感染、特殊炎症,同意两位主任的意见,尽快在CT引导下行多点穿刺。
后续诊治过程
2017年9月29日,患者重新行腰部病灶穿刺活检。山东省胸科医院病理报告:炎性纤维组织及横纹肌见较多慢性炎细胞及嗜酸性粒细胞浸润,并可见灶性可疑肉芽肿性炎(图16~20)。免疫组化:巨噬细胞标记物CD68、LAC阳性,Ki-67个别细胞阳性。山东省病理质量控制中心会诊报告:增生纤维肉芽组织及变性萎缩骨骼肌组织,其中见较多嗜酸性粒细胞和淋巴单核细胞浸润,部分纤维组织胶原化。结合临床及免疫组化标记CD68阳性、S100和CD1a少量阳性,考虑骨嗜酸性肉芽肿可能性大。

图16~20 2017年9月29日,穿刺活检病理(HE ×100)显示炎性改变的纤维组织及横纹肌见较多淋巴单核细胞及嗜酸性粒细胞浸润,并可见灶性可疑肉芽肿性炎 图21,22 2017年11月3日,首都医科大学附属北京胸科医院病理会诊:纤维结缔组织增生,并见不典型肉芽肿样病变及坏死,散在少量异型细胞,嗜酸性粒细胞浸润
患者继续行抗结核、抗炎及糖皮质激素治疗,腰腿疼痛症状继续加重,应用止痛药物无效,患者不能忍受,再次于2017年10月初就诊于山东大学齐鲁医院。胸腹部及盆腔CT:左肺下野结节,左肺炎症,右侧胸膜增厚,左侧腹膜后及盆腔骶前多发占位性病变,并相邻腰骶椎骨破坏。考虑恶性神经源性肿瘤可能性大,增殖性肉芽肿性结核不除外,腹膜后多发淋巴结肿大。腰椎MRI:胸12~骶1椎体多发占位,考虑转移瘤不除外。为缓解腰痛和获取足够标本明确诊断,患者于2017年10月10日在山东大学齐鲁医院行手术治疗。术中见腰3椎体水平以下腰大肌膨大增生,质地硬,周围粘连水肿,快速病理检查显示“炎性病变”。手术方式为:腰4椎体、腰大肌和骶骨病变切除、植骨术(术后病理结果见手术后病理检查及会诊结果)。
2017年10月29日,患者再次就诊于我院,症状未见减轻。患者多次行穿刺活检及手术病理检查均未能明确诊断,也未能完全排除结核,建议患者到北京继续进行诊治。
患者于2017年11月初停止服用所有抗结核药物。2017年11月29日无明显诱因出现皮肤、巩膜明显黄染,皮肤瘙痒,少尿、尿色加深,伴恶心、呕吐胃内容物,伴憋喘。2017年12月4日就诊于北京协和医院。行胸腹盆腔CT检查:胰头部占位(5.3 cm×3.9 cm),胰管扩张,肝内外胆管扩张,胰腺周围、腹膜后、肠系膜根部、肝门区、肝肾间隙、盆腔双侧髂血管旁及左侧腹股沟多发肿大淋巴结;脾大,肝右叶可疑低密度灶,胆囊增大、胆汁淤积;双肾上腺增粗;左侧腰大肌、竖脊肌肿胀并软组织密度块影。腰4椎体、骶椎及左侧髂骨骨质破坏,腰4椎体病理性骨折。腹部超声:胰头区低回声(5.9 cm×3.9 cm);主胰管扩张(0.6 cm);肝内外胆管扩张(胆总管宽1.1 cm,左、右肝管均宽约0.7 cm,肝内三级胆管可见);胆囊内胆汁淤积;脾大;腹腔积液(深约4.6 cm);肝内中高回声,血管瘤?急诊行经内镜逆行性胰胆管造影术:胆总管下段线样狭窄,长度约3.5 cm,近端胆管扩张,直径约1.2 cm,行乳头预切开+胆总管塑料支架置入术,引流胆汁通畅。病理科考虑诊断为IMT;胸部影像学考虑双肺存在细菌感染可能性,可疑晕征需警惕真菌感染,结核可能性小;骨科考虑恶性肿瘤可能性大,无法再次行活检病理或病原学及手术治疗;结合其临床表现考虑其恶性程度较高,出现椎体骨质破坏,腹腔、盆腔多发淋巴结转移,胰腺转移,同时不除外肝转移所致肝功能衰竭,肺转移所致肺不张、感染。
虽经各种积极治疗,疗效不佳。因病情危重,患者于2017年12月15日自动出院。2018年1月因病死亡。
术后病理检查及会诊结果
山东大学齐鲁医院病理结果(病理号42712.17):腰椎、骶骨及盆腔组织多灶性坏死伴炎细胞浸润,成肌纤维细胞增生及局部瘢痕形成,考虑为炎症所致,请临床实验室检查,排除结核和其他感染,但组织形态不是典型结核改变,建议治疗观察。免疫组化:CD68阳性,CK、上皮膜抗原(EMA)、结蛋白(Desmin)、平滑肌肌动蛋白(SMA)、CD34、间变性淋巴瘤激酶(ALK)、CD1a、langerin、CD21、CD35均为阴性,抗酸染色阴性,Ki-67阳性率约10%。
首都医科大学附属北京胸科医院病理科会诊:第一次会诊(2017年11月8日):(腰椎、骶骨及盆腔病变)纤维组织增生,灶状坏死,部分区域呈梭形细胞肿瘤样改变,不除外低度恶性肿瘤;免疫组化检查:AAT和CD68灶性阳性,S100少量细胞阳性,CD34血管阳性,CD1a少量细胞阳性,CD30少量细胞可疑阳性,SMA、Desmin、Langerin、ALK、Sox-10、CK、CD15、肌动蛋白(Actin)、EMA均为阴性,PAS染色阴性。第二次会诊(2017年11月8日):(腰椎、骶骨及盆腔病变)纤维结缔组织增生,并见不典型肉芽肿样病变及坏死,散在少许异型细胞,嗜酸性粒细胞浸润;免疫组化:CD68阳性,S100部分细胞阳性,Langerin、CD117、Desmin、SMA、ALK、Dog-1、CD35、CD1a、CD21均为阴性,Ki-67约10%,抗酸染色、PAS染色均为阴性,结核分枝杆菌脱氧核糖核酸(MTB-DNA)阴性。病理未找到诊断结核病原学依据,不除外肿瘤性病变(图21~22)。
解放军总医院病理科会诊:梭性细胞恶性肿瘤,考虑成肌纤维细胞或纤维组织细胞来源。
北京协和医院病理会诊(病理号42712.17;特殊染色 ×1;免疫组化染色 ×17)诊断为:“低度恶性IMT伴坏死”。
第二次病例讨论
侯代伦(原山东省胸科医院影像科,现首都医科大学附属北京胸科医院影像科主任医师):该例患者系青年男性,因“间断腰腿疼痛”入院。2017年4月19日曾行PET-CT发现“腰4椎体骨质破坏伴左侧腰大肌内高代谢病变,骶骨右半部代谢异常”,行椎旁病变穿刺活检示“腰大肌纤维及骨骼肌组织中见大量嗜酸性粒细胞及组织细胞聚集伴嗜酸性脓肿形成”,考虑炎性病变。随后2017年5月15日行第2次腰椎穿刺活检显示“脓性病变”,查布鲁杆菌病抗体阴性,给予抗感染治疗,效果不佳。
2017年6月,患者再次行腰椎穿刺考虑结核可能,但是此时进行了MR检查显示腰4椎体呈长T1长T2信号,腰3~5椎体左侧腰大肌旁见略短T1略长T2信号软组织肿物,椎旁病变与左侧腰大肌分界不清,骶1~3椎体左侧部亦受累,局部见骨质破坏及软组织肿物,增强扫描上述病变呈现明显不均匀强化。MRI提示该病变不是典型的“腰椎结核并椎旁脓肿”。2017年7月11日胸部CT检查显示左肺下叶基底段可见结节、片状影,可以考虑为继发性肺结核,但这个部位单独出现病变不首先考虑结核,病灶位于肺外周胸膜下恰好是IMT的CT特征。此时临床积极排查结核,行PPD皮肤试验,硬结平均直径为10 mm×11 mm(中度阳性),γ干扰素释放试验阳性,开始进行抗结核及抗感染治疗。2017年8月23日复查胸部CT显示胸部病变及腰椎病变均有进展,2017年9月28日复查腰椎CT显示腰大肌病灶进一步增大,抗结核抗感染没有控制住病情发展,CT增强扫描图像显示腰椎旁病灶可见不均匀强化,其内有少许液化坏死灶,但液化不充分,腰大肌肿胀明显,也没有出现脓肿;结核的CT增强扫描表现一般呈薄环形强化,CT征象也不是典型的结核影像。IMT的CT增强扫描一般呈均匀或不均匀,中度至显著强化。据此,病灶的逐渐增大不得不考虑肿瘤性病变的可能,于是行第4次穿刺活检,病理为炎性改变的纤维组织及横纹肌见较多慢性炎细胞及嗜酸性粒细胞浸润,并可见灶性可疑肉芽肿性炎。最后只能采取外科手术,最终通过病理及免疫组化检查考虑为低度恶性IMT伴坏死。
上述影像学分析是基于明确了患者诊断和预后以后,回顾性提示IMT可能的影像学特点。总体来说,影像学在IMT的诊断中作用有限,确诊还需依赖病理检查。
孙青(山东省千佛山医院病理科教授):会诊的病理为2017年9月29日穿刺标本,量较少但足以用于病理诊断。根据镜下病理改变,我们倾向于骨嗜酸性肉芽肿诊断。骨嗜酸性肉芽肿是指局限于骨的组织细胞增殖症,属于郎罕细胞增多症的一种类型,通常以骨骼病变为主,病因不明;基本的病变为肉芽肿,色棕黄或灰黄,如有出血,则为暗红色,有韧性而不像坏死组织那样脆弱,边界清晰,穿破骨皮质后可侵入软组织,镜下见有大量良性的组织细胞和成熟的嗜酸性粒细胞,其间夹杂有不同程度的纤维肉芽组织增生及出血、坏死灶。骨盆、颌骨、肋骨及肩胛骨以溶骨性破坏为主,周围软组织肿胀,增强扫描破坏的椎体和周围肿胀的软组织均明显强化,通常需与骨尤文肉瘤、骨纤维结构不良、结核及慢性骨髓炎鉴别。而IMT通常发生于软组织,表现为肥大的成肌纤维细胞呈肿瘤样增生,不发生胶原化;可见嗜酸性粒细胞浸润但量极少,一般不破坏骨组织。免疫组化染色显示SMA、Desmin阳性,而S100、CD68、CD1a阴性,均不符合此例患者病理表现。
影像学中肺部病变及淋巴结肿大并不符合肿瘤转移的表现,用结核也可以解释,或者是同一疾病多发病灶。因为炎性成肌纤维细胞性肿瘤几乎不转移,而核分裂像在炎症反应性增生常见,并不是恶性病变所特有,此例无病理性核分裂,Ki-67表达未增高,都表明不是恶性转移性特征。此外,免疫组化检查ALK表达不是肺癌里的融合基因,是间变大细胞淋巴瘤的一种表型,两者不可同日而语。
限于细针穿刺标本的局限性,也不能完全排除2种疾病甚至多种疾病共存的可能性;此病理会诊报告也仅为对2017年9月29日穿刺的标本做出的结论。
金锋(山东大学附属山东省胸科医院胸外科主任医师):恶性肿瘤的预后,与肿瘤类型、患者就医时是否转移、分期早晚有关,也与患者的身体素质诸如免疫状态等有关,还与是否并发其他疾病有关。本例患者就诊时就有肺部、淋巴结、椎体、腰大肌等广泛病变,但影像报告提示“结核”诊断,加之PPD皮肤试验阳性、T-SPOT.TB阳性、结核抗体阳性,临床对于结核的诊断顺理成章。但在患者抗结核药物治疗后病灶出现进展,临床医生还是及时考虑到了肿瘤或者并发肿瘤的可能,并反复行病灶穿刺病理检查,可惜多次活检均未查到恶性肿瘤细胞,这也与疾病本身特殊的病理改变有关。根据相应病理改变,试采用糖皮质激素治疗,由于考虑结核感染播散因素又限制激素剂量的应用。最后通过手术切除病灶,手术中快速病理检查结果仍然为“炎症可能”。经多家医院会诊结合临床表现才最终诊断为IMT。一方面说明这种争论半个多世纪的疾病争论的理由十分充分,另一方面也说明还有继续争论下去的必要。
IMT的病因不明,但考虑与炎症和免疫有关。本例患者结核分枝杆菌潜伏感染明确,影像学与结核有很多相似之处,疾病是否在结核感染的基础上恶变?病理没有结核的证据是否完全排除曾经的结核病变?笔者就曾经有多例手术前确诊结核,经过抗结核药物治疗后因遗留并发症而手术的患者,术后病理并没有结核感染的痕迹,分子病理学检查对此可能会有帮助。本例患者经过4次病灶穿刺病理均未给出确切诊断,即使最后手术后组织样本量足够多,病理也未能及时做出确切诊断。本例患者临床有明确的结核感染证据,对于肺部、椎体和腰大肌病变,影像学又没有一锤定音的鉴别要点,进一步增加了诊断的难度。 当然,本例患者最后IMT诊断是否与结核感染有关,两者之间的关系也值得思考。病理难以做出确切诊断是该例患者诊断困难的最大原因。对于病理诊断困难的患者,及时求助有诊治经验的上级医院也是一种重要策略。
讨 论
Brunn于1939年首次报道了2例肺梭形细胞良性肿瘤,Umiker和Iverson于1954年提出肺内这种梭形细胞增生是炎症后肿瘤的观点,以后过渡为“炎性假瘤”,并成为疾病分类学的一个病种[2]。20世纪80年代后陆续发现炎性假瘤与某些真正肿瘤关系密切,以往的许多命名如浆细胞肉芽肿、纤维黄色肉芽肿、成肌纤维细胞瘤、黏液样错构瘤、假肉瘤、炎症性纤维肉瘤等都曾用来描述本病[1-5]。从最初的个案报道到近年来大宗病例的系列研究,提供了机会探讨临床表现和病理形态,认识到该病可出现浸润、复发、恶变和转移,通过免疫组化、细胞遗传学和分子生物学协同研究,支持它是一种真性肿瘤。2002年,WHO软组织肿瘤国际组织学分类专家组正式命名为“炎性成肌纤维细胞瘤”(inflammatory myofibroblastic tumor,IMT),定义为“由分化的成肌纤维细胞性梭形细胞组成的,常伴有大量浆细胞和(或)淋巴细胞的一种肿瘤”,将60多年来有关炎性假瘤的学术讨论基本划上了一个句号。
IMT是一种间叶组织来源的肿瘤,呈中间性或低度恶性,有局部侵袭,偶有远处转移。由于临床及影像学表现侵袭性占位性病变,组织形态变化多样,加之认识模糊,极易误诊。本例患者即为腰大肌IMT侵及腰椎,并有肺转移、多发淋巴结转移。IMT的肿瘤细胞是成肌纤维细胞,显微镜下表现为肥胖的嗜伊红染色梭形细胞。病理表现有3种类型[3]:(1)黏液型(血管型);(2)梭形细胞型;(3)纤维型。体积较大的肿瘤内部还可见点状或大片状钙化,还可见坏死灶,恶性IMT还可见局部浸润。IMT瘤细胞的胞质SMA、MSA和desmin呈不同程度阳性,部分患者局灶性CK呈阳性[6-8]。组织细胞样细胞CD68局灶阳性,与ALK基因突变一致,Tsuzuki等[9]报道50%~60%的患者肿瘤细胞显示ALK阳性。
IMT的病因尚不明确,危险因素有手术、创伤、炎症及病毒(EB病毒、人类疱疹病毒8型)或特殊细菌感染,也有文献报道发生于肿瘤治疗后[10-12]。IMT可发生于任何年龄,好发于儿童及青年,男女发病率无明显差异,可发生于体内各部位,多见于肺内,其次为肠系膜、网膜、肝脏、女性生殖系统、泌尿系统、纵隔、头颈部,其他部位软组织及骨骼偶有报道[6-18]。IMT可在一个部位出现多个病灶,也可于多个组织器官内出现多处病灶,后者往往提示恶性转变。大部分IMT起病隐匿,进展缓慢,无特异性临床表现,患者可出现相应的压迫症状,主要表现为疼痛,少部分患者还有慢性消耗表现,如低热、乏力、体质量减轻,实验室辅助检查可显示贫血、血小板升高,血红细胞沉降率加快、C反应蛋白升高、丙种球蛋白血症等,与慢性炎症病变区分困难。
IMT的影像学检查同样缺乏特异性表现,多数为肿块样病变,包膜不明显,与周围组织分界不清,周围脏器往往受压移位变形,肿块密度与肌肉组织相近,其内部密度多较均匀,部分可出现钙化、出血、坏死、囊性变,强化程度不一,可有环形强化[8];PET-CT表现为放射性浓聚影,但浓聚程度较典型肿瘤性病变低。发生于肺内的IMT多为单发病灶,多位于肺外周胸膜下。肺外的IMT多为单发软组织肿物,CT增强扫描呈均匀或不均匀,中度至显著强化,无明显特异性表现。
IMT的临床表现与影像学表现均缺乏特异性,其诊断依赖病理学。IMT的诊断除根据前述组织学特点外,需要与多种梭形细胞肿瘤鉴别。鉴于IMT病变特殊的临床、影像学及组织病理学表现、术中冰冻活检的局限性,IMT的诊断不提倡依赖针吸活检或术中冰冻切片检查,以避免诊断的片面性。需要取材全面,以至完全切除肿块进行常规石蜡包埋切片检查,以及借助免疫组化染色检查方可确诊。
手术是IMT的主要治疗方法;放疗、化疗疗效不确定,尚有争论[6,13,15-17];有少数患者报道皮质类固醇和非甾体消炎药有一定治疗效果[19];多部位IMT尤其是深部病灶完全切除困难,预后不佳。本例患者一开始就诊时就表现为多部位病灶,存活时间仅为1年,凸显部分多灶性IMT患者的预后不佳。
