18个月化疗方案对耐多药肺结核患者的治疗效果分析
2019-03-18李琦姜晓颖高孟秋刘宇红杨坤云阚晓红梁建琴田明刘锦程崔文玉刘文余德美谭守勇唐神结刘玉琴梁煊邱丽华邵世峰高飞接力蔡宝云卜建玲马丽萍刘智徐麟杜娟操敏高静韬舒薇李亮
李琦 姜晓颖 高孟秋 刘宇红 杨坤云 阚晓红 梁建琴 田明 刘锦程 崔文玉 刘文 余德美 谭守勇 唐神结 刘玉琴 梁煊 邱丽华 邵世峰 高飞 接力 蔡宝云 卜建玲 马丽萍 刘智 徐麟 杜娟 操敏 高静韬 舒薇 李亮
作者单位:101149 首都医科大学附属北京胸科医院 中国疾病预防控制中心结核病防治临床中心(李琦、姜晓颖、高孟秋、刘宇红、唐神结、蔡宝云、卜建玲、马丽萍、操敏、高静韬、舒薇、李亮);湖南省结核病防治所耐药专科(杨坤云);安徽省胸科医院科教科(阚晓红);中国人民解放军总医院第八医学中心全军结核病研究所(梁建琴);成都市公共卫生临床中心(田明);陕西省结核病防治院(刘锦程);长春市传染病医院(崔文玉);枣庄市王开传染病医院(刘文);西安市结核病胸部肿瘤医院结核内科(余德美);广州市胸科医院(谭守勇);黑龙江省传染病防治院(刘玉琴);沈阳市第五人民医院(梁煊);山东省胸科医院五病区(疑难结核病)(邱丽华);天津市海河医院(邵世峰);内蒙古自治区第四人民医院(高飞);新疆维吾尔自治区胸科医院结核二科(接力);深圳市第三人民医院肺病三科(刘智);宁夏回族自治区第四人民医院呼吸一科(徐麟);贵州医科大学附属医院呼吸科(杜娟)
据世界卫生组织(WHO)2018年报告[1],全球3.6%的新发肺结核患者和17%的复治肺结核患者罹患耐多药肺结核(multidrug-resistant pulmonary tuberculosis,MDR-PTB)或利福平耐药肺结核(rifam-picin resistant pulmonary tuberculosis,RR-PTB),均低于中国的罹患率(分别为7.1%和24%);然而,全球MDR-PTB和(或)RR-PTB患者的平均治疗成功率为55%,中国仅为41%;显然MDR-PTB和(或)RR-PTB的疗效不尽如人意,尤其是我国更为突出。迄今为止,国内外MDR-TB相关治疗指南中明确的化疗方案为20~24个月[2-3],这种长疗程的确定主要基于耐药结核分枝杆菌的生长代谢特点、现有抗结核药物的作用机制及其疗效等。Ahuja等[4]通过对相关文献的Meta分析发现,24个月以上的疗程有助于保证MDR-TB患者的治疗成功率。然而,长疗程化疗可增加患者的药物不良反应、加重经济负担、降低治疗依从性,导致患者丢失率增高、治疗成功率降低。因此,制定合理、有效的化疗方案,缩短MDR-TB患者的疗程已是国内外研究的热点。2016年,WHO发布《耐药结核病治疗指南(2016更新版)》[2],重点对具有使用二线药物≤1个月等适应证的MDR-TB和(或)RR-TB患者推荐采用9~12个月的短程化疗方案。但是,国内外的统计学分析显示,复治涂阳患者的耐药率较初治涂阳患者高4倍左右[1,5],加之目前国内尚未推广应用氟喹诺酮类、二线注射剂[如丁胺卡那霉素(Am)、卷曲霉素(Cm)等]及其他二线抗结核药物的快速分子药物敏感性试验(drug sensitivity test,DST),难以确定有效方案,致使现阶段很多MDR-TB患者、特别是复治MDR-TB患者不得不采用5种药物、24个月疗程的化疗方案为最优选择[2-3]。为此,笔者观察和分析了由6种抗结核药物组成、18个月疗程的化疗方案对MDR-PTB患者的治疗效果,为缩短MDR-PTB治疗疗程提供依据。
对象和方法
一、研究对象
1.患者选择:选择2009年7月至2015年12月就诊于首都医科大学附属北京胸科医院、中国人民解放军总医院第八医学中心、安徽省胸科医院、湖南省结核病防治所、黑龙江省传染病防治院、沈阳市第五人民医院、广州市胸科医院、山东省胸科医院、同济大学附属上海市肺科医院(唐神结医师原工作单位)、陕西省结核病防治院、深圳市第三人民医院、内蒙古自治区第四人民医院、长春市传染病医院、天津市海河医院、西安市结核病胸部肿瘤医院、成都市公共卫生临床中心、贵州医科大学附属医院、枣庄市王开传染病医院、新疆维吾尔自治区胸科医院、宁夏回族自治区第四人民医院并被确诊的、且同意被纳入“十一五”和“十二五”国家科技重大专项课题的681例MDR-TB患者。按照所采用的化疗方案将患者分为观察组(18个月方案组)和对照组(24个月方案组)。
2. 患者分组:采用随机、对照、多中心方法进行研究。按照“十一五”和“十二五”国家科技重大专项课题的任务要求,将观察组与对照组按3∶1设置,即样本量应分别为500例与167例。按试验中心分层模拟产生随机数和可供受试者随机分组的编码表下发至各合作单位,各单位按照患者前来就诊的时间顺序,再根据随机编码表将患者分别纳入观察组和对照组。最终本研究纳入观察组515例,对照组166例。收集两组患者的一般人口学特征(性别、年龄等)、耐药资料(类型、数量)、临床资料[病程、治疗史、影像学表现、体质量指数(BMI)、症状(发热、咳嗽、咳痰、咯血、胸痛等)]等进行评分[6],以及既往核心药物[吡嗪酰胺(Z)、Am、莫西沙星(Mfx)、克拉霉素(Clr)]应用情况和本研究中DST结果及选择的药物情况等,具体结果见表1。
3.纳入标准:(1)按照中华医学会结核病学分会制定的《肺结核诊断和治疗指南》[7]进行肺结核诊断;(2)经细菌学检查(痰结核分枝杆菌培养及菌种鉴定为结核分枝杆菌复合群)和DST[显示对包括异烟肼(H)和利福平(R)在内的2种及2种以上抗结核药物耐药]确诊的MDR-TB患者,且对氟喹诺酮类(FQs)药物和Am敏感;(3)所有结核病相关检查和诊断均符合纳入治疗时WHO[8]和中国防痨协会[9]制定的MDR-PTB相关指南或意见;(4)年龄18~65岁;(5)胸部X线摄影显示肺内结核病变,有或无空洞;(6)自愿成为受试者并签署知情同意书。住院期间由医院负责患者管理;非住院期间,根据患者意愿和具体情况,在课题承担单位门诊或由确诊患者的课题单位负责联系患者居住地的结核病防治机构进行患者管理。本研究经首都医科大学附属北京胸科医院伦理委员会批准。
4.排除标准:(1)MDR-TB患者并发HIV感染者;(2)对FQs或二线注射剂耐药的MDR-TB患者;(3)广泛耐药结核病(extensively drug-resistant tuberculosis,XDR-TB)患者;(4)罹患严重心、肝、肾、免疫系统疾病及血液系统等功能异常者,以及妊娠期妇女。
二、研究方法
1.DST检测:采用改良罗氏培养或MGIT 960液体培养的方法筛选受试者。培养阳性者利用MPB64检测试剂盒或对硝基苯甲酸(PNB)鉴别培养基生长试验进行菌种鉴定。将鉴定为结核分枝杆菌复合群者根据其培养方法行DST,如改良罗氏培养阳性者采用比例法DST,MGIT 960液体培养阳性者采用液体DST。检测药物种类至少包括H、R,氧氟沙星(Ofx)和卡那霉素(Km)。
2.化疗方案:观察组化疗方案为6Z-Am-Mfx-Clr-X-Y/12Z-Mfx-Clr-X-Y;对照组化疗方案为6Z-Am-Mfx-X-Y/18Z-Mfx-X-Y。上述方案中,Z为500 mg/次,3次/d,口服;Am为400 mg/次,1次/d,静脉滴注;Mfx为400 mg/次,1次/d,口服;Clr为250 mg/次,2次/d,口服;X、Y为按照MDR-TB患者DST结果选择的2种敏感的一线或二线抗结核药物(表1),包括丙硫异烟胺(Pto:200 mg/次,3次/d,口服)、对氨基水杨酸钠(PAS:8 g/次,1次/d,静脉滴注,避光)、乙胺丁醇(E:750 mg/次,1次/d,口服)。强化期(注射期)为6个月,巩固期为12(观察组)或18个月(对照组)。
3.治疗中检测项目:MDR-TB患者在治疗中每个月行血常规、肝肾功能、尿常规(注射期)等检查,每2个月按照WHO相关指南[8]行结核分枝杆菌培养和心电图检查,每6个月行影像学复查。
4.药物不良反应监测:收集患者的药物不良反应发生情况,如肝功能指标[如丙氨酸氨基转移酶(ALT)和天冬氨酸氨基转移酶(AST)]增高、中性粒细胞减少、肾功能损伤[如尿蛋白阳性、尿素氮(BUN)和(或)肌酐(Cr)高于正常高限]、过敏反应(如皮疹、过敏性休克)、听力减退和胃肠道反应等。
5.治疗转归评估:在疗程末按照WHO[10]发布的《结核病定义和报告框架——2013年修订版》标准对患者的治疗转归进行评估。(1)治愈:患者按国家推荐方案完成治疗且无证据显示失败,强化期后至少3次连续痰培养阴性,每次间隔至少30 d。(2)完成治疗:患者按国家推荐方案完成治疗,且无证据显示失败,但强化期后缺少每次间隔至少30 d的至少3次连续痰培养阴性结果。(3)治疗成功:治愈与完成治疗者。(4)死亡:在治疗过程中患者由于各种原因导致的死亡。(5)失败:由于强化期末痰菌未阴转、或痰菌阴转后在巩固期复阳、或对FQs或二线注射剂继发耐药或药物不良反应导致治疗终止或化疗方案必须更换至少2种抗结核药物。(6)丢失:治疗中断连续2个月或以上。(7)无法评估:未登记治疗转归的患者(包括迁出和治疗转归不详的患者)。
三、统计学处理
采用Excel表格建立数据库,以SPSS 22.0软件进行数据分析。计量资料采用t检验或Z检验,计数资料采用χ2检验,当理论频数<1时,采用Fisher确切概率法检验。均以P<0.05为差异有统计学意义。以治疗成功率为因变量,以观察组和对照组治疗前基本情况中有差异的指标作为协变量,进行logistic回归分析疗效影响因素。
结 果
一、两组患者治疗前基本情况
观察组患者的平均年龄低于对照组、病程长于对照组、化疗方案中E和PAS的选择率高于对照组,差异均有统计学意义(P值均<0.05),其他指标在两组间差异均无统计学意义(P值均>0.05)。具体见表1。
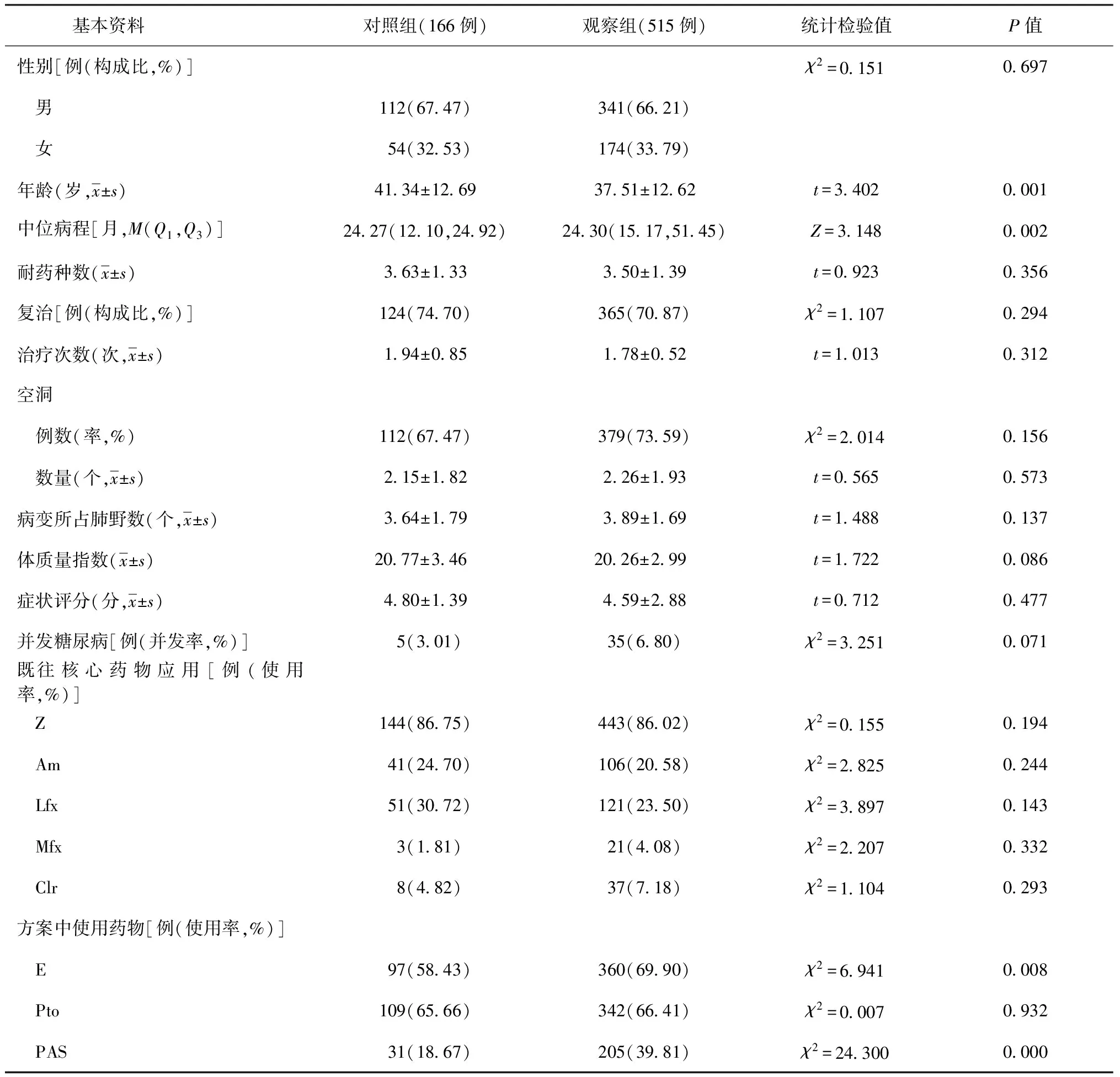
表1 基本资料在两组患者中的分布情况
注Z:吡嗪酰胺,Am:丁胺卡那霉素,Lfx:左氧氟沙星,Mfx:莫西沙星,Clr:克拉霉素,E:乙胺丁醇,Pto:丙硫异烟胺,PAS:对氨基水杨酸钠
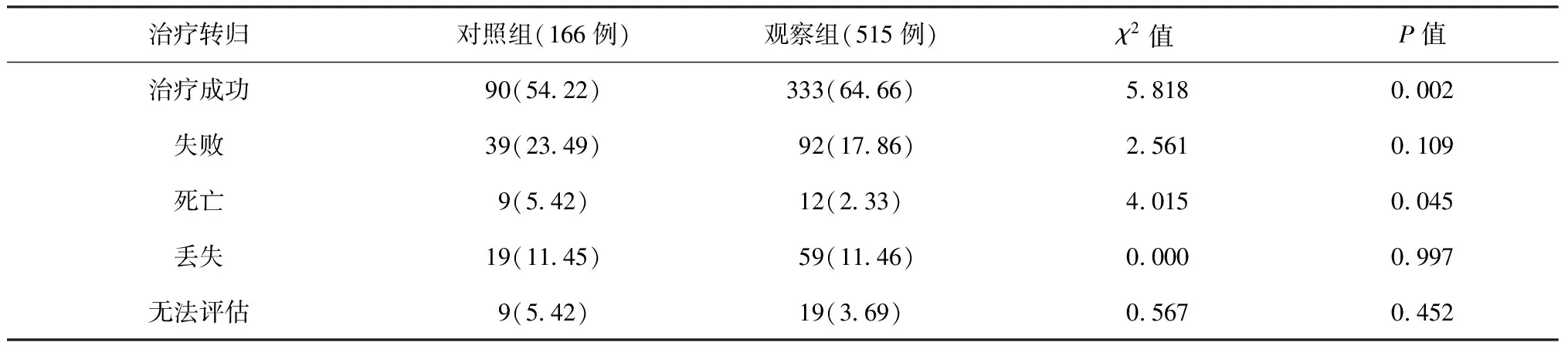
表2 治疗转归在两组患者中的分布情况
注括号外数值为患者例数,括号内数值为构成比(%)
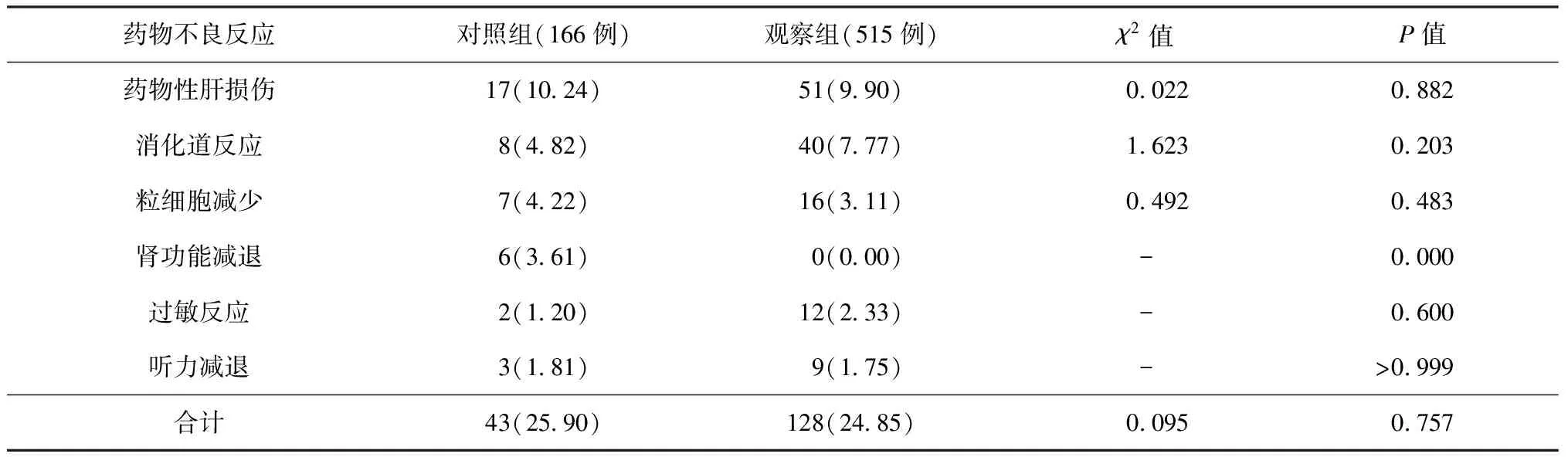
表3 不同药物不良反应在两组患者中的发生情况
注括号外数值为患者例数,括号内数值为发生率(%);“-”为Fisher确切概率法检验
二、两组患者治疗转归情况
观察组的治疗成功率(64.66%)高于对照组(54.22%)、死亡率(2.33%)低于对照组(5.42%),差异均有统计学意义(P值均<0.05);而其失败率、丢失率和无法评估率与对照组相接近(P值均>0.05)。见表2。
三、两组患者主要药物不良反应发生情况
观察组患者药物不良反应的总发生率(24.85%)与对照组(25.90%)接近,差异无统计学意义(χ2=0.095,P>0.05)。两组患者不良反应发生情况相比较,仅对照组患者肾功能减退的发生率(3.61%)高于观察组(0.00%)(P<0.05)。此外,两组患者位列前3位的不良反应均依次为药物性肝损伤、消化道反应和粒细胞减少。见表3。
四、治疗前患者的基本情况与治疗成功率的相关性分析
以治疗成功率作为因变量,以两组间有差异的指标(年龄、病程、方案中E和PAS的使用率)作为协变量,采用logistic回归分析两组患者治疗前临床资料对治疗成功率的影响。其中,年龄以50岁、病程以2年作为分类变量的界限值,赋值见表4。logistic分析结果见表5,显示年龄≥50岁和方案中使用E是治疗成功率的风险因素。

表4 两组患者治疗前有差异临床资料的logistic回归分析赋值表
讨 论
缩短MDR-TB患者化学治疗的疗程是结核病控制的难点与热点。Brigden等[11]提出未来在应用抗结核新药(Mfx、利奈唑胺、氯法齐明、贝达喹啉、德拉马尼和硝基咪唑类抗生素PA-824等)的基础上,有望将MDR-TB的化疗疗程缩短至6个月。2016年,WHO有条件推荐9~12个月的短程化疗方案用于MDR-TB患者的治疗[2]。但此方案的适应证较为严苛,二线抗结核药物应用超过1个月的MDR-TB患者均无法应用此方案,导致此方案的推广受限。因此,利用现有抗结核药物优化化疗方案、逐步缩短疗程是提高MDR-TB治疗成功率的重要措施之一。
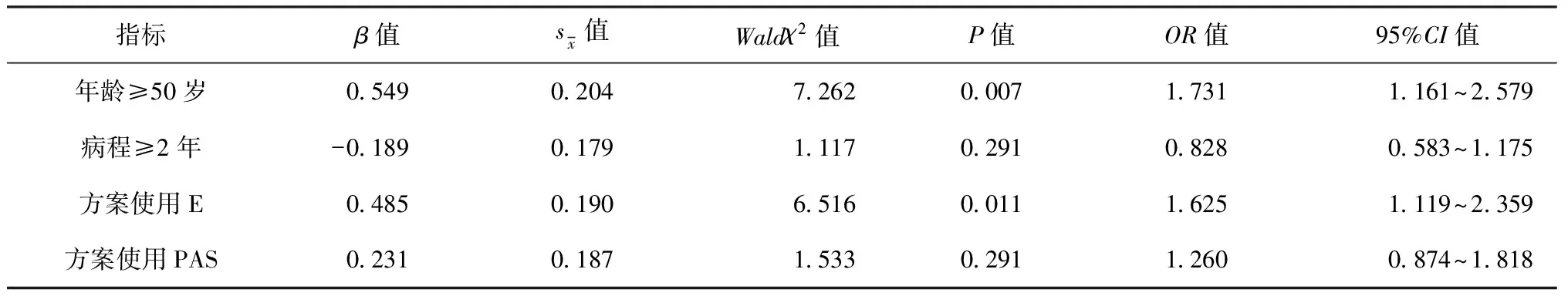
表5 与治疗成功率相关因素的logistic回归分析结果
本研究所采用的化疗方案符合本研究设计及实施时(2008—2015年)国内外指南和意见的要求[3,8-9],基于国内药品供应情况和患者DST检测结果,在5组抗结核药物中选择6种敏感、有效的抗结核药物组成化疗方案,并缩短疗程至18个月。其特点为:(1)与对照组方案相同,均采用具有较高杀菌和(或)灭菌活性的Mfx、Am和Z作为核心药物。其中,Mfx可抑制结核分枝杆菌DNA旋转酶(拓扑异构酶)的A亚单位,阻止结核分枝杆菌DNA复制,具有较强的早期杀菌和灭菌作用,其治疗MDR-TB小鼠4周时的肺、脾菌落形成单位(CFU)计数均降至0 CFU/g[12]。Z主要在酸性环境下对胞内的结核分枝杆菌有杀菌活性,MDR-TB患者肺内常并发其他病原菌的感染[8,13],为Z的杀菌作用提供了适宜的酸性环境。虽然,有文献报道近50%的MDR-TB患者对Z耐药[14],但因本研究对象纳入时Z的DST尚未普及,故仍作为本方案的核心药物。这3种药物的组合为提高早期痰菌阴转率和治愈率、缩短疗程奠定了基础。(2)与对照组方案相同,均联合应用核心药物与2种按照患者DST结果选择的药物共同组成化疗方案,将标准化治疗和个体化治疗相结合,前者符合WHO药物选择的原则,后者以DST结果为基础,避免了标准化治疗针对性较差的局限,也避免了个体化治疗管理成本高的缺点。(3)观察组方案采用6种药物联合应用,较5种药物可更多的覆盖不同生长代谢特点的菌群,特别是相对静止的菌群及持留菌,从而提高疗效、缩短疗程。Ahuja等[4]发现强化期6种药物、巩固期5种药物亦有助于治疗成功。(4)观察组方案选择Clr作为核心药物,系因20世纪90年代,Cavalieri等[15]及Mor和Esfandiari[16]分别报道了Clr与E、Z联合应用可明显降低单一药物应用时的最低抑菌浓度(minimum inhibitory concentration,MIC),提示Clr与一些抗结核药物具有较好的协同作用,期望通过Clr对本方案中部分核心药物(如Z)和备选药物(如E)的协同作用,提高化疗方案的杀菌和抑菌作用,为缩短疗程至18个月奠定基础。尽管Andini和Nash[17]认为Clr对结核分枝杆菌具有耐药性,WHO指南(2016版)亦因Clr的耐药性高和安全性差而将其从抗结核药物中剔除[2],但在本研究纳入患者时Clr仍属于第五组抗结核药物[8]。近年来,亦有文献报道MDR-TB患者长程服用Clr后耐受性较好[18-19],也有体外实验显示Clr与利奈唑胺等药物具有良好的协同作用[20],但其作用机制还有待临床进一步验证。
治疗转归是评价化疗方案疗效的综合指标。本研究显示,观察组患者的平均治疗成功率(64.66%)高于对照组(54.22%)(P<0.05),也高于全球(55%)和国内(41%)的数据[1],提示疗程为18个月的化疗方案(6Z-Am-Mfx-Clr-X-Y/12Z-Mfx-Clr-X-Y)达到或优于疗程为24个月的化疗方案(6Z-Am-Mfx-X-Y/18Z-Mfx-X-Y)的疗效,获得较好的治疗转归,使缩短疗程具有临床可行性。这可能与化疗方案中Mfx和Z的杀菌与灭菌作用有关,但也不能排除Clr对持留菌的杀灭作用[18]以及Clr与其他抗结核药物的协同作用[15-16]。此外,也可能与6种抗结核药物联合应用能够杀灭或抑制处于不同生长代谢期的菌群有关,因为Ahuja等[4]通过Meta分析发现,强化期联用5~6种药物、巩固期联用5种药物与治疗成功率密切相关,其aOR值均高于联用不足5种药物的方案。但究竟是6种药物联用的疗效还是Clr的协同作用,或者尚有其他机制应做进一步的研究和探讨。
对于不良治疗转归而言,观察组的病死率(2.33%)低于对照组(5.42%),至少提示6种药物联用并未增加MDR-TB患者死亡的风险,但也不能完全排除联用Clr的疗效,尚需药效学等研究进一步证实;此外,两组患者的病死率也低于全球的平均水平(16%)[1],可能与两组化疗方案有效性较强有关,但也不能完全排除本研究未纳入MDR-TB并发HIV感染患者的影响,因为MDR-TB并发HIV感染患者的死亡率明显高于非HIV感染患者[1]。观察组与对照组的失败率分别为17.86%和23.49%,差异无统计学意义,进一步证实缩短疗程至18个月并未增加治疗失败的风险;但两组的失败率均高于全球平均水平(8%)[1],可能与本研究纳入的MDR-TB患者中复治患者比率高于71%、中位病程超过24个月、治疗次数多于(1.78±0.52)次、病变范围大于(3.64±1.79)个肺野、空洞数量多于(2.15±1.82)个、营养状况差(平均体质量指数<20.26±2.99)、症状评分高于(4.59±2.88)分等临床特点有关,但也不排除本方案中未应用利奈唑胺、氯法齐明、环丝氨酸等药物有关。虽然目前利奈唑胺、氯法齐明、环丝氨酸在MDR-TB治疗中的疗效已广泛报道[21-23],但在本研究实施期间因利奈唑胺过于昂贵,一般患者难以支付治疗费用而未予以应用;而氯法齐明和环丝氨酸在研究实施初期尚未在国内广泛应用,且缺乏药品供应也未予以应用。患者丢失是MDR-TB治疗中的常见问题,本研究两组患者的丢失率与全球水平[1]相接近,主要为治疗中的失访,可能与患者的依从性低、经济状况差、对结核病治疗的知晓率低等有关。
在MDR-TB患者的治疗中,药物不良反应的发生率较高,可能与联合用药多、疗程长以及患者自身因素(营养不良、肝炎、酗酒等)等原因有关。国内外就MDR-TB患者治疗中药物不良反应发生率的报道不尽相同,国内王飞等[24]的报道为92.5%,而Nathanson等[25]的报道为32%。本研究显示,观察组共有128例次发生药物不良反应,发生率为24.85%,与对照组相接近。提示尽管观察组化疗方案的药物种类较对照组多,但并未增加研究患者的药物不良反应发生率,特别是未出现与Clr相关的严重药物不良反应,如肝功能损伤、QT间期延长等,提示此方案具有较好的安全性。在常见药物不良反应中,两组患者药物性肝损伤(包括高胆红素血症)、消化道反应和粒细胞减少均居前三位,且其发生率在两组间差异无统计学意义,与国外文献[25]的报道不尽相同。这可能与本研究所采用的化疗方案中所应用的药物种类、药物工艺与质量、人种、纳入观察患者的一般情况等有关,特别是较高的药物性肝损伤发生率不排除与国内较高的肝炎发生率、饮酒率等有关。
分析本研究纳入患者时发现,两组患者治疗前在年龄、病程、使用E和PAS比率的差异均有统计学意义。为观察这些差异指标对治疗转归的影响,本研究采用logistic回归的方法分析这些差异指标与治疗成功率的相关性。结果显示,年龄≥50岁和方案中使用E是治疗成功的风险因素。前者可能与高龄患者免疫功能下降影响耐药结核分枝杆菌的清除,以及各脏器功能减退导致药物不良反应增多等因素有关。但就本研究而言,观察组年龄的平均值低于对照组并非是观察组治疗成功率高于对照组的惟一决定性因素,原因如下:(1)观察组病程长于对照组(P<0.05),由于病程长易导致肺组织反复破坏与修复使肺功能降低,但观察组在病程较长的情况下依然取得较高的治疗成功率,提示治疗成功率受多种因素影响。(2)有关年龄对治疗成功率的影响可能会因样本量、分析方法、分析指标不同而异。Ahmad等[26]对来自25个国家、50项研究、12 030 例MDR-TB患者的Meta分析显示,年龄不是治疗成功率的风险因素,其治疗成功率主要与抗结核新药(利奈唑胺、Mfx、贝达喹啉)的应用、肺内无空洞、既往未应用二线抗结核药物、对FQs药物敏感等因素有关;而方案中使用E是治疗成功的风险因素,可能与E是抑菌药有关,即使在对E敏感的情况下也对耐药结核分枝杆菌的作用有限,且对治疗成功率的影响小于FQs、利奈唑胺、贝达喹啉等药物。
综上所述,6种抗结核药物、18个月的化疗方案虽然较24个月化疗方案获得较好的治疗成功率,且未增加药物不良反应发生率,具有临床可行性。但队列尚小,还有待多中心、大样本的论证。此外,疗程仅缩短到18个月,未达到短程化疗的疗程,还有待于未来引入其他抗结核新药,建立完善的治疗转归评估体系和方法,为制定更符合临床实际的MDR-TB短化方案提供依据。
